Rapport d'information n° 79 (2008-2009) de Mme Marie-Thérèse HERMANGE , fait au nom de la commission des affaires sociales, déposé le 4 novembre 2008
Disponible au format Acrobat (843 Koctets)
-
AVANT-PROPOS
-
I. L'INTÉRÊT THÉRAPEUTIQUE DES
CELLULES SOUCHES EXTRAITES DU SANG DE CORDON
-
II. GARANTIR LE MEILLEUR USAGE DU SANG DE CORDON
OMBILICAL
-
I. L'INTÉRÊT THÉRAPEUTIQUE DES
CELLULES SOUCHES EXTRAITES DU SANG DE CORDON
-
PRÉCONISATIONS
-
TRAVAUX DE LA COMMISSION
-
LISTES DES PERSONNES AUDITIONNÉES
-
ANNEXES
N° 79
SÉNAT
SESSION ORDINAIRE DE 2008-2009
|
Annexe au procès-verbal de la séance du 4 novembre 2008 |
RAPPORT D'INFORMATION
FAIT
au nom de la commission des Affaires sociales (1) sur le potentiel thérapeutique des cellules souches extraites du sang de cordon ombilical ,
Par Mme Marie-Thérèse HERMANGE,
Sénateur.
|
(1) Cette commission est composée de : M. Nicolas About , président ; Mme Isabelle Debré, M. Gilbert Barbier, Mme Annie David, M. Gérard Dériot, Mmes Annie Jarraud-Vergnolle, Raymonde Le Texier, Catherine Procaccia, M. Jean-Marie Vanlerenberghe , vice-présidents ; MM. François Autain, Paul Blanc, Mme Muguette Dini, M. Jean-Marc Juilhard, Mmes Gisèle Printz, Patricia Schillinger , secrétaires ; Mmes Jacqueline Alquier, Brigitte Bout, M. Jean Boyer, Mme Claire-Lise Campion, MM. Jean-Pierre Cantegrit, Bernard Cazeau, Mme Jacqueline Chevé, M. Yves Daudigny, Mme Christiane Demontès, M. Jean Desessard, Mmes Sylvie Desmarescaux, Bernadette Dupont, M. Guy Fischer, Mme Samia Ghali, MM. Bruno Gilles, Jacques Gillot, Mme Colette Giudicelli, MM. Jean-Pierre Godefroy, Alain Gournac, Mmes Sylvie Goy-Chavent, Françoise Henneron, Marie-Thérèse Hermange, Gélita Hoarau, M. Claude Jeannerot, Mme Christiane Kammermann, MM. Marc Laménie, Serge Larcher, André Lardeux, Dominique Leclerc, Jacky Le Menn, Jean-François Mayet, Alain Milon, Mmes Isabelle Pasquet, Anne-Marie Payet, M. Louis Pinton, Mmes Janine Rozier, Michèle San Vicente-Baudrin, MM. René Teulade, Alain Vasselle, François Vendasi, René Vestri. |
AVANT-PROPOS
Mesdames, Messieurs,
L'humanité dispose d'une ressource thérapeutique abondante, simple d'accès et ne posant aucun problème éthique majeur. Il s'agit du sang placentaire, appelé plus communément sang de cordon ombilical car c'est dans cette partie du placenta qu'il est collecté. Le sang transitant par le cordon ombilical, qui alimente en oxygène l'enfant à naître, a été considéré depuis le début du XX e siècle comme un moyen de soigner les pathologies sanguines en raison de sa grande richesse cellulaire. On sait aujourd'hui plus précisément qu'il s'agit d'une richesse en cellules souches capables de reconstruire les tissus humains lésés.
Cette propriété du sang de cordon est à l'origine de trois types d'application. La première, déjà courante, est la thérapie des maladies du sang, où le cordon ombilical remplace avantageusement les greffes de moelle osseuse. Plus de dix mille personnes ont bénéficié d'une greffe de cellules extraites du sang de cordon depuis la première opération réalisée voici vingt ans par le professeur Eliane Gluckman et son équipe de l'hôpital Saint-Louis.
La deuxième est une perspective dont la réalisation se dessine à court terme : il s'agit de collecter dans le sang les cellules souches capables de reconstituer la peau, ce qui permettra d'une part, de soigner les grands brûlés, d'autre part, de donner aux pharmacologues des tissus humains constituant une alternative pour tester leurs nouveaux médicaments, susceptibles de remplacer en tout ou partie les modèles animaux, voire humains, sur lesquels ils travaillent.
Le dernier type d'application est attendu à moyen ou long terme. Il s'agit de développer à partir des cellules souches extraites du sang de cordon des thérapies régénérant différents organes, allant du muscle cardiaque à la rétine et sans doute jusqu'aux neurones du cerveau. L'enjeu de santé publique se double ici d'une question stratégique pour permettre à la recherche française de se maintenir au plus haut niveau, dans un contexte de concurrence internationale exacerbé.
La France, pionnière en matière de thérapies issues du sang de cordon, ne peut se passer d'une politique publique en ce domaine d'autant que, malgré ses avantages objectifs (plus de huit cent mille naissances chaque année, une pratique de collecte et de stockage d'une excellence internationalement reconnue), elle accuse un retard considérable en matière de nombre d'unités disponibles par habitant et ne se situe qu'au seizième rang mondial derrière de nombreux pays européens et émergents. Cette politique publique est nécessaire pour ne plus traiter comme un simple déchet opératoire ce qui demain pourrait sauver des vies. D'une part, il s'agit de concrétiser l'espoir né des découvertes de la médecine en matière de biologie puis de thérapie cellulaire au cours des vingt dernières années. D'autre part, il apparaît nécessaire, dans le domaine facilement fantasmatique des cellules souches, d'informer véritablement et pleinement l'opinion publique.
En effet, le constat d'une plus grande artificialisation de la vie humaine est largement répandu. L'homme est de moins en moins dépendant de la nature mais de plus en plus dépendant de ses propres créations. Le développement de la science du vivant depuis le XIX e siècle, et surtout depuis l'essor des biotechnologies, donne pour la première fois à notre espèce la possibilité de connaître, pour les imiter, les processus fondamentaux de la vie que sont la création et la division cellulaires. Ainsi, l'homme voit se dessiner la possibilité de s'affranchir de la fatalité biologique qui marque sa condition. Ces progrès offrent la promesse de guérir de nombreuses maladies, voire de remédier à des handicaps, et en cela le progrès est porteur d'un espoir que les pouvoirs publics doivent accompagner. Il faut néanmoins prendre garde que l'homme, de moins en moins soumis à la fatalité, ne se considère également comme affranchi de toute hérédité et de toute filiation. Ceci impliquerait qu'il ne serait plus redevable de son existence qu'à lui-même, indépendamment de tout lien familial ou social. Rien ne s'opposerait donc à ce qu'il développe, avec l'aide de la science, ses capacités jusqu'à leur plus extrême limite, voire se lance dans la quête illusoire de l'immortalité. Si pareille recherche paraît très minoritaire, il ne faut pas négliger l'impact que ces notions, édulcorées, peuvent avoir au sein de la population. Les annonces très médiatiques de régénération d'organes qui pourraient un jour éventuellement être « réparés » ou « recréés » sont génératrices d'attentes déraisonnables. Il est donc nécessaire qu'une limite éthique soit posée au fantasme d'une humanité auto-fondée et parvenant à s'affranchir une fois pour toutes de la nature. Ceci permettra l'élaboration d'un discours politique clair, susceptible d'informer le citoyen relativement aux perspectives médicales et lui permettant d'agir en tant que membre responsable de la collectivité et de l'humanité. Ainsi, toute atteinte au principe de solidarité qui fonde l'approche française des produits issus du corps humain depuis les lois de bioéthique, c'est-à-dire le principe du don anonyme, gratuit et non dirigé, doit être envisagée avec la plus grande prudence.
Afin de concrétiser l'espoir tout en gardant la raison, ce rapport s'interroge sur les finalités de la collecte de sang de cordon liée aux progrès des connaissances et au développement des thérapies, avant de se pencher sur les moyens à engager pour permettre le meilleur usage du sang collecté.
I. L'INTÉRÊT THÉRAPEUTIQUE DES CELLULES SOUCHES EXTRAITES DU SANG DE CORDON
Le sang de cordon ombilical est une ressource thérapeutique particulièrement riche qu'une politique de santé publique efficace et prévoyante se doit de préserver. Afin de mesurer l'ampleur des avancées déjà acquises ou prévisibles, il est nécessaire de comprendre quels ont été les progrès en matière de connaissance du fonctionnement des cellules et de mesurer l'intérêt scientifique, fondamental et médical de ce qu'on ne peut plus considérer comme un simple « résidu opératoire ».
A. COMPRENDRE LA STRUCTURE DU VIVANT
Connaissance du corps humain et thérapeutique sont indissolublement liées. Le progrès de l'une suppose et provoque à la fois l'amélioration de l'autre. La recherche en matière de biologie humaine n'est donc jamais loin des applications cliniques. Un domaine en particulier a vu le lien entre recherche fondamentale et application s'accélérer, voire s'inverser, au cours des dernières décennies : la biologie cellulaire. Appréhender théoriquement la composition des tissus vivants encourage à la maîtriser pratiquement, c'est-à-dire à réparer les tissus ou à les remplacer en en créant de nouveaux. Comprendre les perspectives ouvertes par l'utilisation des cellules extraites du sang de cordon ombilical impose donc de saisir comment s'articulent, dans ce domaine spécifique, progrès des connaissances et prise en compte du potentiel thérapeutique des nouvelles découvertes.
1. Les progrès dans la connaissance du vivant
A partir de bases posées à la fin du XIX e siècle, la connaissance des structures du vivant a progressé peu à peu jusqu'aux avancées majeures des années quatre-vingt qui ont permis le développement des thérapies cellulaires fondées sur l'identification, la reproduction et la greffe de certains types de cellules souches.
a) Fondements de la théorie cellulaire
La première observation de cellules est liée au développement du microscope et date de 1665. Son auteur, le savant anglais Robert Hooke, est également à l'origine de l'analogie entre les structures closes qu'il avait identifiées dans le liège et les cellules monacales. De cette analogie est né le nom des cellules vivantes. Cependant, malgré l'ancienneté de l'identification des cellules, leur nature et leur fonctionnement n'ont pu être établis que très progressivement et après de nombreux débats 1 ( * ) . Georges Canguilhem 2 ( * ) associe la théorie cellulaire à deux postulats qui se trouvent réunis pour la première fois en 1849 dans la Pathologie cellulaire de l'Allemand Rudolf Virchow :
1. tout organisme vivant est un composé de cellules, la cellule étant tenue pour l'élément vital porteur de tous les caractères de la vie ;
2. toute cellule dérive d'une cellule antérieure.
Il en découle que l'oeuf d'où naissent les organismes vivants sexués est une cellule dont le développement s'explique uniquement par la division.
Canguilhem date la consécration de la théorie cellulaire de 1874, année où Claude Bernard, étudiant du point de vue physiologique les phénomènes de nutrition et de génération communs aux animaux et aux végétaux, écrit : « Dans l'analyse intime d'un phénomène physiologique on aboutit toujours au même point, on arrive au même agent élémentaire, irréductible, l'élément organisé, la cellule ». La cellule, c'est « l'atome vital » .
La composition du vivant une fois connue, se posait alors la question suivante : « si le corps est réellement une somme de cellules indépendantes, comment expliquer qu'il forme un tout fonctionnant de manière uniforme ? 3 ( * ) ». Au-delà des mécanismes de division cellulaire, c'est donc la manière dont elles parviennent à exercer une fonction spécifique dans l'organisme, leur spécialisation, qui est devenue un objet d'étude. Les recherches effectuées en ce domaine ont permis, au cours du dernier demi-siècle, la découverte de cellules encore non spécialisées, les cellules souches.
b) Découverte des cellules souches
Le terme de cellule souche apparaît, semble-t-il, dans les années soixante comme équivalent du terme anglais « stem cell » , littéralement « cellule tige » , apparu en 1883. Le terme « souche » ne renvoie donc pas à une dimension statique mais à une dynamique « végétative, c'est-à-dire support de vie et de transformation vitale » 4 ( * ) . Dès les années vingt, des cellules souches étaient découvertes chez le poulet mais ce n'est que trente ans plus tard qu'une telle découverte est faite également chez le mammifère, puis spécifiquement chez l'homme. Le terme a rencontré un très grand succès médiatique à partir des années quatre-vingt-dix, qui a pu faire oublier que sa définition a longtemps fait l'objet de controverses.
Selon les termes employés par François Gros, professeur honoraire au collège de France et spécialiste reconnu de cette question : « Les cellules souches sont des cellules indifférenciées qui, comme leur nom l'indique, sont à l'origine de la formation des divers tissus de l'organisme, soit au cours de l'embryogénèse normale, soit chez l'adulte, au cours de la régénération de ces tissus consécutive à un traumatisme, ou encore après avoir été greffées sur un animal receveur (exemple : greffes de moelle). Elles apparaissent dans les tout premiers stades du développement de l'embryon alors que les tissus ne sont pas encore formés par les mécanismes de différenciation. Le fait remarquable est cependant qu'elles ne se convertissent pas toutes in vivo en cellules spécialisées puisqu'elles persistent à l'état de cellules souches multipotentes en très petit nombre certes, mais de façon pérenne dans la plupart des tissus des organismes à l'état adulte 5 ( * ) . »
Définition d'une cellule souche
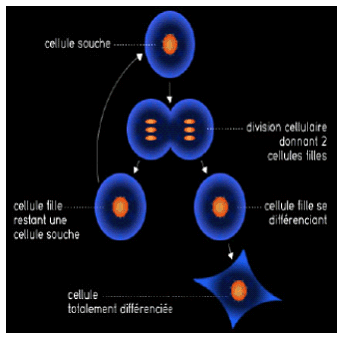
Copyright SO2 média pour la Cité des Sciences et de l'industrie, 2001
On en déduit une répartition principale entre deux types de cellules souches :
- les unes sont issues de l'ovocyte fécondé à différents stades de son développement. Elles sont dites, selon l'état d'avancement du processus, embryonnaires ou foetales ;
- les autres sont issues du cordon ombilical ou du corps humain constitué. Elles peuvent être regroupées sous le terme de cellules souches somatiques, le terme de cellule souche adulte étant réservé aux cellules souches présentes dans le corps humain.
Cette division en deux catégories apparaît comme la summa divisio en termes de recherche, de thérapeutique et d'éthique. On leur ajoute néanmoins parfois un autre groupe de cellules dites « précurseurs » , que l'on trouve dans tous les types de tissus, qui sont issues de la division des cellules souches et sont plus spécialisées ; elles sont déjà fonctionnelles 6 ( * ) .
Divers types de cellules souches spécialisées ont été progressivement identifiées dans les tissus adultes. Le bilan de la recherche dressé en 2000 7 ( * ) pouvait ainsi affirmer :
« Des cellules souches (...) capables de « réparer » les tissus suivants ont été identifiées avec certitude chez l'homme : cellules souches nerveuses, hématopoïétiques, épidermiques, intestinales, osseuses, pancréatiques, hépatobiliaires, musculaires lisses, musculaires squelettiques. » Les différents types de cellules souches se différencient donc en divers types de cellules spécialisées.
Elles permettent aux différents organes de se régénérer, certaines quotidiennement et d'autres en cas de traumatisme. Comme le note le rapport de 2000, dans le corps humain : « Les cellules souches de trois tissus (sang, peau, intestin) fonctionnent en permanence, pendant la vie, pour renouveler régulièrement l'ensemble des cellules. (...) Quant à celles des autres tissus, elles ne sont activées que lorsque la nécessité d'une réparation se fait sentir. Elles sont par exemple présentes dans la moelle et, une fois greffées, reforment tous les éléments du sang (lesquels sont d'ailleurs en constant renouvellement). On les retrouve à l'état de cellules satellites dans les muscles adultes dont elles assurent la régénération post-traumatique. Elles permettent de reconstituer le derme et une partie de l'épiderme chez les brûlés. On est parvenu à les mettre en évidence dans le cerveau adulte et, sous certaines conditions, dans le foie » .
L'enjeu pour la recherche médicale est donc d'identifier ces cellules souches puis de connaître et de maîtriser leur processus de spécialisation afin de reconstruire non seulement les tissus atteints de lésions ou de malformations qui se réparent spontanément mais également ceux qui ne le font pas ou pas entièrement. Dans cette perspective, des travaux sont engagés tendant à permettre la reconstruction du muscle cardiaque, de la rétine, des dents, voire des neurones. Le potentiel thérapeutique des différents types de cellules souches doit donc être précisé.
Les différents types de cellules souches adultes et leur descendance
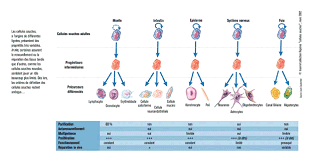
http://science-citoyen.u-strasbg.fr/dossiers/souches/html/partie4/index.html
2. Le potentiel thérapeutique
Au-delà de l'origine tissulaire des cellules souches, c'est leur capacité à se diviser en un plus ou moins grand nombre de cellules spécialisées qui détermine leur intérêt thérapeutique. L'étude du potentiel original des différents types de cellules souches doit s'appuyer sur les perspectives d'augmentation offertes par la recherche.
a) Potence et plasticité
La recherche fondamentale en biologie a élaboré une catégorisation devenue classique dans laquelle on range les différents types de cellules souches 8 ( * ) ; on parle de cellules :
- totipotentes, lorsque le type cellulaire peut se différencier en donnant tous les types cellulaires de l'organisme ;
- pluripotentes, lorsque le type cellulaire peut se différencier en un nombre plus restreint de types spécialisés ;
- multipotentes, lorsque le type cellulaire peut produire des cellules de morphologie et de fonction très différentes, généralement groupées au sein d'un même organe ou tissu (ainsi les cellules souches hématopoïétiques qui produisent l'intégralité du sang) ;
- unipotentes ou différenciées, lorsque le type cellulaire est stable et ne peut plus évoluer vers d'autres types.
L'intérêt porté par la recherche aux cellules souches embryonnaires ou foetales vient de ce qu'elles conservent le plus grand nombre de cellules totipotentes ou pluripotentes puisque, par nature, elles ne se sont pas encore spécialisées pour former un organe particulier. Il convient cependant de souligner que certaines cellules somatiques (donc issues des tissus adultes ou du sang de cordon) demeurent multipotentes voire pluripotentes. Elles offrent donc théoriquement le même intérêt que celles ayant le même potentiel mais issues du foetus ou de l'embryon. De plus, elles présentent l'avantage de ne pas se trouver confrontées à un problème éthique. La difficulté de leur étude et de leur utilisation thérapeutique est pratique : d'une part, elles sont peu nombreuses par rapport aux cellules de même type contenues dans les tissus foetaux ou embryonnaires ; d'autre part, elles sont moins nombreuses dans les tissus adultes et dans le sang de cordon que les autres types de cellules. Elles sont de ce fait moins facilement identifiables et plus difficiles à extraire. Il faut donc espérer que le progrès des techniques de recherche permettra rapidement de mieux isoler ces cellules.
Mais avant même d'atteindre ce résultat, les connaissances acquises au cours des dernières années ont prouvé l'intérêt des cellules différenciées en matière thérapeutique : non seulement elles peuvent être utilisées pour réparer les tissus dont elles sont issues, mais il apparaît en outre que, malgré leur spécialisation, ces cellules peuvent, en fonction du milieu où elles sont placées, se diviser en cellules d'un type nouveau. On parle de leur « plasticité ». Ainsi en 2003, dans un article consacré aux cellules souches adultes, le professeur Ali Turhan 9 ( * ) pouvait écrire : « Jusqu'à une date récente, les cellules souches adultes, définies classiquement par leurs propriétés d'autorenouvellement et de différenciation, étaient considérées comme étant spécifiques d'organes. Cette notion a été défiée par des expériences montrant que la greffe de certains tissus, notamment la moelle osseuse, pouvait générer chez l'animal létalement irradié, non seulement des cellules hématopoïétiques mais aussi des cellules musculaires, hépatiques et même neuronales ». La recherche laisse cependant subsister une incertitude, soulignée à l'époque par le professeur Turhan : des cellules totipotentes, dont la présence n'aurait pas été repérée, pourraient en fait être à l'origine de la formation des nouvelles cellules. Néanmoins, la plasticité des cellules souches adultes spécialisées semble désormais établie.
Ainsi l'organisme adulte et le sang de cordon contiennent des cellules souches à fort potentiel et des cellules souches déjà spécialisées mais capables de « transdifférenciation », c'est-à-dire de produire des cellules spécialisées qui ne soient pas celles du tissu dont elles proviennent mais du tissu dans lequel elles sont implantées. La recherche tend donc à leur reconnaître un potentiel thérapeutique plus grand qu'on ne le pensait à l'origine ; en outre elle a désormais les moyens d'améliorer ce potentiel.
b) Les perspectives offertes par la recherche
Le nombre de thérapies cellulaires efficaces reste en effet réduit par rapport aux possibilités de reconstruction des tissus, mais il augmente progressivement grâce à divers types de travaux, qui ouvrent des perspectives en matière thérapeutique. « Il est clair que l'ensemble de ces travaux a ouvert un nouveau chapitre de la biologie du développement et, peut-être, à plus ou moins long terme, de la médecine régénérative » affirme François Gros 10 ( * ) . Ainsi, la valeur thérapeutique des cellules souches dépend à l'évidence des progrès de la science. Ceux-ci sont à attendre à plusieurs niveaux.
Au niveau fondamental tout d'abord, si les mécanismes de division cellulaire sont bien connus depuis longtemps, ce n'est pas encore le cas des mécanismes de spécialisation. En dehors de toute pression pour l'obtention de résultats immédiatement traduisibles sur le plan thérapeutique, il est donc important que des équipes de recherche puissent se consacrer à la mécanique cellulaire. Leurs travaux permettront de comprendre le fonctionnement des cellules souches, les raisons de leur permanence dans certains tissus une fois passé le stade embryonnaire et les moyens par lesquels elles en viennent à créer certains types, et non d'autres, de cellules spécialisées puis définitivement différenciées.
Ensuite, en ce qui concerne le nombre de cellules disponibles, plusieurs pistes s'avèrent porteuses d'espoir. Tout d'abord, la possibilité de reproduire en laboratoire des cellules souches est devenue un axe essentiel de la recherche. L' « expansion cellulaire » qui permettrait l'accroissement du nombre de cellules cultivées en laboratoire à partir d'un faible nombre de cellules prélevées pourrait un jour permettre de s'affranchir de la contrainte liée à la taille des greffons nécessaires pour pratiquer une thérapie.
Par ailleurs, la transdifférenciation des cellules souches adultes peut déjà être obtenue en laboratoire. Une cellule souche déjà spécialisée peut donc, par transfert de noyau, être transformée en cellule souche d'un autre type de tissu. Il est même possible, depuis les travaux du professeur Shinya Yamanaka de l'Université de Kyoto dont les premiers résultats ont été annoncés en novembre 2007 et dont le perfectionnement a été obtenu moins d'un an plus tard, le 9 octobre 2008 11 ( * ) , de faire régresser une cellule souche adulte déjà spécialisée vers la pluri voire la totipotence. Ces cellules sont dites « cellules souches pluripotentes induites » ou iPS (de l'anglais induced pluripotent stem cells ) Le « matériau » vivant ayant le plus fort potentiel de reconstruction tissulaire est donc actuellement accessible à partir des tissus adultes, ce qui a incité plusieurs équipes de chercheurs à se détourner des recherches sur le foetus et l'embryon qui présentent moins d'intérêt, étant donné les contraintes imposées par leur cadre légal et la difficulté éthique que posent de tels travaux 12 ( * ) .
D'une cellule somatique à une cellule souche pluripotente par transfert de noyau
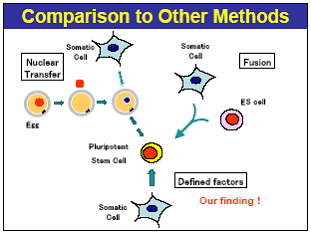
http://www.frontier.kyoto-u.ac.jp/rc02/index.html
Enfin, en ce qui concerne plus précisément les cellules extraites du cordon ombilical, qui devraient être la ressource cellulaire la plus facilement accessible, deux choix doivent être faits pour permettre à la recherche d'approfondir les connaissances déjà acquises. D'une part, les échantillons prélevés qui ne peuvent servir de greffon en raison de la quantité insuffisante de sang recueilli ou de sa qualité, doivent être rendus disponibles pour les chercheurs. D'autre part, il est important que la recherche de cellules puisse se faire non seulement sur le sang extrait du cordon mais, comme c'est le cas déjà dans de nombreux pays et systématiquement en Chine, sur le cordon lui-même et sur le placenta qui peuvent également être des ressources importantes de cellules souches.
Le nombre de cellules disponibles et leur potentiel de différentiation peuvent donc tous deux être améliorés grâce aux travaux de recherche actuellement en cours. Un accent complémentaire à celui mis sur la recherche appliquée doit être placé sur la recherche fondamentale afin que soient mieux connus, et donc plus facilement reproduits, les mécanismes par lesquels les cellules souches permettent de réparer les tissus lésés.
La découverte des cellules souches a fait profondément évoluer notre connaissance du corps humain et a ouvert de nouvelles perspectives thérapeutiques que les recherches actuelles ne font que préciser. Les cellules extraites du sang sont déjà couramment utilisées dans un but thérapeutique, et avec succès.
B. LE DÉVELOPPEMENT DES THÉRAPIES CELLULAIRES À PARTIR DU SANG DE CORDON OMBILICAL
Les thérapies utilisant les cellules souches ont au moins quarante ans puisque la première greffe de moelle osseuse à été pratiquée en 1969 par Edward Donnall Thomas, prix Nobel de médecine en 1990, en se fondant sur la recherche qu'il avait menée depuis les années cinquante. Or, on sait désormais que les greffes de moelle osseuse sont en fait des greffes de cellules souches hématopoïétiques. Quatre mille deux cent trente-neuf greffes ont été pratiquées en France en 2007 13 ( * ) . L'idée d'utiliser les cellules contenues dans le sang de cordon ombilical est ancienne, un article paru dans la revue The Lancet envisageait cette possibilité dès 1939 et la première tentative pour soigner par transfusion une patiente atteinte d'un cancer date de 1963. Mais c'est seulement en 1988 que l'équipe du professeur Eliane Gluckman à l'hôpital Saint-Louis a établi le protocole désormais suivi en opérant avec succès la première greffe pour soigner un enfant atteint de la maladie de Franconi. Les thérapies issues du sang de cordon, que ce soit pour soigner les maladies de la moelle osseuse ou reconstituer le derme, appellent l'implication de l'Etat qui doit agir en tant que force d'impulsion sous peine de voir un jour sa responsabilité potentiellement engagée du fait du manque d'informations fournies.
1. Les thérapies existantes
C'est d'abord vers les maladies du sang qu'ont porté, avec succès, les efforts thérapeutiques fondés sur le sang de cordon ombilical. Dans un second temps, les progrès dans la connaissance des différents types de cellules souches et de leur fonctionnement permettront, sans doute bientôt, l'élaboration de nouvelles thérapies susceptibles de réparer le derme des irradiés et des grands brûlés.
a) Thérapies actuelles liées aux maladies du sang
Les cellules souches hématopoïétiques contenues dans le sang de cordon remplacent avantageusement celles de la moelle osseuse pour plusieurs raisons. D'une part, la plus grande immaturité des cellules souches du sang de cordon permet une meilleure efficacité des greffes. D'autre part, les chances de trouver un échantillon de sang de cordon compatible avec un malade sans lien de parenté avec le donneur sont très nettement supérieures à celles de trouver un donneur de moelle osseuse pour une greffe dite allogénique 14 ( * ) . Les chiffres donnés par le professeur Gregory Katz-Benichou 15 ( * ) pour les Etats-Unis en témoignent : un tiers environ des patients en attente d'une greffe de moelle sont amenés à chercher un donneur à l'extérieur de leur famille et moins d'un tiers d'entre eux (9 % du nombre total de patients) trouvent un donneur compatible ; à l'inverse, dans le monde entier, toutes les recherches faites sur les bases recensant les greffons de sang de cordon disponibles sont fructueuses. Ainsi tous les patients devant subir une greffe de sang de cordon trouvent un greffon compatible. Plus de 20 000 personnes ont donc pu être greffées depuis 1988 et il n'est pas étonnant de constater que la part des greffes de sang de cordon croît chaque année aux dépens des greffes de moelle. En 2007, les greffes de sang de cordon représentaient 27 % des greffes allogéniques pratiquées en France 16 ( * ) .
Une découverte thérapeutique a considérablement renforcé l'utilisation du sang de cordon comme alternative à la moelle osseuse : en raison de la relative facilité avec laquelle ils sont acceptés par l'organisme, les greffons de sang de cordon peuvent être combinés avant d'être greffés. Ceci implique que la greffe, un temps limitée aux enfants en raison de la taille du greffon, peut désormais être effectuée sur des adultes par combinaison de deux greffons.
Au total, la greffe de sang de cordon est utilisée aujourd'hui dans près de quatre-vingt-cinq indications thérapeutiques. Elle « traite de nombreux cancers du sang (leucémies, lymphomes), des thalassémies et des drépanocytoses, des maladies auto-immunes et de nombreuses maladies rares (Tay-Sachs, Niemann-Pick, Krabb, Hurler, Gaucher, etc.). En France, environ 126 000 personnes sont touchées chaque année par ces quatre-vingt-cinq maladies 17 ( * ) » .
b) Thérapies en cours d'élaboration
La France se situe à la pointe des thérapies visant à reconstituer les os en cas de lésions particulièrement importantes, ou le derme des victimes d'irradiation ou des grands brûlés. Depuis 2002, le service du médecin en chef Lataillade à l'hôpital militaire Percy à Clamart a obtenu des résultats remarquables pour ces blessures d'une particulière gravité en utilisant les cellules souches mésenchymateuses issues de la moelle osseuse 18 ( * ) . Celles-ci permettent la reconstruction de tissus osseux sur des fractures qui ne peuvent guérir spontanément, la réparation de lésions dues aux irradiations et la constitution de greffons de peau. Un projet commun à plusieurs partenaires, dont l'Inserm, est en cours pour permettre d'isoler les cellules souches mésenchymateuses contenues dans le sang de cordon, dont les effets devraient être particulièrement bénéfiques pour les malades : les cellules extraites du sang de cordon seront immédiatement disponibles en grand nombre, ce qui permettra un traitement rapide alors que le prélèvement et la mise en culture des cellules extraites de la moelle osseuse des malades eux-mêmes peut prendre jusqu'à quinze jours, ce qui affecte les chances de survie. Une fois encore, la richesse et la disponibilité de la ressource sont les facteurs qui renforcent l'utilité thérapeutique du sang de cordon.
En dehors de ce cas précis, plusieurs équipes françaises et internationales travaillent sur les applications thérapeutiques liées au sang de cordon, parmi lesquelles celle du professeur Colin McGuckin à l'Université de Newcastle. Ce dernier est également le président du consortium Novus Sanguis qui se consacre particulièrement à la recherche en ce domaine. Lors de son lancement à Paris, le 14 mai 2008, quatre principales voies d'avenir ont été tracées en matière thérapeutique : le diabète juvénile, la neurologie, les maladies du foie et du rein et la cardiologie. Au travers notamment de bio-implants constitués à partir de cellules souches extraites du sang de cordon, différentes thérapies, dont certaines en sont déjà au stade de l'essai clinique (par exemple les bio-implants de valves cardiaques au Deutsches Herzentrum de Berlin qui offrent l'avantage de pouvoir être implantés dès la petite enfance et de grandir avec le porteur), pourraient voir le jour au cours des quinze prochaines années.
Il est également important de mentionner une application importante et immédiate des cellules souches sur laquelle travaille l'équipe du docteur George Uzan au sein de l'Inserm. En matière de pharmacopée, que ce soit par l'intermédiaire de la constitution de tissus en laboratoires ou sur les cellules souches elles-mêmes, il est désormais possible d'effectuer des essais de médicaments sans avoir recours à des modèles vivants. Les résultats sont donc plus fiables, car effectués sur des cellules humaines, et plus conformes aux principes éthiques.
On l'a vu, les thérapies fondées sur l'utilisation du sang de cordon existent depuis au moins vingt ans et vont vraisemblablement se multiplier au cours des prochaines années, bien au-delà des maladies du sang. Si la richesse cellulaire du sang de cordon est un élément déterminant de son succès thérapeutique, sa disponibilité n'est pas moins importante : cela engage l'action de l'Etat.
2. L'implication nécessaire de l'Etat
Le rôle de l'Etat est essentiel en matière de développement des thérapies utilisant le sang de cordon. Il doit ainsi avoir un rôle d'impulsion, garant d'une politique de santé publique vigilante et tournée vers l'avenir ainsi que de la place de la France dans un contexte de concurrence scientifique devenue mondiale. Il doit également garantir la pleine information des citoyens afin de les prévenir contre toute illusion dangereuse.
a) Une impulsion nécessaire dans un contexte de concurrence scientifique exacerbée
Le développement de la recherche sur le sang de cordon et des thérapies cellulaires est lié depuis l'origine aux politiques étatiques. C'est la nécessité de se préparer à une éventuelle guerre nucléaire qui a favorisé le financement public des recherches sur le sang de cordon dans les années soixante aux Etats-Unis, car il constitue une ressource facilement collectable et mobilisable pour soigner les irradiés dont les tissus doivent être régénérés.
Mais l'action de l'Etat ne se cantonne pas, fort heureusement, à l'anticipation des conflits. Elle doit aussi construire l'avenir en ayant à coeur le souci de préserver la vie des malades et la place de la France au premier rang des sciences de la vie. Il est frappant de constater comment les pays d'Asie se sont saisis de la question des cellules souches somatiques pour allouer les moyens nécessaires à leur utilisation. Au Japon, en Corée et en Chine, des instituts spécifiques dotés de moyens importants ont été créés pour prolonger les découvertes des scientifiques nationaux. Le nombre de centres de recherches sur les cellules souches d'importance mondiale recensés par l'université du Minnesota en 2004 fait apparaître cette tendance ainsi que la prédominance des Etats-Unis en la matière.
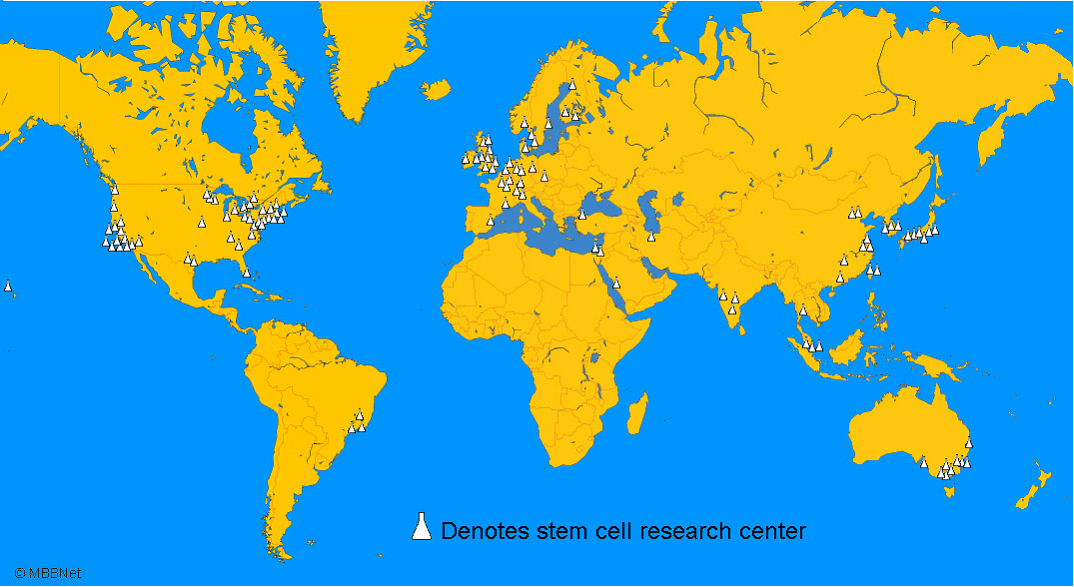
Principaux centres de recherche sur les cellules souches
Source :http://www.mbbnet.umn.edu/scmap/scresearchmap.html
A la suite de l'annonce, en 2007, des résultats obtenus par le professeur Yamanaka en matière de reprogrammation des cellules souches adultes pour leur redonner les capacités de pluripotence que l'on trouve d'ordinaire dans les cellules souches embryonnaires, le gouvernement japonais a annoncé un programme de financement de 10 milliards de yens (plus de 65 millions d'euros) sur cinq ans et la création d'un grand centre de recherche à l'université de Kyoto 19 ( * ) . Aux Etats-Unis, un appel à projet spécifique a été lancé en décembre 2007 par le National Institute of Health (NIH) pour des projets utilisant les cellules souches reprogrammées 20 ( * ) . Au cours de l'année 2007, le NIH a financé des projets relatifs aux cellules souches somatiques pour plus de 200 millions de dollars 21 ( * ) . En Allemagne, le ministère de la recherche a annoncé un doublement des fonds alloués à la recherche sur la reprogrammation des cellules souches qui passe de 5 à 10 millions d'euros par an 22 ( * ) . En France, aucune mesure de ce type n'a été prise. Sur la période 2005-2007, l'agence nationale de la recherche a financé quatorze projets relatifs aux cellules souches somatiques pour un montant total de 7,467 millions d'euros. Par ailleurs, les informations communiquées à votre rapporteur par le ministère de la recherche indiquent qu'environ trente-six laboratoires français travaillent actuellement sur la question des cellules souches somatiques avec un budget global de 3,671 millions d'euros par an.
Le retard de notre pays est actuellement important et une impulsion politique forte est donc nécessaire pour maintenir la France parmi les acteurs majeurs de la recherche sur les cellules souches somatiques.
b) Le devoir d'information
L'immense potentiel thérapeutique offert par les cellules souches extraites du sang de cordon doit par ailleurs faire l'objet d'une information complète et transparente pour la population. Ce devoir d'information incombe à l'Etat. En effet, il paraîtra rapidement intolérable aux familles que le cordon ombilical soit traité comme un simple déchet opératoire dès lors qu'elles sauront qu'il pourrait permettre de traiter les maladies déclarées et futures de leurs proches. Or, une information parcellaire sur l'état de la recherche médicale, des thérapies existantes et des protocoles de collecte est de nature à entraîner des dérives liées à l'insatisfaction et ouvrant la voie à une exploitation de l'ignorance et des attentes déçues.
Laisser entendre que le sang de cordon peut un jour sauver l'enfant ou un membre de sa famille, sans autre forme d'explication, ne peut que susciter la demande pressante des familles qui, comment ne pas le comprendre, souhaitent garantir la santé et la survie des leurs. Si elles ne disposent pas, sur le territoire national, de la possibilité de faire prélever et stocker le sang du cordon ombilical dans des conditions acceptables pour elles, il est plus que probable que l'on assistera au développement d'exportations frauduleuses ou à un recours plus fréquent à l'accouchement à l'étranger dans les pays limitrophes ayant une politique de collecte plus développée. Les auditions menées par votre rapporteur ont révélé l'amorce de ce phénomène qui repose sur quelques praticiens complaisants ou intéressés et sur des entreprises étrangères peu scrupuleuses, n'hésitant pas à faire illégalement de la publicité en France et spécialement dans les zones frontalières. L'ignorance dans laquelle se trouvent les familles sur le danger de telles pratiques est doublement dommageable. D'une part, le risque de pure et simple escroquerie est important puisque la collecte de sang ne se fait pas selon un protocole validé et que l'exportation ne peut pas s'effectuer dans des conditions permettant la bonne conservation des cellules. Dans bien des cas donc, les frais demandés par les collecteurs, qui peuvent s'élever jusqu'à 3 500 euros, ne correspondent à aucun service rendu puisque le prélèvement sera inexploitable. Seules les familles les mieux informées et les plus fortunées peuvent se permettre de contourner en toute sécurité l'absence d'une politique française de conservation du sang de cordon, par un accouchement à l'étranger ou par une exportation illégale organisée avec le plus grand soin. A l'inégalité entre familles liée à la connaissance ou non de la possibilité médicale du prélèvement vient s'en ajouter une nouvelle, liée au niveau de revenus, qui paraît plus choquante encore dans le cadre d'une politique de santé publique.
Une information exacte sur les connaissances scientifiques et thérapeutiques liées aux cellules souches est également indispensable. A titre d'exemple, une mystérieuse clinique implantée en Allemagne et baptisée « X-Cell Center » a lancé une offre publicitaire à destination de tous ceux qui cherchent des informations sur les cellules souches au moyen d'un des moteurs de recherche sur Internet. Cette clinique prétend utiliser la thérapie cellulaire pour guérir ou améliorer nettement les conditions de vie de patients sans que les traitements pratiqués correspondent à des pratiques reconnues. On peut également noter qu'une autre institution, le « Deutsches Zentrum für Frischzellentherapie Dr. Block GMBH », propose pour sa part des traitements, non seulement à partir de greffes autologues mais également de greffes de cellules de mouton. Ici encore, ne pas informer revient à livrer les plus fragiles, les plus désespérés peut-être aussi, aux mains des apprentis sorciers ou des moins scrupuleux.
La responsabilité potentielle de l'Etat est donc doublement engagée, car son inaction laisse se développer des approximations plus ou moins pernicieuses et pourrait un jour s'analyser comme une perte de chance pour les familles françaises n'ayant pu faire stocker le sang du cordon ombilical si des thérapies autologues ou intrafamiliales venaient à être développées.
L'intérêt thérapeutique des cellules extraites du sang de cordon étant désormais scientifiquement établi et la nécessité d'une politique publique en la matière soulignée, il est nécessaire de s'intéresser aux modalités pratiques de collecte et de conservation du sang de cordon.
II. GARANTIR LE MEILLEUR USAGE DU SANG DE CORDON OMBILICAL
Le sang extrait du cordon ombilical faisant partie du placenta, il est couvert par l'article L. 1245-2 du code de la santé publique introduit par la loi du 6 août 2004 relative à la bioéthique, qui dispose que « les tissus, les cellules et les produits du corps humain, prélevés à l'occasion d'une intervention chirurgicale pratiquée dans l'intérêt de la personne opérée, ainsi que le placenta peuvent être utilisés à des fins thérapeutiques ou scientifiques, sauf opposition exprimée par elle après qu'elle a été informée des finalités de cette utilisation ». En l'absence de collecte, le placenta, et donc le cordon et son sang, sont considérés comme de simples résidus ou déchets opératoires. La perte de ressource thérapeutique est de ce fait très importante, que la collecte soit refusée par les parents ou qu'elle soit impossible. Or ce dernier cas est fréquent : en effet, la collecte ne peut être faite que dans une maternité habilitée, disposant d'un personnel formé et de moyens matériels spécifiques. Dans le cas où la collecte est matériellement possible et où les parents y consentent, de nombreuses règles l'entourent. Dès sa collecte, le sang de cordon change de statut et devient un produit cellulaire à finalité thérapeutique au sens de l'article L. 1243-1 du code de la santé publique. Il n'est donc possible de le collecter que s'il fait l'objet d'un don anonyme gratuit et non dirigé pour la collectivité. Sa conservation est également soumise à autorisation de l'agence française de sécurité sanitaire des produits de santé (Afssaps) après avis de l'agence de la biomédecine, selon les modalités définies à l'article R. 1243-20 et suivants du code. Le prélèvement et la collecte du sang de cordon sont également soumis, en vertu de l'article L. 1211-6 du code, au respect des règles de sécurité sanitaire définies aux R. 1211-11 à R. 1211-23.
Ce cadre légal garantit la qualité des greffons mais doit sans doute être complété à la marge. En effet, le meilleur usage du sang de cordon suppose une mobilisation des moyens financiers et humains au service d'objectifs ambitieux et grâce à une clarification du statut et du rôle des acteurs en ce domaine.
A. MOBILISER LES MOYENS FINANCIERS ET HUMAINS
En termes de nombre d'unités de sang de cordon disponibles par habitant, la France se situe au seizième rang aujourd'hui 23 ( * ) derrière des pays aussi divers que la Corée du Sud, située à la première place, l'Australie, la Belgique, la Finlande, l'Espagne, Israël, les Etats-Unis, Singapour, l'Allemagne, le Japon et la République tchèque notamment. Cette situation entraîne des coûts importants et que le développement d'un réseau de maternités et de banques de sang pourrait éviter.
1. Une dépendance coûteuse aux importations de greffons
Face à un taux de dépendance excessif, il est nécessaire d'augmenter le nombre d'unités de sang de cordon stockées en France en s'appuyant sur les avantages dont dispose notre pays, en particulier la qualité de ses greffons.
a) Des objectifs insuffisants
Les objectifs en matière de nombre d'unités de sang de cordon stockées sont fixés par l'agence de la biomédecine qui a pour mission de contribuer au développement maîtrisé de toutes les thérapies utilisant des éléments du corps humain, dont les cellules. Initialement, ceux-ci étaient de 5 000 unités avant d'être doublés et portés à 10 000 unités en 2010. D'après les informations fournies par l'établissement français du sang, principal opérateur en matière de stockage, il y aurait, au 3 juin 2008, 7 022 greffons stockés en France, ce qui rend vraisemblable la réussite et même le dépassement de l'objectif fixé puisque le flux d'unités stockées est croissant et que plus de 2 800 unités ont été stockées en 2007.
|
Nombre de greffons disponibles en banque pour 10 000 habitants |
||||
|
Nombre d'unités de sang de cordon par habitant (2005) |
||||
|
Pays |
Nb habitants en millions |
Nb d'unités de sang de cordon |
Nb d'unités pour 10 000 habitants |
|
|
1 |
Corée du Sud |
48,2 |
45 000 |
9,3 |
|
2 |
Australie |
19,7 |
11 565 |
5,8 |
|
3 |
Belgique |
10,2 |
4 900 |
4,8 |
|
4 |
Finlande |
5,2 |
2 311 |
4,4 |
|
5 |
Espagne |
40,2 |
16 831 |
4,1 |
|
6 |
Israël |
6,1 |
2 043 |
3,3 |
|
7 |
USA |
290,3 |
87 333 |
3 |
|
8 |
Italie |
58 |
14 082 |
2,4 |
|
9 |
Singapour |
4,1 |
834 |
2,0 |
|
10 |
Pays-Bas |
16,1 |
2 889 |
1,7 |
|
11 |
Allemagne |
82,3 |
13 353 |
1,6 |
|
12 |
Japon |
127,2 |
19 889 |
1,5 |
|
13 |
République tchèque |
10 |
1 451 |
1,4 |
|
14 |
Royaume-Uni |
60 |
5 889 |
0,9 |
|
15 |
Suisse |
7,3 |
686 |
0,9 |
|
16 |
France |
60,2 |
4 794 |
0,7 |
|
17 |
Argentine |
38,7 |
70 |
0,01 |
|
18 |
Pologne |
38,6 |
41 |
0,01 |
|
Source : Netcord, Bone marrow donors worldwide -EFS,
Sang de cordon en France :
|
||||
Cet objectif est néanmoins trop modeste et un consensus semble établi parmi les spécialistes : il est souhaitable, pour répondre aux besoins en matière thérapeutique, d'atteindre un objectif moyen de 50 000 unités. A titre de comparaison, l'Espagne a un stock de 26 200 unités et s'est fixé un objectif de 60 000 unités stockées pour 2015.
|
Plan de développement des banques
allogéniques en France
|
||
|
France |
Espagne |
|
|
Agence de la biomédecine |
Organizacion Nacional de Trasplantes |
|
|
Nombre de greffons allogéniques en 2008 |
Environ 6 100 |
Environ 26 200 |
|
Nombre de greffons par habitant en 2008 |
Environ 0,9 |
Environ 5,7 |
|
Objectif national |
10 000 |
60 000 |
|
Calendrier |
Non défini |
2015 |
|
Stockage annuel |
800 unités |
5 000 unités |
|
Maternités collectrices |
6 |
21 |
|
Nombre de greffons par habitant en 2015 |
Environ 1,6 |
Environ 12 |
|
Source: G. Katz, Chaire ESSEC Innovation
Thérapeutique, d'après le rapport de l'Agence de la
Biomédecine. Données parues dans les Echos le 19 juin 2008,«
Pénurie de sang de cordon :
|
||
Le nombre relativement faible d'unités stockées a une conséquence directe en matière financière : il augmente la probabilité qu'il n'y ait pas de greffon compatible en France pour un malade. Il est alors fait appel à l'importation de greffons référencés sur des registres comme celui du Bone marrow donors worldwide qui en recense plus de douze millions cinq cent mille. Le taux de dépendance de la France était en 2007 de 64 %, ce qui, avec un coût moyen d'importation de 18 000 euros, a entraîné un déficit de 3,6 millions d'euros pris en charge par l'assurance maladie. Etant donné le coût de stockage des unités, soit 2 136 euros, le coût produit par les importations de greffons aurait pu permettre de stocker près de 1 700 unités supplémentaires en France. Certes, rien ne garantit que parmi ces unités supplémentaires se seraient trouvés les greffons dont avaient besoin les malades : l'autosuffisance ne signifie pas l'absence totale de recours à l'importation mais le retard français en matière de stockage ne fait que croître, et son coût avec lui.
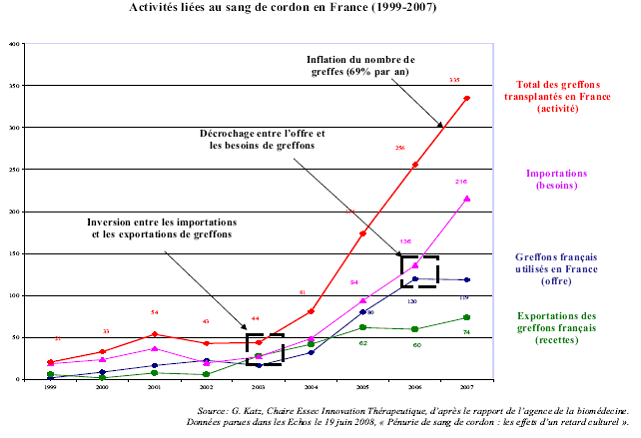
b) Garantir la qualité des unités prélevées
Avec plus de 800 000 naissances par an, la France est particulièrement bien placée pour assurer une collecte d'ampleur. De plus, la qualité des échantillons prélevés en France est particulièrement grande étant donné les critères fixés par les articles R. 1211-11 à R. 1211-23 du code de la santé publique en matière de tests préalables ainsi que ceux fixés par l'agence de la biomédecine en matière de pureté. Dès 1997, les entités collectrices ont fait le choix de retenir une haute qualité pour les unités collectées soumises au contrôle national de qualité 24 ( * ) . De plus, l'inscription sur les fichiers de France greffe de moelle est l'occasion d'une nouvelle sélection qui ne retient environ qu'un quart des greffons collectés (718 sur 2 808 en 2007). Lors de son déplacement à Newcastle, votre rapporteur a ainsi pu constater que les greffons français servaient de référence en matière européenne et qu'ils étaient recherchés. Ceci explique que malgré la faible quantité relative du stock dont elle dispose, la France se situe au troisième rang mondial sur le plan de l'exportation de greffons et au deuxième rang mondial pour le ratio unités cédées/unités stockées. La qualité des greffons collectés en France est donc reconnue et la démarche de qualité mise en place depuis plusieurs années doit être poursuivie. Celle-ci repose sur un protocole précis dont certains points peuvent être améliorés pour une efficacité maximale.
Concrètement, le prélèvement suppose une évolution des pratiques suivies dans les maternités puisqu'il est nécessaire d'extraire la plus grande quantité possible, et au moins soixante-dix millilitres de sang. Notons qu'il va de soi pour tous que la collecte du sang de cordon est accessoire par rapport au bon déroulement de la naissance. A l'heure actuelle, lors de la naissance, le cordon ombilical est clampé en son milieu pour faire bénéficier le bébé du dernier afflux sanguin. Il est désormais prouvé que cet afflux n'est pas nécessaire au bien-être du nouveau-né et il est donc recommandé de clamper au plus près de l'enfant avant de couper le cordon. Ceci permet en effet de collecter une quantité maximale de sang et d'atteindre plus souvent l'objectif minimal de soixante-dix millilitres. Le sang du cordon doit ensuite être récolté et congelé dans les vingt-quatre heures suivant la naissance, sous peine de voir diminuer sa viabilité cellulaire. Le sang prélevé est soumis à une série de tests, notamment le typage HLA (de l'anglais Human Leucocyte Antigens ) c'est-à-dire l'identification des six antigènes les plus importants pour mener à bien les greffes d'organe et la première étape pour déterminer la compatibilité entre le greffon et le receveur potentiel. Le sang est alors congelé et soit stocké en une seule poche, soit en deux parties, l'une contenant 80 % du sang et destinée à la greffe, l'autre 20 % aux fins de recherche et d'expansion cellulaire. La durée de conservation actuellement prévue est de vingt ans. Cette considération pose la question du lieu de stockage, et donc des banques.
Le processus de collecte du sang de cordon est bien établi et garant de la haute qualité des greffons stockés. Il suppose néanmoins une adaptation des pratiques entourant la naissance.
2. La nécessité d'un réseau de maternités
Le premier des acteurs d'une politique publique du sang de cordon essentielle pour atteindre l'objectif de 50 000 unités stockées est la maternité. Un maillage territorial de cliniques doit être organisé afin de donner aux familles une véritable liberté de choix.
a) L'intérêt de la collecte dans différents bassins de population
A l'heure actuelle, seules huit maternités sont habilitées à collecter le sang de cordon. Il s'agit des maternités :
- du centre hospitalier universitaire de Besançon,
- de la polyclinique de Franche-Comté,
- du centre hospitalier de Belfort Hôpital Pellegrin,
- du centre hospitalier universitaire de Bordeaux,
- Bel Air - polyclinique Bordeaux Nord,
- de la clinique Cenon - polyclinique Bordeaux Rive droite,
- de la clinique du CHU de Limoges,
- et du centre hospitalier universitaire Robert Debré à Paris.
Cette possibilité doit en outre être mise en place sous peu à Marseille.
Ces maternités présentent un intérêt considérable pour l'augmentation de la collecte. Leur nombre a plus que doublé depuis l'origine car elles n'étaient que quatre lors du lancement du réseau français de sang placentaire en 1999. Elles restent néanmoins peu nombreuses. Leur activité devrait être complétée par celles des cliniques privées réunies au sein de la Société générale de santé qui a signé en octobre un accord avec l'Etablissement français du sang tendant à la création d'une fondation tournée vers la formation des personnels, le prélèvement, la promotion du don et la recherche sur le sang de cordon. Le sang de cordon pourra donc être prélevé au sein des maternités gérées par cette société dans les conditions imposées par la loi, c'est-à-dire le don volontaire, anonyme, gratuit et non dirigé. Il semble également qu'un programme de recension des maternités susceptibles de constituer un maillage du territoire national est en cours d'élaboration au sein l'agence de la biomédecine, ce qui constitue une avancée utile.
L'augmentation du nombre de maternités permet l'augmentation non seulement du nombre d'unités collectées mais aussi de leur diversité. En effet, la collecte au sein des différents bassins de population permet d'augmenter les chances de conserver l'ensemble des types HLA présents sur le territoire. La France, pays d'immigration, a une forte variété de types. Ceci implique de les conserver pour pouvoir soigner les malades compatibles. Il y a là un enjeu de santé publique ainsi qu'une forme de solidarité internationale. A titre d'exemple, les Français originaires du continent africain, s'ils font un don de sang de cordon, peuvent permettre de soigner des malades dans les pays d'Afrique où aucune collecte n'est organisée.
Au-delà donc des questions liées au nombre, c'est également la diversité des types qui fait la qualité du répertoire national de greffons, ce qui implique que les maternités collectrices soient réparties sur l'ensemble du territoire national. Un plus grand nombre de maternités est également la condition d'une véritable liberté de choix pour les familles.
b) Permettre le choix du don
La limitation du nombre de maternités constitue une limite physique à la possibilité pour les familles de choisir de faire le don du sang du cordon ombilical de leur enfant. Ce choix repose également sur une information complète dont les enjeux ont été signalés précédemment. L'opinion publique semble très favorable à la collecte du sang de cordon et au don. Une étude 25 ( * ) réalisée en avril 2008 par la chaire Essec - Sanofi-Aventis innovation thérapeutique indique que 98 % des femmes souhaitent stocker le sang de cordon de leur enfant plutôt que de le détruire ; 75 % souhaitent spontanément le stocker dans une banque publique, 23 % dans une banque mixte et 2 % dans une banque autologue. En cas d'impossibilité de stocker en France, 59 % des femmes interviewées souhaiteraient que le sang de cordon soit détruit, tandis que 41 % seraient prêtes à exporter le greffon dans une banque à l'étranger (36 % des femmes auraient recours à une banque mixte à l'étranger et 5 % à une banque privée à l'étranger). Seules 18 % des femmes interrogées seraient prêtes à accoucher dans une autre maternité si la leur ne collectait rien. Enfin, 98 % des femmes enceintes réclament une information détaillée de la part du personnel médical concernant l'utilisation thérapeutique du sang de cordon. Ces chiffres sont très encourageants et l'enthousiasme de la population justifie la mise en place d'une politique publique active, notamment en matière d'information. D'autant que, pour l'instant, l'Etablissement français du sang (EFS) constate que, contrairement à ce que les chiffres ci-dessus pourraient faire espérer, sur 4 000 naissances dans une maternité habilitée, seuls 1 200 accords 26 ( * ) pour le don sont obtenus, soit moins du tiers. Cela pourrait être lié au manque d'information sur l'innocuité du procédé pour le nouveau-né et sur l'utilisation thérapeutique qui sera faite du sang de cordon. Ceci renvoie à la question de la formation des personnels et de son financement, qui est parfois assurée par l'EFS dans le cadre des conventions signées avec les maternités et dont nous avons vu qu'elle constitue un des volets de l'action de la fondation créée par la Générale de santé : l'effort de formation des personnels doit être intensifié afin de mieux informer les familles et de permettre le don dans les meilleures conditions techniques.
Une gestion plus performante des moyens liés au sang de cordon passe par une augmentation du nombre des unités stockées, à qualité constante mais en en accroissant la diversité par la multiplication des centres de collecte. Cette organisation matérielle conditionne la liberté de choix des familles qui, malgré des intentions altruistes, trouve peu à s'exercer dans les faits. Une question se pose toutefois : elle est liée à l'intervention de l'EFS, gestionnaire de la majeure partie de la conservation, dans le mécanisme de collecte. Il apparaît nécessaire de clarifier le rôle des acteurs et leur statut.
B. LES ACTEURS
En dehors des maternités, les principaux acteurs de la conservation du sang de cordon sont les banques de sang placentaire. Leur statut est cause de nombreux débats. Mais force est de constater que l'opposition classique entre banques publiques et banques privées est largement un faux problème dès lors que les principes de transparence, d'information et de solidarité sont préservés. Afin de garantir une meilleure efficacité de la collecte, il est également nécessaire de clarifier le rôle des autres acteurs, qu'ils soient opérateurs, régulateurs ou organismes de recherche.
1. La complémentarité possible entre banques publiques et privées.
La France a été, avec raison, prudente face à l'émergence d'acteurs privés en matière de stockage du sang de cordon ombilical. Toutefois, le rejet total des banques privées ne peut être une solution durable : elles sont en effet susceptibles d'apporter un complément utile aux banques publiques.
a) Les banques privées : un pari sur l'avenir qui doit être encadré
Il est important de conserver à l'esprit, quand on aborde le débat sur les banques privées, que, s'il est important que les familles puissent faire le choix de donner le sang du cordon ombilical de leur enfant à la collectivité, prélever l'ensemble des sangs de cordon n'est ni utile, ni possible, ni souhaitable.
Cela n'est pas utile, car nous avons vu qu'avec 50 000 greffons en stock la France approcherait de l'autosuffisance en termes de besoins thérapeutiques. Certes, deux facteurs entraîneront probablement une augmentation des besoins en sang de cordon dans les années à venir : le développement souhaitable des thérapies et le développement d'une solidarité internationale qui devraient entraîner le traitement de patients de pays en développement grâce à des greffons français. Néanmoins, même si l'on prend en compte cette double évolution, les besoins ne seront jamais tels qu'on aurait besoin de conserver tous les cordons.
Cela n'est pas non plus possible, car tous les cordons ombilicaux ne comportent pas les soixante-dix millilitres de sang qui permettent d'espérer en extraire des cellules à des fins thérapeutiques. De plus, beaucoup ne franchissent pas l'ensemble des tests qui sont imposés ; dans certains cas également, il est impossible de déterminer clairement leur identité, ce qui entraîne leur destruction. En moyenne, seuls 27 % des unités de sang collectées peuvent être stockés dans des conditions permettant un usage thérapeutique efficace. Cela rend illusoire l'idée d'un stockage privé destiné à la greffe autologue ou au sein de la famille.
Enfin, il n'est pas souhaitable de collecter le sang de cordon de tous les bébés nés en France car le coût lié au prélèvement systématique du sang de plus de 800 000 cordons chaque année dépasserait de beaucoup les capacités physiques et financières de l'assurance maladie alors qu'un stock permanent d'environ 6 % de ce nombre suffit.
Surtout, conserver le sang du cordon ombilical à titre privé, pour son enfant ou sa famille, dans l'espoir qu'un traitement futur sera développé à partir des cellules qu'il contient et permettra de guérir une éventuelle pathologie, malgré les 73 % de chance que le sang prélevé soit inutilisable, est un pari sur l'avenir qui n'est pas validé par les connaissances actuelles en matière médicale. En matière de thérapie, il est le plus souvent préférable d'avoir recours à un donneur extérieur. En effet, la récurrence des mêmes pathologies (exprimées ou inscrites dans les gènes) à l'intérieur d'une même famille est fréquente : il est donc préférable d'utiliser le sang d'un donneur extérieur à la famille, dont les cellules ne seront pas porteuses des mêmes pathologies que le malade. De fait, les thérapies existantes qui font usage du sang de cordon reposent sur les greffes allogènes, c'est-à-dire extrafamiliales.
Cependant, dès lors que l'Etat ne s'engage pas dans la collecte excessivement coûteuse de l'ensemble des sangs de cordon d'enfants nés en France, il paraît illusoire d'espérer empêcher les familles qui le souhaitent de conserver le sang du cordon ombilical de leur enfant : le respect de la liberté de choix des familles incite en effet à leur permettre d'accomplir cette démarche. Ceci suppose toutefois la réalisation d'une condition suspensive. Il faut que leur information sur les possibilités offertes par le stockage payant soit complète - car le stockage public prend la forme d'un don qui suppose que la prise en charge soit faite par l'Etat, au contraire du stockage privé qui resterait à la charge des familles. Or, les banques privées, très nombreuses (près des trois quarts des banques de sang placentaire au monde sont privées, et la France est le seul pays européen à ne pas autoriser leur implantation) font souvent des promesses irréalistes ; les obligations de rentabilité commerciale qui s'imposent à ces entreprises pourraient d'ailleurs entrer en conflit avec les intérêts de l'enfant et de sa famille. Ces risques sont au coeur de l'avis n° 74 donné par le comité consultatif national d'éthique en 2002. Insistant sur le fait que la conservation à des fins autologues (pour soi-même ou sa famille) risquait de porter atteinte au principe de solidarité qui fonde l'approche française en matière d'utilisation thérapeutique des organes et des produits du corps humain, l'avis concluait sur le refus d'autoriser le développement des banques privées en France et sur la nécessité d'augmenter le financement des banques publiques. Cet avis est également celui de l'office parlementaire d'évaluation des choix scientifiques et technologiques 27 ( * ) . L'avis n° 19 du groupe européen de bioéthique, en date du 16 avril 2004, reprend ces préoccupations mais considère qu'une interdiction stricte des banques privées représenterait une restriction trop importante de la liberté d'entreprendre et priverait les parents de leur liberté de choix.
A condition de respecter les obligations liées à la solidarité et à la transparence de l'information sur les bénéfices à attendre du stockage, il semble effectivement que les banques privées, qui prennent en charge à titre onéreux le stockage des greffons à visée intrafamiliale, peuvent être un complément utile aux banques publiques.
b) La participation des banques privées au financement du stockage et de la recherche
Les banques publiques sont susceptibles de répondre à la quasi-intégralité des besoins de stockage de la France depuis l'appel d'offres lancé par l'agence de la biomédecine (ABM), clos le 15 octobre 2007 et ayant abouti à l'ouverture de quatre nouvelles banques dont deux implantées dans des centres hospitaliers universitaires (CHU), ceux de Poitiers et Montpellier, et deux sites gérés par l'EFS, l'un à Grenoble et l'autre au sein de l'hôpital Henri Mondor à Créteil. Le financement de 900 000 euros sur trois ans par l'agence de la biomédecine, dont 150 000 euros d'aide à l'investissement la première année et le paiement de la moitié des unités conservées dans la limite de 250 unités par an sur trois ans, devrait éviter une renouvellement du cas de la banque de l'hôpital Saint-Louis contrainte à la clôture en 2002 par manque de financement avant de pouvoir ouvrir à nouveau ses portes en 2008. Avec les banques gérées par l'EFS à Bordeaux et à Besançon, ce sont en tout sept banques 28 ( * ) , ayant chacune une capacité de stockage de 7 000 unités, qui sont actuellement ouvertes, soit la possibilité de stocker 49 000 des 50 000 unités souhaitables 29 ( * ) . Ouvrir de nouvelles banques, à statut privé de surcroît, peut donc paraître inutile.
Pour autant, il ne faut pas minimiser le coût associé à l'ouverture et à la gestion d'une banque pour l'EFS comme pour les CHU. Le coût de l'investissement en matériel spécifique permettant la congélation et la miniaturisation des unités est ainsi d'environ 250 000 euros, frais auxquels s'ajoutent ceux liés aux autres matériels, aux consommables et au personnel. L'EFS estime ainsi le montant de son investissement dans les banques de sang de cordon sur la période 1999-2005 à 9,9 millions d'euros. Il est donc impossible de constituer une banque sans faire appel à des fonds extérieurs à ceux de l'ABM. Cette situation, on l'a vu, est particulièrement contraignante pour les CHU. Ils sont dans l'obligation d'y consacrer des ressources importantes : si celui de Poitiers dispose de la possibilité de se financer sur fonds propres, celui de Montpellier bénéficie d'une dotation de l'agence régionale d'hospitalisation.
Sachant qu'il est presque impossible d'équilibrer financièrement une activité de banque allogénique publique, il paraît utile de faire appel à l'entreprise privée pour venir abonder les frais de stockage. Cette activité privée, autologue, pourrait être exercée par les établissements publics à titre complémentaire. Elle peut surtout être exercée par les banques privées qui garantissent le respect de la solidarité et dont il existe plusieurs modèles, notamment en Espagne, en Italie et au Royaume-Uni.
Le projet de la banque Cryosave, créatrice du modèle de l'autologue solidaire en Italie, est intéressant. Dans ce modèle, le stockage est fait à titre payant dans une perspective autologue mais les greffons, inscrits sur la liste nationale, sont susceptibles d'être mobilisés pour des besoins allogéniques solidaires. La société Cryosave rembourse alors le propriétaire du greffon. Ayant développé le fonctionnement de ce système en Italie, la société Cryosave souhaite s'implanter aujourd'hui en France et négocie actuellement la possibilité de s'installer à Lyon où elle créerait également un grand centre de recherche en matière d'expansion cellulaire et de thérapies innovantes issues des cellules du sang de cordon. Ce projet mérite d'être autorisé à titre expérimental par les autorités compétentes étant donné les contreparties proposées à l'implantation de la banque privée qui s'inscrit dans le respect des principes de solidarité qui guident la politique publique de la France. Ces contreparties ne sont d'ailleurs que l'expression des intérêts communs entre la collectivité et l'entreprise privée qui a intérêt à ce que l'expansion lui permette de répondre à une éventuelle demande solidaire sans se départir du greffon de ses clients et à voir se développer des thérapies nouvelles qui pousseront des familles plus nombreuses à s'engager dans la voie de l'autologue.
Ouvrir la possibilité d'une conservation privée impose néanmoins de clarifier préalablement le statut des acteurs.
2. Le statut des acteurs
Deux points méritent d'être approfondis : les relations entre opérateurs et régulateurs d'une part, et le statut des intervenants en matière de recherche, d'autre part.
a) La séparation entre opérateurs et régulateurs
Le retard français en matière de stockage du sang de cordon est davantage imputable à un manque d'ambition politique qu'à un défaut dans la répartition des responsabilités. Plutôt que de tenter une modification dont les effets pourraient se révéler contreproductifs, il convient de préserver l'équilibre actuel, peut-être en le clarifiant. Celui-ci repose sur le rôle d'impulsion et de régulation confié à l'ABM. Cette institution, qui anime déjà le réseau français de sang placentaire, devrait se voir conforter dans son activité de régulation par le développement de ses capacités de contrôle sur la qualité des prélèvements et du stockage. La pluralité des opérateurs du stockage, EFS et CHU, est également un gage de diversité et donc de possibilité de faire émerger des pratiques innovantes dans un secteur en constante évolution technique et managériale. Il ne peut donc être question de confier à l'EFS un monopole du stockage du sang de cordon, qu'il ne réclame d'ailleurs pas malgré sa position prédominante du fait de son expérience en matière de gestion des produits sanguins et des moyens dont il dispose. Dans un domaine qui prolonge le stockage, il paraît toutefois impératif de conforter l'activité de recherche de l'EFS et la possibilité de développements thérapeutiques à partir de la recherche fondamentale qui y est menée en garantissant ses liens avec une entreprise susceptible de les développer sans encourir le risque que son activité soit jugée comme découlant d'une aide d'Etat contraire au droit de la concurrence européen. Il existe néanmoins une solution susceptible de permettre le développement de médicaments à partir des recherches menées au sein de l'EFS tout en restant dans la sphère publique et avec un haut degré d'exigence éthique. En effet, l'ordonnance du 28 juillet 2005 transformant le groupement d'intérêt public dénommé « Laboratoire français du fractionnement et des biotechnologies » (LFB) en société anonyme, a crée une société de droit privé mais à capitaux majoritairement publics liée à l'exploitation des produits associés au sang. Un partenariat entre ce qui est désormais le groupe LFB et l'EFS paraît donc indiqué. Il est pour cela nécessaire de faire évoluer le cadre légale qui, pour des raisons historiques, empêche la mise en place d'une telle relation de complémentarité.
Il convient donc de conforter la répartition actuelle des rôles entre les différents acteurs afin de marquer la distinction entre régulation, stockage et développement des thérapies. Un effort plus important doit être fourni pour permettre de clarifier le statut des organisations en charge de l'accréditation des banques et du suivi de la recherche.
b) Accréditation et recherche
Des initiatives privées ont tenté de mettre de l'ordre dans le maquis des banques de sang de cordon développées selon des principes éthiques, des modèles économiques et des modalités pratiques pour le moins variables. Deux associations ont en particulier mené une action reconnue mais pour laquelle leur statut est de plus en plus inadapté : Netcord en matière d'accréditation et Eurocord en matière de recherche.
Netcord, fondation privée de droit hollandais, a développé un ensemble de critères de qualité du stockage du sang de cordon qui s'impose actuellement à 336 banques dans le monde et qui devient rapidement une référence internationale (cf. carte) 30 ( * ) . Le mécanisme d'accréditation, qui coûte 20 000 euros, et le contenu des normes émises sont toutefois source de nombreuses questions de la part des opérateurs. Faire une place en droit national ou plus vraisemblablement en droit européen à cette structure serait de nature à garantir sa transparence et à conforter son action.
Distribution mondiale des centres de transplantation
Netcord VO - septembre 2008

De même, l'association Eurocord, créée en 1995 par le professeur Eliane Gluckman, assure le suivi de l'ensemble des greffes de sang de cordon au niveau mondial et valide les données cliniques qui sont récoltées à cette occasion 31 ( * ) . Ce travail, d'un intérêt capital pour les progrès de la recherche, a longtemps été financé par l'Union européenne mais ne peut durablement exister sous la forme d'une simple association dépendant de la bonne volonté de quelques chercheurs et du temps qu'ils peuvent y accorder. L'octroi d'un statut public, éventuellement par rattachement à une structure française existante, paraît la solution la plus adaptée pour assurer la pérennité de cette action pour la science et la médecine.
PRÉCONISATIONS
1. Porter le plus rapidement possible et au plus tard d'ici 2020 le nombre d'unités de sang de cordon stockées en France à 50 000 ;
2. Assurer un maillage territorial de maternités habilitées à effectuer le prélèvement qui garantisse la collecte au sein de tous les bassins de population ;
3. Développer la formation des personnels médicaux et les campagnes d'information à destination des parents, de manière à permettre aux familles de faire le choix du don en toute connaissance ;
4. Permettre, à titre expérimental, l'implantation de banques privées respectant les principes de solidarité liés aux greffes de sang de cordon, ainsi que le développement d'une activité privée par les banques publiques afin de consolider leur financement ;
5. Orienter les fonds publics vers la recherche fondamentale en matière de biologie cellulaire et vers les cellules souches somatiques comme le font les autres Etats qui se situent à la pointe de la recherche. Ceci passe notamment par la définition d'un objectif spécifique en la matière par l'agence nationale de la recherche ;
6. Favoriser la recherche sur le cordon lui-même et le placenta ;
7. Renforcer les pouvoirs de contrôle de l'agence de la biomédecine (ABM) sur les pratiques de collecte et de stockage ;
8. Conforter la possibilité pour la recherche faite au sein de l'établissement français du sang (EFS) de se traduire par des thérapies et des médicaments nouveaux en permettant son partenariat avec le Groupe LFB ;
9. Accorder un statut public à Netcord et à Eurocord ;
10. Développer la solidarité de la France avec les pays en développement en matière de greffe de sang de cordon.
TRAVAUX DE LA COMMISSION
Réunie le mardi 4 novembre 2008 , sous la présidence de M. Nicolas About, président , la commission a procédé à l' examen du rapport d'information de Mme Marie-Thérèse Hermange sur le potentiel thérapeutique des cellules souches extraites du sang de cordon ombilical.
Mme Marie-Thérèse Hermange, rapporteur, a fait valoir que la France dispose d'une ressource thérapeutique disponible, abondante et ne posant pas de problème majeur, qu'elle gaspille pourtant en le traitant comme un déchet opératoire : il s'agit du sang placentaire prélevé dans le cordon ombilical.
Certes, les cellules qui en sont extraites ne pourront jamais guérir toutes les maladies, mais leur intérêt thérapeutique justifie que l'on accroisse l'effort de collecte et de recherche en France. Il faut également assurer l'information des familles pour les protéger de certains discours pseudo-scientifiques, parfois relayés par la presse, qui font naître des espoirs illusoires de guérison et cachent souvent des escroqueries.
Après avoir présenté les différents types de cellules souches qui se distinguent par leur capacité à donner une variété plus ou moins grande de cellules spécialisées, elle a indiqué que ces cellules ne se trouvent pas uniquement dans les tissus foetaux et embryonnaires mais également dans le sang de cordon et les tissus adultes. On parle alors de cellules souches somatiques. Des chercheurs parviennent même à faire régresser une cellule unipotente à un stade où elle recouvre des capacités pluripotentes. Ceci implique qu'il est désormais possible de travailler sur des cellules ayant un fort potentiel thérapeutique sans avoir recours aux recherches sur l'embryon. Les cellules extraites du sang de cordon sont, elles aussi, pluripotentes et sont utilisées dans quatre-vingt-cinq indications thérapeutiques qui touchent plus de 126 000 personnes par an en France. En 1988, l'équipe du professeur Eliane Gluckman de l'hôpital Saint-Louis a pratiqué une première greffe de sang de cordon parvenant ainsi à guérir un malade atteint du syndrome de Franconi. Depuis lors, 20 000 personnes souffrant de différentes maladies liées au sang ont pu bénéficier d'une greffe.
Les applications thérapeutiques des cellules extraites du sang de cordon ne se limitent d'ailleurs pas aux seules maladies sanguines : les scientifiques pensent pouvoir les utiliser rapidement pour reconstituer le derme des grands brûlés et envisagent leur utilisation pour traiter le diabète juvénile, certaines pathologies neurologiques ou cardiaques, les maladies du foie et du rein.
Dans un contexte de forte concurrence internationale en matière de recherche sur le sang de cordon, l'implication de l'Etat est essentielle pour que la France puisse se maintenir au plus haut niveau en matière thérapeutique, d'autant qu'elle dispose d'un savoir-faire reconnu en matière de collecte. Or, ses objectifs de stockage sont nettement insuffisants pour faire face à ses besoins et elle ne se situe qu'au seizième rang mondial en termes d'unités stockées par habitant. Alors que des pays comme l'Espagne se sont fixé, d'ici à 2015, des objectifs ambitieux de stockage, la France est encore contrainte d'avoir recours à des importations pour répondre aux besoins de ses malades en matière de greffe, importations dont le coût, pour l'assurance maladie, s'est élevé en 2007 à 3,6 millions d'euros. Pour parvenir à l'autosuffisance, la France a besoin d'un stock de 50 000 cordons.
Une politique de stockage efficace devrait inciter à la collecte de greffons dans les différents bassins de population afin que tous les types génétiques soient représentés et que l'on puisse disposer facilement de greffons compatibles avec les besoins des malades. Elle aurait en outre pour mérite de répondre aux besoins éventuels des pays en développement lorsque le type génétique de leurs habitants se trouve aussi au sein de la population française. La France pourrait ainsi remplir son devoir de solidarité internationale à leur égard en leur fournissant les greffons nécessaires.
Mme Marie-Thérèse Hermange, rapporteur, a ensuite précisé que la collecte du sang de cordon repose sur un réseau de maternités collectrices - huit à l'heure actuelle -, qu'il faudrait renforcer pour parvenir à une couverture de l'ensemble du territoire. Une fois les unités collectées, elles doivent être stockées dans des banques qui nécessitent des investissements initiaux et continus très importants. Afin de faciliter le financement des banques publiques, il serait souhaitable d'accorder à celles-ci la faculté d'exercer également une activité de stockage privé. En outre, certaines banques privées qui respecteraient, comme c'est le cas en Italie, le principe de solidarité qui s'impose en matière de greffe, pourraient également être autorisées à exercer leur activité en France afin de favoriser le développement de la recherche.
Il est important de souligner que le stockage à titre privé représente un faible intérêt thérapeutique pour les familles qui y ont recours : les contraintes de qualité font que seules 27 % des unités prélevées peuvent être stockées. Néanmoins, si certaines familles souhaitent tout de même effectuer un stockage personnel à titre onéreux, pourquoi les en empêcher ? Pareille interdiction prive les banques d'une source de financement et favorise les exportations illégales, souvent faites dans des conditions qui ne permettent pas véritablement la conservation.
Sur le fondement de ces observations, Mme Marie-Thérèse Hermange , rapporteur, a présenté dix préconisations pour mettre en oeuvre une politique véritablement adaptée en faveur de la collecte du sang de cordon en France :
- porter le plus rapidement possible, et au plus tard d'ici 2020, le nombre d'unités de sang de cordon stockées en France à 50 000 ;
- assurer un maillage territorial de maternités habilitées à effectuer le prélèvement qui garantisse la collecte au sein de tous les bassins de population ;
- développer la formation des personnels médicaux et les campagnes d'information à destination des parents, de manière à permettre aux familles de faire le choix du don en toute connaissance ;
- permettre, à titre expérimental, l'implantation de banques privées respectant les principes de solidarité liés aux greffes de sang de cordon, ainsi que le développement d'une activité privée par les banques publiques afin de consolider leur financement ;
- orienter les fonds publics vers la recherche fondamentale en matière de biologie cellulaire et vers les cellules souches somatiques comme le font les autres Etats qui se situent à la pointe de la recherche. Ceci passe notamment par la définition d'un objectif spécifique par l'agence nationale de la recherche ;
- favoriser la recherche sur le cordon lui-même et le placenta ;
- renforcer les pouvoirs de contrôle de l'agence de la biomédecine (ABM) sur les pratiques de collecte et de stockage ;
- conforter la possibilité pour la recherche faite au sein de l'établissement français du sang (EFS) de se traduire par des thérapies et des médicaments nouveaux en permettant son partenariat avec le groupe LFB ;
- accorder un statut public aux organismes qui s'occupent de l'accréditation des banques et du suivi des greffes en matière de recherche : Netcord et Eurocord ;
- développer la solidarité de la France avec les pays en développement en matière de greffe de sang de cordon.
M. Nicolas About, président, a souligné l'importance des recherches sur les cellules souches adultes qui semblent jouer un rôle important dans l'évolution des cancers et de l'apparition des métastases. Des perspectives de recherche intéressantes sont ouvertes par les méthodes d'induction rétrogrades, telle celle pratiquée par le professeur Yamanaka à Kyoto ; il lui semble, en revanche, plus difficile de rendre totipotentes des cellules souches adultes. Il a considéré que le fait d'ouvrir, à des banques privées, la possibilité de pratiquer le modèle de stockage privé solidaire, tel qu'il est mis en oeuvre en Italie, est une bonne idée dès lors qu'on prévoit l'indemnisation des familles qui feront don de leur greffon afin de les rembourser des frais de stockage qu'elles avaient précédemment engagés.
M. Alain Milon s'est étonné du paradoxe selon lequel on traite la quasi-totalité des cordons ombilicaux comme de simples déchets opératoires alors que la France compte plus de 800 000 naissances par an. Si le stockage de 50 000 greffons suffit à répondre aux besoins, pourquoi un tel gaspillage ?
Il a insisté sur la nécessité de continuer les recherches sur l'ensemble des types de cellules souches, y compris les cellules totipotentes. En conséquence, il a demandé que deux modifications soient apportées à cette fin aux préconisations du rapport : dans le cinquième alinéa, indiquer que « des » fonds publics - et non « les » fonds publics - doivent être affectés à la recherche sur les cellules somatiques, pour indiquer clairement que l'on ne vise pas l'intégralité des crédits affectés à la recherche ; dans le sixième alinéa, préciser qu'il faut favoriser « en particulier », et non pas uniquement, la recherche sur le cordon et le placenta pour préserver la recherche sur les cellules totipotentes.
M. François Autain a indiqué qu'il partage les orientations du rapport mais qu'il s'oppose à ce que le secteur privé à but lucratif puisse servir au financement du stockage et de la recherche. Mêler des intérêts privés aux enjeux de santé publique se fait en général au détriment du patient.
M. Nicolas About, président, a précisé que les comparaisons internationales montrent que le stockage privé est un moyen de dynamiser le stockage public et qu'il n'y a donc pas de contradictions entre les deux.
Mme Marie-Thérèse Hermange , rapporteur , a souligné que la France est le seul pays d'Europe à ne pas autoriser l'instauration de banques privées, ce qui crée un risque d'exportation illégale par certaines familles.
M. François Autain a affirmé qu'il n'est pas opposé à ce que les banques publiques aient une activité mixte mais qu'il est hostile à l'implantation des banques purement privées.
Mme Isabelle Debré a insisté sur la nécessité de favoriser, dans tous les domaines, les partenariats public-privé. L'absence de moyens du secteur public a déjà coûté à la France le départ d'un de ses plus grands chercheurs, le professeur Luc Montagnier.
Dans le même sens, M. Alain Milon a fait observer que la grande majorité des lits hospitaliers sont dans le secteur privé non lucratif.
Mme Marie-Thérèse Hermange , rapporteur , a confirmé l'importance de la recherche fondamentale sur les cellules souches, ce qui implique de dégager les fonds publics nécessaires. La France ne s'est, à l'heure actuelle, fermé aucune voie de recherche sur les cellules, y compris embryonnaires, car les financements publics se répartissent à peu près également entre ce type de recherches et les cellules souches somatiques. Il n'y a, par ailleurs, aucune opposition entre le stockage dans des banques publiques ou des banques privées soumises à l'obligation de solidarité, c'est-à-dire à l'obligation d'inscrire les unités stockées sur un registre national qui permet de les utiliser pour un malade qui en aurait besoin quand bien même il ne serait pas membre de la famille qui effectue le stockage. Plus que des questions de statut, c'est l'objectif à atteindre qui importe.
La commission a ensuite modifié les préconisations du rapporteur dans le sens voulu par M. Alain Milon et autorisé la publication du rapport d'information sous le titre suivant : « Le sang de cordon : collecter pour chercher, soigner et guérir ».
LISTES DES PERSONNES AUDITIONNÉES
- Marc Pétry , Cryo-Save
- Eliane Gluckman, professeur, hôpital Saint-Louis, présidente d'Eurocord
- Grégory Katz , professeur, titulaire de la chaire Essec - Sanofi - Adventis d'innovation thérapeutique
- Jacques Hardy , président du conseil d'administration de l'établissement français du sang (EFS)² et Isabelle Desbois , responsable du pôle ingénierie cellulaire banque de tissus
- Jean-Jacques Lataillade , médecin en chef, centre de transfusion sanguine des armées à l'hôpital Percy
- Hélène Esperou , référente cellules souches hématopoïétiques à l'agence de la biomédecine
- Dominique Charron , chef de service immunologie biologie à l'hôpital Saint-Louis
- Thierry de Revel , hématologue des Armées à l'hôpital Percy
- Marc Benbunan , chef de service biothérapies cellulaires et tissulaires à l'hôpital Saint-Louis
- Christian Béchon , président-directeur général des laboratoires français du fractionnement et des biotechnologies, Guillaume Bologna , directeur des affaires publiques, et Rémi Urbain , directeur des partenariats scientifiques
- Patrick Chaussepied , agence nationale de la recherche
- Carine Giovannangeli , directrice du département santé à la direction générale de la recherche et de l'innovation au ministère délégué à la recherche
- Georges Uzan , directeur de recherche au CNRS, Inserm U602, hôpital Paul Brousse
*
- Déplacement à l'université de Newcastle pour rencontrer l'équipe de recherche de Colin Mc Gukin
- Déplacement à la banque de sang placentaire de l'établissement français du sang à Bordeaux
ANNEXES
A. EQUIPES DE RECHERCHE FRANÇAISE TRAVAILLANT SUR LES CELLULES-SOUCHES EXTRAITES DU SANG DE CORDON OU ADULTE
|
Liste des équipes/projets Cellules souches humaines Inserm 2007 |
||||||
|
Cellules souches adultes humaines |
Salaires Inserm (K€ HT) = 877 |
Budget Inserm (K€ HOT) = 1294 |
||||
|
Laboratoire |
Responsable scientifique |
Equipe/projet |
||||
|
U |
583 |
HAMEL |
Christian |
PRIVAT |
Alain |
Physiologie et approches thérapeutiques des pathologies médullaires |
|
U |
592 |
SAHEL |
José-Alain |
GOUREAU |
Olivier |
Etude des mécanismes moléculaires impliqués dans la différenciation des progéniteurs et des cellules souches de la rétine de vertèbre |
|
U |
602 |
BOUCHEIX |
Claude |
LE BOUSSE-KERDILES |
Marie-Caroline |
Différenciation hématopoïétique, mésenchymateuse et vasculaire |
|
U |
608 |
DIGNAT-GEORGE |
Françoise |
DIGNAT-GEORGE |
Françoise |
Physiopathologie de l'endothelium |
|
U |
622 |
HEARD |
Jean-Michel |
HEARD |
Jean-Michel |
Rétrovirus et transfert génétique |
|
U |
632 |
MAUREL |
Patrick |
MAUREL |
Patrick |
Physiopathologie hépatique |
|
U |
638 |
SCHMID-ALLIANA |
Annie |
DESNUELLES |
Claude |
Cellules souches cellulaires et pathologies |
|
U |
645 |
TIBERGHIEN |
Pierre |
TIBERGHIEN |
Pierre |
Interaction hote-greffon et ingenierie cellulaire et génique en transplantation |
|
U |
661 |
JOUBERT |
Dominique |
JAY |
Philippe |
Développement et physiopathologie de l'épithélium intestinal |
|
U |
697 |
MAUVIEL |
Alain |
VERRECCHIA |
Franck |
Signalisation du tgf-beta par la voie des smads : implication physiopathologiques |
|
U |
733 |
LEBOULCH |
Philippe |
BEUZARD |
Yves |
Thérapie génique hématopoïétique |
|
U |
752 |
CHNEIWEISS |
Hervé |
CHNEIWEISS |
Hervé |
Plasticité gliale |
|
U |
765 |
EMMERICH |
Joseph |
GAUSSEM |
Pascale |
Thrombose veineuse et artérielle : facteurs de risque et thérapeutiques innovantes |
|
U |
768 |
FISCHER |
Alain |
CAVAZZANA-CALVO |
Marina |
Thérapeutique des déficits immunitaires |
|
U |
787 |
SASSOON |
David |
MOULY |
Gillian |
Régénération, pathologie et thérapie cellulaire du muscle squelettique humain |
|
U |
790 |
VAINCHENKER |
William |
GODIN |
Isabelle |
Cellules souches hématopoïétiques normales : développement et autorenouvellement |
|
U |
790 |
VAINCHENKER |
William |
LOUACHE |
Fawzia |
Voies de signalisation et autorenouvellement des cellules hématopoïétiques normales et leucémiques |
|
U |
790 |
VAINCHENKER |
William |
GALY |
Anne |
Le système hématopoïétique et immunitaire comme cible de thérapie génique |
|
U |
791 |
WEISS |
Pierre |
LAYROLLE |
Pierre |
Ingenierie tissulaire osseuse |
|
U |
841 |
GUELLAEN |
Georges |
RODRIGUEZ |
Anne-Marie |
Avenir : human mesenchymal stem cells and skeletal muscle : characterization of the connective tissue niche and assessment of mechanisms underlying their therapeutic potential (nuclear fusion and reprogramming) |
|
U |
844 |
JORGENSEN |
Christian |
JORGENSEN |
Christian |
Cellules souches mésenchymateuses, environnement articulaire et immunothérapies de la polyarthrite rhumatoïde |
|
U |
876 |
DE VERNEUIL |
Hubert |
DE VERNEUIL |
Hubert |
Transfert de gènes dans les cellules souches hématopoïétiques et épidermiques |
|
U567/ICG |
4 |
LACOMBE |
Catherine |
DUBART-KUPPERSCHMITT |
Anne |
Equipe 26 : détermination et expansion des cellules hématopoïétiques : approches moléculaires et transfert de gènes |
|
U567/ICG |
4 |
LACOMBE |
Catherine |
FICHELSON |
Serge |
Equipe 27 : expansion et transdifférenciation des cellules souches humaines |
|
U567/ICG |
4 |
LACOMBE |
Catherine |
DUSANTER-FOURT |
Isabelle |
Equipe 28 : thrombopoïétine, cellules souches et plaquettes |
|
U 567/ICG |
4 |
LACOMBE |
Catherine |
PORTEU DE LA MORANDIERE |
Françoise |
Equipe 32 : mécanismes d'activation, cibles et rôles des voies mapk dans les cellules hématopoïétiques |
|
ERI |
5 |
CHARBORD |
Pierre |
DOMENECH |
Jorge |
Microenvironnement de l'hématopoïèse et cellules souches |
|
ERI |
9 |
JUDE |
Brigitte |
JUDE |
Brigitte |
Facteur tissulaire et pathologie cardiovasculaire |
|
ERI |
16 |
BLEICHER |
Françoise |
BLEICHER |
Françoise |
Développement et régénération des tissus dentaires |
Liste des équipes CNRS 2007
|
N° Unité |
Directeur |
% Implication cellules souches |
|
UPR 9040Gif s Yvette |
BAUX Gérard |
10 |
|
UMR 6187 Poitiers |
BECQ Frédéric |
1,25 |
|
URA 2578 Paris Pasteur |
BUCKINGHAM Margaret |
15 |
|
UMR 8104 Paris Cochin |
COURAUD Pierre Olivier |
5 |
|
FRE 2937 Villejuif |
DAUTRY François |
10 |
|
UMR 5166 Paris MNHN |
DEMEINEX Barbara |
5 |
|
UMR 8147 Paris Necker |
DY Michel |
5 |
|
UMR 7622 Paris |
JESSUS Catherine |
10 |
|
UMR 6184 Marseille |
KHRESTCHATISKY Michel |
5 |
|
UMR 7592 Paris IJM |
LEPESANT Jean-Antoine |
4 |
|
UMR 5164 Bordeaux |
MOREAU Jean-François |
18,5 |
|
UMR 6543 Nice |
NOSELLI Stéphane |
5 |
|
UMR 6247 Clermont Fd Ferrand |
VAURY ZWILER Chantal |
7 |
B. PROGRAMME DE RECHERCHE DE L'ÉQUIPE DU MÉDECIN EN CHEF LATAILLADE À L'HÔPITAL MILITAIRE PERCY
SYNTHESE THEMATIQUE DES RECHERCHES
(Hôpital Militaire Percy - Centre de Transfusion Sanguine des Armées)
A. Intérêt des Cellules Souches Mésenchymateuses en Médecine Régénérative
Les Cellules Souches Mésenchymateuses (CSM) ont été initialement identifiées au sein de la moelle osseuse; elles ont également été isolées dans de très nombreux autres tissus (cartilage, thymus, rate, tissu adipeux...) et plus récemment dans le sang placentaire. La dénomination de CSM recouvre à elle seule les principales propriétés de ce type cellulaire d'origine mésodermique: autorenouvellement, capacité proliférative importante et multipotence. Il est en effet possible de les amplifier en nombre de façon très importante dans des conditions de culture standards (expansion in vitro ), et leur capacité à se différencier en divers autres types cellulaires d'origine mésodermique (chondrocytes, ostéoblastes et adipocytes...) mais également endodermique ou ectodermique (concept récent de plasticité cellulaire), a été bien définie pour des milieux de cultures spécifiques.
Les CSM sont caractérisées in vitro comme des cellules adhérentes d'aspect fibroblastique. Leur profil antigénique est bien précisé par l'expression de molécules de membrane telles que le CD105 (SH2), le CD73 (SH3, SH4), le CD90 (Thy1). Ce sont des cellules constitutives du microenvironnement médullaire soutenant fonctionnellement l'hématopoïèse, au-delà de leur rôle proprement structural, par le biais d'une production variée de cytokines et de facteurs de croissance. Ce rôle trophique des CSM existe en réalité au niveau de très nombreux tissus où elles participent au rôle de soutien du microenvironnement spécifique et inductif de chacun d'entre eux.
Des essais cliniques de phase I et II ont démontré l'innocuité de l'administration systémique de CSM amplifiées ex vivo et ont permis d'appréhender le bénéfice potentiel de leur utilisation dans des domaines aussi différents que celui de la médecine réparatrice et des pathologies malignes. Récemment la mise en évidence d'anomalies chromosomiques après culture a ralenti l'enthousiasme porté sur leur utilisation chez l'homme.
La traumatologie de guerre subit les évolutions technologiques des armes qui deviennent à la fois plus précises mais aussi plus délabrantes. Les réparations post-lésionnelles, qu'elles concernent les membres ou bien les organes vitaux (foie, muscles, système nerveux central), peuvent d'ores et déjà pour certaines d'entre elles et dans un avenir proche pour d'autres, bénéficier de nouvelles stratégies thérapeutiques faisant appel à la bio-ingénierie cellulaire et tissulaire. C'est dans ce contexte que nos travaux de recherche ont trouvé pour principales applications cliniques la réparation des pertes de substance osseuse et des brûlures cutanées. Dans ce dernier domaine, l'opportunité récente nous a été donnée de prendre en charge des victimes d'accidents d'irradiation présentant des syndromes cutanés aigus d'irradiation. L'approche de thérapie cellulaire développée pour ces patients pourrait être, dans un second temps, mise à profit pour d'autres types de brûlures. Ces activités de thérapies cellulaires ont pu être mises en oeuvre grâce à des travaux antérieurs qui ont permis de définir des protocoles de production de CSM de grade thérapeutique.
1/ Production de CSM de grade clinique
La réglementation française actuelle dans le domaine de la thérapie cellulaire autorise des procédés de production de cellules qui utilisent de préférence des milieux exempts de quelconque protéine d'origine animale. Dans cet objectif, nous avons mis au point un milieu de culture enrichi en facteurs de croissance humains d'origine plaquettaire. Ces facteurs de croissance sont obtenus à partir d'un lysat de plaquettes humaines qui est particulièrement bien adapté à la culture des cellules fibroblastiques et donc des CSM. En effet, les plaquettes produisent et stockent un grand nombre de facteurs de croissance comme le TGF-â, le bFGF (basic Fibroblast Growth Factor), l'IGF-1 (Insulin-like Growth Factor-1), les PDGF (Platelet-Derived Growth Factors), le VEGF (Vascular Endothelial Growth Factor) pour ne citer que les principaux. Par cryolyse (4 heures minimum à -20°C) d'un nombre standardisé de plaquettes, nous obtenons un sécrétât cellulaire enrichi en facteurs de croissance et en microparticules plaquettaires. L'adition de ce sécrétât dans un milieu de culture à la concentration de 5 à 8% permet de cultiver des CSM et d'obtenir des taux d'expansion cellulaire significativement supérieurs à ceux obtenus avec les conditions standards de culture (10% de Sérum de Veau Foetal (SVF) et 1 ng/mL de bFGF) et d'arriver à la confluence cellulaire en deux semaines au lieu de trois (en primoculture). Ces résultats sont très importants sur un plan thérapeutique si on se place dans une situation où on souhaite, en urgence, obtenir au plus vite un grand nombre de CSM à administrer à un patient.
Récemment, nous avons utilisé ce milieu de culture pour produire des cellules de grade clinique dans le cadre de traitements compassionnels de brûlures cutanées radio-induites. Pour cela le protocole de production de Lysat Plaquettaire a été optimisé pour obtenir un niveau de sécurité sanitaire compatible avec une utilisation injectable.
Un certain nombre de contrôles de qualité sont réalisés en cours et en fin de procédé de production cellulaire. Ils ont, pour certains d'entre eux, un rôle majeur pour la libération finale du produit cellulaire. Parmi ces critères libératoires, citons la stérilité du produit, la viabilité cellulaire et l'absence d'anomalies caryotypiques. En effet il est apparu récemment que les CSM présentaient une certaine instabilité chromosomique et pouvaient acquérir, au cours de la culture, des anomalies caryotypiques. Ces anomalies semblent apparaître de manière totalement aléatoire et semblent dépendantes des conditions de culture. En effet, elles surviennent moins fréquemment quand les cellules sont cultivées dans un milieu de culture enrichi en LP par rapport à des cultures en SVF. Il semble également qu'en fonction de leur origine, les CSM aient une instabilité chromosomique variable : les CSM issues de sang placentaire et de graisse seraient plus stables que celles issues de la moelle osseuse.
2/ Thérapie cellulaire des grandes pertes de substance osseuse
Dans la grande majorité des fractures osseuses, le déficit osseux se répare spontanément. Le processus biologique sous-jacent est considéré comme optimal et l'intervention humaine se limite à stabiliser mécaniquement la lésion. Cependant, dans 5 à 10 % des cas, on observe un retard ou une absence de consolidation. Cette absence de consolidation correspond souvent à la formation d'un mélange de fibrose et de tissus osseux et ne permet pas la restauration de la continuité osseuse. De plus, il existe des indications thérapeutiques spécifiques pour lesquelles il est nécessaire de réséquer des segments osseux de taille importante, par exemple dans certaines pathologies traumatiques de guerre associant délabrement osseux et infection (pieds de mine). La reconstruction d'un os fonctionnel dans ces grandes pertes de substance osseuse reste un problème. La structure simple du tissu osseux, son aptitude naturelle à régénérer et la possibilité d'amplifier aisément des cellules d'origine médullaire ayant un potentiel de différenciation osseuse font du tissu osseux un candidat de choix pour la thérapie cellulaire. Dans le passé, des résultats intéressants ont pu être obtenus par injection extemporanée de moelle osseuse dans les foyers de fracture qui n'ont pas consolidé spontanément. Cependant la moelle osseuse contient peu de progéniteurs ostéoblastiques et le volume de la suspension cellulaire à infuser constitue une limite de cette approche. Compte tenu des insuffisances des techniques actuellement disponibles nous avons évalué une nouvelle approche combinant la thérapie cellulaire à partir de CSM, l'apport de biomatériaux ostéogéniques et de colle biologique d'origine plaquettaire source de protéines adhésives et de biomolécules ostéoinductrices. Il s'agit d'une approche innovante dans la mesure où les thérapies cellulaires rapportées dans la littérature utilisent soit des CSM seules, soit associées à des biomatériaux mais sans colle biologique enrichie en facteurs de croissance.
Ce projet de recherche initié en 2002 se place dans la continuité d'un projet de recherche clinique réalisé en 2000 à l'Hôpital d'Instruction des Armées Percy et qui a montré la faisabilité et l'efficacité clinique de l'autogreffe de cellules mononucléées d'origine médullaire dans les foyers de pseudarthroses (fractures non consolidées mimant une néo-articulation). Nous avons souhaité aller plus loin dans cette approche de thérapie cellulaire autologue, à la fois sur le plan mécanistique in vitro mais également sur le plan physiologique par la mise au point d'un modèle de fracture expérimentale chez l'animal.
L'utilisation de cellules souches à potentiel ostéogénique présentes dans la moelle osseuse en combinaison avec des biomatériaux et de la colle biologique plaquettaire permet une meilleure biodisponibilité in situ des cellules impliquées dans la reconstruction osseuse et un apport local de facteurs de croissance. Il s'agit à notre connaissance du premier travail expérimental avec modèle animal qui évalue la triple association CSM/biomatériau/colle biologique dans la réparation osseuse.
Ce projet regroupant biotechnologies transfusionnelles, cellulaires et substituts osseux couvre à la fois des aspects expérimentaux fondamentaux mais également une application au modèle animal qui est un pré-requis indispensable à une application clinique chez l'homme.
Il s'agit d'un travail collaboratif qui regroupe des compétences multiples au sein du Service de Santé des Armées :
- le Centre de Transfusion Sanguine des Armées pour la préparation des produits dérivés du sang (Plasma Riche en Plaquettes et colle biologique plaquettaire) et pour son savoir-faire en matière d'ingénierie cellulaire de grade thérapeutique,
- l'IMASSA (Institut de Médecine Aérospatiale du Service de Santé des Armées) par son expertise exploratoire en physiologie osseuse in vitro (département de physiologie intégrée) et sa primaterie équipée d'un bloc opératoire.
- le service de Chirurgie Orthopédique de l'Hôpital Percy pour son expérience dans la chirurgie orthopédique de « guerre ».
Enfin, nous venons de mettre en place l'organisation d'un consortium européen centré sur l'utilisation de biomatériaux cellularisés en médecine réparatrice pour répondre à un appel à projet de la Commission Européenne dans le cadre du 7 ième PCRDT (Programme Cadre pour la Recherche Développement et la Technologie). Nous avons réuni 15 laboratoires partenaires européens spécialisés dans le domaine de la réparation osseuse et travaillons sur l'élaboration d'un projet de recherche associant expérimentations pré-cliniques et essais cliniques chez l'homme.
3/ Thérapie cellulaire des brûlures cutanées radio-induites
La fréquence des accidents d'irradiation aiguë à de fortes doses, a augmenté ces dernières années [Georgie (1998), Turquie (1999), Pérou (2000), Panama (2001), Pologne (2001), Georgie (2002), Chili (2005), Sénégal (2007), France (2006-2007), Tunisie (2008)], en raison notamment de la mauvaise utilisation de sources radioactives dans le milieu industriel et médical. Si le phénomène est généralement limité quant au nombre de personnes atteintes, il n'en est pas moins catastrophique sur le plan humain et particulièrement lourd sur le plan de la prise en charge.
La pathogenèse des irradiations aiguës localisées est assez bien décrite dans la littérature mais la réponse médicale faite à ce type de pathologie reste encore une tâche extrêmement complexe et délicate. Le retour d'expérience des cliniciens en charge de la gestion médicale de ces patients (Centre de Traitement des Brûlés de l'HIA Percy) met en avant la nécessité de développer de nouvelles stratégies thérapeutiques. La Thérapie Cellulaire pourrait amener dans ce domaine un progrès significatif.
Une des caractéristiques de la réponse cutanée aux irradiations localisées à forte dose est le développement d'une nécrose tissulaire apparaissant après une phase cliniquement silencieuse et évoluant par poussées successives difficilement prévisibles. Cette nécrose est à relier à un processus inflammatoire local intense et caractérisé par sa récurrence. L'évolution redoutée des lésions de radionécrose, sous tendue par l'expérience rapportées dans la littérature, et par les données très précises de dosimétrie dont on peut disposer aujourd'hui, permet d'envisager la mise en oeuvre d'une nouvelle thérapie combinant les mesures conservatoires symptomatiques déjà mises en oeuvre à une thérapie cellulaire locale par cellules souches mésenchymateuses.
Les CSM trouvent leur place dans cette thérapie non pas du fait de leur propriété de multipotence mais plutôt du fait de leur rôle trophique. En effet, elles produisent certaines cytokines et facteurs de croissance qui auraient un rôle bénéfique dans le contrôle des manifestations inflammatoires locales qui caractérisent la brûlure radiologique. Ainsi le potentiel thérapeutique des CSM a été étudié dans le domaine de la radiopathologie par des équipes du Centre de Recherche du SSA (CRSSA) et de l'Institut de Radioprotection et de Sûreté Nucléaire (IRSN) sur des modèles animaux. Ces deux dernières années, trois patients ont pu bénéficier de cette thérapie cellulaire en association avec un traitement chirurgical d'exérèse et d'autogreffe d'épiderme. Pour chacun d'eux, il s'agissait de brûlures radio-induites sévères et très localisées (mains, bras, fesse) avec un risque important d'évolution vers une chirurgie radicale d'amputation. Les CSM ont été obtenues à partir de prélèvements de moelle osseuse autologue après une expansion in vitro de 15 à 17 jours. Les cultures ont été réalisées en milieu additionné de 8% de Lysat Plaquettaire de grade Clinique (LPC). Les contrôles de qualité réalisés, en particuliers les caryotypes, ont été tous normaux autorisant l'administration des cellules produites. 150 à 180.10 6 de cellules par injection ont été administrées localement au niveau des lésions après exérèse chirurgicale des tissus nécrosés en complément d'une autogreffe d'épiderme. En fonction de la gravité et de la rapidité d'évolution de chaque patient, 2 à 5 administrations ont été réalisées au total. Un effet spectaculaire sur la douleur a été constaté chez tous les patients dès le lendemain des administrations de cellules. Cet effet antalgique était fugace et disparaissait en quelques jours incitant à la réalisation d'injections supplémentaires. Un effet sur la rapidité et la qualité de la prise de greffe épidermique est également apparu significatif aux chirurgiens. Aucune récidive de nécrose n'est survenue chez ces patients après un recul de deux ans et demi pour le premier d'entre eux. Nous pensons que les CSM ont participé au contrôle local de l'inflammation, permettant une meilleure prise de greffe et une meilleure cicatrisation globale des lésions.
Un projet de recherche multicentrique visant à démontrer chez l'animal le mécanisme d'action des CSM dans la réparation de ces lésions radio-induites est planifié pour 2009.
B. Projets en perspective
La perspective de nouveaux projets mérite d'être soulignée, soit parce qu'il s'agit de projets faisant suite à des projets en cours, soit parce qu'il s'agit de thématiques nouvelles nées sous l'impulsion de l'actualité bibliographique ou de nouvelles hypothèses scientifiques.
1/ Projet de Recherche et Développement dans le domaine de la thérapie cellulaire des grands brûlés
Les risques d'exposition à des chimiques et à des radioéléments, ainsi que le risque terroriste, doivent être considérés aussi bien à un niveau civil que militaire. Les brûlures cutanées sévères qui peuvent en résulter nécessitent une prise en charge spécialisée qui peut être assurée à l'HIA Percy. Cependant, une limitation est que la structure n'est à ce jour pas autonome pour générer les greffons de peau qui peuvent être nécessaires. Ceux-ci sont actuellement produits aux Etats-Unis (Epicel ® , Genzyme Tissue Repair), à partir de biopsies prélevées chez le brûlé au niveau de zones saines. Les kératinocytes sont alors extraits, puis amplifiés en culture, selon la technique de Green, de manière à générer une surface de greffons suffisante pour permettre la couverture cutanée nécessaire. L'important coût inhérent à cette logistique représente à ce jour, un facteur limitant la mise en oeuvre de ces traitements. Par ailleurs, il faut préciser que cette technique est difficile d'emploi car les épithéliums produits sont fragiles et particulièrement sensibles à tous les traumatismes mécaniques ou infectieux. Les résultats obtenus sont spectaculaires en terme de survie mais restent frustrants par la qualité des cicatrices obtenues. Bien qu'il existe en Europe quelques tentatives de production d'épiderme cultivé, aucune ne semble, à ce jour, être capable de fournir des greffons d'aussi bonne qualité que ceux produits par Genzyme. On peut affirmer aujourd'hui que la clé d'une bonne prise de greffe repose sur la qualité de la culture et en particulier sa richesse en kératinocytes souches.
La Société l'Oréal produit des peaux équivalentes qui sont utilisées pour tester leurs produits cosmétiques avant leur mise sur le marché. Afin de faire bénéficier les grands brûlés de leurs avancées technologiques, l'Oréal et le Service de Santé des Armées se sont rapprochés sous la forme d'une coopération scientifique et technique qui permettra de mettre en place des essais cliniques de greffe de kératinocytes cultivés au sein d'un laboratoire de culture spécialisé. Ainsi est né le projet d'élaboration d'une « Unité de Thérapie Cellulaire Cutanée » (UT2C) localisée dans l'îlot Percy à Clamart.
Une collaboration scientifique avec le Laboratoire de Génomique et de Radiobiologie de la Kératinopoïèse (LGRK) du CEA a également été initiée et nous permettra d'acquérir des connaissances et un savoir faire de pointe dans le domaine de la kératinopoïèse.
2/ CSM de sang placentaire
Disposer d'une quantité importante de CSM en urgence serait d'un grand intérêt à la fois dans des situations cliniques où les CSM pourraient être administrées dès l'admission du patient (exemple de la victime d'un accident d'irradiation aigue) ou bien pourraient servir de stroma nourricier à la mise en culture de kératinocytes chez un grand brûlé sans attendre l'obtention de CSM autologues. La mise en place croissante de banques de sang placentaire pourrait répondre à cette attente. Les CSM issues de sang placentaire ont les mêmes caractéristiques que celles issues de tissus adultes (moelle, tissus adipeux) mais seraient plus immatures sur le plan immunologique. L'isolement des CSM de sang placentaire n'est pas aussi simple que celui de cellules issues de moelle osseuse ; Cela serait en partie du au fait de leur statut circulant. Dans le cadre d'un projet financé par l'Agence Nationale de la Recherche (ANR) en collaboration avec l'unité INSERM 602 dirigée par le Dr Georges UZAN, le Laboratoire de thérapie cellulaire de l'hôpital Saint Louis et une industrie spécialisée dans les dispositifs médicaux, nous travaillons sur la mise au point d'un protocole d'isolement des CSM de sang placentaire en vue de leur expansion en culture à visée thérapeutique. Les cellules ainsi produites seront caractérisées sur le plan fonctionnel en particulier vis-à-vis de leur utilisation dans les applications cliniques qui nous intéressent à savoir la réparation cutanée des brûlures, la réparation osseuse et le support nourricier des kératinocytes.
Médecin en Chef LATAILLADE
C. LA CONSERVATION DU SANG PLACENTAIRE - ETUDE DE LÉGISLATION COMPARÉE
(cf http://www.senat.fr/lc/lc187/lc187.html )
* 1 Cf. François Duchesneau, Genèse de la théorie cellulaire, Montréal, Bellarmin ; Paris, Vrin, 1987, et article « cellule » in Dictionnaire de philosophie des sciences, sous la direction de Dominique Lecourt, Presses universitaires de France, Quadrige, 2004.
* 2 « La théorie cellulaire » in La connaissance de la vie, Vrin, 2006 (1965).
* 3 Idem.
* 4 Alain Rey « Les cellules-souches sont-elles bien nommées », M/S : médecine sciences, vol. 19, n os 6-7, p. 645, http://id.erudit.org/iderudit/006815ar
* 5 Article « Biologie et médecine (Perspective) » in Dictionnaire de la pensée médicale, sous la direction de Dominique Lecourt, Puf, 2004.
* 6 Rapport remis en novembre 2000 sur « Les cellules souches adultes et leurs potentialités d'utilisation en recherche et en thérapeutique, comparaison avec les cellules souches embryonnaires » - Rapport établi à la demande de Roger-Gérard Schwartzenberg, ministre de la recherche, par le groupe de travail présidé par François Gros, secrétaire perpétuel de l'académie des sciences - http://www.ladocumentationfrancaise.fr/rapports-publics/014000287/index.shtml.
* 7 Idem.
* 8 Pascal Nouvel, article « Thérapie génique de seconde génération » in Dictionnaire de la pensée médicale, op. cit.
* 9 « Plasticité des cellules souches adultes » (résumé), Hématologie, 2003, vol. 9, n o 2, pp. 105-116.
* 10 Article « Biologie et médecine (Perspective) », op. cit.
* 11 Ccf. http://www.bloomberg.com/apps/news?pid=20601124&sid=audCgl.ZSJ4Q&refer=home
* 12 C'est le sens de l'annonce faite par le professeur Ian Wilmut, « inventeur » de la brebis Dolly, le 18 novembre 2007.
* 13 Agence de la biomédecine, rapport annuel 2007, p. 203.
* 14 Greffe provenant d'un donneur par opposition à une greffe autologue.
* 15 « Umbilical cord banking : economic and therapeutic challenges », International Journal of Healthcare Technology and Management, vol. 8, n° 5, 2007, pp. 464-477.
* 16 Agence de la biomédecine, op. cit. p. 204.
* 17 Gregory Katz, « Pénurie de sang de cordon : les effets d'un retard culturel », Les Echos, supplément L'art d'entreprendre, 19 juin 2008.
* 18 Cf. la communication du médecin en chef à votre rapporteur en annexe.
* 19 http://search.japantimes.co.jp/cgi-bin/ed20080111a1.html
* 20 http://grants.nih.gov/grants/guide/pa-files/PA-08-043.html
* 21 http://www.stemcellforum.org/about_the_iscf/members/us_national_institutes_of_health.cfm
* 22 http://www.dw-world.de/dw/article/0,2144,2972580,00.html
* 23 BMWD, Netcord, 2005.
* 24 Cf. Annales du contrôle national de qualité des analyses de biologie médicale, Affsaps, 2003, http://afssaps.sante.fr/htm/10/cnq/annales/an03c341.pdf
* 25 Gregory Katz op. cit.
* 26 EFS, Sang de cordon en France : 20 ans après la première greffe, quel état des lieux ?, 10 avril 2008, http://www.dondusang.net/content/medias/media111_dMvIqcSefOdZsYO.pdf
* 27 Rapport sur les recherches sur le fonctionnement des cellules humaines, n° 101, Alain Claeys session 2006-2007.
* 28 Une banque de l'EFS à d'Annemasse se charge de la conservation à long terme des greffons dans l'azote liquide.
* 29 La banque de l'Institut Paoli-Calmette de Marseille doit également être mentionnée. Elle ouvrira ses portes en 2009 et devrait travailler avec une maternité privée et avec celle de l'hôpital Nord de Marseille.
* 30 https://www.netcord.org/
* 31 http://www.eurocord.org/







