PREMIÈRE PARTIE :
LE RISQUE ÉPIDÉMIQUE EST
OMNIPRÉSENT
« Je pense que ce sujet est excessivement important. J'ai souhaité venir parce que je crois que l'on peut évoquer de nombreux sujets en médecine, croire que tout est réglé, mais le risque épidémique est le plus dangereux, et il est permanent. Nous avons tendance, dans nos sociétés modernes et occidentales, à l'oublier. Nous vivons chaque jour avec ce risque épidémique...Si le risque épidémique est aujourd'hui d'actualité, ce n'est pas tant en raison de la grippe saisonnière, qu'en raison du SRAS et de la pandémie grippale d'origine aviaire. L'épidémie de SRAS, plus que toutes les autres semble-t-il, a montré à quel point la survenue d'une infection inconnue - j'insiste sur le mot « inconnue » -, capable de se diffuser en quelques semaines sur la planète, grâce aux moyens de communication modernes, pouvait répandre la peur, déstabiliser les sociétés et les systèmes de santé les plus évolués. »
Philippe Douste-Blazy
Ministre de la Santé 16
CHAPITRE I : LES FACTEURS D'ACCROISSEMENT DU RISQUE ÉPIDÉMIQUE DANS LES PAYS TEMPÉRÉS
« La définition de base d'une épidémie est simplement l'augmentation significative de la fréquence d'une maladie, au-delà de ce qui est observé habituellement. Cette définition est relative... Les épidémies ne sont pas toutes d'origine infectieuse, cette définition englobe les épidémies comme celle de diabète qui se développe aujourd'hui, d'autres maladies auto-immunes et même l'obésité, dont les sources sont assez mal comprises, connues et contrôlées, possiblement liées aux comportements et à l'environnement. Cela a été dit, la lutte contre les maladies infectieuses, puisqu'il s'agit principalement d'elle, est une lutte qui ne peut avoir de fin... »
Cette définition donnée par le Directeur général de l'Institut Pasteur 17 illustre la difficulté de parler aujourd'hui du risque épidémique dans les pays développés dans la mesure où les média attribuent le terme d' « épidémie » à toute maladie concernant plusieurs personnes, sans référence au caractère infectieux.
Ne pouvant aborder l'ensemble de ces questions, notre étude se limitera au risque infectieux qui, loin de disparaître, suscite aujourd'hui l'inquiétude des responsables de la santé publique.
En effet, plusieurs facteurs conduisent au contraire à un accroissement du risque épidémique. Nous sommes aujourd'hui dans une situation pour le moins paradoxale : le risque épidémique diminue, voire est éradiqué pour certaines maladies, mais l'apparition de nouvelles épidémies est un fait et des maladies connues génèrent de nouvelles problématiques, par exemple la résistance aux antibiotiques.
La distinction entre les pays du nord et les pays de la zone tropicale que nous avons retenue garde sa pertinence car de nombreuses maladies, comme le paludisme, ne se trouvent à l'état endémique que dans les pays du Sud et, il est un fait, le risque épidémique varie considérablement selon la zone géographique, même si le mode de vie moderne et le développement des transports et des migrations peuvent entraîner une certaine dispersion de pathologies d'origine tropicale.
Section 1
Les
sources de l'accroissement du risque épidémique
L'effet des migrations sur les épidémies a été illustré historiquement lors de la conquête de l'Amérique latine par les conquistadors. Les populations indiennes ont été décimées par des virus amenés par le conquérant, par exemple la rougeole et la variole ; ceux-ci se sont révélés être extrêmement virulents sur des organismes qui, du fait de la coupure absolue que représentait l'océan Atlantique, n'avaient jamais été à leur contact. En sens inverse, les conquérants ont ramené en Europe des maladies telles que la syphilis.
Aujourd'hui, la rapidité et l'ampleur des échanges humains font de la lutte contre les maladies infectieuses une problématique mondiale car aucun état ne peut songer à s'abriter derrière ses frontières.
Le risque épidémique est universel. Tous les pays connaissent des épidémies et les pays développés ont leurs propres épidémies internes : par exemple, l'épidémie de « vache folle » est née en Europe, et elle est directement issue d'un mode d'alimentation du bétail 18 .
Nous sommes donc confrontés à des facteurs d'accroissement du risque épidémique endogène et exogène.
1) Les conditions de vie
La très forte chute de la mortalité liée aux épidémies au cours du vingtième siècle résulte d'abord de l'amélioration de l'hygiène qui, pour bon nombre de scientifiques, a eu un impact supérieur au progrès de la médecine. Deux facteurs ont été absolument déterminants au cours du XIXème siècle : l'apport d'eau dans les villes qui a été multiplié par un facteur allant de cinq à vingt en un siècle, ainsi que l'invention de la tinette à évacuation par l'eau.
Paradoxalement, aujourd'hui, les populations ont tendance à abandonner des règles élémentaires d'hygiène tout en exigeant, en particulier dans le domaine de l'alimentation, des produits de plus en plus aseptisés qui peuvent les fragiliser car nos organismes ne sont plus immunisés contre des germes auxquels ils ne sont plus confrontés.
S'il est impératif d'avoir une bonne hygiène, l'excès d'asepsie peut être contre-productif. Ce sujet n'est pas encore parfaitement exploré par les scientifiques. Il convient de se garder de toute conclusion catégorique mais l'une des sources de la recrudescence des allergies pourrait se situer dans le fait que les petits citadins, à la différence des ruraux, ne sont pas assez confrontés aux micro organismes dans leur enfance et ont pour cette raison un système immunitaire moins résistant à l'âge adulte. Les défenses immunitaires ont besoin d'être stimulées pour se renforcer. Dans le cas des enfants des villes, une autre source repérée est l'accroissement de la pollution de l'air.
2) L'âge
La vulnérabilité de la population des pays occidentaux s'accroît également du fait du vieillissement de la population car les défenses immunitaires déclinent avec l'âge.
Certaines maladies infectieuses touchent de ce fait beaucoup plus durement les personnes âgées, il en est ainsi de la légionellose ou de la grippe. Ce fait est déjà intégré dans certains aspects de la législation puisque le fonds national de prévention de la grippe prend en charge la vaccination de 5,2 millions de personnes âgées de plus de soixante cinq ans ou en affection de longue durée.
Nous pouvons estimer que cette action permet de sauver, suivant l'ampleur des épidémies, entre 3000 et 6000 vies chaque année, la grippe étant toutefois à l'origine du décès annuel de 1500 à 1800 personnes ; 8 millions de prises en charge sont envoyées aux personnes âgées de plus de soixante cinq ans et se traduisent par 5,2 millions de personnes vaccinés.
Le coût de l'action conduite par la CNAMTS s'élève entre 12 et 13 millions d'euros chaque année, excluant la prise en charge des consultations. Il est difficile d'évaluer le coût de ces dernières car nous ne constatons pas d'augmentation du nombre des consultations lors de la période de vaccination antigrippale, ce qui conduit à penser que les patients procèdent à la vaccination à l'occasion de visites auxquelles ils se seraient rendus de toute façon. Si, malgré cette réserve, nous intégrons les visites, le coût global de cette action peut être évalué à 140 millions d'euros.
La Caisse nationale d'assurance maladie évalue l'avantage financier qu'elle retire de cette vaccination à 30 millions d'euros par an. Il convient de noter qu'une étude américaine montre un retour financier de 9 par investi pour les personnes âgées de plus de 65 ans, cette vision comptable s'ajoutant, et non se substituant à l'aspect humain.
L'exemple de la grippe illustre la nécessité de prendre en compte le vieillissement de la population dans la mise en oeuvre des politiques de santé. La part grandissante des personnes âgées dans les sociétés occidentales, phénomène heureux car il est la traduction de l'allongement de la durée de vie, implique la présence d'un nombre croissant de personnes plus fragiles devant les maladies infectieuses.
Les 14 800 décès 19 de personnes essentiellement âgées survenus lors de la canicule d'août 2003 ont dramatiquement illustré cette donnée nouvelle et montré qu'elle était encore insuffisamment intégrée dans les politiques publiques
3) L'urbanisation
L'accroissement de la population urbaine constitue historiquement le principal facteur ayant permis la propagation des épidémies . La dernière épidémie de peste connue par la France est arrivée à Marseille, s'est propagée par le non respect des règles de quarantaine et ensuite par les échanges commerciaux.
De ce fait, très tôt, ceux qui le pouvaient, cherchaient à se réfugier à la campagne. Ses contemporains ont, par exemple, beaucoup reproché à Montaigne de ne pas être resté dans la ville de Bordeaux, dont il était le Maire, confrontée à une épidémie. Bien que l'épidémie débutât souvent dans les quartiers portuaires pauvres et insalubres, on réalisa très vite que la mort frappait sans distinction sociale ou sexuelle. Et qu'en conséquence, l'isolement à la campagne était l'unique protection.
Aujourd'hui, ce n'est pas tant l'urbanisation que les conséquences de l'organisation sociale des grandes cités, avec la nécessité de prendre des transports en commun et la promiscuité pouvant en résulter aux heures de pointe, qui sont facteurs de diffusion des épidémies. La surveillance rigoureuse des réseaux de distribution d'eau est également facteur de prévention en permanence.
Machupo
Quand une révolution
pousse l'homme vers les forêts...
Le virus
Machupo
est
apparu en Bolivie en 1952. Une révolution avait alors poussé les
populations vivant dans la plaine du Béni, à l'est du pays,
à proximité de la limite de la forêt amazonienne, où
ils développèrent une agriculture de subsistance. Le rongeur
réservoir du virus
Machupo
(Callomys callosus) est plutôt
antropophile : il pénètre dans les maisons. Une
épidémie a fait 650 malades et 122 morts en 1963-64. Grâce
à une lutte engagée contre ce rongeur, les contaminations
humaines ont ensuite disparu, dès 1974. Mais durant l'été
1994, le virus a frappé à nouveau, au même endroit,
contaminant sept personnes d'une même
famille...
Guanarito
Ou comment attraper un virus en
défrichant une forêt...
Ce virus a été découvert lors d'une épidémie survenue au Venezuela en 1989, qui a touché 104 personnes dont 26 ont décédé. Les 15 premiers cas sont survenus dans une communauté rurale du centre du pays, qui avait entrepris de défricher une zone forestière. Le réservoir du virus est désormais connu : le rongeur Zygodontomis brevicauda . Lorsque les paysans se sont mis à défricher la forêt, ils ont soulevé des poussières infectées par les urines ou les excréments desséchés des rongeurs. La contamination a donc eu lieu par voie respiratoire, un des modes de transmission les plus fréquents de ces virus.
Source Institut Pasteur
4) L'importance des migrations
Ce n'est pas un hasard si aujourd'hui les principaux foyers de tuberculose se situent dans des lieux où il existe une certaine promiscuité. La peste noire, arrivée d'Asie par les routes de la soie maritimes et terrestres, est réputée avoir exterminé la moitié de la population européenne, soit entre 20 et 30 millions de personnes. Ceci nous rappelle que les déplacements humains sont les vecteurs naturels des épidémies et par là de tentations xénophobes.
L'hémorragie humaine causée par la « grande peste » a exacerbé la haine de populations qui accusèrent les juifs et les lépreux de répandre le mal en empoisonnant l'eau des puits. Le pape Clément VI dut alors ouvrir les portes des Etats pontificaux d'Avignon et du Comtat Venaissin à tous ces persécutés, interdisant rigoureusement les massacres, comme celui qui eut lieu à Strasbourg (alors territoire de l'empire germanique) où 900 juifs furent brûlés vifs.
La propagation des maladies infectieuses par les transports est aujourd'hui une donnée permanente du monde et des méthodes efficaces pour enrayer les épidémies, telles l'autarcie et la quarantaine, sont aujourd'hui difficilement praticables. Or, la peste de 1347 est passée directement de Bordeaux à Londres par le commerce du vin, avec une escale à Rouen, grâce à laquelle elle est remontée via la Seine jusqu'à Paris.
Il serait trompeur de raisonner sur la base d'exemple comme le SRAS où la maladie a été rapidement enrayée car la transmission d'épidémie à travers le monde se réalise également pour des maladies, telle la tuberculose, auxquelles les média accordent peu d'attention.
Les microbes ne connaissent pas les frontières, ils voyagent avec les avions, de façon extrêmement rapide. Ils ne sont d'ailleurs pas les seuls à voyager puisque la résistance aux antibiotiques voyage également à grande vitesse et, lorsqu'un nouvel antibiotique est créé, nous voyons la résistance apparaître en un lieu et se propager en quelques semaines dans d'autres pays de la planète.
« Les circonstances de survenue sont toujours les mêmes, on observe la contamination au départ d'un petit nombre de personnes, généralement à partir d'une même source environnementale... Souvent, ces épidémies sont des foyers qui se révèlent limités dans l'espace et dans le temps.... Le seuil de cas atteint le niveau où une épidémie de grande ampleur risque de se développer, c'est du moins ce que montrent les modèles mathématiques qui sont divers, mais qui montrent tous un effet de seuil en matière de développement des épidémies » 20
Les échanges sont aujourd'hui, à l'évidence, le principal vecteur de diffusion des épidémies et en tous cas de la rapidité de propagation.
5) Le réchauffement climatique
Le réchauffement climatique aura des effets sensibles, bien avant que nous constations de visu l'élévation du niveau des océans, par la remontée vers le nord de maladies tropicales. La remontée vers le nord d'algues marines ou de poissons en constitue déjà un signe indiscutable 21 .
La notion de réchauffement climatique n'implique pas une augmentation considérable de la température ambiante. Par exemple la fièvre catarrhale ovine, propagée par un petit diptère, a beaucoup progressé ces dernières années sur le pourtour méditerranéen. Or, une augmentation de 1° centigrade de la température moyenne permet à ce vecteur d'accroître son aire de répartition de 90 en latitude et de 150 m en altitude ce qui, s'agissant d'un insecte qui se trouve sur le pourtour méditerranéen, est suffisant pour lui permettre d'atteindre la France.
S'agissant des maladies infectieuses « Le réchauffement climatique a un impact de remontée vers le Nord de ces vecteurs et donc sur un certain nombre de maladies, dont des zoonoses, par exemple :
- La fièvre du Nil occidental (West Nile) a envahi tous les États-Unis en quelques mois et nous avons connu quelques épisodes en France et en Europe. C'est un Culicoides qui est responsable de cette transmission, il remonte vers le Nord à la faveur du réchauffement climatique.
- Il est également possible de citer des zoonoses bien plus graves, comme la fièvre de la vallée du Rift qui n'a pas encore touché l'Europe, mais qui le pourrait, au travers de l'arrivée de moustiques (Aedes et Culex) ; là encore il s'agit d'une conséquence du réchauffement climatique avec une remontée vers le Nord de ces moustiques. » 22
L'Agence française de sécurité sanitaire des aliments (AFSSA) a publié, le 11 avril 2005, un rapport particulièrement intéressant sur l'évaluation du risque d'apparition et de développement de maladies animales compte tenu d'un éventuel réchauffement climatique. Ce rapport est riche en informations et, surtout il permet de préciser ce qu'intuitivement nous ressentons.
A l'issue d'un processus de hiérarchisation des risques, les experts de l'Agence ont identifié six maladies à surveiller en priorité compte tenu des éventuelles répercussions sanitaires et économiques de leur développement :
• la fièvre de la vallée du rift ;
• la fièvre de West Nile ;
• la leishmaniose viscérale ;
• les leptospiroses ;
• la fièvre catarrhale ovine ;
• la peste équine.
Principaux impacts du changement climatique sur les
écosystèmes
(d'après Chan et al. 1999)
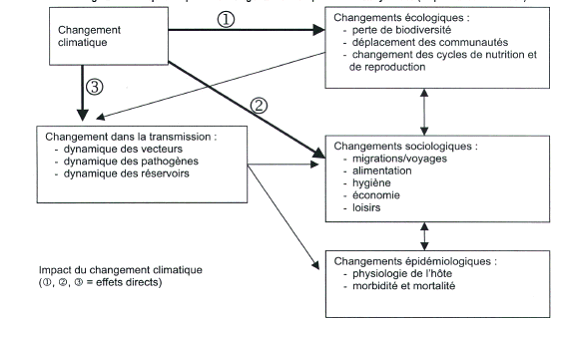
Source : Rapport de l'AFSSA sur l'évaluation du risque d'apparition et de développement de maladies animales compte tenu d'un éventuel réchauffement climatique - 11 avril 2005
L'AFSSA recommande :
• un renforcement de la surveillance de ces maladies sur le territoire, la mise en place de systèmes d'alerte et la définition de plans d'urgence ;
• le développement de la recherche sur la prévention et de traitement de ces maladies et la création de réseaux de compétences à l'échelle européenne pour favoriser les collaborations ;
• la formation et l'information du public et des professionnels de santé.
Les tableaux qui suivent, extraits de ce rapport, nous donnent une idée extrêmement précise des risques encourus.
Probabilité d'évolution épidémiologique des maladies examinées en fonction du changement climatique
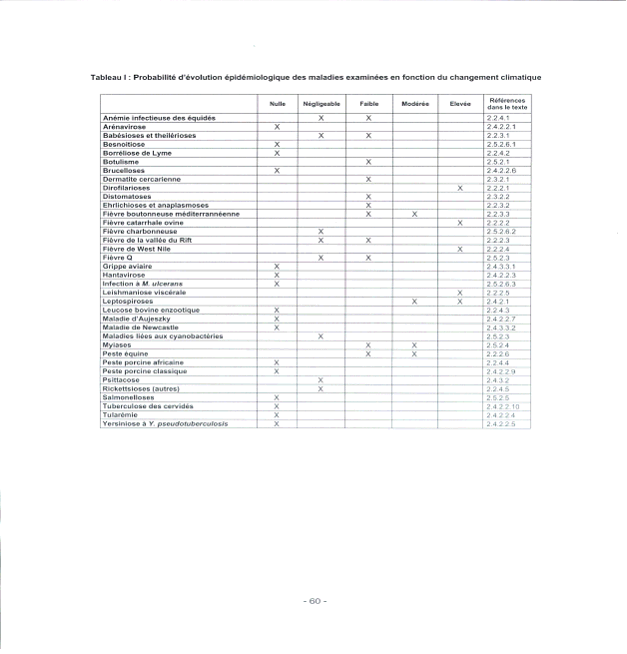
Source : Rapport de l'AFSSA sur l'évaluation du risque d'apparition et de développement de maladies animales compte tenu d'un éventuel réchauffement climatique - 11 avril 2005
Conséquences sanitaires des maladies retenues pour les populations animales (en fonction de la prévalence actuelle et de la gravité clinique moyenne chez l'animal)
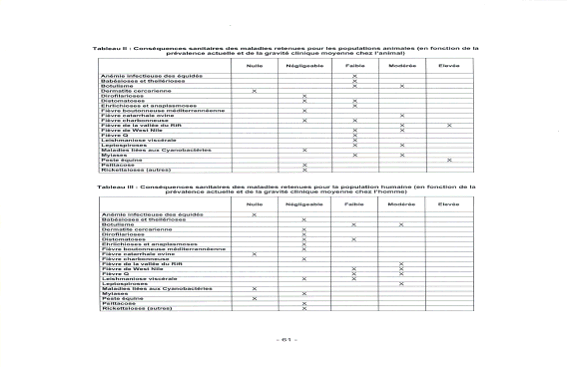
Conséquences sanitaires des maladies retenues pour la population humaine (en fonction de la prévalence actuelle et de la gravité clinique moyenne chez l'homme)
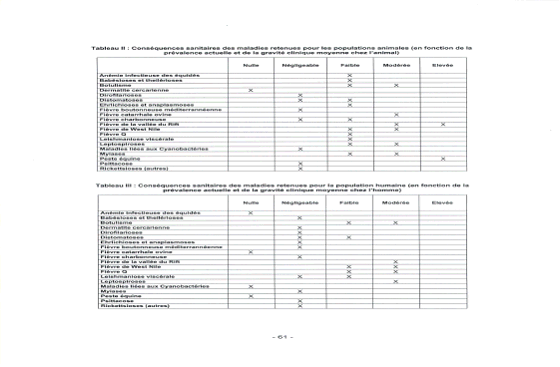
Source : Rapport de l'AFSSA sur l'évaluation du risque d'apparition et de développement de maladies animales compte tenu d'un éventuel réchauffement climatique - 11 avril 2005
Conséquences économiques collectives chez l'animal des maladies retenues examinées dans un contexte de changement climatique en France métropolitaine
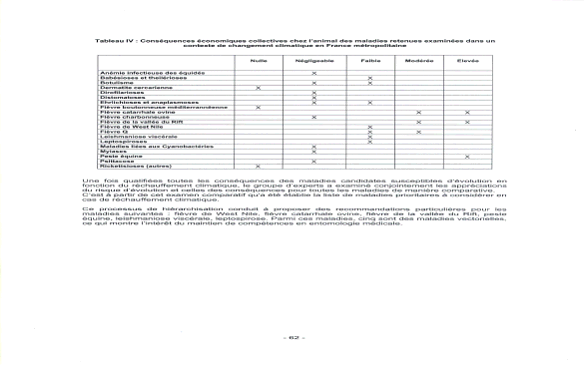
Source : Rapport de l'AFSSA sur l'évaluation du risque d'apparition et de développement de maladies animales compte tenu d'un éventuel réchauffement climatique - 11 avril 2005
6) L'évolution des comportements humains et des modes d'alimentation
Longtemps nous avons cru que l'homme était protégé des virus des animaux par la notion de barrière d'espèce .
Le franchissement de la barrière d'espèce peut-être définie comme une mutation imprévisible d'un virus, modifiant son pouvoir de réplication et ses effets pathogènes chez un hôte différent, en particulier l'homme. Elle est favorisée par la concentration des espèces qui augmentent le risque d'exposition.
Il est maintenant avéré que des modifications dans le cycle de multiplication d'un virus peuvent conduire à des réplications pouvant passer d'une espèce à l'autre, en particulier de l'animal à l'homme. Ces phénomènes sont favorisés par la concentration des animaux ce qui induit une forte augmentation des opportunités d'échanges de matériel génétiques entre virus (recombinaison) et de souches entre espèces (contamination).
Certains virus qui, à l'état naturel, sont incapables d'infecter l'homme lors d'un contact direct avec des animaux infectés ou un environnement souillé peuvent représenter un danger lors de l'utilisation de produits médicamenteux d'origine animale. Par ailleurs de nouvelles maladies infectieuses peuvent émerger suite à l'introduction d'un nouvel agent pathogène ou l'adaptation d'un agent existant ou à une modification dans les pratiques d'élevage.
L'agriculture a bouleversé ses méthodes de production au cours des cinquante dernières années et cela n'est pas sans liens avec le développement de nouvelles maladies infectieuses qui trouvent leur origine chez l'animal
L'élevage extensif, qui semble plus respectueux des animaux, de leur bien-être et de la santé, présente l'inconvénient de faciliter les contacts entre les animaux domestiques et la faune sauvage et, par là, peut devenir un facteur de risque.
La description de l'exemple de la grippe, qui suit, illustre ce phénomène :
Un virus qui vient des oiseaux : L'exemple de la grippe
Où dorment ces virus pendant des années ?
Sans
doute chez les animaux et notamment les porcs et les oiseaux.
Les
oiseaux sont vraisemblablement l'hôte original des virus de la
grippe
: ils servent de réservoirs à tous les sous-types
de virus A.
Les réservoirs animaux jouent un rôle
important dans l'apparition de nouveaux virus chez l'homme
. L'exemple
le plus documenté est l'apparition du virus de Hong Kong en 1968. Ce
nouveau virus s'est rapidement étendu aux pays voisins puis au monde
entier en l'espace d'une année. Les virus humains qui circulaient seuls
depuis 1957 appartenaient au sous-type A (H2N2). Deux gènes dont un
gène majeur ont alors été remplacés par leurs
équivalents de virus aviaires : H3 a remplacé H2.
Les pandémies de grippe prennent souvent naissance en Extrême-Orient où la population très dense vit en contact étroit avec les animaux . L'élevage conjoint du porc et du canard favorise le passage du virus de l'animal à l'homme. Les canards domestiques sont contaminés par des canards sauvages migrateurs. Les porcs respirent de grandes quantités de virus aviaires. Si le porc est également contaminé par un virus humain, un virus hybride peut apparaître. Ensuite, les fermiers sont contaminés par voie respiratoire par le nouveau virus. Après quelques mutations, le virus s'adapte à l'homme et commence à se répandre dans la population.
Les virus grippaux des oiseaux constituent un gisement de gènes viraux. On pensait jusqu'à récemment que ces virus n'infectaient pas l'homme mais pouvaient infecter le porc, que des virus humains peuvent aussi contaminer. Le porc semblait être l'intermédiaire obligatoire entre l'oiseau et l'homme. L'épisode de "la grippe du poulet" survenu à Hong-Kong en 1997 a cependant montré que des virus aviaires pouvaient directement provoquer des cas humains de grippe, parfois sévères : 18 personnes furent touchées dont 6 décédèrent. Le même virus aviaire (H5N1) infecta en 2003 deux autres personnes dont une mourut, toujours à Hong Kong. Deux cas en 1999 et un en décembre 2003 ont encore été recensés dans cette ville, mais dûs à un autre virus aviaire A(H9N2). Un troisième virus aviaire A(H7N7) a provoqué la mort d'un vétérinaire et touché 83 personnes aux Pays-Bas en avril 2003.
(source : Institut Pasteur)
Le risque d'épizooties animales est très important et des alertes ont lieu régulièrement comme cela est illustré dans le tableau ci-dessous 23 .
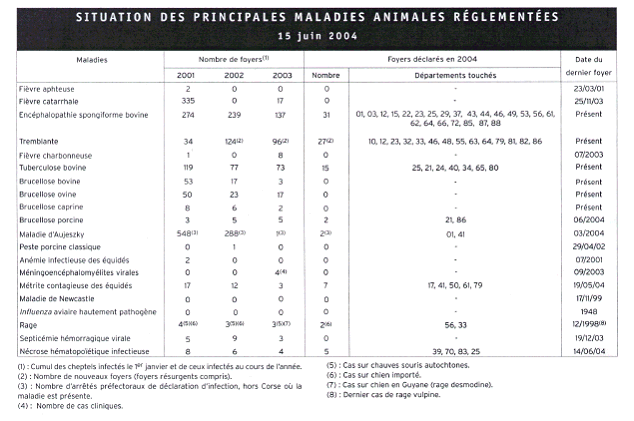
En Europe, les élevages industriels concentrent le risque à cause de la promiscuité et de l'homogénéité des espèces. Ceci les oblige à une très haute biosécurité acquise au prix d'une hygiène quasi-clinique, de vaccinations et d'antibiotiques, aux dépens de la vie extérieure du cheptel et de son caractère de viande « naturelle ».
Inversement, le retour accru à des exploitations en plein air, à partir d'espèces issues des élevages, permet un contact étroit avec la faune sauvage, notamment les oiseaux migrateurs, qui favorise certaines épizooties.
Des recherches intensives dans ce domaine seront nécessaires pour trouver un équilibre satisfaisant entre l'élevage extensif qu'intuitivement nous appelons de nos voeux et la sécurité sanitaire offerte par des élevages fermés.
Toutefois les conditions diffèrent entre le reste du monde et l'Asie du Sud-Est où l'augmentation rapide de la densité des petits élevages liée à la proximité sur un même territoire d'élevages de porcs et de poulets, crée un environnement favorable à la grippe aviaire.
Ce mouvement se constate notamment en Asie du Sud-Est où se sont développés le SRAS, l'influenza aviaire et, peut-être, en Afrique avec l'Ebola, liée à des nouveaux commerces, à des nouveaux marchés où l'on trouve un grand nombre d'animaux, des espèces différentes sur le même lieu et, bien entendu, une forte concentration humaine.
Si l'influenza aviaire découle de conditions commerciales tout à fait particulières, le SRAS provient d'une région de Chine où l'on consomme une variété de civette palmée dont nous ne sommes pas encore certains qu'ils sont à l'origine du virus.
Le cas du virus de l'Ebola (et probablement de la fièvre de Marburg) est également très intéressant : à l'instar d'autres virus elle peut avoir des sources simiesques telles que les rétrovirus ou la déforestation. Les contacts de la population humaine et des chasseurs avec le dépeçage des grands singes peuvent amener une sortie de ces virus par un contact étroit avec la population animale.
Un autre facteur réside dans l'évolution des procédés technologiques de l'industrie agro-alimentaire, par exemple l'origine des encéphalites spongiformes bovines (ESB) viendrait de la modification des procédés technologiques de traitement des farines animales.
Il est important de relever qu'il n'y a plus aujourd'hui que 300 vétérinaires spécialisés dans les productions alimentaires en France sur 14 000 et que ce phénomène, allié à la désertification rurale qui rend plus difficile le suivi des cheptels par les vétérinaires, est extrêmement inquiétant.
Le dernier facteur particulièrement important réside dans les mouvements illégaux ou incontrôlés d'animaux et de produits d'origine animale.
1. Le trafic d'espèces protégées et l'insuffisance patente des contrôles vétérinaires pour les animaleries peuvent être à l'origine d'importations de maladies tropicales.
2. Les fêtes religieuses imposant le sacrifice d'animaux peuvent, lorsque l'abattage se fait en dehors de tout contrôle sanitaire, conduire à des TIAC (toxi-infection alimentaire collective).
3. La fièvre aphteuse, qui n'est pas une zoonose 24 et qui s'est développée au Royaume-Uni en 2001, trouve son origine dans les eaux grasses (déchets de cuisine) d'un restaurant asiatique qui ont été données, sans respect des réglementations européennes, à un élevage de porc qui a ensuite contaminé tout le pays et une grande partie de l'Europe.
4. Enfin, en cas de contamination non déclarée, les transports d'animaux vivants, comme la diffusion d'aliments frelatés sont facteurs d'extension de l'épidémie.
Section
2 :
L'apparition de pathologies nouvelles liées au mode de
vie : L'exemple de la légionellose
« La protection de la vie individuelle est plus que jamais au coeur de nos sociétés fortement sécularisées. L'entretien des corps par le sport, la diététique, les préoccupations esthétiques, l'ampleur de la demande des soins médicaux en fournit des indices. La manifestation de phénomènes épidémiques est par conséquent perçue par nos contemporains comme une incongruité au coeur de nos sociétés riches, comme une sorte de menace de régression et de déclassement sur l'échelle internationale dont la cause ne peut finalement se situer que dans quelques dysfonctionnements plus ou moins coupables ou inattentifs de notre société » 25 .
Due à une bactérie, hôte naturel de l'environnement hydro tellurique, la légionellose a été identifiée il y a une trentaine d'années dans les pays occidentaux, où elle se développe en relation avec le progrès technique et l'augmentation de la fréquence du terrain favorable aux infections de la population (vieillissement, maladies chroniques, terrain pulmonaire, tabagisme...).
Cette infection pulmonaire est causée par une bactérie qui fut découverte à la suite d'une épidémie de pneumonie affectant de nombreux participants d'un congrès d'anciens combattants de la légion américaine réunis dans un hôtel à Philadelphie en 1976 : elle fut en conséquence dénommée Legionella .
La contamination se fait par voie respiratoire, par inhalation d'eau contaminée diffusée en aérosol. Aucune transmission inter humaine n'a été à ce jour démontrée et la période d'incubation est de 2 à 10 jours.
La légionellose affecte essentiellement les adultes et touche plus particulièrement les personnes présentant des facteurs favorisants : âge avancé, maladies respiratoires chroniques, diabète, maladies immunodépressives, traitements immunosuppresseurs, tabagisme, alcoolisme.
La légionellose se traduit par un état grippal fébrile et une toux initialement non productive. Certains patients peuvent présenter des douleurs musculaires, une anorexie et quelquefois des troubles digestifs (diarrhées) et/ou un état confusionnel. L'état grippal s'aggrave rapidement et fait place à une pneumopathie sévère nécessitant une hospitalisation . La maladie peut être mortelle dans 10 à 30 % des cas.
Le diagnostic clinique doit être confirmé par un des examens biologiques suivants : isolement de la bactérie dans un prélèvement bronchique, présence d'antigène soluble dans les urines, augmentation des titres d'anticorps par quatre entre deux prélèvements sanguins successifs, immunofluorescence directe positive.
Dans la majorité des cas, avec la mise sous traitement antibiotique du patient (macrolides ou fluoroquinolones), l'évolution est favorable. Le traitement est d'autant plus efficace qu'il est mis en oeuvre rapidement.
En France, il y a eu 1 044 cas déclarés en 2003, l'incidence représente 1,8 cas pour 100 000 habitants.
Légionellose :
Le point sur la situation
nationale au 25 août 2004 (source InVS)
A ce jour, l'Institut de veille sanitaire a répertorié 550 cas de légionellose en France pour l'année 2004 (de janvier au 25 août). En 2003, 1 044 cas de légionellose (parmi lesquels 129 personnes décédées) avaient été recensés, dont 597 sont survenus avant la fin du mois d'août 2003.
La légionellose affecte essentiellement les personnes fragilisées. Elle se traduit par une pneumopathie sévère. Le diagnostic clinique doit, dans tous les cas, être confirmé biologiquement. Dans la majorité des cas, avec un traitement antibiotique précoce et adapté, l'évolution est favorable. La contamination se fait par voie respiratoire, par inhalation d'eau contaminée diffusée en aérosol. Il n'y a pas de transmission interhumaine pour cette maladie . La période d'incubation est de 2 à 10 jours.
Pour les cas sporadiques, qui sont les plus fréquents, l'identification de la source de contamination est difficile et rare, ce qui rend leur prévention difficile. Les dernières données de surveillance, disponibles sur le site de l'Institut de veille sanitaire indiquent qu'en 2003, trois épidémies de légionellose communautaires sont survenues (à Montpellier, à Poitiers et dans le Pas-de-Calais), impliquant 141 personnes et causant 22 décès. Cet été, deux épidémies communautaires définies par une concentration inhabituelle de cas dans le temps et dans l'espace ont été identifiées : l'une à Nancy (11 cas du 15 juillet au 7 août) et l'autre, à Strasbourg (9 cas du 9 au 20 août). Chacun de ces deux épisodes de cas groupés a été détecté respectivement par la Ddass de Meurthe-et-Moselle et du Bas-Rhin précocement (à partir du 2ème cas). Les Ddass de Meurthe-et-Moselle et du Bas-Rhin, en collaboration avec les Drire de Lorraine et d'Alsace, avec le soutien de l'InVS et du CNRL et sous la supervision de la DGS ont entrepris une recherche active de la source de contamination pour ces 2 épisodes.
Pour l'épidémie de Nancy, qui semble en régression, 3 tours aéro-réfrigérantes (TAR) sur 57 répertoriées comme sources potentielles étaient contaminées. Cependant, la comparaison des souches de ces TAR avec celle identifiée chez un des malades de l'épidémie n'a pas permis d'identifier formellement la source de cet épisode.
L'enquête de l'épisode de Strasbourg est en cours. Une information du public et de la communauté médicale a été effectuée par la Ddass dans un but de détection et de prise en charge précoce des malades.
Si on exclut ces deux épisodes, le nombre de cas survenus depuis le 1 er juin 2004 en Lorraine et en Alsace reste comparable à ceux de 2003 et 2004.
Les données disponibles, à ce jour, à l'InVS permettent d'affirmer qu'il n'existe par actuellement de recrudescence de la légionellose en France . Le nombre de cas notifiés à l'InVS à la date du 25 août 2004 n'est pas supérieur à celui observé pour la même période lors des 2 années précédentes...
Par ailleurs, le niveau d'incidence dans notre pays (nombre de nouveaux cas annuels rapporté à l'ensemble de la population) de 1,8 pour 100 000 habitants est dans la moyenne européenne, le pays le plus touché étant l'Espagne avec 2,9 cas pour 100 000 habitants...
1) Le risque de contamination par légionelle est omniprésent
Comme l'a souligné le Professeur Jérôme Etienne 26 , « la bactérie responsable de la légionellose se retrouve d'abord naturellement dans l'eau des lacs et des rivières et c'est l'homme, en développant des réseaux d'adduction d'eau, notamment les réseaux d'eau chaude, qui a créé toutes les conditions pour la multiplication des légionelles. Cette bactérie est l'une des rares capables de se multiplier entre 37° et 42°C, ce qui implique que lorsque l'eau se retrouve à une chaleur optimale, dès que le circuit est entartré et que le débit d'eau est insuffisant, les légionelles peuvent se multiplier et atteindre des concentrations très importantes... Actuellement, la construction d'un bâtiment avec un réseau d'eau bouclé, une circulation permanente de l'eau, une température suffisamment chaude, un entretien régulier et programmé des circuits sont les garants de la prévention d'une multiplication des légionelles et donc de la survenue de la maladie, la légionellose » .
On estime actuellement à 50 % le nombre de prélèvements d'eau réalisés contenant des légionelles. Mais, fort heureusement l'isolement des légionelles, dans un circuit d'eau, est rarement associé à une maladie.
« La grande difficulté des acteurs du système de santé impliqués dans la prévention des légionelloses est de cerner les situations à risque, et notamment celles qui sont potentiellement épidémiques. Il faut d'abord comprendre que le taux d'attaque de la bactérie est faible : si mille personnes respirent un aérosol d'eau contenant des légionelles, seule une personne développera la légionellose ».
Cet aspect de la contamination est à la fois très important et très difficile pour les autorités car la présence de légionelles ne signifie pas du tout le développement d'une épidémie. Comme nous l'examinerons dans la section suivante, le développement de légionelles dans les centrales nucléaires suscite des inquiétudes mais n'est à ce jour à l'origine d'aucun cas connu de maladie. Du moins s'agissant des installations nucléaires, pour être tout à fait exact, un cas de légionelle a eu lieu à Gravelines dans un vestiaire à cause d'une douche.
Ce sont les personnes âgées qui paient le plus lourd tribu. Comme nous l'avons constaté l'an passé lors de l'épidémie survenue dans la région Nord-Pas-de-Calais, la moyenne d'âge des patients était de 76 ans. Au plan national, la médiane d'âge des patients atteints est, en 2003, de 62 ans. Depuis que la surveillance de la légionellose a été renforcée en 1995, le tabagisme est apparu comme un facteur associé à la légionellose dans 40 % des cas. Dans la région Nord-Pas-de-Calais, la silicose était apparue comme un autre facteur de risque significatif de survenue de la légionellose.
Mais il existe une problématique particulière pour les grandes tours et les autorités ont, après l'affaire de Lens, lancé un programme de recensement des tours aéroréfrigérantes 27 car l'épidémie de Lens a démontré qu'une source d'émission pouvait avoir des retombées sur 14 Km.
2) La difficulté majeure réside dans l'identification précoce de l'épidémie
Certaines souches de légionelle ne sont pas pathogènes, et nous ne savons pas aujourd'hui distinguer une souche virulente d'une souche non virulente. Cette incertitude complique beaucoup la politique de prévention.
De nouveaux procédés devraient aboutir à une identification précoce des souches de légionelles.
La biotechnologie devrait permettre de ramener le diagnostic de 11 jours à 3 heures à partir de l'examen de l'ADN, sans les désagréments pour le patient qu'impliquent les méthodes actuelles de diagnostics. De jeunes entreprises françaises sont en pointe sur ces questions d'utilité publique et il conviendrait que les pouvoirs publics les soutiennent efficacement.
Si le système de surveillance est actif et permet la détection précoce des cas groupés, la majorité des cas est sporadique et survient de façon isolée : il peut s'agir d'une contamination à domicile à partir d'un pommeau de douche entartré chez une personne immunodéprimée et présentant des facteurs de risque d'acquisition d'une légionellose, il peut s'agir d'une personne ayant inhalé une particule d'eau contenant des légionelles, provenant de toute autre source de contamination.
Dans moins de 10 % des cas, la légionellose est contractée à l'hôpital et il faut souligner l'énorme effort accompli par les établissements hospitaliers depuis la diffusion de la circulaire du 22 avril 2002 et l'épidémie survenue à l'ouverture de l'hôpital Georges Pompidou 28 , pour améliorer les circuits d'eau des établissements hospitaliers. La proportion des cas nosocomiaux de légionellose diminue régulièrement depuis 2000.
Les cas groupés épidémiques 29 ont représenté 12 % des cas de légionellose en 2003, ils étaient 5 % en 2002 et cette différence est notamment due à l'épidémie survenue en 2003 dans le Nord-Pas-de-Calais qui a atteint 86 malades.
La surveillance de la légionellose en France repose sur la déclaration obligatoire des cas par les cliniciens et les biologistes à la Ddass qui notifie ensuite les déclarations à l'InVS. Le Centre National de Référence des Légionelles (CNRL), localisé à Lyon et dirigé par le Professeur Jérôme Etienne, auditionné par vos rapporteurs qui se sont rendus à Lyon dans son laboratoire, assure la caractérisation des souches de Legionella isolées dans les laboratoires hospitaliers et dans l'environnement et leur comparaison par des techniques génomiques. Son rôle est particulièrement important pour relier les sources environnementales aux épisodes de cas groupés humains.
La suspicion de cas groupés repose sur le rapprochement des cas déclarés à la Ddass en termes de date de survenue, de résidence ou de lieu de fréquentation ; quand les autorités constatent plusieurs cas groupés de légionellose, elles mettent immédiatement en place la procédure d'identification de la souche afin d'en déterminer le caractère épidémique.
C'est ainsi que l'épidémie du Pas-de-Calais ou les épisodes récents de Nancy ou Strasbourg ont pu être suspectés très rapidement. Notons que, depuis 1998, 15 épisodes de cas groupés ou d'épidémies communautaires ont fait l'objet d'une enquête approfondie ; pour 7 d'entre eux, une tour aéro-réfrigérée a été identifiée comme source de contamination.
L'enquête de l'épisode du Pas-de-Calais et notamment les travaux de modélisation menés par l'INERIS ont montré que la diffusion de gouttelettes d'eau (dont on sait qu'elles peuvent véhiculer la Legionella) issues d'une tour aéro-réfrigérée, du type de celle impliquée dans l'épidémie du Pas-de-Calais, pouvait, dans des conditions météorologiques favorables et un environnement plat, atteindre et dépasser 10 km.
Zone de diffusion de l'épidémie de légionellose
(Source : INERIS)
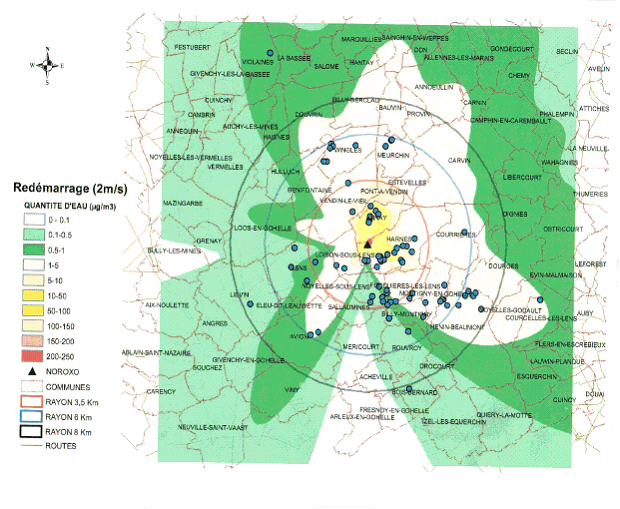
3) La prévention de la légionellose
L'épidémie de légionellose du Pas-de-Calais a sans doute permis d'accélérer la mise en oeuvre d'une politique de prévention de cette maladie.
La première étape a consisté à recenser les tours aéro-réfrigérantes ; à partir de ces tours, de l'eau chaude s'évapore et ces aérosols peuvent contenir des légionelles potentiellement pathogènes. L'action doit être préventive par l'entretien systématique de ces tours, la législation actuelle exige l'arrêt de fonctionnement d'une tour aéro-réfrigérante si l'eau de celle-ci contient plus de 100 000 Unités Formant Colonie de légionelles par litre.
Cette décision est difficile à prendre lorsque l'arrêt d'une tour aéro-réfrigérante implique celui du fonctionnement d'une entreprise. Il convient donc, dans l'intérêt de l'économie, d'agir en amont par des actions préventives empêchant de façon déterminante la prolifération de légionelles. Rappelons que l'usine Noroxo, mise en cause dans l'épidémie de légionellose du Pas-de-Calais, a définitivement fermé ses portes sans aucune injonction des pouvoirs publics, saisissant ce motif pour cesser son activité.
« Il n'est pas envisageable de penser que les légionelles pourraient être éradiquées de la nature qui nous a appris à respecter les équilibres écologiques pouvant nous protéger, l'éradication systématique d'un monde microbien saprophyte 30 nous fait courir le risque de remplacement par une flore inconnue plus agressive. Les leçons doivent être développées pour définir les traitements les plus optimums pour détruire les légionelles » 31 .
Le renforcement de l'action de prévention des légionelloses fait partie des actions prioritaires du Plan national Santé Environnement 2004-2008 qui comprend des objectifs portant respectivement sur la gestion des risques, l'investigation et la surveillance épidémiologique, l'estimation des risques et leur prévention. Il associe tous les partenaires de la lutte et de la prévention contre la légionellose, dont la Direction de la prévention des pollutions et du risque du ministère de l'environnement et du développement durable.
Il existe des zones d'incertitude que seules la science et la recherche scientifique pourront résoudre.
4) La problématique « légionelles » des tours aéro-réfrigérantes du parc nucléaire d'EDF
Vos rapporteurs, en apprenant la présence de légionelles dans les tours aéro-réfrigérantes des centrales nucléaires, ont enquêté. Ils ont auditionné EDF et l'Autorité de sûreté nucléaire.
A) Le point de vue d'EDF
Ce point de vue est exprimé dans la note, adressée à vos rapporteurs, qui suit :
« Depuis plusieurs années, nous surveillons régulièrement la présence éventuelle de légionelles dans tous nos sites de production. Outre les mesures classiques prises vis-à-vis de nos installations sanitaires présentes dans les vestiaires ou vis-à-vis des installations de climatisation, les grandes tours de réfrigération font l'objet de surveillance, mais aussi de nettoyages et d'entretiens réguliers pour limiter les niveaux de colonisation. En effet, à l'intérieur de ces tours, on trouve de grands bassins d'eau dont la température est souvent comprise entre 10° et 40°C. Aussi notre objectif est bien d'avoir ces bassins et les équipements reliés aussi détartrés que raisonnablement possible A titre d'exemple, et pour témoigner de la collaboration très transparente établie avec EDF, je citerai la façon de déterminer les risques potentiels de transmission des légionelles à partir des panaches des vapeurs d'eau émises par les centrales nucléaires. Il convient de supprimer totalement ce risque potentiel et une analyse très précise a été établie en concertation avec EDF et le Centre national de référence des légionelles, pour éradiquer les légionelles potentiellement présentes dans les réacteurs de 19 centrales nucléaires françaises. Ainsi, il convient de décliner un à un les lieux à risque - cette tâche n'est pas aisée en ce qui concerne les réseaux d'eau des domiciles individuels. Ainsi que je l'ai signalé, la seule présence de tartre sur un pommeau de douche représente en soi un risque potentiel. La prévention doit d'abord être axée sur les grandes sources de contamination, comme celles que nous avons décrites, sur l'amélioration des politiques de construction dans la mise en place de réseaux d'eau adaptés à la non-prolifération des légionelles.
« Depuis 2000, des études approfondies ont été menées sur ces tours de réfrigération, à la fois sur les aspects sanitaires et sur les phénomènes de dispersion atmosphérique.
« A ce jour il n'existe pas de cas connus de légionellose apparus dans l'environnement des centrales du fait des tours aéroréfrigérantes d'EDF. Il est à noter d'ailleurs, que l'ensemble de nos centrales équipées de telles tours se trouvent à la campagne, éloignées des habitations.
« Une enquête comparant les taux d'anticorps légionelles réalisée sur la population d'un site témoin (sans aéroréfrigérant), de sites avec des tours de grande hauteur (Cattenom et Belleville) et d'un site avec des aéroréfrigérants de moyenne hauteur (Chinon) ne fait pas apparaître d'écart entre les différents groupes d'exposition. Les taux retrouvés chez le personnel des centrales sont très inférieurs à ceux publiés pour la population générale. De tels résultats ont déjà été présentés dans des congrès internationaux et mis à la disposition des autorités administratives.
« Les tours aéroréfrigérantes des centrales sont différentes des autres tours industrielles. Leur conception assure un meilleur arrêt des gouttelettes et une dispersion importante par le panache du fait de leur très grande taille. Des calculs comparatifs de dispersion entre petites tours habituellement à l'origine d'épidémies et les grandes tours, basés sur des expositions enveloppes ont établi que le niveau d'exposition des grandes tours de plus de 125 m de haut était à minima 100 fois plus faible que pour les petites tours de climatisation.
« Le cas de la centrale de Chinon est plus spécifique. Pour des raisons d'intégration dans le paysage, les 4 unités de production sont équipées chacune d'une tour de moyenne hauteur, de 30 m environ. Les mêmes calculs de dispersion ont établi que le niveau d'exposition pour ces tours était a minima 10 fois plus faibles que pour les petites tours de climatisation. Les taux relevés dans l'eau des bassins dépassant parfois en été et en automne les 10 5 UFC /l (UFC : Unité Formant Colonie), les autorités administratives, tenues régulièrement au courant, nous ont demandé par arrêté préfectoral du 6/08/2004 de «procéder en tant que de besoin, à un traitement par chloration dans le bassin froid des tranches de production en marche, de telle manière que la concentration en légionelles dans l'eau n'excède pas la valeur de 5 10 5 UFC/l ».
« Un traitement biocide par chloration massive périodique a été immédiatement mis en oeuvre sur les 4 installations concernées. Ce type de traitement constitue une solution provisoire car pour être totalement efficace, il nécessiterait d'être appliqué en continu. Aussi, nous avons prévu la mise en service mi 2005 d'un traitement continu à la monochloramine, dont l'impact sur l'environnement est moindre. Pour cela, la construction de stations de traitement sur Chinon a été entreprise au plus tôt, représentant un investissement de plus de 10 Millions d'euros. Ces stations seront mises en service avant l'été 2005, une fois leur construction terminée et les autorisations administratives de traitement obtenues.
« Nous tenons régulièrement au courant les autorités administratives sur ce sujet (CSHPF : Conseil Supérieur d'Hygiène Publique de France ; DGS ; DGSNR). Nous leurs présentons régulièrement nos résultats et les mesures que nous prenons. Nous répondons aux sollicitations. Début 2005, un courrier de la DGSNR nous demande de « mettre en oeuvre des mesures de prévention adaptées destinées à maintenir la concentration en légionelles mesurée dans les circuits de refroidissement des circuits secondaires en dessous de 5 10 6 UFC/l pour les centrales munies de tours de taille élevée et de 5 10 5 UFC/l pour la centrale de Chinon, équipée de tours de taille moyenne ». Ce courrier nous notifie également les dispositions à prendre en cas de dépassements ponctuels ou durables des valeurs indiquées.
« En parallèle de l'ensemble de ces actions, nous poursuivons nos travaux de recherche afin de progresser dans nos connaissances sur l'écologie de ces bactéries. Plusieurs axes sont à souligner :
« Nous cherchons à mesurer de manière fiable et représentative les légionelles dans les panaches des tours de Chinon. De même, nous cherchons à connaître le sérotypage et le génotypage des légionelles présentes dans les installations de refroidissement du site.
« Nous cherchons à mettre au point un procédé qui permet de mesurer plus rapidement les légionelles.
« Enfin, nous cherchons à mesurer le taux de survie de ces bactéries une fois dispersées dans l'atmosphère, phénomène non pris en compte jusqu'à présent, mais particulièrement important pour nos tours, du fait du temps nécessaire pour que les gouttelettes arrivent au niveau du sol. Pour cela, nous travaillons avec Clim'Espace sur des tests en chambre.
« Afin de nous aider dans ces travaux, nous avons réuni, notamment pour le premier volet ci-dessus, un « Comité Scientifique », présidé par le Professeur Maisonneuve et composé des meilleurs spécialistes mondiaux de la légionelle : le Professeur Etienne, ainsi que Janet Stout, Ingegerd Kallings, John Lee, Christian Lück. Ce Comité nous aide pour les méthodologies, mais aussi pour la validation de nos mesures et des axes à creuser spécialement.
« En conclusion, outre les travaux déjà menés et que nous poursuivons, les dispositions prises à l'été 2004 sur la centrale de Chinon et qui seront renforcées avant cet été par un traitement pérenne à la monochloramine permettent d'éviter tout risque tant pour la population que pour les salariés travaillant sur nos installations. Les enquêtes épidémiologiques réalisées comme les observations effectuées autour de nos centrales ».
B) L'analyse des rapporteurs
Le débat qui nous préoccupe n'a rien à voir avec l'énergie nucléaire car les tours aéro-réfrigérantes ne font pas partie de l'îlot nucléaire, et les centrales refroidies par la mer n'en sont d'ailleurs pas dotées.
La problématique est la même que pour les autres tours aéro-réfrigérantes, il n'y a que la taille qui différencie ces installations des autres. Faute de certitudes scientifiques, il convient d'être très prudent mais il apparaît que paradoxalement les problèmes de concentrations de légionelles sont plus importants dans les tours de Chinon qui ont été arasées pour ne pas être visibles depuis le château de Chambord. De ce fait, elles ont une configuration particulière, dite à tirage forcé, et sont d'une taille d'environ trente mètres ; or, il nous a été indiqué que la concentration des tours de plus de 125 mètres de haut est 100 fois inférieure à celle de moins de trente mètres.
Vos rapporteurs ont retenu plusieurs enseignements de leurs investigations :
- Le procédé actuellement retenu de mélange d'ammoniaque et d'eau de javel n'est pas satisfaisant sur le plan environnemental et doit être regardé comme un expédient provisoire jusqu'à l'automne et le choix d'éradiquer les légionelles, au risque d'enrichir en nitrates l'eau de la Loire, a été fait sans information publique.
- La mise en place d'un procédé plus rapide de mesure des légionelles est une absolue nécessité, comme la poursuite des recherches pour être capable d'identifier celles qui sont pathogènes.
- La mesure du taux de survie des bactéries dans les panaches des tours doit être engagée.
La présence de légionelles dans le milieu hydro tellurique est quelque chose de tout à fait normal mais une grande vigilance est nécessaire sur ce sujet pour lequel vos rapporteurs ont le sentiment d'une assez grande transparence d'EDF vis-à-vis de leurs demandes.
En conclusion, vos rapporteurs se félicitent que le ministère de la santé considère le sujet de la légionellose comme prioritaire et l'ait inscrit dans le plan national santé environnement.
La prévention de la prolifération des légionelles dans les réseaux d'eau chaude sanitaire est encadrée soit par des textes de portée très générale, soit par des circulaires administratives ou des recommandations d'experts spécifiques à certains établissements. L'interprétation et le caractère obligatoire de ces règles s'en trouvent grandement compliqués.
Les installations d'eau chaude sanitaire forment des systèmes complexes avec souvent une implication de plusieurs intervenants sur l'ensemble du réseau. Cette pluralité d'acteurs (propriétaires, gestionnaires exploitants) peut intervenir de manière séparée, sans moyens d'agir sur l'ensemble des facteurs concernés. La dispersion des responsabilités qui en résulte complique singulièrement la maîtrise du risque qui, pourtant, nécessiterait une approche globale.
Les améliorations pourraient s'articuler autour de quatre axes :
• mieux définir les responsabilités de chacun des intervenants, en particulier entre propriétaires et gestionnaires d'installations ;
• fixer, suivant le type des installations, des objectifs de sécurisation et des règles de suivi :
- seuil d'alerte et mode d'action définie pour tous les types d'installations,
- fréquence d'analyse et de contrôle ;
• respecter des règles simples de gestion :
- température de production et de distribution,
- équilibrage des réseaux pour éviter la stagnation des eaux,
- traitement de l'eau pour prévenir l'entartrage et la corrosion.
• La diffusion obligatoire des résultats d'analyses des gestionnaires de réseaux d'eau chaude sanitaire aux autorités de tutelle serait certainement à promouvoir.
Il semble important sur cette question de ne pas empiler les arrêtés et les circulaires mais de développer une stratégie globale visant à la prévention des légionelles, souvent difficile à mettre en oeuvre sur le plan technique, ainsi qu'un guide de bonnes pratiques en cas de problème s.
Un bon exemple est fourni par le recensement des tours aéro-réfrigérantes (cf annexe n°4):
• Les installations soumises à autorisation sont recensées par la direction régionale de l'industrie de la recherche et de l'environnement.
• Les installations soumises à déclaration sont recensées par la préfecture.
• La direction départementale de l'action sanitaire et sociale recense le reste, sans succès, en essayant de se rapprocher des mairies, des entreprises de maintenance dans la mesure où même les climatiseurs à eau sont concernés.
Malgré ces difficultés, une procédure exemplaire d'alerte a été mise en place dans le Nord Pas-de-Calais : en cas d'incident, le trajet du malade est confronté à une cartographie des tours dans un rayon de 3 km. La direction régionale de l'industrie de la recherche de l'environnement est saisie, elle se rapproche des industriels et s'il y a un doute compare les souches avec l'aide du centre national de référence.
Section 3 :
Les infections et
toxi-infections alimentaires collectives (TIAC)
Plus de 200 maladies infectieuses, bactériennes, virales et parasitaires ou toxiques sont transmises par l'alimentation, la situation actuelle constitue un progrès majeur par rapport à la situation qui prévalait il y a une quarantaine d'années, la gravité des TIAC est en décroissance sensible et nous sommes aujourd'hui très loin des trois à quatre mille décès, évoqués par certains interlocuteurs, il y a une trentaine d'années. 32
Tout d'abord il est important de souligner que la qualité des aliments est bien meilleure qu'autrefois sur le plan de la sécurité sanitaire. Le nombre de personnes intoxiquées par des aliments a beaucoup diminué. Le fait que la restauration collective se développe et que les aliments soient plus industrialisés qu'autrefois explique que des cas d'intoxication alimentaire puissent toucher un nombre élevé de personnes, ce qui entraîne une large médiatisation mais, ne signifie pas pour autant que globalement le nombre de personnes touchées soit supérieur à ce qu'il était antérieurement 33 , au contraire. Par exemple, la surveillance du nombre de cas de salmonelloses témoigne d'une baisse de 33 % du nombre d'intoxications entre 1997 et 2001 34 .
Leur nombre est relativement bien connu car toute TIAC doit faire l'objet d'une déclaration obligatoire à l'autorité sanitaire départementale (DDASS ou DSV).
L'institut national de veille sanitaire a évalué en 2004 le nombre des cas d'infections, d'hospitalisations et de décès pour 23 agents (13 bactéries, 2 virus, 8 parasites). Il estime que les agents infectieux étudiés sont à l'origine de 238 836 à 269 085 cas d'infections d'origine alimentaire dont 51 269 à 81 927 dues à des bactéries, principalement Salmonella et Campylobacter, 70 600 à des virus, principalement les rotavirus. Nous rencontrons également 116 517 cas d'infestation par des parasites, notamment Toxoplasma gondii et Taenia saginata.
Le nombre total annuel de cas hospitalisés est estimé entre 10 188 et 17 771. Les salmonelloses en sont la première cause (5 691 à 10 202 cas), suivi par les infections à Campylobacter (2598 à 3 516 cas) et la listériose (304 cas). La toxoplasmose (426 cas) apparaît comme la principale cause d'hospitalisation parmi les infections parasitaires.
L'estimation du nombre annuel total de décès se situe entre 228 et 691. Les infections bactériennes sont responsables de la majorité des décès attribuables aux salmonelloses, première cause de décès (entre 92 et 535) et à la listériose, deuxième cause de décès (78).
En 1998, les médecins libéraux ont effectué 32% des déclarations, les médecins hospitaliers 30%, les directeurs d'établissement 11%, les malades 6% et les services de santé scolaire 2,5%. Les autres sources de déclaration étaient représentées par les centres antipoison, laboratoires, mairies, presse et lieux de distribution.
800 foyers de salmonellose et de shigellose ont été signalés au centre national de référence en 1998.
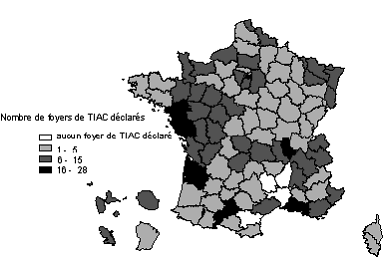
Répartition départementale du nombre de foyers de salmonellose
et de shigellose notifiés au CNR. France, 1998.

L'agent responsable de la TIAC a été identifié, par mise en évidence de l'agent dans des prélèvements humains ou alimentaires, dans 56,6% des cas. Une salmonelle a été isolée dans 71% des foyers pour lesquels l'agent a été identifié.
Les progrès enregistrés ont été particulièrement spectaculaires ces dernières années en termes de rapidité d'identification de l'origine des sources d'épidémies puisque nous sommes passés, par exemple pour les listérioses, d'un délai de 28 à 4 jours.
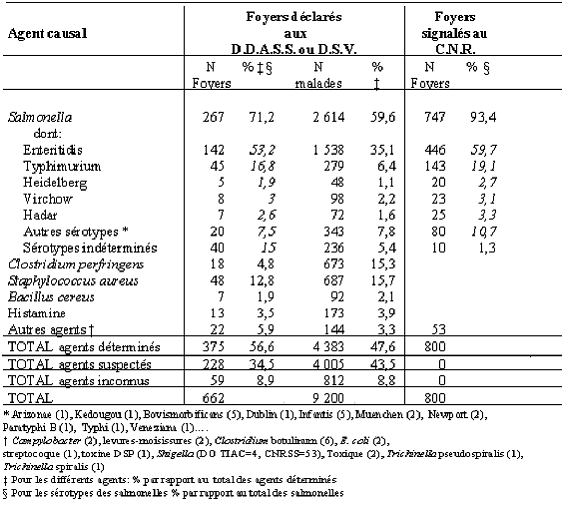
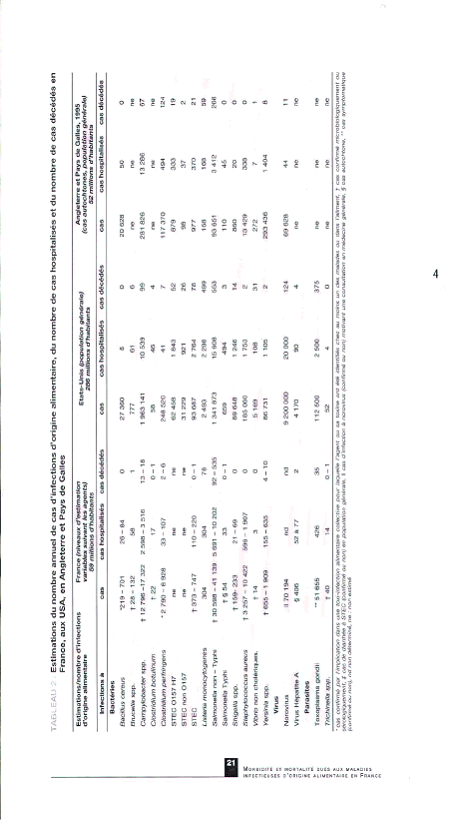
Comme l'illustre le tableau ci-dessous, les salmonelles demeurent de très loin l'agent infectieux le plus répandu mais nous enregistrons une grande stabilité du nombre de cas des toxi infections alimentaires et l'inquiétude de vos rapporteurs se situe non au niveau des aliments préparés par l'industrie mais plutôt à celui des produits sensibles comme les coquillages qui peuvent concentrer les effets de la pollution et, pour lesquels, les effets du réchauffement climatique sont relativement sensibles.
D'autant que, comme l'illustre le tableau ci après, le nombre de TIAC est sensiblement plus élevé en période estivale.
Répartition mensuelle par type d'agent identifié ou suspecté.
TIAC déclarées aux DDASS ou DSV. France, 1998. (N=662)
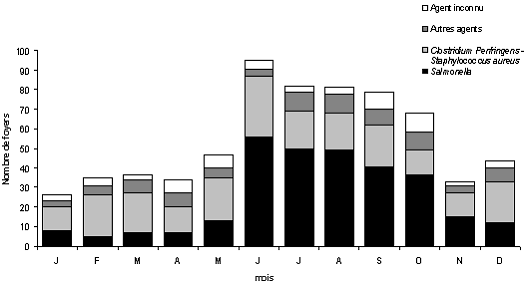
LES SALMONELLOSES
Les salmonelloses sont des maladies provoquées par des entérobactéries du genre Salmonella. La plupart des Salmonella sont des parasites intestinaux des animaux vertébrés et des oiseaux transmis à l'homme par le biais d'aliments contaminés. En pathologie humaine, les salmonelloses comprennent deux principaux types d'affections: gastro-entérites et fièvres typhoïde et paratyphoïdes .
Epidémiologie
Vu le large spectre d'animaux pouvant être porteurs de Salmonella, une grande variété de produits alimentaires peut être à l'origine d'une contamination humaine : viande - et particulièrement volaille -, produits carnés, oeufs et produits laitiers. Les salmonelloses d'origine alimentaire peuvent donner lieu à des foyers très importants, qui peuvent atteindre une échelle nationale (et même internationale) si un aliment commercialisé à large diffusion se trouve contaminé. En 1994 aux Etats-Unis, par exemple, une épidémie provoquée par une crème glacée a touché 224 000 personnes. En France, une des plus importantes épidémies, dont la source n'a pu être identifiée, survenue fin 1985, aurait touché 25 000 personnes d'après l'estimation la plus faible. En France toujours, en 2001, 64% des toxi-infections alimentaires déclarées, avec agent pathogène identifié, ont été provoquées par des Salmonella et ont touchées plus de 2 500 personnes. En 2003, près de 50% des 382 foyers français de cas groupés signalés au Centre National de Référence étaient causés par Salmonella sérotype Enteritidis suivi par le sérotype Typhimurium (24% des foyers). Il est difficile d'avoir une idée du nombre réel de cas annuels de salmonelloses, mais on estime que les cas déclarés peuvent être multipliés par 20 à 100. Les toxi-infections alimentaires collectives doivent obligatoirement être déclarées aux DDASS ou aux DSV par les médecins, les biologistes, les responsables d'établissements ou les particuliers.
Symptômes et traitement
Les gastro-entérites sont provoquées par des Salmonella ubiquistes présentes chez l'homme et les animaux. La durée d'incubation est généralement de 1 à 2 jours et dépend de la dose ingérée, de la santé de l'hôte et des caractéristiques de souche de Salmonella. Les salmonelloses provoquent une forte fièvre accompagnée de diarrhées, vomissements et douleurs abdominales. Chez des adultes de condition physique normale, une gastro-entérite disparaît sans traitement après 3 à 5 jours en moyenne. En revanche, une antibiothérapie doit être prescrite chez les personnes âgées, les nourrissons, ou les personnes immuno-déprimées chez lesquels l'infection peut être plus sévère, voire mortelle.
Prévention
La meilleure protection contre le risque de salmonellose est une bonne cuisson des aliments, en particulier des viandes, à au moins 65C pendant 5 à 6 minutes. Pour le steak haché congelé ou surgelé, la cuisson doit être effectuée sans décongélation préalable car elle augmente le risque de multiplication bactérienne. Le froid bloque le développement des bactéries mais ne les tue pas. De 1985 à 1997, Salmonella Enteridis a fortement augmenté en France : elle touche les élevages de volaille et a la particularité d'être présente non seulement à la surface de la coquille de l'oeuf, mais dans le contenu même d'oeufs intacts. Il est pour cette raison conseillé de conserver les oeufs au réfrigérateur, de maintenir au froid les préparations à base d'oeufs sans cuisson (mayonnaise, crèmes, pâtisseries ...) et de les consommer le plus près possible de leur fabrication. De plus, les personnes les plus vulnérables (personnes âgées, malades, nourrissons, femmes enceintes) devraient éviter la consommation d'oeufs crus ou peu cuits.
Source : Institut Pasteur
Nombre de foyers selon l'agent responsable. TIAC déclarées aux DDASS ou DSV et foyers de salmonellose et de shigellose déclarés au CNR. France, 1998
Les TIAC déclarées en France en 1999-2000.
Chiffres et tendances
|
Nombre total de foyers |
1267 |
|
Nombre total de malades |
17378 |
|
Nombre de décès |
10 |
|
% de cas hospitalisés |
8 % |
|
% de TIAC à agent inconnu |
59 % |
|
% de TIAC à Salmonella |
64 % |
(par foyers à pathogène identifié)
Source : Bulletin épidémiologique - Décembre 2003
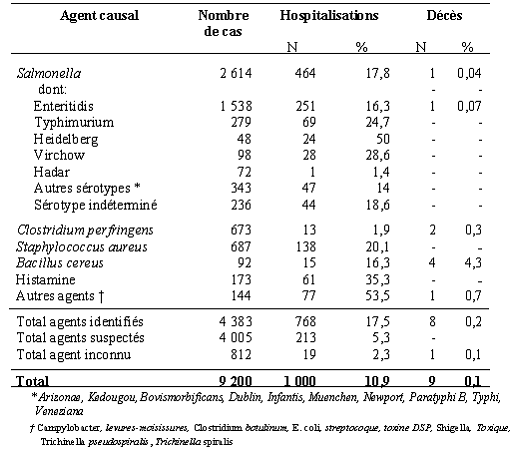
Hospitalisations et décès selon l'agent responsable.
TIAC déclarées aux DDASS ou DSV. France, 1998.
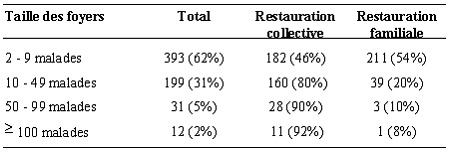
Taille des foyers selon le type de restauration.
TIAC déclarées aux DDASS ou DSV. France, 1998.
Agents identifiés ou suspectés et aliments responsables ou suspectés.
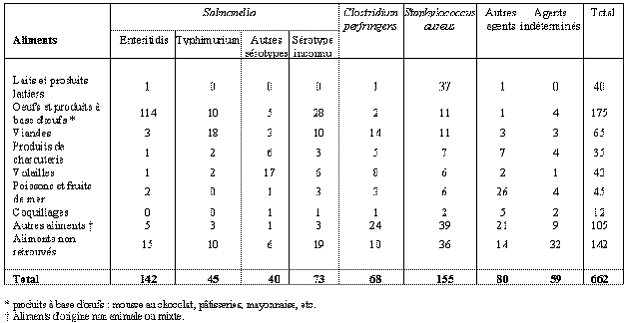
Estimations les plus plausibles, par agents pathogènes, du nombre annuel moyen de cas, de cas hospitalisés et de cas décédés par infections d'origine alimentaire en France métropolitaine dans les années 1990
Source : InVS - 10 mai 2004
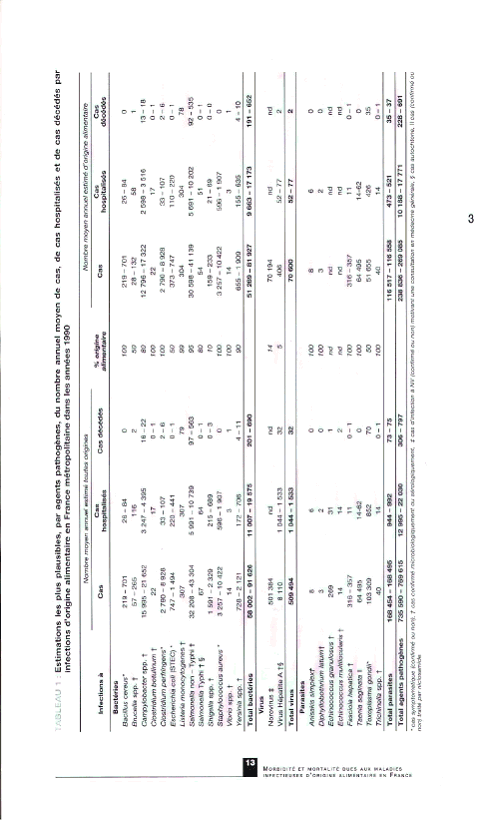
Estimations du nombre annuel de cas d'infections d'origine alimentaire, du nombre de cas hospitalisés et du nombre de cas décédés en France, aux USA, en Angleterre et Pays de Galle
Source : InVS - 10 mai 2004
Section 4 :
Les infections
nosocomiales
Le terme d'infection nosocomiale signifie infection acquise en milieu de soins, hospitaliers ou non. Il serait préférable de dire à l'occasion des soins car toute infection est présumée acquise à l'hôpital si elle survient au bout de deux jours ; cette définition est large car des infections peuvent avoir été contractées en dehors des soins, par exemple à l'occasion d'un accident, et se révéler au cours d'une hospitalisation 35 .
La fréquence des infections nosocomiales est comparable en France à ce qui est observé dans les autres pays développés : on estime que, dans notre pays, 7% des patients hospitalisés (soit 21 010 patients en 2001) 36 présentent une infection nosocomiale. Les statistiques étrangères font état d'un pourcentage variant de 5 à 12%.
Il est important de relever que de plus en plus de pathologies lourdes sont traitées en hôpital de jour, à domicile ou en soins privés et que l'hôpital est loin d'être le seul lieu où surviennent les infections nosocomiales.
Il convient également de distinguer au sein des infections nosocomiales entre celles qui résultent de l'activité médicale proprement dite et celles qui résultent de problèmes de logistique, par exemple les épidémies de légionellose au sein de l'hôpital (environ 200 par an qui sont davantage liées à des problèmes d'eau et de tuyauterie qu'à des problèmes d'organisation de l'activité médicale).
Les données sur l'évolution des infections nosocomiales doivent être manipulées avec beaucoup de prudence car beaucoup de patients très fragiles se trouvent aujourd'hui hospitalisés et ne l'auraient pas été il y a quelques années car ils seraient décédés prématurément. L'âge moyen des patients lors de l'enquête précitée s'élevait à 61,5 ans et 55 % des patients avaient 65 ans ou plus. Les nouveau-nés (enfants de moins de 28 jours) représentaient 3 % des patients. 22,3 % des patients souffraient d'une pathologie sévère, ils étaient immunodéprimés dans 9 % des cas. Le problème des infections nosocomiales demeure un problème grave de santé publique , d'autant que l'opinion publique admet très mal que des maladies graves, voire mortelles, puissent être contractées à l'occasion d'une hospitalisation 37 .
Ces infections nosocomiales sont mal admises par l'opinion. Une action portant sur trois points essentiels permettrait d'en diminuer la fréquence, sans pour autant éradiquer ce phénomène:
- la formation des personnels y compris de ceux qui travaillent en milieu libéral,
- une action de prévention forte au quotidien par des mesures simples d'hygiène telles que le lavage des mains,
- une architecture hospitalière qui intègre mieux les problèmes de sécurité nosocomiale, en particulier au niveau des blocs opératoires, des circuits de soins et des spécificités propres à certains services tels que la réanimation ou la néonatalogie.
Il existe une somme considérable de circulaires sur ce thème qui doivent absolument être respectées aussi bien au niveau des règles élémentaires d'hygiène que des bonnes pratiques médicales.
Une situation qui implique une grande vigilance
Il convient d'être très vigilant car, s'agissant de risques viraux de type transmission de l'hépatite C, 30% des cas pourraient être d'origine nosocomiale.
Les enquêtes de prévalence montrent que, sur une journée donnée, 6 à 10% des patients présentent une infection nosocomiale. Parmi ces infections, les infections urinaires sont les plus fréquentes, suivies par les infections respiratoires et les infections du site opératoire.
Nous voyons apparaître, à partir des données qui suivent, la concentration des problèmes d'infections nosocomiales sur quelques pathologies :
• Comme l'illustre le graphique ci-dessous, plus du tiers des infections nosocomiales concerne les problèmes urinaires.
• Les malades, suites à des interventions de type chirurgical ou à un état de faiblesse générale, sont particulièrement exposés. En effet, parmi les patients victimes infections nosocomiales, 21 % d'entre eux ont eu une intervention dans les 30 jours, 22 % avaient un cathéter, 9 % une sonde urinaire et 17 % un traitement anti-infectieux.
Erreur ! Argument de commutateur inconnu.
Les services les plus touchés sont par ordre décroissant : la réanimation avec des taux de prévalence moyens de l'ordre de 30%, la chirurgie avec des taux de 7 à 9%, et la médecine avec des taux de prévalence de 5 à 7%. Les services à moindre risque sont les services de pédiatrie et de psychiatrie. Les infections sont aussi fréquentes dans les services de moyen et long séjour qu'en court séjour.
En chirurgie, les infections sur site opératoire sont rares mais elles sont toutefois catastrophiques pour l'image des hôpitaux qui ne sont pas toujours responsables des infections en cause ; par exemple lorsqu'un accidenté de la route est opéré d'une fracture ouverte, il n'est pas du tout évident que l'infection du patient ait été contractée à l'hôpital. Cela ne minimise en rien le drame vécu par celui-ci ou la compréhensible révolte de l'opéré d'une articulation, contaminé puis handicapé suite à une infection.
Or, environ 3% des interventions se compliquent en chirurgie d'une infection du site opératoire. Ce taux moyen recouvre une très grande hétérogénéité : les taux d'infections du site opératoire varient de 1% pour le groupe d'interventions à faible risque d'infection chez les patients avec peu d'antécédents médicaux, à 20-25% en moyenne pour le groupe d'interventions à risque élevé d'infection, chez les patients les plus fragiles 38 .
En matière d'outil de surveillance et de prévention beaucoup de choses ont été réalisées , la France dispose aujourd'hui de centres de référence dotés d'une coordination nationale, avec un niveau régional et un CLIN 39 dans chaque hôpital. Ce système est bien meilleur que celui du début des années 90 où il existait des réseaux de surveillance basés sur le volontariat avec les limites liées à celui-ci.
Il convient de noter que, depuis 2001, le signalement de certaines infections nosocomiales est obligatoire.
Nous pouvons estimer aujourd'hui que la France a rattrapé son retard dans le domaine de la connaissance et du dépistage des infections nosocomiales.
Il existe probablement des progrès à faire dans le domaine de l'identification des microorganismes responsables et de la définition des indicateurs limités aux infections constatées.
Il faut noter que l'Institut de veille sanitaire a été chargé, en mars 2003, d'une mission de définition des indicateurs de lutte contre l'infection nosocomiale susceptible de constituer un tableau de bord pour l'ensemble des établissements de santé. Cet outil devrait permettre d'établir des comparaisons au sein d'un établissement et d'aider les hôpitaux à se situer les uns par rapport aux autres.
Un programme national de lutte contre les infections nosocomiales vient d'être établi pour la période 2005-2008. Il comporte cinq orientations principales :
• adapter les structures et faire évoluer le dispositif de lutte contre les infections nosocomiales
• améliorer l'organisation des soins et des pratiques des professionnels
• optimiser le recueil et l'utilisation des données de surveillance et du signalement des infections nosocomiales
• mieux informer les patients et communiquer sur le risque infectieux lié aux soins
• promouvoir la recherche sur les mécanismes, l'impact, la prévention et la perception des infections nosocomiales.
Il est bien entendu trop tôt pour porter un jugement sur un ensemble de mesures très techniques qui vont dans le bon sens et qui sont détaillées en annexe numéro six.
Section 5 :
La
question de la résistance aux antibiotiques
L'accroissement de la résistance aux antibiotiques est un phénomène naturel aggravé par un abus de prescriptions, le non respect des posologies et l'alimentation animale 40 . Il risque, si nous n'y prenons pas garde, de poser des problèmes redoutables aux pays industrialisés qui sont fortement médicalisés.
La résistance du pneumocoque à la pénicilline et aux macrolides devient un problème sérieux en Europe car elle tend à se généraliser. La France y occupe le premier rang européen pour la résistance à la pénicilline G et le deuxième pour les macrolides 41 , comme en témoignent les résultats pour 2002 du système de surveillance européen 42 . Cette résistance est, en France, la plus importante chez les enfants de 0 à 4 ans.
La résistance du staphylocoque doré à la méticilline est plus élevé dans les pays du Sud de l'Europe (Grèce 44 %, Italie 38 %, Portugal 38 %, France 33 %, Espagne 23 %) que dans plusieurs pays du Nord (Pays-Bas, Finlande, Danemark, Suède) où les taux restent inférieurs à 5 %. Il a progressé sensiblement au Royaume-Uni. Les pourcentages de résistance de haut niveau à la gentamicine de certains entérocoques (E. faecalis et E faecium) restent élevés en Europe (médiane de 37 % -38%), excepté en France (10 -15 %), en Autriche (17-20%) et en Finlande (13 %).
Or, les antibiotiques ont permis de soigner des maladies massivement mortelles telles que la tuberculose ; de ce fait ils revêtent un statut particulier auprès des médecins mais aussi auprès des patients. Avec 100 millions de prescriptions par an , la France détient le record européen de la consommation d'antibiotiques. En 1999, le taux de résistance des pneumocoques aux pénicillines atteint 42% contre 0,5 % en 1984.
DU COTE DES PATIENTS
>
un
manque d'information :
• Seuls
30%
des
patients savent que les antibiotiques n'agissent que sur les
bactéries.
•
35%
n'ont jamais entendu parler de
résistance.
>
des idées reçues :
•
64%
pensent que les antibiotiques accélèrent la
guérison, quelle que soit l'infection.
•
39%
croient que les antibiotiques font baisser la fièvre.
>
des pratiques inadaptées :
•
19%
arrêtent le traitement quand les symptômes
disparaissent.
•
12%
déclarent avoir
déjà pris des antibiotiques sans prescription
médicale.
*Source : Etude Ipsos réalisée pour
l'Assurance Maladie entre mars et juin 2002 auprès de 1000 patients et
800 médecins.
DU COTE DES PRATICIENS
>
une
pleine conscience du problème :
•
86%
des généralistes sont convaincus que la consommation
d'antibiotiques est trop élevée en France.
•
52%
pensent que l'augmentation des résistances est le
plus souvent liée à une prescription inadaptée.
•
1 généraliste sur 2
déclare être
parfois confronté à des phénomènes de
résistance
>
la pression de certains patients
:
•
33%
des médecins estiment que
leurs patients leur suggèrent implicitement une prescription
d'antibiotiques.
•
60%
déclarent difficile de
ne pas prescrire un antibiotique à un patient qui en fait la demande.
Les résultats du sondage, exposé ci-dessous, réalisé par la Caisse nationale d'assurance maladie sont à cet égard révélateurs.
Pour la consommation d'antibiotiques en ville qui représentent plus de 90 % de la prescription totale, la France occupe toujours la première place en Europe, malgré les campagnes de sensibilisation.
Néanmoins, une baisse relative de la consommation (5,6 %) a pu être observées entre 1999 et 2002. À l'hôpital, en moyenne, 16 % des patients reçoivent des antibiotiques, 24 % parmi ceux qui sont hospitalisés en court séjour et près de la moitié de ceux qui sont en réanimation.
Il est très rare que les bactéries deviennent résistantes à tous les antibiotiques connus mais il est admis aujourd'hui que les médecins ont tendance à trop prescrire les antibiotiques, source d'apparition de souches résistantes, alors que certains pays arrivent à limiter ce phénomène.
Par exemple le Danemark, après avoir connu une épidémie de staphylocoques dorés dans les années 70, a pris des mesures drastiques pour réduire la consommation des antibiotiques et la durée des séjours hospitaliers ; depuis le taux de résistance aux antibiotiques est devenu quasi nul dans ce pays.
La création au sein des hôpitaux d'un médecin prescripteur d'antibiotiques, référent pour ses collègues, qui est particulièrement pertinente, peut constituer un outil extrêmement utile. Il est certain que, pour la médecine hospitalière, comme pour la médecine ambulatoire, il faut arriver à généraliser des référentiels de bonne pratique.
De même, il est important que les médecins soient informés en temps réels, dans une région donnée, de la présence des virus en circulation afin d'éviter la prescription inutile d'antibiotique. Il semble que le mécanisme d'alerte pour les virus respiratoire mis en place dans certaines régions ait donné des premiers résultats encourageants.
D'autre part, des aides au diagnostic, tels les tests rapides sur les angines bactériennes, peuvent jouer un rôle important dans la diminution de la consommation d'antibiotiques en médecine libérale.
Enfin une réflexion sur l'usage des antibiotiques dans les élevages doit être menée à l'aune des résistances induites.
La progression de la résistance bactérienne aux antibiotiques est actuellement plus rapide que la découverte de nouveaux antibiotiques. Des progrès ont été faits dans l'identification des mécanismes de résistance, de transmission, dans la surveillance, la détection de l'émergence de nouvelles souches résistantes ; néanmoins, beaucoup reste à faire pour en assurer la maîtrise, notamment par un meilleur usage des antibiotiques en médecine de ville, à l'hôpital et également en médecine vétérinaire. Un effort de surveillance doit se poursuivre, notamment sur la consommation des antibiotiques dans les établissements de santé, et des études épidémiologiques devraient être approfondies sur un thème qui est essentiel à la santé publique.
Suivi des ventes de médicaments vétérinaires contenant des antibiotiques en France en 2002
En 2002, en France, 1295 tonnes d'antibiotiques ont été vendues sous forme de spécialités de médicaments vétérinaires. On constate que quatre familles d'antibiotiques (Tétracyclines, Sulfamides, Bêta-lactamines, Macrolides) représentent près de 81,4 % du tonnage d'antibiotiques vendus.
Les tétracyclines représentent, à elles seules, 46,4 % du total des ventes.
Près de 86,8 % des ventes d'antibiotiques ont été réalisées pour des présentations orales ; la voie parentérale représente 11,9 % et les autres voies 1,3 %.
92,3 % du tonnage d'antibiotiques vendus est destiné aux animaux dont les produits sont destinés à la consommation humaine (animaux consommables), 1,18 % est destiné aux animaux de compagnie et 6,54 % sont administrés à la fois aux animaux consommables et aux animaux de compagnie sur la base de l'AMM.
Une analyse de l'évolution des ventes entre 1999 et 2002 a été effectuée. Les ventes d'antibiotiques ont fortement diminué (- 6,23 %) en France entre 2001 et 2002 pour atteindre un niveau de 1,75 % inférieur à celui de 1999. Cette diminution ne s'explique que partiellement par une diminution de la population animale totale (- 3,15 % exprimée en kg de poids vif).
La diminution observée est essentiellement due à celles des ventes de Sulfamides et de tétracyclines malgré l'augmentation des Macrolides.
Seules les quantités d'antibiotiques utilisés par voie intra-mammaire restent stables, les quantités d'antibiotiques utilisés par les autres voies d'administration ont diminué.
L'interprétation des chiffres de ventes par espèce est rendue difficile par le fait qu'un même médicament vétérinaire peut être destiné à plusieurs espèces animales.
Chez les bovins et les porcins la diminution de la quantité d'antibiotiques corrigée par l'évolution de la population est relativement importante (bovins - 9,9 %, porcins - 7%). On constate par contre une augmentation (données corrigées par l'évolution de la population) chez les volailles (11,5 %), les poissons (13,9 %) et les animaux de compagnie (8,1 %).
Face à l'augmentation progressive de la résistance bactérienne aux antibiotiques et en l'absence de nouvelles molécules, un bon usage de l'antibiothérapie est une nécessité qui s'impose à tous les médecins, quels que soient leur mode d'exercice et leur spécialité.
La prescription d'un traitement antibiotique n'est pas aisée. Elle requiert un diagnostic précis, le choix d'un traitement validé et excluant toute contre-indication, des modalités de prescription visant à une efficacité maximale et à la meilleure tolérance possible du ou des antibiotiques choisis, sans négliger leur impact écologique et leur coût. Le nombre important d'antibiotiques disponibles rend ces critères de choix encore plus complexes.
Les modalités de toute antibiothérapie doivent être soigneusement exposées, par le médecin prescripteur, au patient qui la reçoit, condition indispensable à une observance optimale.
La France est le pays européen où la consommation des antibiotiques est la plus forte. Un plan national destiné à préserver leur efficacité a été défini en 2001 et se poursuivra jusqu'en 2005 ; il s'inscrit dans un ensemble de mesures telles que la rédaction de Recommandations de Bonnes Pratiques, renforcées par des Conférences de Consensus destinées aux praticiens et des campagnes d'information ciblant le grand public. Cette démarche, dont les premiers résultats semblent encourageants, rejoint les actions européennes déjà mises en oeuvre.
En pratique de ville, l'utilisation excessive des antibiotiques doit être soulignée. Cette situation relève, en particulier, d'un nombre élevé de consultations médicales et de prescriptions d'antibiotiques au cours d'infections respiratoires bénignes, le plus souvent virales. Des innovations telles que le test de diagnostic rapide de l'angine, des recommandations de traitement court pour favoriser une meilleure observance ont déjà apporté la preuve de leur intérêt. Il est essentiel que ces mesures soient développées auprès de tous les praticiens, sous l'égide du Conseil de l'Ordre et des organismes de Formation Médicale Continue, auprès des étudiants, dans le cadre de l'enseignement de la thérapeutique et à l'égard du grand public. Rien ne saurait remplacer le dialogue singulier entre le médecin et son patient. A l'hôpital, une utilisation non contrôlée d'antibiotiques, délivrés à litre curatif ou prophylactique, accroît la prévalence des souches bactériennes multirésistantes, avec le risque de transmission interhumaine de ces souches et d'infections nosocomiales graves. A côté des mesures d'hygiène et d'isolement, qui restent essentielles et des programmes déjà développés dans chaque établissement (Comité de Lutte contre les Infections Nosocomiales, équipe opérationnelle d'hygiène hospitalière, etc.), la promotion du bon usage des antibiotiques a suscité diverses démarches (Conférences de Consensus, publication, en mai 2002, d'une circulaire DHOS/DGS...). Chaque établissement hospitalier doit prendre, en priorité, plusieurs mesures telles que la désignation d'un médecin réfèrent en antibiothérapie, la création d'une Commission des anti-infectieux, l'élaboration de recommandations consensuelles et la mise en place d'un système de dispensation contrôlée. Il est essentiel que ce programme fasse l'objet de dispositions réglementaires et soit respecté par tous les soignants.
Une politique rationnelle d'antibiothérapie ne saurait toutefois se limiter à la seule prescription médicale. Elle doit s'intégrer dans un large ensemble de directives concernant tous les modes d'utilisation des antibiotiques.
Source : Professeur Jacques Frottier







