II. LA PÉNÉTRATION LIMITÉE DES GÉNÉRIQUES EN FRANCE S'EXPLIQUE PAR DIFFÉRENTS FACTEURS
1. Etat des lieux des génériques en France : seulement 26 % du marché du médicament remboursable en volume et 14 % en valeur
En 2012, les génériques représentaient près de 14 % du marché des spécialités remboursables en valeur et plus de 26 % en quantités, soit un peu plus d'une boîte sur quatre. Ces taux ont crû continûment depuis l'introduction effective des génériques à la fin des années 1990. Cependant, on peut noter que la progression a été nettement plus importante en volume qu'en valeur, ce qui révèle - s'il en était besoin - l'intérêt économique du développement des génériques pour les finances publiques. A cet égard, la Cnam évalue à 8,5 milliards d'euros les économies réalisées entre 2002 et 2012 grâce aux génériques du seul fait de la substitution , montant auquel il faut ajouter environ 2 milliards d'euros de baisses de prix des princeps concernés par la commercialisation des génériques.
Evolution de la part des génériques
dans le marché des spécialités
remboursables
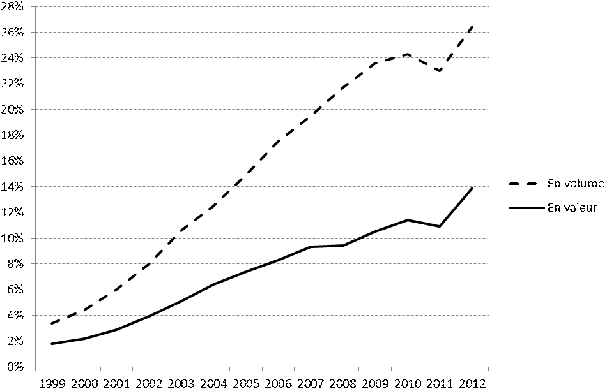
Source : Mecss, d'après données de l'ANSM
Le marché des génériques a particulièrement progressé en 2012 du fait de la réactivation de la mesure « Tiers-payant contre générique » par l'assurance maladie et les pharmaciens : généralisé, ce dispositif constitue une forte incitation financière pour les patients, même si son application ne constitue aucunement un déremboursement.
Aujourd'hui, le taux de pénétration des génériques est particulièrement élevé lorsqu'il est rapporté au seul répertoire (84 % à la fin de 2012). Pourtant, ces médicaments ne représentent que 26 % des volumes du marché total . Il existe donc encore de nombreux princeps qui ne sont pas « inscrits au répertoire », soit pour des raisons juridiques de propriété intellectuelle, soit pour des raisons d'opportunité ; ils ne peuvent donc pas être « génériqués ». En outre, les prescriptions « hors répertoire » sont également élevées ( cf. infra ).
Même si les comparaisons internationales doivent être regardées avec circonspection en raison des champs d'étude parfois différents, elles montrent toutes une marge de progression importante par rapport à la plupart des pays occidentaux. Ainsi, selon une étude citée par l'ANSM, la part de marché des génériques dans celui des médicaments non protégés par un brevet s'élève à 52 % en France contre 71 % au Royaume-Uni, 75 % en Allemagne, 81 % au Canada et 89 % aux Etats-Unis. Certes, les pays « latins » sont dans une situation inverse puisque ce taux de pénétration est proche de 40 % en Espagne et en Italie.
2. Les stratégies des laboratoires pour limiter le développement des génériques
Longtemps, les laboratoires pharmaceutiques qui exploitent des princeps ont logiquement développé des stratégies pour protéger leurs ventes. Ces procédés ont diminué - d'ailleurs, de nombreuses entreprises ont créé des filiales dédiées à la production de médicaments génériques - mais certaines perdurent.
Les laboratoires déposent par exemple une multitude de brevets secondaires peu avant l'expiration du brevet principal, ce qui rend plus complexe et moins sûr juridiquement le développement par un autre industriel du médicament générique correspondant. Des recours en justice, plus ou moins fondés sur des bases sérieuses, peuvent également retarder la mise sur le marché de génériques.
Par ailleurs, les laboratoires peuvent parfois conclure des accords qui, directement ou indirectement, aboutissent à limiter la concurrence ou le développement des génériques.
Surtout, une partie des ressources en recherche et développement de certains laboratoires a été utilisée pour créer des « mee-too » : ces produits, qui n'ont pas tout à fait le même principe actif que le produit initial mais le même profil thérapeutique et qui en sont globalement très proches, sont commercialisés peu de temps avant l'échéance du brevet précédent. Ainsi, ce soi-disant nouveau produit est efficace et rend, par construction, le même service médical que le princeps initial mais il est inutile pour les patients et la collectivité, en n'améliorant pas ce même service médical. Or, du fait des règles d'admission au remboursement et de fixation des prix des médicaments en France, les « mee-too » ont souvent permis d'empêcher en pratique le développement des génériques du premier princeps. Le comité économique des produits de santé (Ceps) prend en compte, depuis peu, cette particularité lors de la fixation du prix.
La stratégie des « mee-too », qualifiée à juste titre par l'Igas de « financement inutile par la collectivité de fausses innovations », n'a pu fonctionner qu'en raison de l'appétence des prescripteurs pour la nouveauté. Or, celle-ci est particulièrement stimulée par le procédé des « visites médicales », part essentielle de la stratégie des laboratoires. Les visiteurs médicaux ne promeuvent auprès des médecins que des médicaments princeps, la communication des laboratoires de génériques s'orientant principalement vers les pharmaciens.
Au-delà de la visite médicale « classique », les laboratoires ont également développé une stratégie plus subtile mais très efficace vis-à-vis des « leaders d'opinion » en santé.
3. La question de la prescription
a) Un cas d'école : les statines
Dans son dernier rapport « charges et produits » cité en annexe, la Cnam met en avant la question de la prescription des statines , médicaments destinés à traiter l'excès de cholestérol dans le sang, qui constituent l'une des plus importantes classes thérapeutiques en France avec 6,4 millions de patients et 1,2 milliard d'euros de remboursements annuels par l'assurance maladie. Cinq molécules sont commercialisées en France, dont quatre sont inscrites au répertoire et sont « génériquées » (atorvastatine 2 ( * ) , simvastatine, pravastatine et fluvastatine) et une ne l'est pas (rosuvastatine 3 ( * ) ).
Déjà en juillet 2010 4 ( * ) , la Haute autorité de santé estimait que, « en termes comparatifs, aucune différence significative n'a été démontrée entre les statines sur le critère de mortalité toutes causes . » En outre, « la hiérarchie des prix constatés n'est pas strictement proportionnelle à la progression de l'efficacité des différentes statines . » La HAS en conclut que, « compte tenu de l'efficacité biologique moyenne des différentes statines en termes de baisse attendue de LDL-c et des prix français de ces molécules en septembre 2010, la prescription d'une simvastatine générique est à envisager en priorité pour les hypercholestérolémies faibles à modérées, avec un dosage adapté à la valeur cible recherchée. » Elle estime que la délivrance de la rosuvastatine n'est à « envisager en priorité » que dans un nombre très limité de cas.
Entre 2010 et 2012, la Cnam a mené une vaste étude portant sur 165 000 patients : elle ne montre pas non plus de différence significative d'efficacité sur la morbimortalité entre la rosuvastatine 5 mg et la simvastatine 20 mg.
Or, la rosuvastatine, seule spécialité non « génériquée », totalise 30 % des volumes prescrits contre 4 % au Royaume-Uni ou 0,5 % en Allemagne ! Dans sept pays européens (Allemagne, Royaume-Uni, Pays-Bas, Italie, Finlande, Norvège et Espagne), cette molécule représente moins de 8 % des volumes.
De ce fait, le coût moyen journalier des traitements par statine est deux fois plus élevé en France qu'en moyenne dans ces pays , alors que l'équivalence thérapeutique des statines est largement démontrée et sans que l'on puisse avancer soit que la population française souffre d'une affection qui nécessite une thérapie particulière par rapport aux autres Européens, soit qu'elle est nettement mieux soignée ainsi...
b) Le choix français de la « substitution » : une fragilité, voire un péché originel
Les volumes de médicaments vendus en France ont moins progressé ces dernières années que dans les autres pays européens mais, partant d'un niveau élevé de consommation, la France se situe encore dans le haut de la moyenne européenne : selon les comptes nationaux de santé pour 2012, la consommation française mesurée en unités standards par habitant reste 22 % supérieure à celle observée dans les pays voisins.
Surtout, la structure des prescriptions reste orientée vers les molécules les plus onéreuses et est défavorable aux médicaments appartenant au répertoire des génériques. La Cnam a ainsi évalué que, pour un ensemble de huit classes thérapeutiques 5 ( * ) , la France connaît le coût moyen de traitement par habitant « de loin le plus élevé » parmi huit pays de comparaison 6 ( * ) .
Cette situation provient largement du choix de ne pas agir dès la prescription du médicament mais au moment de sa délivrance par le pharmacien. La loi de financement de la sécurité sociale pour 1999 a accordé à ce dernier le droit, sous certaines conditions, de substituer au produit explicitement prescrit par le médecin l'un de ses génériques. Un fort intéressement financier, à la fois au niveau de la marge et du prix d'achat, a été décidé pour que les pharmaciens opèrent bien cette substitution ; cette décision ne rend que plus dépendants encore les pharmaciens du volume de boîtes vendues, ce qui n'est guère satisfaisant.
La politique de « substitution » a bien permis le développement important du médicament générique, mais elle présente de redoutables inconvénients : sans accompagnement particulier, elle ne peut qu'instiller un doute dans l'esprit du patient, qui ne se voit pas délivrer le « bon médicament », tandis que le médecin, largement écarté de la procédure, n'est guère incité à modifier ses prescriptions. Certes, les conventions médicales successives ont mis en place quelques dispositifs incitatifs pour améliorer la qualité de la prescription mais les résultats sont très lents.
La plupart des autres pays ont adopté des politiques différentes, souvent plus directives vis-à-vis des médecins : par exemple, la prescription obligatoire en « dénomination commune internationale » (DCI), c'est-à-dire avec le nom de la molécule et non le nom commercial du produit, permet de lever largement les doutes du patient sur le produit finalement délivré.
Une politique basée sur la seule substitution ne peut qu'entamer la confiance des médecins et des patients dans le médicament générique ; elle explique largement les prises de position de certains leaders d'opinion, relayées par nombre de media, sur la qualité de ces médicaments, la France étant d'ailleurs le seul pays à connaître ces polémiques récurrentes.
c) La prescription hospitalière
Si le marché du médicament se concentre dans les pharmacies de ville (23 milliards d'euros de dépenses remboursées en 2011), les prescriptions par les médecins hospitaliers en constituent un déterminant essentiel. Ces derniers agissent en effet comme des « primo-prescripteurs » pour de nombreux traitements, dont les plus coûteux car concernant des pathologies lourdes ou des phases aiguës de la maladie, les médecins de ville procédant au renouvellement de la prescription. En outre, les médecins hospitaliers jouent plus généralement un rôle de « leader » d'opinion en santé.
Depuis plusieurs années, la croissance du marché est alimentée par les médicaments de spécialités destinés aux pathologies lourdes et graves (cancer, sida, hépatites, DMLA...), alors que les dépenses liées aux maladies chroniques ou saisonnières tendent à diminuer du fait du développement des génériques ou des baisses de prix décidées par les pouvoirs publics. La Cnam a ainsi estimé qu'en 2009, 70 % de la croissance des dépenses de médicaments délivrés en officine provient en fait des prescriptions hospitalières.
Or, alors que le prix des médicaments est « administré » pour la délivrance en pharmacie, les établissements de santé procèdent à des appels d'offres et les entreprises consentent souvent des prix très bas, voire fournissent des médicaments quasi-gratuitement . Dans les classes très concurrentielles comme les statines, les niveaux de remise sont très élevés : le prix médian d'une dose journalière est divisé par sept en CHU par rapport à celui en officine pour les inhibiteurs de l'enzyme de conversion (IEC).
Certains laboratoires ont d'ailleurs pu, là aussi, mettre en place des stratégies agressives visant à limiter le développement des génériques. La société GlaxoSmithKline a par exemple été sanctionnée en mars 2007 par le Conseil de la concurrence, mais cette décision a été réformée par la Cour d'appel de Paris, notamment au regard de la définition exacte du marché concerné, arrêt confirmé par la Cour de cassation 7 ( * ) . Dans son communiqué de presse, le Conseil de la concurrence utilisait des termes particulièrement sévères : « Le laboratoire Glaxo a vendu, en 1999 et 2000, un produit à un prix inférieur à ses coûts afin de dissuader les génériqueurs d'entrer efficacement sur le marché hospitalier. [...] Les prix proposés par Glaxo sur ce médicament [ont] eu un caractère prédateur . [...] Un prix prédateur est un prix anormalement bas, c'est-à-dire inférieur aux coûts variables de l'entreprise qui le pratique. Le mécanisme de prédation est le suivant : l'entreprise offre dans un premier temps des prix très bas dans le but d'évincer ou de décourager l'arrivée de la concurrence sur un marché donné. Une fois la concurrence éliminée, l'entreprise peut alors remonter ses prix et récupérer les pertes consenties pendant la première phase, au détriment du consommateur. »
Finalement, établissements de santé et laboratoires trouvent chacun un intérêt au fonctionnement actuel : les premiers bénéficient de prix bas, y compris pour certains médicaments innovants et théoriquement coûteux, ce qui est bénéfique pour les finances publiques ; les seconds influencent un marché plus large par un mécanisme qui peut s'apparenter à du « dumping » dans certaines situations, ce qui pénalise de ce point de vue les finances publiques.
Ainsi, la Drees a récemment montré une corrélation significative entre les référencements de médicaments dans un CHU et leur poids dans les prescriptions des médecins libéraux exerçant dans son bassin d'attraction : plus le CHU utilise un médicament donné, plus celui-ci est consommé dans cette zone.
* 2 Par exemple commercialisée par Pfizer sous le nom Tahor en France.
* 3 Commercialisée en France par Astrazeneca sous le nom Crestor.
* 4 « Efficacité et efficience des hypolipémiants - Une analyse centrée sur les statines ».
* 5 Antibiotiques, antidiabétiques oraux, asthme et BPCO, hypocholestérolémiants dont statines, antihypertenseurs, antidépresseurs, anxiolytiques et antiulcéreux (IPP).
* 6 France, Italie, Espagne, Allemagne, Finlande, Norvège, Pays-Bas et Royaume-Uni.
* 7 Décision 07-D-09 du 14 mars 2007, puis arrêt de la Cour d'appel de Paris du 8 avril 2008 et arrêt de la Cour de cassation du 17 mars 2009.







