II. S'APPRÊTANT À SORTIR DES LABORATOIRES, LES « ALIMENTS CELLULAIRES » SONT DES PRODUITS ENCORE MÉCONNUS, QUI SUSCITENT LE SCEPTICISME EN FRANCE
A. UN SEGMENT DES « PROTÉINES ALTERNATIVES » EN PLEIN ESSOR TECHNIQUE ET ÉCONOMIQUE, MAIS SANS PRESQUE AUCUN PRODUIT COMMERCIALISÉ À CE JOUR
1. Les « aliments cellulaires », une famille d'aliments aux caractéristiques et aux procédés de fabrication variés, mais développant une même idée
a) Une protéine alternative d'origine animale, à distinguer de trois autres familles de « protéines alternatives »
Les entreprises développant des « aliments cellulaires » insistent sur le fait qu'il s'agit de « produits d'origine animale, directement à partir de cellules animales », mais que « la viande grossit en dehors de l'animal » (Mark Post, co-fondateur de Mosa Meat). Co-fondateur et PDG de l'entreprise israélienne Aleph Farms, le français Didier Toubia a en audition présenté les aliments cellulaires comme une troisième catégorie distincte, entre la viande à proprement parler et les produits d'origine animale tels que le fromage ou le miel.
Il est théoriquement possible de reproduire tout produit d'origine animale, y compris des espèces exotiques (lion, éléphant...) ou de compagnie (chat, chien...) la technologie étant « hautement transférable » d'une espèce à l'autre, selon un document de travail de la FAO7(*) publié en 2022. Certaines entreprises travaillent déjà simultanément sur plusieurs espèces, comme Meatable, qui développe du porc et du boeuf. Les entreprises Mosa Meat et Gourmey, cherchant respectivement à reproduire du boeuf et du foie gras cellulaires, ont indiqué à la mission vouloir développer d'autres viandes dans le futur.
À l'origine de nombreux fantasmes, les « aliments cellulaires » est cependant souvent évoquée dans le débat public de façon abstraite, aucun produit n'étant commercialisé en Europe. Cela favorise les confusions avec trois autres familles de protéines alternatives, que sont, des plus proches aux plus éloignés, les produits par fermentation de précision, les analogues végétaux et les insectes :
· les « aliments cellulaires » font partie d'un ensemble plus large, appelé par ses promoteurs « industrie cellulaire ». Cette famille comprend aussi la fabrication de produits d'origine animale, comme le blanc d'oeuf, la caséine (une protéine du lait) ou même le cuir, par fermentation de précision, une technologie qui comporte certains points communs avec les aliments cellulaires (prolifération cellulaire, bioréacteurs), mais demeure différente en ce qu'elle n'utilise pas de cellules animales à proprement parler. Les produits par fermentation de précision entrent dans le champ du règlement européen « nouveaux aliments » en tant que « nouveaux procédés de production », nécessitant une autorisation de mise sur le marché, puisqu'il s'agit de denrées dont la consommation était négligeable avant 1997 (cf. I, B, 1, a) ;
La fermentation de précision :
plus prometteuse, mais moins médiatique que les « aliments cellulaires »
Moins médiatique que les aliments cellulaires, la fermentation de précision n'en est pas moins une technique beaucoup plus avancée, les premiers produits étant commercialisés aux États-Unis depuis 2020, et ayant fait l'objet de levées de fonds très importantes ces dernières années. Selon le Good Food Institute, ce sont plus de 900 millions de dollars qui ont été levés en 2021 dans ce domaine. Technique ancestrale, la fermentation a connu ses premières ruptures technologiques dans les années 1980 avec la production de l'insuline suivant ce procédé. Dans le domaine alimentaire, des enzymes et vitamines furent développées, les enzymes permettant notamment de faire cailler le fromage pour créer de la présure artificielle. Aujourd'hui, grâce aux techniques de bio-ingénierie, il devient possible de « programmer » des micro-organismes pour produire une vaste palette de molécules utilisables dans de nombreux processus de productions alimentaires. Le lait est particulièrement concerné par cette innovation, par l'intermédiaire de la production de caséine, à tel point que certaines projections pour les États-Unis anticipent un effondrement de la production de lait « classique » de 90 % d'ici 20358(*). D'autres productions telles que le fromage, le boeuf ou encore le cuir seraient également bouleversées. La fermentation de précision permettrait en outre de faire baisser drastiquement les coûts de production d'aliments cellulaires, en fournissant des facteurs de croissance à moindre coût.
En France, trois entreprises se sont positionnées sur ce segment : Bon Vivant, Nutropy et Standing Ovation, cette dernière ayant réalisé une levée de fonds de 12 millions d'euros en 2022, avec un procédé permettant de produire de la caséine. Fin 2022, elle a noué un partenariat stratégique avec le groupe Bel, distributeur des marques Babybel, Kiri ou encore Boursin.
· Les « aliments cellulaires » sont à distinguer clairement des substituts végétaux à la viande (steaks de soja, etc.), produits à base d'oléagineux (soja), de protéagineux (lentilles, fèves, etc.) ou de fruits à coque (noix de cajou) qui ne sont pas de la viande et ne prétendent pas l'être, si ce n'est qu'ils en reprennent certains codes et la forme. Ces alternatives sont développées en France par des entreprises telles que La Vie ou Les Nouveaux Fermiers, et aux États-Unis par l'entreprise Beyond Meat. Puisqu'elles sont issues d'ingrédients déjà régulièrement consommés, elles n'ont pas besoin d'autorisations de mise sur le marché au titre du règlement européen « nouveaux aliments » et sont déjà disponibles à la vente ;
· enfin, les confusions sont plus rares avec les insectes qui sont consommés depuis longtemps dans diverses parties du monde, mais pas au sein de l'UE, ce qui nécessitera de passer par une autorisation de mise sur le marché au titre du règlement « nouveaux aliments ». Avec trois sociétés, Ynsect, Innovafeed et Agronutris, la France est l'un des leaders mondiaux de ce marché, dont les plus gros volumes semblent davantage orientés vers l'alimentation animale que vers l'alimentation humaine.
Si ces catégories doivent être distinguées intellectuellement pour une bonne compréhension des protéines alternatives, il n'en reste pas moins que la fabrication de produits issus de combinaisons entre certaines de ces familles est très plausible, pour des raisons aussi bien techniques (texture) que de coût (bien moindre pour les analogues végétaux que pour les « aliments cellulaires »).
Ainsi, les premières bouchées de poulet commercialisées à Singapour par la société Upside Foods sont déjà un « hybride » entre des cellules de poulet et des analogues végétaux. Les entreprises européennes travaillent, de même, sur un produit composé entre 10 et 50 % de matière végétale.
b) Les dénominations usuelle, réglementaire et commerciale des « aliments cellulaires » ne sont pas fixées
(1) Dans le langage courant, parmi plusieurs termes candidats, la mission privilégie le terme « aliments cellulaires »
Au début de ses travaux, le syntagme « viande in vitro » a été préféré par la mission d'information à celui de « viande artificielle » ou « viande de synthèse », la notion d'artificialité étant difficile à définir9(*).
Les travaux de la mission lui ont toutefois permis de constater que le produit était en passe de sortir des laboratoires pour entrer dans les ateliers de fabrication. Elle a donc cherché une autre dénomination usuelle que « viande in vitro » parmi les termes en circulation.
Commune en anglais, la notion de « viande propre » (clean meat) ne s'est pas imposée en français ; elle est, du reste, mensongère, et dénigre implicitement la viande issue de l'élevage. La mission ne juge donc pas pertinent de la retenir.
En anglais, ce sont les termes « cultivated meat » (« viande cultivée ») qui semblent s'être imposés dans le langage courant. Ces termes peuvent cependant prêter à confusion avec les analogues végétaux. Les termes « cultured meat » (« viande de culture ») prêtent en outre à confusion avec la fabrication de yaourt ou l'aquaculture et devraient donc être évités.
Dans un document de travail paru en 202210(*), la FAO identifie « cell-based food » (« alimentation à base de cellules » ou « alimentation cellulaire ») comme étant la dénomination la plus descriptive et la plus neutre pour décrire le produit. Par conséquent, la mission retient dans le présent rapport cette dénomination générique d'« aliments cellulaires ».
(2) En l'état actuel du droit, l'usage du terme « viande » ne semble pas interdit pour ce type de produits
Les deux seules mentions des aliments cellulaires dans le droit alimentaire de l'UE11(*) et de la France12(*) font référence, dans les mêmes termes, à des « denrées alimentaires qui se composent de cultures cellulaires ou tissulaires dérivées d'animaux ou qui sont isolées ou produites à partir de cultures cellulaires ou tissulaires dérivées d'animaux ».
Cette dénomination est a priori exclusive des catégories qui lui préexistaient d'autant que, comme le rappelle Mme Anne-Marie Vanelle, inspectrice générale honoraire de la santé publique vétérinaire, la catégorie « viandes » désigne depuis 1984 « les parties comestibles des animaux visés aux points 1.2 à 1.8 [ongulés domestiques, volailles, lagomorphes, petit et gros gibier sauvage, gibier d'élevage, y compris le sang13(*) ».
Toutefois, ces différentes références juridiques aux « aliments cellulaires » et à la viande conventionnelle ne concernent la dénomination de ces produits que de façon incidente14(*). Comme le confirme le bureau des viandes du ministère de l'agriculture et de la souveraineté alimentaire, il n'est donc pas certain que la définition donnée des viandes par le règlement de 1984 ait une portée juridique allant au-delà du champ de ce règlement, et, partant, qu'elle constitue la dénomination légale de la catégorie.
C'est pourquoi, en l'état actuel du droit15(*), rien ne semble empêcher explicitement d'apposer le terme « viande » sur ces « denrées alimentaires composées de cultures cellulaires ».
(3) Contestée par les filières de production animale, la dénomination commerciale « viande » devrait être exclue au profit d'« aliments cellulaires »
La catégorie usuelle « aliments cellulaires », retenue par la mission par commodité ne sera sans doute pas, pour autant, la dénomination commerciale de ce produit.
Elle est en effet contestée autant par les promoteurs de l'industrie cellulaire - pour qui le terme « cellulaire », rarement associé à l'alimentation, véhiculerait un imaginaire peu attrayant - que par ses critiques - selon qui les cellules musculaires ainsi développées ne peuvent prétendre être appelées « viande ».
MM. Hocquette, Chriki et Mme Ellies-Oury considèrent qu'il faudrait en toute rigueur parler de « cellules musculaires cultivées » ou de « fibres musculaires cultivées », d'autres composants du muscle comme les nerfs, les vaisseaux sanguins, et le collagène qui compose la trame conjonctive étant souvent absents du produit.
Les filières de productions animales, réunies en table ronde et représentées par le collectif « Les Z'Homnivores », ont insisté sur la nécessité de refuser la dénomination commerciale « viande » pour les produits à base de cellules, au motif que ce serait sinon accepter une forme de « colonisation du langage ».
Le terme « viande » n'étant, du reste, pas même pour les produits de l'élevage utilisé comme une dénomination commerciale sur les emballages des produits, son interdiction pour les produits de l'industrie cellulaire ne devrait pas avoir d'impact économique majeur.
S'agissant de la forme du produit, le législateur a entendu interdire l'utilisation des « dénominations utilisées pour désigner des denrées alimentaires d'origine animale [...] pour décrire, commercialiser ou promouvoir des denrées alimentaires contenant des protéines végétales », lorsque ces denrées dépassent une certaine part de protéines végétales16(*). Le décret d'application de cette disposition17(*) a été suspendu18(*) à l'occasion d'un recours en référé de l'association Protéines France19(*), pour deux motifs qui semblent davantage porter sur la forme du décret, que sur le fond :
- d'une part, le champ des dénominations interdites (« terminologie spécifique de la boucherie, de la charcuterie ou de la poissonnerie » et « dénomination d'une denrée alimentaire d'origine animale représentative des usages commerciaux ») n'était pas assez clairement défini ;
- d'autre part, les entreprises d'analogues végétaux auraient dû, dans un délai très rapide, « modifier la dénomination d'un grand nombre de leurs produits, y compris en renonçant à des appellations parfois utilisées de longue date ou installées dans l'esprit des consommateurs ».
Le ministère de l'agriculture et de la souveraineté alimentaire indique qu'un nouveau décret est en cours d'élaboration. Bien qu'applicable aux seuls analogues végétaux, cette disposition législative de protection des filières animales pourrait de façon relativement aisée être étendue aux « aliments cellulaires », si cela était jugé pertinent.
S'agissant des noms des espèces et groupes d'espèces animales d'origine, les dénominations faisant référence « à la morphologie ou à l'anatomie animale » pourraient de même être interdites si cela était jugé pertinent. Cependant, les entreprises du secteur insistent bien sur le fait que ce sont, à proprement parler, des cellules de l'espèce en question. Elles soulignent que le produit cellulaire « peut présenter le même niveau de risques de réactions allergiques20(*) » que le produit issu de l'élevage, et que le nom de l'espèce devrait par conséquent figurer sur l'emballage de façon visible. Par ailleurs, dans leur majorité, les végétariens ne consommeraient pas ce produit, qu'ils assimilent bien à de la viande.
En résumé, sur les étiquettes des produits préemballés en grande surface, la dénomination commerciale pourrait être « poulet/boeuf/crevette cellulaire » comme, du reste, le préconise la FAO dans son document de travail publié en 202221(*).
c) L'application à l'alimentation de biotechnologies issues notamment de la recherche médicale
Les « aliments cellulaires » sont le fruit de recherches en ingénierie tissulaire. Ce champ de recherche visait au départ des applications plutôt médicales, par exemple en régénération des tissus pour les grands brûlés.
Cette technologie étant en phase de recherche et développement, il convient de souligner la diversité des techniques de production expérimentées et des produits finis recherchés. Comme l'a indiqué le cofondateur et président de Gourmey Nicolas Morin-Forest lors de la table ronde, « il y a mille et une façons de produire de la viande de culture ».
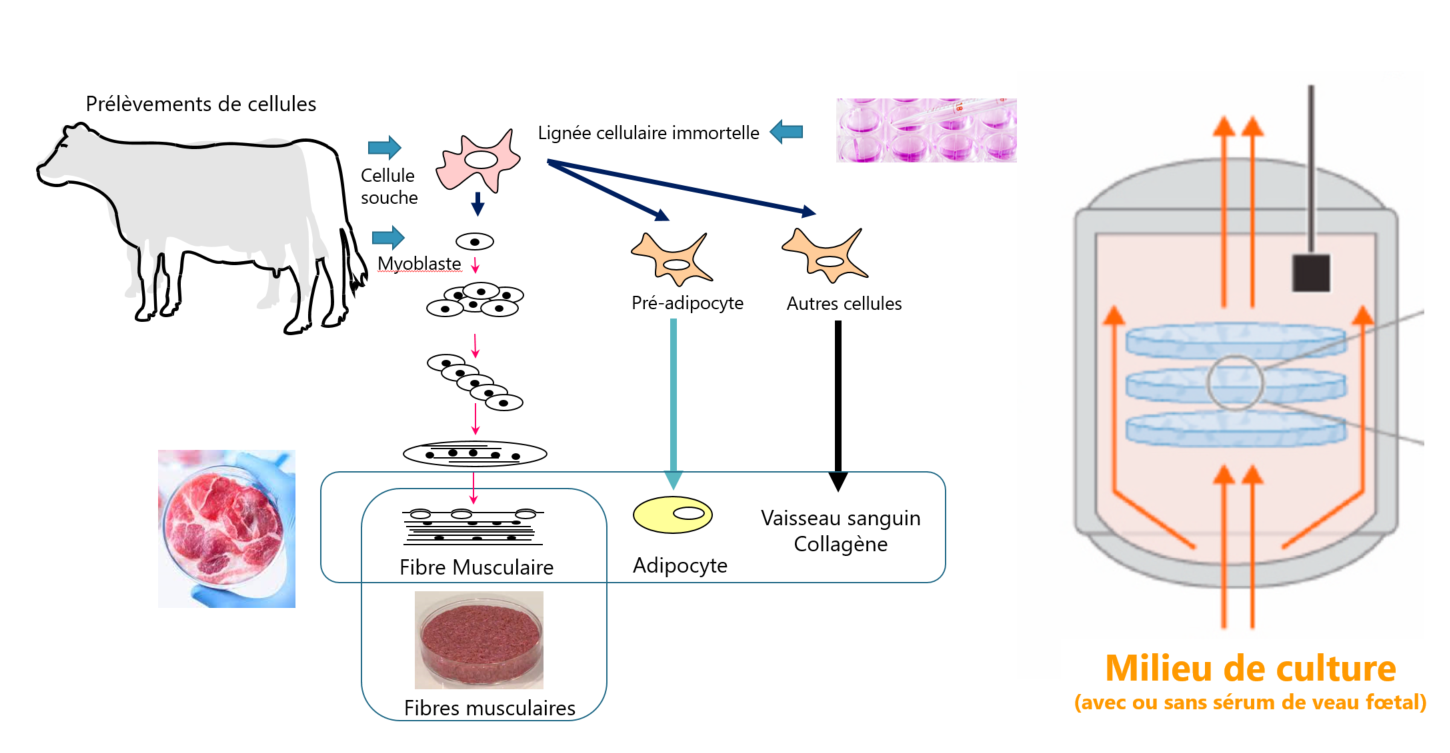
Toutefois, le procédé de fabrication d'aliments cellulaires implique invariablement quatre étapes, voire une cinquième selon les typologies :
1) des cellules sont conservées congelées dans des banques de cellules. Elles peuvent provenir :
o soit de biopsies régulières (prélèvement d'un échantillon de tissu) sur un animal d'élevage, auquel cas il peut s'agit de cellules souches, pluripotentes22(*), ou de myoblastes (précurseurs du tissu musculaire)
o soit de lignées cellulaires (cellules possédant la capacité de se reproduire indéfiniment) ;
2) puis, placées dans un bioréacteur (ou fermenteur) avec un milieu de culture composé d'une cinquantaine de nutriments (cf. I, A, 1, d) et en particulier des facteurs de croissance, les cellules se différencient, c'est-à-dire qu'elles se spécialisent, par exemple en fibres musculaires (myotubes) ou de gras ;
3) vient ensuite l'étape de la prolifération dans ce même bioréacteur, maintenu à température physiologique (autour de 37 ° C pour un mammifère, moins pour les animaux aquatiques). Un lot placé dans un bioréacteur de 40 litres, 200 litres ou plus, prend en moyenne quelques semaines, et au moins 15 à 20 jours environ, pour arriver à maturité.
o Quand une pièce d'« aliments cellulaires » pure est visée (c'est-à-dire quand elle n'est ni un simple ingrédient, ni destinée à entrer dans la composition d'un hybride avec du végétal), un échafaudage (« scaffold ») d'origine végétale peut fournir, dans le bioréacteur, une structure permettant aux tissus de s'organiser. La « co-culture » de cellules musculaires et adipeuses est aussi, de plus en plus, recherchée, pour reproduire la complexité d'une pièce de viande conventionnelle.
4) Dans la mesure où la prolifération cellulaire fonctionne par duplication, il s'agit d'un processus exponentiel, l'essentiel de la production ayant lieu dans les derniers jours. À la fin de cette étape, un bioréacteur peut contenir jusqu'à plusieurs millions de cellules par millilitre. Vient alors l'étape de la récolte des fibres musculaires, de la graisse, des vaisseaux sanguins ou des tissus conjonctifs ;
5) enfin, les cellules récoltées connaissent un processus de transformation alimentaire classique, pour prendre la forme, par exemple, d'un steak, de boulettes ou de nuggets.
Source : contribution de MM. Hocquette, Chriki et de Mme Ellies-Oury
Au-delà de la biologie cellulaire, il semblerait que la production puisse impliquer d'autres procédés, notamment moléculaires ou informatiques. À titre d'exemple, en février 2021, l'entreprise Aleph Farms a fabriqué un « faux-filet » en 3D, et l'entreprise chilienne NotCo utilise le machine learning pour la production de ses analogues végétaux.
d) La « boîte noire » du milieu de culture et de ses intrants
Le secret est bien gardé par les entreprises sur cet élément indispensable à la prolifération et à la différenciation des cellules, à tel point que plusieurs entreprises indiquent ne pas souhaiter déposer de brevet sur leur milieu de culture pour ne pas révéler un avantage compétitif.
Il faut dire qu'il existe à peu près autant de « recettes » que d'entreprises, et qu'au sein d'une même entreprise, différentes compositions sont testées pour chaque nouveau lot puisque les entreprises en sont encore au stade de la R&D. En outre, les entreprises du secteur ont rapidement fait évoluer la composition des milieux de culture, ceux-ci constituant jusqu'alors la quasi-totalité des coûts de production.
La présence de sérum foetal bovin et de facteurs de croissance dans les milieux de culture
Alors que les milieux de culture utilisés dans la recherche médicale et pharmaceutique étaient classiquement composés de sérum foetal bovin (cf. II, A, 2, b), réputé pratique car concentrant une grande partie des nutriments nécessaires à la croissance cellulaire, des considérations de coût et de bien-être animal ont conduit à rechercher des alternatives dites « sans sérum », à base de végétaux (hydrolysats d'orge, de champignons, d'algues...). Une publication démontrant l'existence d'alternatives a été publiée dans la revue Nature23(*) en 2022.
Même ce qui semblait indispensable à la culture cellulaire ne semble plus l'être tout à fait. Ainsi, plusieurs entreprises du secteur indiquent ne pas être loin de pouvoir se passer de protéines recombinantes voire pouvoir, d'ores et déjà, s'en passer. Les facteurs de croissance (dont l'insuline et les hormones de la thyroïde) sont un type de protéine recombinante classiquement utilisé pour aider à diriger la différenciation cellulaire. Les entreprises indiquent travailler sur une forme de « sevrage » des cellules, qui limiterait fortement, voire rendrait inutile, l'utilisation de ces facteurs de croissance. En tout état de cause, ces facteurs de croissance sont à distinguer, selon M. Hocquette, des hormones de croissance, telles que les stéroïdes. Les entreprises françaises indiquent ne pas utiliser celles-ci, dont l'usage est interdit au sein de l'Union européenne pour l'élevage, en dépit d'une zone grise.
En dépit de cette évolution rapide, il n'en reste pas moins quelques invariants.
De façon constante, les milieux de culture sont composés à 95 % d'eau. Pour le reste, les composants nécessaires sont au nombre « de 30 à 50 » selon l'une des entreprises interrogée, et de l'ordre « de dizaines » selon une autre.
C'est parmi les protéines que les variations sont les plus importantes d'un procédé de fabrication à l'autre. L'albumine ou les transferrines sont ainsi présentes en quantité variable.
Sont nécessairement présents également des acides aminés, dont ceux dits « essentiels » au bon développement des cellules, dont le nombre peut varier en fonction de l'espèce (vingt pour le boeuf, douze pour le porc, onze pour le poulet). Ces acides aminés sont notamment présents sous la forme de peptides.
Des acides gras et du cholestérol entrent également dans la composition des milieux de culture.
Sont enfin ajoutés des sels minéraux, qui ont la même odeur caractéristique que ceux ajoutés dans les rations des bovins pour complémenter leur alimentation. Parmi ces minéraux, on peut trouver le soufre, le fer, le chlore, le chrome, le cobalt, le cuivre, le zinc, le manganèse, le molybdène, l'iode et le sélénium.
2. Le produit est aujourd'hui exclusivement développé par des entreprises, dont le principal défi dans les prochaines années sera de passer à une échelle industrielle
a) Environ 110 entreprises dans plus de vingt pays à travers le monde
Les premières entreprises ont été fondées en 2015 aux États-Unis et en 2016 en Europe. D'après Cellular Agriculture Europe, aujourd'hui, « il existe environ 110 entreprises dans le monde qui travaillent sur différentes espèces et utilisent différentes technologies et nutriments. » La majorité de ces entreprises sont des start-up ou, dans certains cas, des filiales de plus grands groupes, dans plus d'une vingtaine de pays. En Europe, il existe aujourd'hui une quinzaine d'entreprises, dont les intérêts sont représentés par Cellular Agriculture Europe.
Le Good Food Institute, think tank américain spécialisé dans l'étude et la promotion des protéines alternatives, dont les aliments cellulaires, conduit un recensement régulièrement mis à jour de ces entreprises à travers le monde24(*).
Source : Kind Earth Tech25(*) ( http://protein.ketmaps.com/)
(1) En l'absence presque complète de produit commercialisé...
Les équipes des entreprises travaillent à la pré-production des « aliments cellulaires » et préparent les autorisations de mise sur le marché.
Bien que la technologie soit au départ la même, les ambitions de ces entreprises ne sont pas les mêmes.
En raison de leur antériorité, de leur taille, de leur important travail de communication et de relations publiques pour l'acceptation du projet et de leur horizon à très long terme, Mosa Meat et Aleph Farms apparaissent davantage comme des « majors » européens. Ces deux entreprises ont pour point commun de procéder par biopsies et non par lignées cellulaires, de chercher à reproduire des pièces de viande entières et de viser le marché européen.
Le modèle de Meatable et de Vital Meat, semble reposer davantage sur des succès rapides en matière de commercialisation, avec en ligne de mire des marchés plus faciles d'accès, tels que le singapourien.
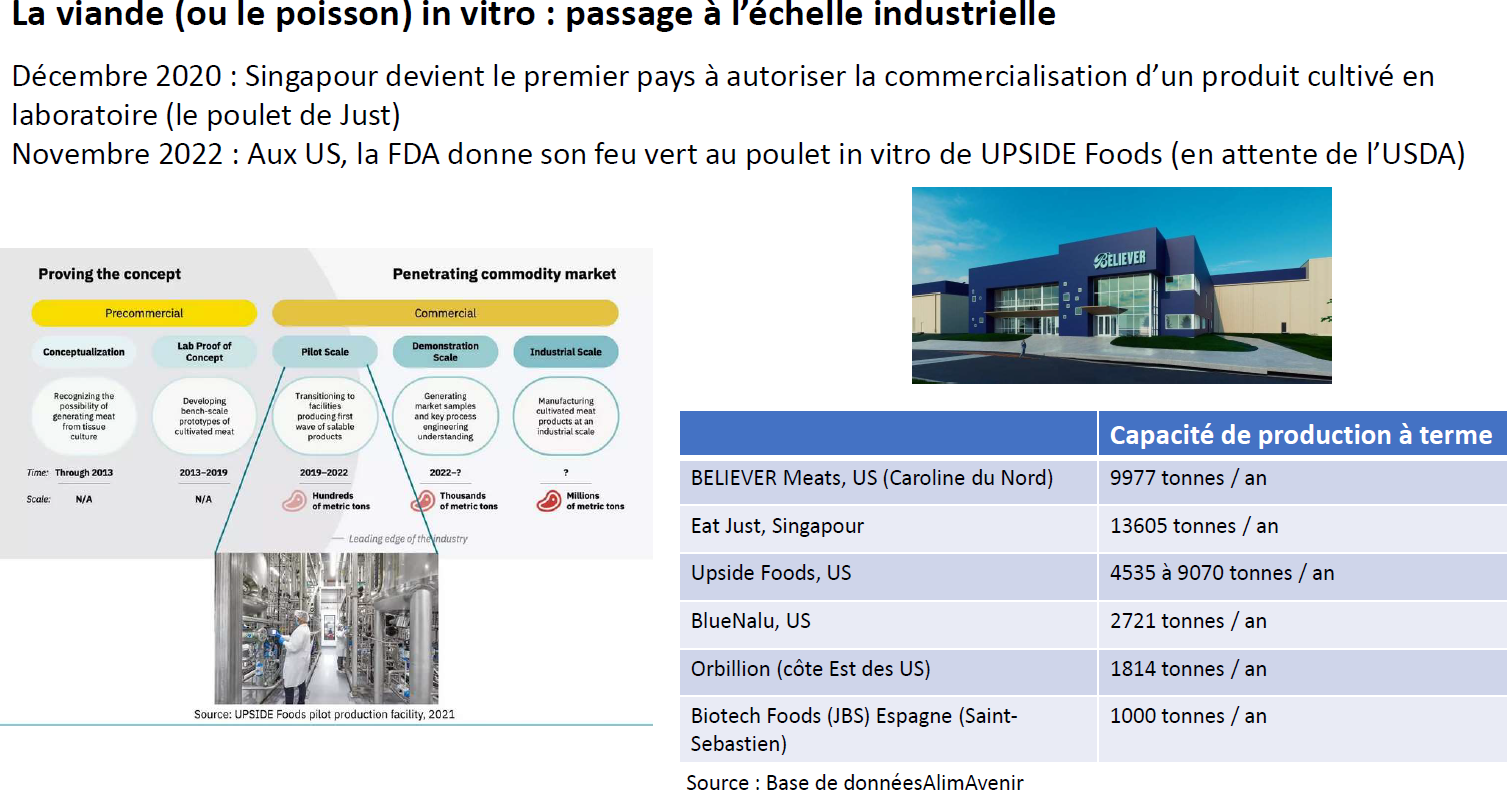
Les entreprises américaines se sont positionnées comme les acteurs dominants du point de vue de la commercialisation. Le premier produit commercialisé dans le monde26(*) l'a été à Singapour en décembre 2020 par une filiale de l'entreprise Eat Just (San Francisco, Californie). Une nouvelle autorisation a été accordée en janvier 2023 à cette même entreprise, à Singapour, pour le même produit, avec un procédé de fabrication cette fois « serum free » (cf. II, A, 2, b). En novembre 2022, aux États-Unis, une pré-approbation a été accordée au poulet cellulaire de l'entreprise Upside Foods (Berkeley, Californie), par la FDA, en attendant une approbation par le ministère américain de l'agriculture. En mars 2023, l'entreprise Eat Just a obtenu une pré-approbation similaire aux États-Unis.
Pour justifier l'absence de demande d'autorisation de leur part, les entreprises européennes rencontrées soulignent qu'il faut être « plus que prêt » pour déposer un dossier et se livrent difficilement à des pronostics.
Quoi qu'il en soit, la commercialisation du produit à une échelle industrielle prendra nécessairement plusieurs années.
Source : Mosa Meat
(2) ... des entreprises essentiellement financées par des levées de fonds
La production d'« aliments cellulaires » reste un projet très risqué en raison de nombreuses incertitudes techniques et réglementaires. En outre, en l'absence de produit commercialisé, les entreprises du secteur ne réalisent aucun chiffre d'affaires pendant plusieurs mois voire plusieurs années.
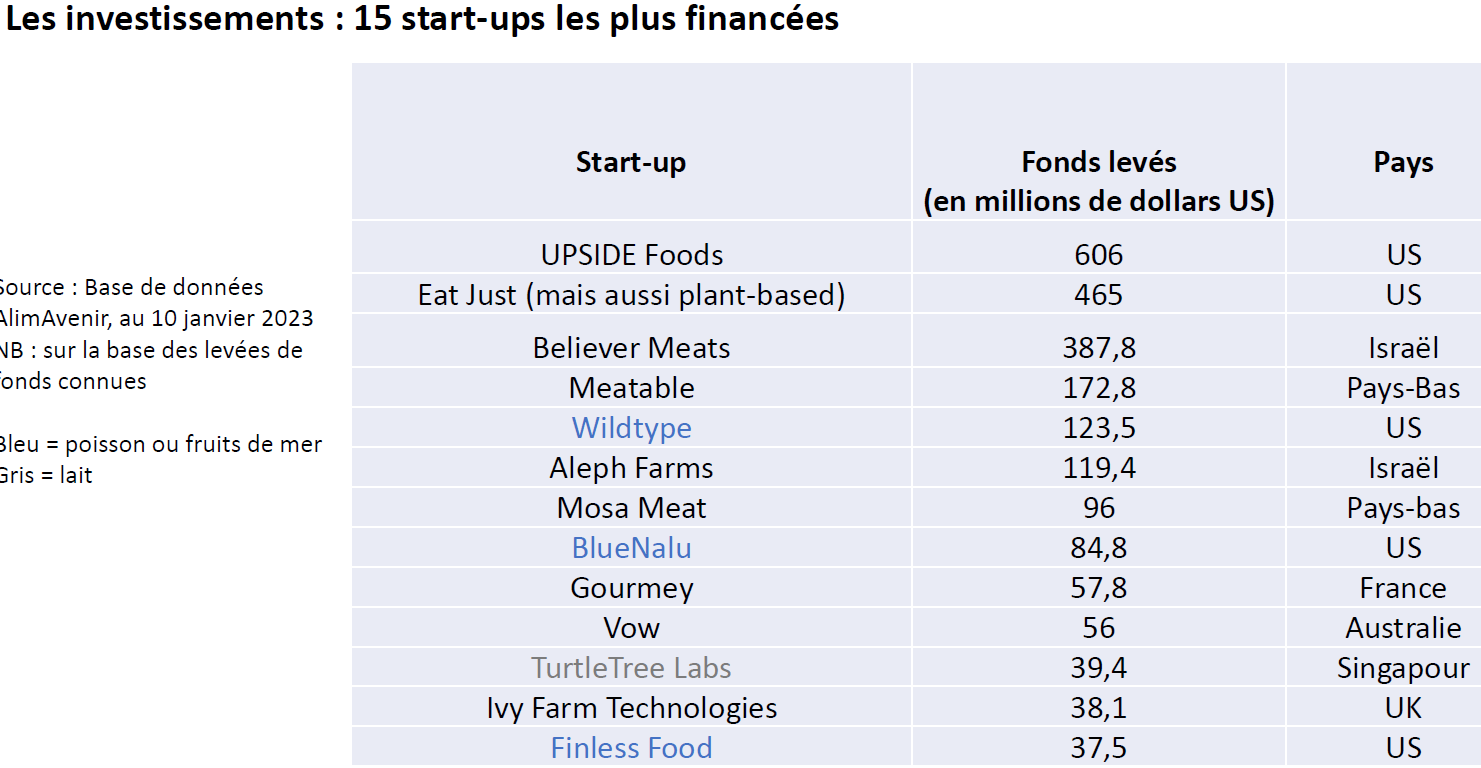
Pour se développer, ces entreprises recourent donc en majorité à des levées de fonds grâce au capital-risque. Selon un décompte effectué par la consultante spécialiste des protéines alternatives, Mme Céline Laisney, « une quarantaine de start-up ont levé au total 2,6 milliards d'euros », dont la moitié aux États-Unis. Parmi celles-ci, les principales sont référencées dans le tableau ci-dessous :
Source : Céline Laisney
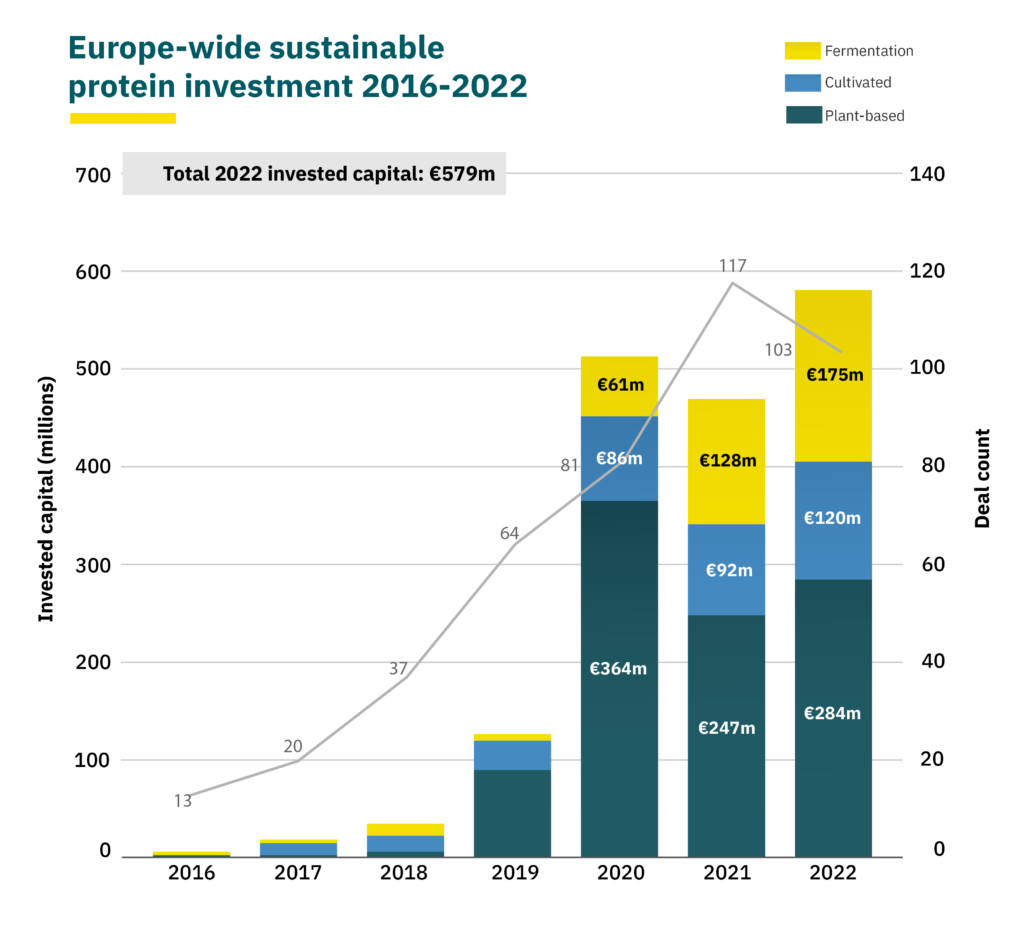
Selon les données les plus récentes du Good Food Institute, think tank d'analyse et de promotion des protéines alternatives, les entreprises européennes d'« aliments cellulaires » ont attiré 120 millions d'euros en 2022, après 92 millions d'euros en 2021.
Source : Good Food Institute Europe27(*) [sur l'échelle de
droite,
le nombre d'investissements dans les protéines
alternatives]
À titre d'exemple, l'entreprise Gourmey a levé environ 48 millions d'euros en octobre 2022 auprès de fonds européens en capital-risque.
Mosa Meat avait levé environ 85 millions de dollars en février 2021, précisant qu'en plus des fonds de capital-risque, plusieurs des investisseurs sont des « partenaires industriels de long terme » apportant, en plus des capitaux, leur savoir-faire, comme Bell (viande), Nutreco (alimentation animale) ou Merck (pharmaceutique).
En Israël, Aleph Farms a levé environ 105 millions de dollars auprès de grandes entreprises mondiales de l'alimentation et notamment de la viande, dont Migros, Thai Union, BRF et CJ CheilJedang.
Ces investissements servent notamment au recrutement d'équipes, à l'acquisition des intrants, des équipements et des bâtiments, ainsi qu'aux dépenses courantes.
Si, dans le monde, la plupart des entreprises n'emploient pas plus de 10 à 20 salariés (c'est par exemple le cas de l'entreprise Vital Meat), on compte parmi les membres de Cellular Agriculture Europe des équipes désormais plus importantes : les néerlandaises Mosa Meat (165 employés) et Meatable (plus de 90 employés), l'israélienne Aleph Farms (155 employés), les françaises Gourmey (« plus d'une centaine de personnes d'ici à l'année prochaine »).
Les sites industriels, en cours de construction ou au stade de projet, nécessitent des investissements en capital fixe importants.
b) La production à l'échelle industrielle pose de nouveaux défis techniques et sociétaux
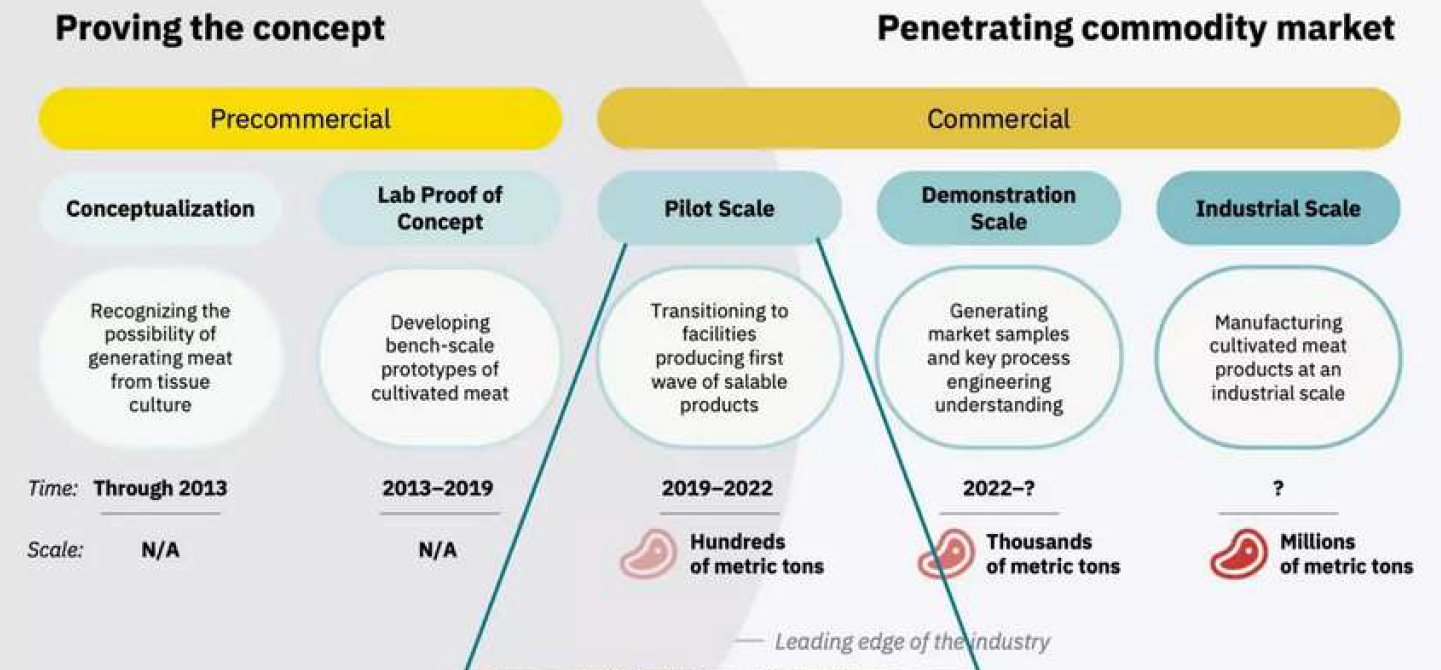
(1) Après les prototypes dans les laboratoires et les ateliers-pilotes, de premiers sites industriels s'apprêtent à voir le jour
La mission d'information a pu se rendre dans les laboratoires et ateliers-pilotes d'entreprises françaises (Vital Meat) et néerlandaises (Mosa Meat et Meatable), à un moment charnière entre l'étape de la R&D en laboratoire et les prémices de l'industrialisation.
La visite de ces installations a permis de mesurer le degré variable d'avancement de ces entreprises, ainsi que la similarité, du moins apparente, des équipements et des procédés de fabrication.
L'entreprise Mosa Meat à Maastricht a ainsi montré un nouveau bâtiment qui est en cours d'aménagement pour la production à plus grande échelle d'« aliments cellulaires ».
L'entreprise Gourmey prépare, elle, la construction d'un atelier de production de 4 300 m2 dans le Val-de-Marne, qui emploierait 80 personnes, en vue de la commercialisation de son produit. Vital Meat indique projet un site industriel d'une surface équivalente.
Les capacités de production actuelles ou projetées les plus importantes sont toutefois aux États-Unis.
Source : Céline Laisney
La taille des bioréacteurs est communément retenue comme un jalon de l'avancée technologique des entreprises, quand bien même la quantité produite, en général de quelques centaines de kg/an, n'en est pas une preuve formelle dans cette phase encore expérimentale.
Il semble que la plupart d'entre elles travaillent sur des bioréacteurs de 40 ou de 200 litres pour les lots qui seront candidats à une approbation réglementaire.
Toutefois, les entreprises ne se communiquent pas cette information les unes les autres, et il y aurait, de l'aveu de certaines d'entre elles, une course à la communication, en particulier aux États-Unis, afin de lever les fonds d'investisseurs potentiels.
(2) En changeant d'échelle, la production pourrait changer non seulement de degré, mais aussi de nature
La mise à l'échelle (scale-up) est toujours une étape délicate pour une start-up, car il n'est pas certain que le design industriel donnant de bons résultats à petite échelle soit reproductible à une plus grande échelle.
Passer du stade de l'expérimentation scientifique à la production de masse constitue d'abord un défi technique.
Il en va ainsi de l'augmentation de la taille des bioréacteurs employés, aujourd'hui de taille variable, mais qui ne devraient pas dépasser dans les premières étapes 30 à 50 000 litres. Dans le monde médical, le maximum habituel est de 20 000 litres, et dans le domaine de la fermentation alcoolique, les cuves les plus grandes peuvent dépasser 125 000 litres. L'entreprise Gourmey confirme que « des bioréacteurs allant jusqu'à 40 000 litres sont possibles, mais pas encore des bioréacteurs de 100 000 ou 200 000 litres », parlant à ce sujet de « blocage technique » et de « défi d'ingénieur ». Le poids exercé par l'eau sur les cellules pourrait par exemple ralentir leur prolifération.
Au-delà de ces blocages techniques, et en dépit de probables économies d'échelle liées à l'industrialisation, celle-ci risquerait d'annuler certains avantages que les preuves de concept laissent entrevoir, en matière économique, sanitaire ou environnementale.
C'est notamment le cas en ce qui concerne la répartition de la valeur, ces nouveaux acteurs industriels pouvant acquérir un pouvoir de marché très important. Une production à si grande échelle poserait en outre la question de la concentration du risque sanitaire ou du volume des déchets industriels à traiter.
3. La cartographie des soutiens et financeurs de l'alimentation cellulaire montre à quel point les logiques à l'oeuvre dans son développement peuvent différer
Rattachée à la commission des affaires économiques, la mission d'information sur les aliments cellulaires a cru bon de s'intéresser aux sources de financement de celle-ci.
Or, il est rapidement apparu qu'en plus des espérances de profit au fondement de toute entreprise, des motivations de nature plus philosophique, liées à l'impact que le développement d'aliments cellulaires pourrait avoir sur le bien-être animal et l'environnement, occupaient une place prééminente parmi les motivations des entrepreneurs et des investisseurs.
En cherchant à savoir qui soutenait les aliments cellulaires, la mission d'information a ainsi été conduite à se demander pourquoi elle était soutenue.
a) À l'origine, une démarche de valorisation de leur recherche par des scientifiques entrepreneurs
L'idée des « aliments cellulaires » provient de recherches conduites dans des laboratoires et des universités publics. L'innovation a ensuite suivi les étapes classiques de la valorisation par des chercheurs qui se sont alors mués en entrepreneurs.
C'est aux Pays-Bas que le premier brevet a été déposé par un chercheur, Willem van Eelen, en 1999. Une première preuve de concept a été présentée en 2013, à Londres, par M. Mark Post, chercheur de l'université de Maastricht. Ce dernier a co-fondé l'entreprise Mosa Meat en 2016, qui est désormais l'une des principales dans le monde.
En France, deux des trois co-fondateurs de Gourmey sont des biologistes, et l'entreprise est hébergée à Évry par le Génopole, pôle de compétitivité spécialisé dans les biotechnologies. De même, la société Aleph Farms a été cofondée par un professeur du Technion - Institut de technologie d'Israël et un incubateur.
b) La prégnance d'un militantisme inspiré de l'altruisme efficace qui contribue à attirer les investisseurs
L'argument de l'impact sociétal maximal est classiquement destiné à emporter l'adhésion d'investisseurs s'inscrivant dans une démarche de responsabilité sociale et environnementale.
On peut noter chez les promoteurs des « aliments cellulaires28(*) » l'influence particulièrement forte de l'altruisme efficace29(*), transposé notamment à l'écologie et au bien-être animal. Très compatible avec la recherche d'impact présente dans la philanthropie contemporaine, cette éthique contribue à attirer les investisseurs (cf. I, A, 3, c).
(1) Le souci de la condition des animaux de rente est bel et bien présent dans le développement des « aliments cellulaires »
Dès les premiers développements des « aliments cellulaires », l'espérance de réduire voire d'éliminer la souffrance animale était présente chez M. Jacob Van Eelen, le chercheur néerlandais qui dirigeait l'équipe ayant conduit les premières recherches en la matière. Elle demeure au centre de l'argumentaire des entreprises du secteur.
L'innovation a par ailleurs attiré l'attention de penseurs et de militants de la cause animale, et suscité l'adhésion de personnalités inspirées par ce courant.
Philosophe reconnue de la cause animale, Mme Florence Burgat estime ainsi que la consommation de viande par l'être humain tient d'abord à des raisons symboliques, liées à la réaffirmation d'une différence de statut avec l'animal et, partant, que les « aliments cellulaires » serait un moyen efficace de maintenir la « fiction » de cette différence par la consommation de viande, sans abattage d'animaux.
Chez les associations de protection animale dites « welfaristes30(*) », l'impression qui prédomine est celle d'une « curiosité bienveillante » envers le produit, mais sous certaines conditions (cf. II, A, 2).
Chez les associations « abolitionnistes », l'association américaine PETA, ainsi que ses sections européennes, se dit explicitement favorable au développement des aliments cellulaires, considéré comme une solution de substitution à la viande d'élevage. L'association belge GAIA est, de même clairement en faveur du produit.
Étonnamment, l'attention médiatique s'est focalisée sur la seule association n'ayant, explicitement, pas pris position en faveur des aliments cellulaires, L214.
L'association est décrite par les filières de productions animales, par M. Luneau ou par Mme Porcher comme « préparant le terrain » des entreprises développant des « aliments cellulaires » et est parfois accusée de faire directement la promotion de ce produit. Les allégations visant L214 ne sont toutefois jamais claires, et renvoient toujours à un soutien par « porosité » ou par « transitivité31(*) ».
Interrogée plusieurs fois par les rapporteurs à ce sujet, L214 a répondu que ce n'est « pas plus fondé que d'accuser les associations qui promeuvent le vélo pour réduire les émissions des véhicules thermiques d'être instrumentalisées par les “industriels des voitures électriques”. »
Les dirigeants de L214 ont même décliné l'invitation de la mission en raison du « manque de lien avéré entre [les aliments cellulaires] et l'objet de [leur] association », soulignant que « rien ne démontre avec certitude à ce jour que le développement de ce type de produits contribuerait à la réduction du nombre d'animaux abattus à des fins de consommation ».
A ce jour, donc, rien ne prouve le soutien de l'association L214 à l'« alimentation cellulaire ».
(2) Les motivations relatives à la préservation de l'environnement semblent avoir peu à peu pris une importance croissante
L'idée que les « aliments cellulaires », plus efficients en ressources, permettraient de réduire grandement l'impact environnemental de la production de viande, est devenue un lieu commun de la communication des entreprises du secteur.
On peut toutefois noter une difficulté de positionnement de la part des associations environnementales.
Leur opinion dominante est que l'industrie cellulaire n'est pas un enjeu immédiat, mais plutôt un horizon lointain, voire un « chiffon rouge » qui serait agité pour ne pas parler de la réalité de l'élevage aujourd'hui et éluder la nécessité de le réformer radicalement pour respecter nos engagements climatiques.
Ainsi, selon M. Cannet, directeur du plaidoyer de WWF, « en matière de protection du climat et de la biodiversité, les solutions clefs à explorer et les marges de manoeuvre à exploiter résident surtout dans la modification de nos régimes alimentaires, de nos systèmes agraires et des pratiques de production agricoles. Sans ces avancées, la viande in vitro apparaît comme une fuite en avant technique, sans remise en cause de l'industrialisation croissante de l'agroalimentaire et le recours excessif aux calories d'origine animale. »
Les aliments cellulaires constitueraient, selon cette vision, une forme de « technosolutionnisme ».
Cependant, un courant « éco-optimiste », émergent bien que minoritaire au sein du mouvement écologiste, s'intéresse de façon croissante à cette innovation, en particulier dans les pays anglo-saxons selon plusieurs associations. On peut citer dans cette catégorie l'éditorialiste anglais Georges Monbiot32(*).
c) Technophiles et inspirés par ces causes, plusieurs riches investisseurs soutiennent le développement des aliments cellulaires
L'idée que les aliments cellulaires seraient financés voire développés par les Gafam ou la Nasa revient régulièrement dans le débat public, sur fond de suspicion à l'égard des États-Unis, qui mèneraient une guerre culturelle ou informationnelle contre l'Europe, sa culture, et notamment la place particulière qu'elle réserve à l'élevage et à l'alimentation.
Ces allégations relèvent dans bien des cas de l'extrapolation.
Il est vrai que la NASA a financé en 2002 M. Morris Benjaminson, professeur dans une université new-yorkaise, pour expérimenter la culture de tissus musculaires de poisson, afin de rechercher une nouvelle source d'alimentation pour les astronautes, dans le cadre d'un programme abandonné depuis lors.
Il est vrai aussi que plusieurs entrepreneurs des nouvelles technologies de l'information et de la communication ont soutenu ou soutiennent le développement des aliments cellulaires :
- influencé par le transhumanisme, Sergueï Brin, l'un des cofondateurs de Google et actuel président du groupe Alphabet, a co-financé le premier burger présenté au monde par Mark Post en 2013 à Londres ;
- Bill Gates, fondateur de Microsoft, et Richard Branson, fondateur de Virgin, ont investi dès les premières étapes dans Memphis Meat, devenue Upside Foods ;
- Dustin Moskovitz, l'un des cofondateurs de Facebook, a, dix ans après avoir quitté l'entreprise, accordé plusieurs subventions, via l'Open Philanthropy Project33(*), sa fondation à impact social, au think tank d'analyse et de promotion des protéines alternatives, le Good Food Institute. La fondation a toutefois exprimé ses doutes quant à la capacité du secteur à surmonter le défi de la production à un coût suffisamment compétitif34(*). Elle a même clairement indiqué préférer investir dans les analogues végétaux et « ne pas donner la priorité à l'investissement dans la R&D pour la viande cultivée, en particulier pour la viande entière (c'est-à-dire pas la viande hachée) parce qu'[elle pense] que la faisabilité technique est actuellement faible (en particulier en ce qui concerne l'obtention de coûts suffisamment bas35(*)). »
De façon générale, la Californie est une terre d'élection naturelle pour cette innovation, autant culturellement par l'appétence qui y existe pour les nouvelles technologies, que pour des raisons économiques, le capital-risque y étant très développé. Basé dans la baie de San Francisco, comme les entreprises Upside Foods et Eat Just, le podcast “Cultured Meat and Future Food36(*)” témoigne de cette fascination.
Toutefois, Bill Gates, fondateur de Microsoft, Jack Dorsey, cofondateur de Twitter, Jeff Bezos, fondateur d'Amazon ou encore Alexis Ohanian, cofondateur de Reddit ont tous investi dans des entreprises produisant des analogues végétaux, mais il ne semble pas qu'ils aient investi dans les aliments cellulaires, de même qu'en France, Xavier Niel, fondateur de Free et Marc Simoncini, fondateur de Meetic.
Engagé dans la protection de l'environnement, l'acteur Leonardo DiCaprio a investi dans Mosa Meat en septembre 2022 et est même devenu « conseiller » de l'entreprise à cette occasion37(*), après avoir précédemment investi dans les analogues végétaux.
Mêlant préoccupations pour le bien-être animal, l'environnement, et probablement l'espérance de retours sur investissement, un certain nombre de célébrités du sport (Serena Williams, Roger Federer, Lewis Hamilton, Sergio Busquets...) et du spectacle (Oprah Winfrey, Natalie Portman, Jessica Chastain, Jay-z, Katy Perry, Rihanna...)38(*) avaient, eux, investi dans les analogues végétaux.
d) Les acteurs traditionnels du marché de la viande prennent des participations en suivant une logique de diversification de leurs activités traditionnelles
La dernière catégorie d'acteurs intervenant dans le financement de cette technologie est plus rarement mentionnée dans le débat public.
Il s'agit des groupes de production et de transformation de viande, dont beaucoup des plus importants à l'échelle mondiale ont des participations dans le développement des aliments cellulaires.
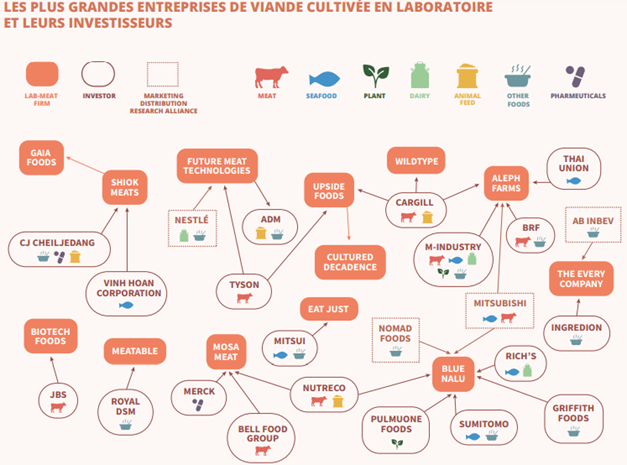
Le think tank IPES Food retrace dans son rapport très documenté, « Politique des protéines39(*) », la multiplicité des liens capitalistiques entre les entreprises des « aliments cellulaires » et les acteurs établis du secteur de la viande et des produits de la mer. IPES Food s'inquiète de la concentration croissante de la production de protéines dans le monde, tant pour la viande et les analogues végétaux que pour les « aliments cellulaires ».
Source : IPES Food, La Politique des protéines, 2022.
Parmi ces groupes traditionnels du secteur de la viande ayant investi dans les « aliments cellulaires », on retrouve :
· le géant brésilien du boeuf JBS ;
· le géant américain du boeuf Tyson ;
· le transformateur de viande brésilien BRF ;
· le canadien Maple Leaf ;
· le suisse Bell Food Group ;
· l'allemand PHW-Gruppe ;
· le transformateur de produits de la mer Thai Union.
On peut ranger dans cette catégorie le groupe Grimaud frères, implanté dans le Maine-et-Loire, qui est l'un des leaders européens de la génétique animale, non seulement pour les volailles et les palmipèdes, mais aussi pour le porc, les lapins, les crevettes, les insectes et les mouches, avec des applications notamment dans la recherche médicale40(*).
On trouve aussi de grands groupes alimentaires plus diversifiés, tels que les Américains Cargill et Archer-Daniels-Midland (ADM), ou encore des entreprises spécialisées dans l'alimentation animale, telles que le néerlandais Nutreco. Le fabricant de tofu Pulmuone entre aussi dans cette catégorie. On peut souligner enfin que le groupe Nestlé est « membre associé » de Cellular Agriculture Europe, l'association représentant les intérêts des entreprises d'aliments cellulaires, de la même façon que des groupes laitiers ont noué des partenariats avec des start-up de la fermentation de précision.
La prégnance de ces acteurs rend le tableau du financement des « aliments cellulaires » plus complexe à appréhender, et peut même s'avérer déconcertante pour ceux qui verraient avant tout un intérêt environnemental et en termes de bien-être animal de cette innovation.
Il semble clair en effet que les acteurs traditionnels du marché de la viande ont investi dans une recherche de diversification de leurs activités :
· il peut s'agir, tout simplement, de la perspective de nouveaux débouchés et de revenus importants si la technologie s'avérait viable à grande échelle ;
· il peut s'agir, aussi, d'« acquisitions tueuses » de jeunes pousses par des acteurs établis, dans une logique analogue à celle que l'on peut trouver dans le domaine des biotechnologies et des nouvelles technologies de l'information et de la consommation. Dans ce schéma, un acteur ayant des parts de marché significatives sur un marché peut être tenté de barrer l'entrée sur ce marché de nouveaux acteurs pour échapper à la concurrence.
* 7 https://www.fao.org/3/cc2241en/cc2241en.pdf
* 8 Think-tank RethinkX, Rethink Food and Agriculture 2020-2030, 2019
* 9 La viande d'élevage est elle-même le fruit d'un long processus d'amélioration génétique. En outre, il serait difficile de prétendre, par exemple, que la viande issue d'élevage en feed-lots soit particulièrement naturelle.
* 10 https://www.fao.org/3/cc2241en/cc2241en.pdf
* 11 Article 3 du règlement (UE) n° 2015/2283 du Parlement européen et du Conseil du 25 novembre 2015 relatif aux « nouveaux aliments ». https://eur-lex.europa.eu/legal-content/FR/TXT/PDF/ ?uri=CELEX :32015R2283
* 12 Article 230-5 du code rural et de la pêche maritime, depuis l'entrée en vigueur de l'article 254 de la loi n° 2021-1104 du 22 août 2021 portant lutte contre le dérèglement climatique et renforcement de la résilience face à ses effets.
* 13 Annexe I du règlement (CE) n° 853/2004 du Parlement européen et du Conseil fixant des règles spécifiques d'hygiène applicables aux denrées alimentaires d'origine animale. https://eur-lex.europa.eu/LexUriServ/LexUriServ.do ?uri=OJ :L :2004 :139 :0055 :0205 :fr :PDF
* 14 Les deux définitions de la « viande cellulaire » ont pour objet de l'assujettir à un régime d'autorisation préalable, et de l'exclure de la restauration collective publique ; la définition des « viandes » figurant simplement dans l'annexe d'un règlement européen relatif aux règles d'hygiène de ces denrées.
* 15 En effet, « la dénomination de la denrée alimentaire est sa dénomination légale. En l'absence d'une telle dénomination, la dénomination de la denrée est son nom usuel. À défaut d'un tel nom ou si celui-ci n'est pas utilisé, un nom descriptif est à indiquer » (article 17 du règlement (UE) n° 1169/2011 concernant l'information des consommateurs sur les denrées alimentaires)).
* 16 Article L. 412-10 du code de la consommation, introduit par l'article 5 de la loi n° 2020-699 du 10 juin 2020 relative à la transparence de l'information sur les produits agricoles et alimentaires.
* 17 Décret n° 2022-947 du 29 juin 2022 relatif à l'utilisation de certaines dénominations employées pour désigner des denrées comportant des protéines végétales.
* 18 Conseil d'État, juge des référés, 27/07/2022, n° 465 844. https://www.legifrance.gouv.fr/ceta/id/CETATEXT000 046 112 967 ?init=true&page=1&query=n %C2 %B0+ 465 844&searchField=ALL&tab_selection=all
* 19 Association professionnelle regroupant de grands groupes agricoles et coopératifs français producteurs de protéines végétales (parmi lesquels Avril, Limagrain, Roquette, Tereos, Vivescia, Happyvore, Herta, La Vie, Soufflet, Terrena, Olga, Ynsect...).
http://www.proteinesfrance.fr/fr/membres
* 20 Hallman et Hallman, 2020, cité dans le document de travail de la FAO publié en 2022.
* 21 https://www.fao.org/3/cc2241en/cc2241en.pdf
* 22 C'est-à-dire qu'elles ont le potentiel de devenir n'importe quelle partie de l'organisme.
* 23 https://www.nature.com/articles/s43016-021-00419-1
* 24 https://gfi.org/resource/cultivated-meat-eggs-and-dairy-state-of-the-industry-report/
* 25 À noter que toutes les entreprises ne sont pas nécessairement répertoriées dans ce tableau. Par exemple, Vital Meat ne figure pas sur cette représentation, peut-être en raison de son statut de filiale d'un autre groupe. La start-up Fudsz, tout récent troisième acteur du secteur en France n'y figure pas non plus, et n'est, du reste, pas représentée par Cellular Agriculture Europe.
* 26 Des nuggets de poulet cellulaire, à Singapour, en 2020.
* 27 https://gfieurope.org/blog/2022-sustainable-protein-investment/
* 28 Les parcours de certains des promoteurs les plus actifs de l'alimentation cellulaire en France, comme MM. Tom Bry-Chevalier, ancien bras droit de la direction de Gourmey et qui rédige une thèse sur l'impact environnemental de ces produits, et Nicolas Bureau, président de l'association Agriculture Cellulaire France, témoignent directement ou indirectement de cette inspiration.
* 29 Éthique conséquentialiste et utilitariste inspirée du philosophe Peter Singer, l'altruisme efficace vise à maximiser le bien-être collectif, non par les actions les plus morales, mais par celles qui produiront le plus grand effet.
* 30 On désigne par « welfaristes » les associations qui ne sont pas opposées à l'élevage en tant que tel mais qui cherchent à améliorer le bien-être des animaux d'élevage, par des aménagements. Entendues en table ronde, l'oeuvre d'assistance aux bêtes d'abattoir (OABA), la fondation droit animal (LFDA) et Welfarm entrent dans cette catégorie.
* 31 Il en est ainsi du financement de L214 par l'Open Philanthropy Project, une fondation qui a aussi financé le secteur des protéines alternatives.
* 32 Jan. 2016, “Lab-grown food will soon destroy farming - and save the planet”, The Guardian https://www.theguardian.com/commentisfree/2020/jan/08/lab-grown-food-destroy-farming-save-planet
* 33 Cette même fondation a octroyé des financements aux associations Compassion in World Farming ( https://www.openphilanthropy.org/grants/ ?q=compassion %20in %20world %20farming) et L214 ( https://www.openphilanthropy.org/grants/ ?q=l214), parmi d'autres organismes militant pour éliminer les pires pratiques de l'élevage. C'est sur ce fondement que plusieurs filières animales ont cherché à établir un lien entre associations animalistes et entreprises développant des aliments cellulaires.
* 34 https://www.openphilanthropy.org/research/animal-product-alternatives/
* 35 https://www.openphilanthropy.org/grants/impossible-foods-rd-investment/
* 36 https://podcasts.apple.com/us/podcast/cultured-meat-and-future-food-podcast/id1364 668 720
* 37 https://mosameat.com/blog/leonardo-dicaprio-invests-in-mosa-meat
* 38 https://foodmatterslive.com/gallery/tech-moguls-sports-personalities-and-celebrities-investing-in-plant-based-food-companies/
* 39 https://ipes-food.org/_img/upload/files/PolitiqueDesProteinesFR.pdf
* 40 Sa filiale Valneva avait par exemple développé un vaccin contre le Covid-19.