TROISIÈME PARTIE :
LA STRATÉGIE « TESTER -
TRACER - ISOLER »
À L'ÉPREUVE DES FAITS
I. TESTER PLUS, TESTER MIEUX : UNE POLITIQUE EN QUÊTE D'EFFICACITÉ
Si lors de la gestion des premiers foyers localisés de circulation du virus la stratégie « tester-tracer-isoler » visant à casser les chaînes de contamination a été mise en place avec une certaine efficacité, la parcimonie des tests disponibles au moment du pic épidémique a été, avec le problème criant de la pénurie de masques - quoique dans une moindre mesure -, au coeur des débats du printemps et n'a pas rendu possible, comme dans la plupart des pays, la poursuite de cette stratégie.
Dans un second temps, la forte montée en puissance de la capacité diagnostique s'est heurtée à la question de son organisation : au-delà des objectifs ambitieux affichés - et atteints - en termes de nombre de tests réalisés, c'est l'efficience d'une politique peinant à identifier sa cible et ses priorités et à s'inscrire dans une prise en charge globale qui concentre les interrogations et, à la veille de la « deuxième vague », remet en question la capacité à la freiner.
A. LE TEMPS DE LA PARCIMONIE : ENTRE MANQUE D'ANTICIPATION, CONTRAINTES TECHNIQUES ET PESANTEURS ORGANISATIONNELLES, UNE MONTÉE EN CHARGE LENTE DES CAPACITÉS À TESTER
1. Un déploiement hésitant et laborieux : le « retard à l'allumage » de la politique de tests dans un contexte de fortes tensions sur les approvisionnements
a) La conception précoce d'une technique de détection des cas initialement destinée aux seuls laboratoires hospitaliers
Quelques jours après le partage par les autorités chinoises - le 11 janvier 2020 - de la séquence complète du génome du SARS-CoV-2, le centre national de référence (CNR) des virus des infections respiratoires (dont la grippe) de l'institut Pasteur, à l'instar d'autres équipes internationales (comme celles de l'hôpital La Charité à Berlin), met en place mi-janvier une technique de détection du virus par RT-PCR ( cf. encadré).
La technique de détection du SARS-CoV-2 par RT-PCR
La réaction de RT-PCR ( reverse transcriptase-polymerase chain reaction ), est un test nucléotidique ou test moléculaire qui permet de détecter la présence dans un prélèvement biologique de l'ARN du virus .
Ce test a été le premier disponible pour diagnostiquer le SARS-CoV-2 car il peut être rapidement développé sur la base de la séquence du virus.
Il comporte une première étape d'extraction de l'ARN du virus qui est ensuite transformé en ADN par une enzyme transcriptase réverse (RT). Cette enzyme prend l'ARN comme modèle pour synthétiser une séquence d'ADN dit complémentaire (ADNc). L'ADNc du virus, si celui-ci est présent dans le prélèvement, est ensuite fortement amplifié par une réaction de polymérase en chaîne (PCR) quantitative.
Cette réaction a lieu en trois phases : une dénaturation de l'ADNc par chauffage pour séparer les deux brins qui le composent, une hybridation des amorces aux extrémités de la séquence recherchée, puis une élongation grâce à l'action d'une enzyme ADN polymérase. Les amorces sont des séquences d'ADN simple brin spécifiques du virus. Ce sont elles qui garantissent la spécificité de la réaction d'amplification. Seuls les brins d'ADNc fixant ces amorces sont amplifiés.
La durée d'un cycle de PCR est de l'ordre d'une minute. Il est répété pour obtenir une multiplication de la séquence d'ADN cible. C'est cette phase d'amplification qui confère au test RT-PCR une très haute sensibilité.
Le test doit être réalisé en laboratoire et nécessite un matériel sophistiqué. En fonction de son automatisation, il prend entre trois et six heures (déballage et étiquetage des échantillons, inactivation du virus, extraction de l'ARN, RT-PCR, validation...). Un résultat n'est donc souvent disponible qu'en 24 heures.
Sa fiabilité dépend de nombreux facteurs, en premier la qualité du prélèvement. Celui-ci doit être réalisé assez profondément dans les cavités nasales du patient à l'aide d'un grand coton-tige ou écouvillon (prélèvement naso-pharyngé). Il a cependant été observé que le virus pouvait être indétectable dans les voies respiratoires supérieures, mais présent dans les poumons. En conséquence, on estime que la fiabilité du test RT-PCR, malgré sa très haute spécificité (? 100 %) et sensibilité, n'est que de 60-80 % pour identifier un individu infecté. Cette fiabilité décroît avec le temps car le virus est éliminé par la réponse immunitaire. Elle n'est plus que de 40-50 % entre 15 et 39 jours post infection. Ce pourcentage est similaire à celui des tests de détection par RT-PCR du virus influenza .
Source : D'après « Covid-19 : comment fonctionnent les tests et quelles sont leurs utilités ? », Eric Muraille, biologiste et immunologiste, The Conversation , 22 avril 2020
Le 24 janvier 2020, les prélèvements effectués sur les trois premiers cas français de patients suspectés (deux à Paris, un à Bordeaux) conduisent à confirmer l'efficacité du processus d'analyse. Comme l'a relevé Agnès Buzyn, cette expertise a alors valu à la France un « satisfecit de l'Europe » , le centre européen de prévention et de contrôle des maladies 505 ( * ) saluant alors la marque d' « un haut degré de préparation pour prévenir et contrôler de possibles infections au coronavirus » 506 ( * ) .
À partir de ces échantillons biologiques, le séquençage complet du virus est établi puis partagé par l'institut Pasteur les 29-30 janvier vers les 38 laboratoires de niveau 3 (P3) des établissements de santé de référence pour la prise en charge des patients covid-19 507 ( * ) .
Concrètement, le nombre de laboratoires hospitaliers disposant de la technique diagnostique passe de 6 à 20 entre le 31 janvier et le 21 février , à un moment où les plus grandes opérations de diagnostic concernent les français rapatriés de Wuhan (tests réalisés par l'IHU de Marseille) et le cluster des Contamines-Montjoie (cas contacts testés à Lyon).
Le niveau d'exigence en termes de sécurité biologique des laboratoires, adapté aux virus hautement pathogènes et appliqué par analogie avec le diagnostic des SARS-CoV ou MERS-CoV, est abaissé après l'avis favorable de la Société française de microbiologie du 14 février sollicité par le centre de crise sanitaire. Cela permet d' élargir progressivement la pratique diagnostique aux 70 établissements de santé sièges de SAMU 508 ( * ) .
Comme l'a relevé le Pr Bruno Lina 509 ( * ) , virologue, ce schéma de déploiement est celui suivi en 2009 face à la pandémie de grippe A (H1N1) : il correspond au cadre fixé par le plan pandémie grippale de 2011 - dont les rapporteurs notent cependant qu'il n'a pas été enclenché par ailleurs - lequel ne mentionne à aucun endroit un déploiement de la détection des cas au-delà des laboratoires hospitaliers , pas plus qu'il n'évoque un déploiement des tests en population générale ; seuls sont testés les cas graves nécessitant une prise en charge hospitalière afin d'avoir une confirmation diagnostique 510 ( * ) . L'ancienne ministre en charge de la santé Agnès Buzyn a indiqué que la réalisation d'un dépistage à grande échelle n'a jamais été évoquée, ni au niveau national ni avec ses homologues internationaux - dont l'OMS - jusqu'à son départ du ministère le 15 février.
La place de la détection des cas dans le plan pandémie grippale de 2011
|
Alerte initiale |
Organisation des laboratoires pour la détection de cas Laboratoires hospitaliers spécialisés en virologie moléculaire appliquée aux virus influenzae et de niveau de sécurité 3 coordonnés par les CNR |
|
Stade 1 Freiner l'introduction du virus |
Organisation des laboratoires pour la détection de cas Tous laboratoires d'analyses de diagnostic virologique des établissements de santé Utilisation des tests virologiques de confirmation |
|
Stade 2 Freiner la propagation du virus |
|
|
Stade 3 Atténuer les effets de la vague épidémique |
Utilisation des tests virologiques de confirmation |
Pour le Pr Lina, il n'y avait pas pour ce nouveau coronavirus, au moins jusqu'au 20 février 2020, de nécessité de développement des tests en dehors du cadre hospitalier puisque tous les cas importés étaient hospitalisés. Pour rappel, « au 21 février, 12 cas ont été confirmés sur le territoire national [et] il n'y a pas de chaine de transmission active en France » comme le note un message DGS-Urgent aux professionnels de santé.
D'après les données de Santé publique France, le nombre de tests pratiqués quotidiennement dans les laboratoires hospitaliers augmente lentement jusqu'à mi-mars : le « cap » de 500 tests par jour est dépassé le 29 février (pour une capacité alors estimée par la DGOS 511 ( * ) entre 2 000 et 2 500 tests par jour) et plus de 1 600 tests par jour sont recensés du 6 au 9 mars 512 ( * ) ; la capacité, estimée par la DGOS à 5 000 tests par jour à la mi-mars, est atteinte effectivement la semaine 11 précédant le confinement (du 9 au 15 mars).
b) Un élargissement plus tardif et contraint aux laboratoires privés
« La question des dépistages à large échelle s'est posée au mois de mars, mais pas avant » a indiqué Agnès Buzyn devant la commission d'enquête.
Le calendrier - qui apparaît, rétrospectivement, plutôt tardif - de mobilisation du réseau des laboratoires de ville - qui réalise 70 % des examens courants et sans lequel une diffusion des tests à plus grande échelle ne pouvait être envisagée - confirme cette analyse : par analogie avec la grippe ( cf. ci-dessus), la diffusion des tests de diagnostic en dehors du cadre hospitalier n'a pas été envisagée ou anticipée avant mars.
Pour le Dr François Blanchecotte, président du syndicat des biologistes médicaux 513 ( * ) , les laboratoires privés d'analyse médicale sont impliqués à partir de l'inscription des tests RT-PCR à la nomenclature des actes de biologie médicale par l'arrêté du 7 mars 2020 514 ( * ) ouvrant la voie à leur prise en charge par l'assurance maladie.
Des groupes de laboratoires privés interrogés par les rapporteurs 515 ( * ) ont ajouté cependant n'avoir été destinataires, alors, d'aucune instruction des autorités sanitaires afin de se préparer à tester massivement , en étant tenus à l'écart de toute décision, en dépit de leurs sollicitations, du fait d'une stratégie délibérément ciblée sur les hôpitaux. La direction du groupe Synlab ajoute que cette situation contrastait nettement avec celle que rencontraient ses collègues allemands en mars .
Le 18 mars, une instruction ministérielle invite en effet timidement les ARS à « faciliter le déploiement de ce dispositif en ville » : « il est maintenant nécessaire de fluidifier l'organisation instaurée à l'hôpital pour le dépistage par RT-PCR du SARS-CoV-2 par la possibilité de recourir aux LBM privés pour effectuer le diagnostic sur des prélèvements effectués dans les établissements de santé et la mise en place d'un circuit de dépistage ambulatoire » 516 ( * ) .
Dès lors, la participation effective du secteur libéral au diagnostic des cas s'est heurtée à plusieurs freins qui se sont avérés d'autant plus contraignants qu'une mobilisation massive des capacités analytiques n'avait pas été anticipée et n'était pas, non plus, explicitement affichée.
Elle est intervenue, d'abord, dans un contexte affectant les capacités des laboratoires . À l'instar des autres acteurs de la médecine de ville, les personnels - initialement oubliés du circuit de distribution aux professionnels de santé des masques en officine 517 ( * ) - ont manqué d'équipement de protection du fait des difficultés d'approvisionnement. Les représentants du secteur ont également mis en avant des conditions contraintes notamment en mars et avril, en raison de l'absentéisme d'une partie des personnels dans la période du confinement (problèmes de garde d'enfant...) ou de la mise en chômage partiel d'une partie des équipes (10 à 20 % selon les groupes privés interrogés), dans un contexte de forte diminution de l'activité « courante ».
L'un des principaux obstacles - qui n'est pas propre d'ailleurs aux laboratoires privés - tient aux spécificités de la technique de détection par RT-PCR et à l'équipement que sa mise en oeuvre requiert .
Comme l'a rappelé le Pr Bruno Lina, la technique développée par le CNR dans le contexte d'un agent émergent est une technique dite « maison » : or, la plupart des laboratoires privés comme des laboratoires hospitaliers de « deuxième ligne » disposent - contrairement aux plus grands laboratoires hospitaliers ou académiques - d' équipements à systèmes « fermés » non adaptés pour une utilisation de tests « ouverts » ou « maison » , comme les y incite d'ailleurs la procédure d'accréditation par le Cofrac 518 ( * ) . Cette situation a rendu les laboratoires dépendants de kits commerciaux développés - le plus souvent en Asie - par le fabricant de l'automate, disponibles progressivement à compter de fin février - début mars . Ce sont ajoutés les délais d'une à deux semaines nécessaires pour valider les techniques avant de lancer ce type d'analyses.
A fortiori , les automates présents dans beaucoup de laboratoires n'étaient pas dimensionnés pour des débits élevés et des cadences inédites.
La semaine du 24 mars, au stade 3 épidémique, 65 laboratoires publics hospitaliers et deux grands groupes de laboratoires privés sont effectivement impliqués dans la réalisation des tests d'après la DGS.
Pour le Dr Blanchecotte, le sous-équipement des laboratoires français est la conséquence d'un sous-investissement chronique en biologie moléculaire : le faible nombre d'actes inscrits à la nomenclature n'incite pas les laboratoires à investir dans une technologie coûteuse qui nécessite l'intervention d'une main d'oeuvre hautement qualifiée. De fait la profession centralise ces faibles volumes sur un nombre réduit de plateformes : 117 plateaux techniques de laboratoires privés sur 900 environ sont ainsi accrédités en biologie moléculaire et plus ou moins bien équipés 519 ( * ) .
Proposition n° 20 : promouvoir l'équipement des laboratoires publics et privés en biologie moléculaire en accélérant la modernisation de la nomenclature des actes de biologie médicale
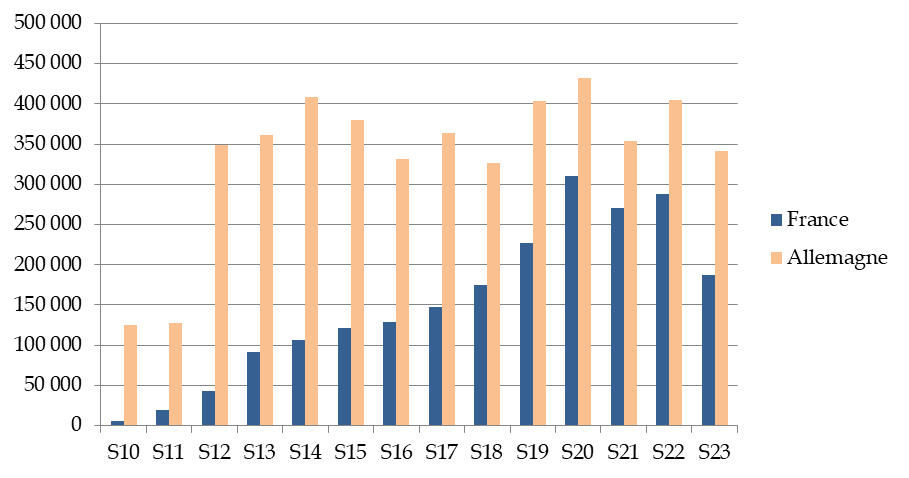
Avec la question de l'anticipation, cette situation explique, pour partie, la faible capacité de biologie moléculaire à grande échelle dont disposait la France au début de l'année 2020 comparativement à un pays comme l'Allemagne où la montée en charge des capacités de test a été plus rapide 520 ( * ) . Au meilleur équipement des laboratoires allemands en biologie moléculaire, avec notamment la présence d'automates à système « ouvert » capables d'accueillir des sondes de différentes origines 521 ( * ) , il convient probablement, pour d'autres experts, de mettre en avant un continuum en recherche et développement qui est aussi la clé de la réussite du modèle de tests à large échelle mis en place en Corée du Sud.
Comparaison du nombre de tests
RT-PCR
réalisés en France et en Allemagne
entre mars et juin 2020
Source
: Commission
d'enquête, à partir des données de l'institut Robert Koch
pour l'Allemagne
et des données de la Drees pour la France
De surcroît, l'activation des capacités analytiques des laboratoires au fil de l'eau est intervenue dans un contexte de forte demande mondiale et donc de vive tension sur les approvisionnements sur le marché international (amorces et sondes, kits d'amplification et réactifs, écouvillons, matériels divers...), ayant conduit des fabricants à imposer un contingentement par pays 522 ( * ) . Tous les acteurs ont été confrontés à ces pénuries, avec une visibilité sur le stock disponible pour répondre à la demande de 2 à 5 jours, selon le Pr Lina, durant tout le mois d'avril et une partie de mai.
Ces tensions ont impacté défavorablement la montée en charge des laboratoires de ville dans la pratique des tests d'autant plus que les réactifs autorisés (validés par le CNR) et pris en charge par l'assurance maladie l'ont été « au compte-goutte » , d'abord limités à six début mars, comme l'a regretté le président du syndicat des biologistes. Certains groupes ont anticipé des commandes mais la plupart ont jugé utile d'attendre pour éviter de se retrouver avec des tests non agréés.
Si la DGS a indiqué que l'État était intervenu auprès de fabricants pour sécuriser des volumes destinés à la France ou fournir directement des laboratoires, les groupes privés interrogés ont indiqué ne pas avoir bénéficié de telles interventions. L'un d'eux explique que la France n'était pas en position de force face aux fournisseurs avec de faibles volumes en mars et avril quand des pays avaient alors une stratégie plus ambitieuse ; par ailleurs, l'État n'avait pas, apparemment, la capacité de payer des sommes substantielles pour « verrouiller » des stocks.
c) Entre navigation à vue et cloisonnements, une mobilisation des ressources disponibles insuffisamment réactive
Le fait que les acteurs de la biologie médicale se soient avérés mal identifiés par les autorités sanitaires, de même que les cloisonnements public-privé ont indéniablement retardé la mise en place d'une organisation territoriale efficiente.
Si l'oubli des biologistes médicaux dans les procédures d'allocation des équipements de protection a illustré, pour les représentants de la profession, une mauvaise connaissance par les ARS du réseau territorial des laboratoires privés et de leur fonctionnement 523 ( * ) , cette situation n'a facilité ni l'identification des capacités de prélèvement à un échelon territorial fin ni l'évaluation des capacités d'analyse à un échelon territorial plus large, qui auraient permis la structuration de filières, la répartition optimale des ressources et la mutualisation des capacités d'analyse.
Le rapport d'étape de la mission Pittet souligne ainsi le frein qu'a constitué le « défaut de connaissance par l'administration des processus et des leviers à mobiliser pour accélérer le déploiement des tests ainsi [que] la difficulté à identifier les bons interlocuteurs » .
Les informations recueillies par les rapporteurs montrent qu'au niveau local, un inventaire des capacités n'a été réalisé que tardivement, par exemple vers le 20 avril en région Centre-Val de Loire, ou parfois sur la base d'hypothèses incompatibles avec les dispositions du code du travail applicables aux personnels des laboratoires privés 524 ( * ) .
La tenue de réunions séparées par les ARS entre les acteurs publics et privés a entretenu les cloisonnements et l'absence de vision claire et partagée sur les capacités effectives de test et les besoins , les personnels compétents, les délais d'analyse ou encore l'état des stocks.
La Drees 525 ( * ) a mis en place à compter du 16 avril une plateforme nationale 526 ( * ) permettant de fluidifier les remontées d'informations et de renseigner les tensions sur les approvisionnements, sans toutefois que cette avancée ne se traduise par des impacts concrets. Cet outil a marqué cependant l'engagement d'un dialogue entre les acteurs et les autorités.
Au niveau national, cette atomisation du secteur s'est traduite par l' absence de recensement exhaustif du nombre de tests réalisés par les laboratoires privés 527 ( * ) avant la mise en oeuvre - saluée par les acteurs - de SIDEP (système d'information de dépistage) à compter du 13 mai (et dont les données sont exhaustives à compter du 7 juin), permettant une indispensable mise en réseau des laboratoires.
Ce contexte n'a pas facilité l'association d'autres acteurs tels que les laboratoires vétérinaires et de recherche qui représentaient une puissance d'analyse complémentaire face à une sollicitation inédite des laboratoires de biologie médicale.
Les laboratoires vétérinaires départementaux ont fait connaître le 30 mars par un communiqué de presse 528 ( * ) qu'ils étaient prêts à mettre à disposition une capacité analytique de 20 000 tests PCR par jour, opérationnelle dans un délai d'une à deux semaines sous réserve de l'accès aux réactifs. Le recours à ces laboratoires a été soutenu par l'Académie vétérinaire de France, l'Académie de médecine et l'Académie de pharmacie, tout comme de nombreux présidents de conseils départementaux.
À la mi-mars, des propositions de partenariat ont pour certaines été rejetées, soit par les ARS (par exemple en Nouvelle-Aquitaine pour des partenariats envisagés entre laboratoires privés et vétérinaires) soit par les acteurs hospitaliers, comme l'a évoqué le Pr Philippe Froguel, responsable d'un laboratoire de recherche en génomique à Lille, lors de son audition 529 ( * ) .
La publication, quoique tardive, du décret du 5 avril 2020 530 ( * ) complété par un arrêté de la même date 531 ( * ) mérite d'être saluée : ces textes ont permis, à titre exceptionnel, de déroger à l'autorisation exclusive des laboratoires de biologie médicale à traiter des échantillons de provenance humaine , sous la responsabilité d'un laboratoire de biologie médicale et dans le cadre d'une convention passée avec lui.
D'après les données de la DGS, fin juin 2020, ont conventionné :
- 44 laboratoires départementaux d'analyses (LDA) vétérinaires, pour un total de 87 conventions passées avec des laboratoires de biologie médicale hospitaliers ou privés, certains LDA ayant conventionné avec plusieurs laboratoires ;
- 8 laboratoires accrédités suivant la norme ISO/CEI 17025 (police scientifique par exemple), pour un total de 10 conventions passées ;
- 12 laboratoires de recherche .
Au 8 mai 2020, le potentiel d'analyse des laboratoires vétérinaires n'était activé qu'à hauteur de 10 % dans une quinzaine de laboratoires réalisant des tests RT-PCR. En dépit d'une nette montée en puissance, ces laboratoires indiquent encore majoritairement, au cours du mois de septembre marqué par l'explosion de la demande de tests, ne pas être sollicités à leur capacité hebdomadaire maximale réévaluée à 109 000 RT-PCR : celle-ci est « activée » entre 54 et 78 % selon les semaines 532 ( * ) .
Comme l'ont relevé certains acteurs, cette « sous-traitance » de la phase analytique a été complexe à organiser et n'allait pas de soi en l'absence de systèmes de transmission de données sécurisées.
Si des collaborations se sont avérées fructueuses, le poids des corporatismes et l'absence d'impulsion des ARS pour les dépasser n'ont pas permis d'optimiser les ressources présentes à l'échelle des territoires en structurant des organisations plus efficientes.
2. Avec des capacités dépassées lors du pic épidémique, une doctrine de détection des cas restrictive
a) « Testez, testez, testez » : une évidence a posteriori qui s'est imposée relativement tard
Pour endiguer l'épidémie, les Prs Dominique Costagliola et Yasdan Yasdanpanah ont estimé que « la meilleure stratégie est claire : c'est tester, tester, tester et associer le résultat des tests à une prise en charge adaptée en termes médical et épidémiologique. » 533 ( * )
Ce constat rejoint la recommandation sous forme d'injonction (« testez, testez, testez » ) formulée par le directeur général de l'OMS le 16 mars 2020, après avoir invité l'ensemble des pays à augmenter leurs capacités en matière de dépistage dans une précédente allocution du 5 marsý :
« Comme je ne cesse de le dire, tous les pays doivent adopter une approche globale. Mais pour prévenir les infections et sauver des vies, le moyen le plus efficace est de briser les chaînes de transmission . Et pour cela, il faut dépister et isoler. Vous ne pouvez pas combattre un incendie les yeux bandés . Et nous ne pouvons pas arrêter cette pandémie si nous ne savons pas qui est infecté par le virus.
Nous avons un message simple pour tous les pays : testez, testez, testez . Testez tous les cas suspects. Si le résultat du test est positif, isolez-les et trouvez avec qui ils ont été en contact étroit jusqu'à deux jours avant l'apparition de leurs symptômes, et testez également ces personnes. »
Rétrospectivement, ce message clé s'impose comme une évidence.
Pour autant, l'appel de l'OMS, qui fait suite à des instructions purement techniques aux laboratoires, pouvait avoir plusieurs niveaux de lecture : comme l'analyse Mme Agnès Buzyn, il ne dit pas précisément si c'est une stratégie de dépistage à large échelle ou juste une capacité de détection précoce qui est visée, à une date où beaucoup de pays n'ont pas encore accès à la RT-PCR pour identifier les cas 534 ( * ) .
En outre, l'analogie avec la grippe n'a pas conduit les autorités à anticiper dès les premières alertes une mobilisation intensive des capacités d'analyse. Des experts en santé publique ont rappelé, à l'instar du Pr Emmanuel Rush, président de la société française de santé publique, que le discours sur des tests à large échelle n'avait pas fait immédiatement consensus au sein de la communauté scientifique en santé publique .
Le Pr Antoine Flahault, médecin de santé publique, a reconnu de même ne pas avoir été initialement « convaincu par le discours d'un Christian Drosten ou d'un Didier Raoult sur la nécessité des tests. [...] À l'époque, je considérais que les tests ne guérissaient pas les gens et que l'on avait surtout besoin de traitements et de mesures de prévention. Pour moi, les tests ne faisaient pas partie des mesures prioritaires à prendre. (...) De fait, on ne réalise pas de tests pour la grippe saisonnière : on se contente de surveiller ce que les généralistes constatent dans leur pratique. (...) À tort, je n'ai pas perçu l'utilité et l'importance du cercle vertueux qu'enclenchent les tests, de leur capacité à enrayer les chaînes de transmission . » 535 ( * )
b) Une priorisation des tests fondée sur la pénurie qui n'a pas permis de poursuivre la stratégie visant à casser les chaînes de contamination
Dans ces circonstances, le conseil scientifique , en préambule de son avis du 23 mars, est conduit à admettre l'impossibilité matérielle de poursuivre la stratégie de détection des malades et de leurs cas contacts : « Le confinement est actuellement la seule stratégie réellement opérationnelle, l'alternative d'une politique de dépistage à grande échelle et d'isolement des personnes détectées n'étant pas pour l'instant réalisable à l'échelle nationale. »
Son président l'a rappelé devant la commission d'enquête : « Début mars, le conseil scientifique a constaté que la France avait une capacité de 3 000 tests par semaine, alors que les Allemands en effectuaient 60 000. Le conseil scientifique était convaincu que la stratégie des tests était la bonne, mais nous n'avions pas suffisamment de tests pour la mettre en oeuvre. » 536 ( * )
La doctrine de priorisation des tests de diagnostic en phase épidémique ( cf. encadré), ciblée sur les cas graves hospitalisés par analogie avec le plan pandémie grippale, s'est avérée stricte dans sa définition , en écartant explicitement les formes peu symptomatiques ou les cas contacts, et encore plus stricte dans sa mise en oeuvre effective.
La définition des publics prioritaires pour les tests RT-PCR (18 mars 2020)
Sur la base de recommandations du HCSP 537 ( * ) , saisi par la direction générale de la santé sur des indications prioritaires du diagnostic par RT-PCR, les consignes diffusées sous la forme d'une fiche ARS en date du 18 mars 2020 538 ( * ) organisent la priorisation des tests diagnostiques en phase épidémique.
Sont identifiés comme indications prioritaires :
- les critères liés à la gravité induisant une hospitalisation, notamment les patients présentant une symptomatologie respiratoire hospitalisés en réanimation et ceux avec des symptômes évocateurs de covid-19 hospitalisés pour une pneumopathie avec signes de gravité ;
- les professionnels de santé avec des symptômes évocateurs ;
- les critères liés à la comorbidité : personnes à risque de formes graves (selon les critères définis par le HCSP dans un avis du 14 mars) présentant des symptômes évocateurs et femmes enceintes symptomatiques ;
- les critères liés à une situation : exploration d'un foyer de cas possibles (en particulier en collectivités de personnes âgées) dans la limite de 3 tests par unité.
Ne sont plus des indications de diagnostic les formes paucisymptomatiques ; il en est de même des cas contacts qui ne sont même plus évoqués dans cette fiche.
Pour la DGS, cette politique est néanmoins en conformité avec les recommandations européennes et internationales dans un contexte de tensions sur les capacités diagnostiques en phase épidémique 539 ( * ) . Elle en donne de facto une lecture minimaliste.
Le 18 mars, la commission européenne, sur l'avis scientifique de l'ECDC, diffuse des recommandations pour la stratégie de test 540 ( * ) : si celles-ci établissent en effet un classement par ordre décroissant des publics prioritaires à tester « pour assurer un usage optimal de la ressource et alléger la pression sur les laboratoires », elles soulignent toutefois l'importance des tests dans la gestion de l'épidémie, y compris pour détecter les cas asymptomatiques susceptibles de diffuser le virus à défaut d'être isolés.
La « stratégie covid-19 » de l'OMS mise à jour au 14 avril 541 ( * ) indique de même que « durant les périodes de transmission locale soutenue, les capacités de diagnostic peuvent s'avérer insuffisantes et il peut être nécessaire de tester en priorité les populations vulnérables risquant de développer une forme grave de la maladie, les personnels de santé et les travailleurs essentiels présentant des symptômes, ainsi que les premières personnes présentant des symptômes dans des environnements fermés [...] afin d'identifier rapidement les flambées épidémiques et d'instaurer des mesures efficaces d'isolement de tous les cas confirmés et présumés. » Elle fixe cependant comme cible nécessaire le fait de détecter « les cas présumés [...] rapidement après l'apparition des symptômes, par une recherche active des cas, par un auto-signalement, par un dépistage aux points d'entrée et d'autres approches » .
La stratégie de tests en Allemagne
Comme indiqué plus haut, l'Allemagne a atteint plus rapidement que la France ou d'autres pays européens comme l'Espagne ou le Royaume-Uni (alors respectivement à environ 15 000 et 12 000 tests par jour début avril) une capacité à tester plus importante.
Dans le même temps, la stratégie définie par l'institut Robert Koch a évolué de la manière suivante.
Depuis fin janvier, la doctrine est de tester toute personne présentant des symptômes ET ayant eu un contact avec une personne infectée OU revenant d'une région à forte circulation du virus (après avis médical). Deux tests de guérison sont effectués exclusivement sur les patients hospitalisés (à intervalle de 24 h). Depuis le 30 mars, le test des personnes asymptomatiques « n'est généralement pas recommandé en raison de la signification peu claire d'un test négatif et pour économiser la capacité à tester ».
Parallèlement, le recours aux tests sérologiques est organisé à compter du 9 avril pour évaluer l'ampleur de l'immunité de la population (étude en 3 phases sur les donneurs de sang, des clusters et des échantillons représentatifs).
À compter de mi-avril, un dépistage massif mais ciblé
Un document de synthèse du ministère fédéral de la santé paru le 17 avril détaille la stratégie d'amélioration en matière de tests pour continuer à tester les plus largement possible et optimiser les processus. Des interfaces numériques permettent d'accéder aux résultats des laboratoires. Les personnes symptomatiques, leurs contacts asymptomatiques et tout cas suspect médicalement justifié doivent être testés. Une attention particulière doit être portée aux hôpitaux, maisons de soins, foyers pour personnes âgées ou handicapées et autres établissements accueillant des personnes vulnérables (test des patients et résidents avant chaque (ré)admission, répété à intervalles réguliers) et à leurs personnels. Un objectif est également fixé de tester en quelques jours la population totale dans des régions où l'incidence est élevée ou de réaliser des tests sentinelles réguliers sur des groupes représentatifs sélectionnés au hasard.
Une stratégie progressivement renforcée
Une deuxième loi sur la protection de la population adoptée le 14 mai par le Bundestag permet au ministère fédéral de la santé d'obliger par décret les caisses d'assurance maladie publique à payer en principe les tests, afin d'accompagner leur réalisation à plus grande échelle. Ce sujet fait toutefois débat entre l'assurance maladie publique et les caisses privées. Parallèlement, il est recommandé d'augmenter les tests dans l'environnement des personnes particulièrement menacées (par exemple dans les maisons de retraite).
Une ordonnance du 8 juin permet le dépistage systématique dans certaines structures et sous certaines conditions (toutes les personnes présentes dans les maisons de retraite, écoles et garderies ou encore des structures comme les prisons si un cas positif est détecté ; dans les établissements de soins même sans cas avéré).
Deux ordonnances des 1 er et 8 août rendent obligatoire le dépistage des résidents allemands revenant de voyages dans les dernières 72 heures et des voyageurs revenant de zones à risques dans les dernières 72 heures.
Une stratégie révisée mi-octobre. Pour éviter une surcharge des centres de tests, la stratégie est ciblée sur des publics prioritaires : les personnes symptomatiques (sur avis médical), les cas contact des personnes positives (considérés comme tels par un médecin ou les autorités sanitaires), le personnel, les patients ou résidents et visiteurs d'un établissement de santé, médico-social, scolaire ou judiciaire dans lequel un cas positif a été détecté dans les 10 derniers jours (ou même en absence de cas confirmé dans les établissements de santé et médico-sociaux), les personnes revenant d'une zone à risque et celles résidant dans une zone à forte incidence.
Source : Délégation aux affaires européennes et internationales des ministères sociaux
c) Une situation qui a fragilisé les publics les plus vulnérables
La priorisation du diagnostic n'est ainsi qu'un pis-aller, conséquence et corollaire de la parcimonie des tests disponibles.
Cette situation a soulevé des incompréhensions chez les patients et leur entourage qui ont eu le sentiment, lors du pic épidémique du printemps, d'avoir été privés de quelque chose. Elle a particulièrement exposé les soignants pour lesquels l'accès aux tests a été, dans les faits, limité . Le président de l'intersyndicale nationale des internes a rappelé qu'au début de la crise, seuls 53 % des internes en médecine mobilisés face à l'épidémie qui présentaient des symptômes ont pu avoir accès à un test ; de surcroît, en cas de résultat positif, plus d'un sur deux a été contraint de continuer à travailler, mettant ainsi en danger sa sécurité comme celle des patients 542 ( * ) .
Cette politique a manqué, enfin, la cible des publics vulnérables .
Le Pr Bruno Lina a expliqué 543 ( * ) que la limitation des tests aux trois premiers patients dans les structures d'hébergement collectif comme les Ehpad reposait sur une logique analogue à l'épidémie grippale, alors que la situation face au coronavirus était différente : à défaut de pouvoir mettre en place une prophylaxie capable de maîtriser l'épidémie, un bilan exhaustif des personnes infectées par le SARS-CoV-2 s'avérait nécessaire.
Des campagnes de tests massives se sont déployées « au fil de l'eau » dans les Ehpad sur la base d'initiatives locales souvent impulsées par les conseils départementaux 544 ( * ) .
Il a fallu attendre la circulaire du 9 avril 2020 des ministres des solidarités et de la santé et de l'intérieur pour acter un élargissement de la doctrine d'emploi des tests en direction de publics prioritaires, dont les soignants et les personnels et résidents d'établissements médico-sociaux.
Comme l'a relevé toutefois la Fehap, « le protocole de dépistage massif, prévu à compter du 14 avril, semble avoir été mis en oeuvre de façon efficace, sans toutefois que les pouvoirs publics organisent véritablement la démarche sur les territoires » .
* 505 ECDC : European Centre for Disease Prevention and Control.
* 506 Audition de Mme Agnès Buzyn, ancienne ministre de la santé, 23 septembre 2020.
* 507 La diffusion de la technique par le CNR s'entend de la fabrication et du contrôle des réactifs spécifiques et de l'accompagnement de sa mise en oeuvre opérationnelle (transmission de protocoles), tout en s'assurant de la fiabilité du test.
* 508 Un courrier du directeur général de la santé à la responsable du CNR des virus respiratoires en date du 25 février 2020 demande officiellement au CNR de procéder au déploiement de la technique dans les établissements dits de 2 e niveau et de procéder à cette fin aux commandes nécessaires auprès des fournisseurs.
* 509 Contribution écrite adressée à la commission d'enquête.
* 510 D'après des indications de la DGS, ces éléments sont corroborés par les recommandations de diagnostic de la grippe et autres virus respiratoires. Il n'est pas recommandé de confirmer biologiquement tout syndrome grippal. La grande majorité des tests PCR grippe/autres virus respiratoires saisonniers (VRS) sont réalisés à l'hôpital pour des pneumonies virales et d'autres formes sévères d'infections respiratoires aiguës. D'après les données issues du réseau RENAL qui comprend une quarantaine de laboratoires de CHU, de 100 000 à 160 000 prélèvements sont réalisés chaque année lors d'une saison hivernale (d'octobre à avril).
* 511 Contribution écrite de la DGOS à la commission d'enquête.
* 512 Cf. Point épidémiologique covid-19 - situation au 10 mars 2020.
* 513 Audition sur la politique de dépistage, 10 septembre 2020.
* 514 Arrêté du 7 mars 2020 portant modification de la liste des actes et prestations mentionnée à l'article L. 162-1-7 du code de la sécurité sociale (inscription de la détection du génome du SARS-CoV-2 par RT PCR). Cet arrêté est pris sur la base de l'avis du 6 mars de la Haute Autorité de santé (HAS) fixant des critères de prise en charge (disposer d'un marquage CE ou avoir été validé par le CNR, s'inscrire dans les indications définies par les autorités sanitaires, comporter au moins deux cibles pour accroître la performance du test).
* 515 Contributions écrites de Biogroup, Synlab et CerbaHealthCare à la commission d'enquête.
* 516 MINSANTE/CORRUSS n°2020_37 : Diffusion lignes directrices médecine de ville, téléconsultation et RT-PCR en ville.
* 517 Les biologistes médicaux sont explicitement ajoutés à la liste des professionnels de santé concernés par la distribution des masques via les officines dans le message DGS-Urgent du 18 mars 2020. Le message DGS-Urgent du 2 mars sur le même sujet ainsi que le communiqué de presse du ministre des solidarités et de la santé en date du 16 mars 2020 visaient quant à eux les médecins généralistes et les médecins spécialistes. Le fait de ne pas être visés explicitement a conduit à priver de facto certains biologistes de la distribution, en cas de lecture restrictive.
* 518 Comité français d'accréditation.
* 519 Audition sur la politique de dépistage, 10 septembre 2020.
* 520 Au 21 juin 2020, les laboratoires allemands (entre 90 et 183 laboratoires impliqués) ont pratiqué 5 412 655 tests PCR (d'après les données transmises par la délégation aux affaires européennes et internationales des ministères sociaux) soit plus du double qu'en France sur la même période (2 599 476 tests PCR d'après les données redressées de la Drees).
* 521 C'est l'un des facteurs principaux expliquant la différence de cadence entre la France et l'Allemagne relevés par plusieurs acteurs interrogés par la commission d'enquête alors que le test a été conçu en même temps dans les deux pays, de même que l'explication principale relevée par la mission indépendante présidée par le Pr Didier Pittet dans son rapport d'étape du 13 octobre 2020. Le Pr Froguel a indiqué que l'Allemagne compte par exemple 8 laboratoires P4 civil en génie moléculaire contre un seul en France (Lyon). L'Allemagne n'avait pas de capacité de production autonome de kits de tests PCR sur son territoire d'après l'association de l'industrie du diagnostic.
* 522 Contribution écrite de l'ARS d'Île-de-France à la commission d'enquête.
* 523 Cette méconnaissance s'est par exemple traduite dans des attitudes initialement restrictives de « certaines » ARS pointées par des syndicats de biologistes, estimant à tort, début mars, que les laboratoires devaient disposer d'un agrément spécifique pour réaliser les tests RT-PCR ou établissant des listes limitées de laboratoires auxquels les fournisseurs devaient se référer : si cette situation a été rapidement corrigée, des laboratoires équipés ont été écartés, contribuant à expliquer un retard dans la mise à disposition des tests sur certains territoires.
* 524 Contribution écrite du syndicat des biologistes médicaux à la commission d'enquête.
* 525 Direction de la recherche, des études, de l'évaluation et des statistiques (Drees) du ministère des solidarités et de la santé.
* 526 https://laboratoires.fabrique.social.gouv.fr/
* 527 En effet, jusqu'à cette date, les données recensées par Santé publique France dans le cadre de la surveillance virologique s'appuyaient sur les données non exhaustives transmises par le « réseau 3 labo » (Cerba, Eurofins-Biomnis, Inovie) pour le secteur privé et par les laboratoires hospitaliers.
* 528 Communiqué de l'ADILVA, Association française des directeurs et cadres des laboratoires vétérinaires publics d'analyses.
* 529 Audition sur la politique de dépistage, 10 septembre 2020.
* 530 Décret n° 2020-400 du 5 avril 2020 complétant le décret n° 2020-293 du 23 mars 2020 prescrivant les mesures générales nécessaires pour faire face à l'épidémie de covid-19 dans le cadre de l'état d'urgence sanitaire.
* 531 Arrêté du 5 avril 2020 complétant l'arrêté du 23 mars 2020 prescrivant les mesures d'organisation et de fonctionnement du système de santé nécessaires pour faire face à l'épidémie de covid-19 dans le cadre de l'état d'urgence sanitaire.
* 532 D'après les données communiquées par l'ADILVA (association française des directeurs et cadres des laboratoires vétérinaires publics d'analyse) - Résultats de l'enquête sur l'état des lieux des tests RT-PCR du SARS-CoV-2 dans le réseau des laboratoires départementaux pour la semaine 41.
* 533 Contribution écrite transmise à la commission d'enquête.
* 534 Contribution écrite transmise à la commission d'enquête.
* 535 Audition d'experts en santé publique, 16 septembre 2020.
* 536 Audition du conseil scientifique covid-19, 15 septembre 2020.
* 537 https://solidarites-sante.gouv.fr/IMG/pdf/hcsp_sars-cov2-priorisationtestsdiagnostiques-2020-03-11.pdf
* 538 Fiche ARS, Recommandations aux professionnels de santé en charge des prélèvements de dépistage par RT-PCR , 18 mars 2020.
* 539 Réponses écrites adressées à la commission d'enquête.
* 540 https://ec.europa.eu/info/sites/info/files/covid19_-_eu_recommendations_on_testing_strategies_v2.pdf
* 541 https://apps.who.int/iris/bitstream/handle/10665/332019/WER9519-185-208-eng-fre.pdf?sequence=1&isAllowed =y
* 542 Audition de syndicats d'internes hospitaliers, 15 octobre 2020.
* 543 Contribution écrite du Pr Lina adressée à la commission d'enquête.
* 544 Cf. supra les développements sur l'impact de la crise dans le secteur médico-social.