TITRE
III
DEVELOPPER L'AMBITION NUMERIQUE EN SANTE
CHAPITRE
IER
Innover en valorisant les données cliniques
Article 11
(art. L. 1460-1, L. 1461-1, L. 1461-3,
L. 1461-4, L. 1461-5, L. 1461-6, L. 1461-7, L. 1462-1 et
L. 1462-2 [nouveau] du code de la santé publique,
art. L. 2223-42
du code général des
collectivités territoriales, art. 30, 66, 72, 73, 76 et 77 de la
loi n° 78-17 du 6 janvier 1978 relative à l'informatique,
aux fichiers et aux libertés)
Élargissement du champ du
système national des données de santé
et
création de la plateforme des données de santé
Objet : Cet article propose d'élargir le champ du système national des données de santé (SNDS) à l'ensemble des données cliniques obtenues dans le cadre de soins remboursés par l'assurance maladie pour favoriser la production et l'utilisation des données de santé, et crée la plateforme des données de santé (PDS).
I - Le dispositif proposé
A. Le droit existant
1. L'architecture globale des données de santé
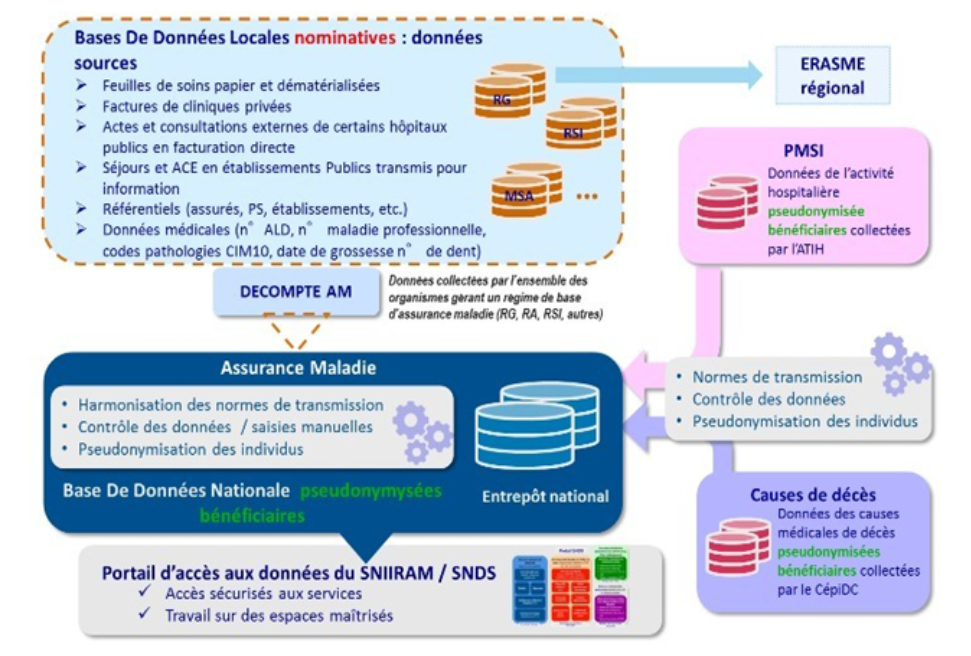
Le système national des données de santé (SNDS), créé par la loi du 26 janvier 2016 80 ( * ) , rassemble cinq grands ensembles de bases de données :
- le système national d'information interrégimes de l'assurance maladie (Sniiram) , alimenté par chaque organisme de sécurité sociale gestionnaire d'un régime de base d'assurance maladie. Ce système compile les dépenses de l'ensemble des régimes d'assurance maladie, organisées par circonscription, par nature de dépenses, par professionnel de santé et par établissement ;
- les systèmes d'informations hospitaliers (SIH) mis en oeuvre par les établissements de santé, publics et privés. Ces systèmes sont alimentés par les différents praticiens de données médicales nominatives , transmises à un médecin responsable de l'information médicale pour l'établissement ;
- le système d'information alimenté par les maisons départementales des personnes handicapées (MDPH), mis en oeuvre par la caisse nationale de solidarité pour l'autonomie (CNSA), qui rassemble, outre plusieurs informations nominatives, la « nature du diagnostic médical, l'origine et la nature des déficiences, les limitations d'activité, les besoins et les attentes » des personnes handicapées dont elles ont à connaître, en plus de certaines personnes âgées dans le cas des maisons départementales de l'autonomie (MDA) ;
- les données sur les causes de décès , restituées sur les certificats d'attestation du décès ;
- un échantillon représentatif des données de remboursement par bénéficiaire transmises par des organismes d'assurance maladie complémentaire et défini en concertation avec leurs représentants.
Architecture globale des données de santé
Source : SNDS
L'ensemble de ces données permet la reconstruction des parcours de santé de 67 millions de personnes sur près de 12 années.
2. La gestion des données de santé
a) Le gestionnaire
La gestion du SNDS revient à la caisse nationale d'assurance maladie (Cnam), désignée comme responsable de traitement. Le SNDS se présente par conséquent sous la forme d'un entrepôt national de données .
b) Les collecteurs
Les organismes collecteurs des données de santé à caractère personnel sont énumérés à l'article L. 1460-1 du CSP. Il s'agit des services ou établissements publics de l'État ou des collectivités territoriales et des organismes de sécurité sociale .
c) Les destinataires
Les destinataires des « données de santé à caractère personnel recueillies à titre obligatoire » sont largement énumérés à l'article L. 1460-1 du CSP : il s'agit des citoyens , des usagers du système de santé, des professionnels de santé, des établissements de santé et de leurs organisations représentatives ainsi que des organismes participant au financement de la couverture contre le risque maladie ou réalisant des recherches, des études ou des évaluations à des fins de santé publique, des services de l'État, des institutions publiques compétentes en matière de santé et des organismes de presse.
L'article L. 1461-2 dispose que, lorsqu'elles sont mises à la disposition du public , ces données ne peuvent prendre la forme que de statistiques agrégées (donc non individuelles) ou de données individuelles constituées de telle sorte que toute indentification directe ou indirecte demeure impossible (données « pseudonymisées ») . La seule exception à ce principe concerne les données relatives à l'activité des professionnels de santé, retracées dans le Sniiram, dont le caractère nominatif est maintenu.
d) Les finalités
Les données de santé à caractère personnel peuvent se prêter à deux finalités distinctes : la simple consultation et le traitement . Contrairement à la première, la seconde suppose des opérations d'appariement destinées à enrichir le sens et la portée des données brutes .
Dans le cas de la consultation , les destinataires des données sont ceux énoncés à l'article L. 1460-1 et les conditions de leur mise à disposition sont celles énoncées à l'article L. 1461-2. Cette mise à disposition a vocation à contribuer à l'information sur la santé ainsi que sur l'offre de soins, à la connaissance des dépenses de santé, à l'information des professionnels sur leur activité ainsi qu'aux recherches dans les domaines de la santé et de la prise en charge médico-sociale.
Dans le cas du traitement , l'article L. 1460-1 dispose que les données de santé à caractère personnel recueillies à titre obligatoire peuvent faire l'objet de traitements « à des fins de recherche, d'étude ou d'évaluation présentant un caractère d'intérêt public ». Les opérations d'appariement effectuées sur ces données présentant un risque important de ré-identification des personnes concernées, le cadre juridique d'exercice de ces traitements de données est substantiellement plus étoffé (cf. infra ) .
Enfin, l'article L. 1461-1 énonce deux finalités interdites :
- la promotion des produits de santé ou de médicaments en direction des professionnels de santé ou d'établissements de santé ;
- l'exclusion de garanties des contrats d'assurance et la modification de cotisations ou de primes d'assurance d'un individu ou d'un groupe d'individus présentant un même risque.
3. Le régime de protection des données de santé à des fins de traitement
a) Le traitement des données de santé fait l'objet d'un régime spécifique
La loi du 6 janvier 1978 relative à l'informatique, aux fichiers et aux libertés 81 ( * ) , qui définit le régime juridique applicable aux traitements des données personnelles, fera l'objet, à partir du 1 er juin 2019, d'une réécriture globale consécutive à l'adoption du règlement européen sur la protection des données (RGPD) du 27 avril 2016 82 ( * ) .
Ce dernier réaffirme le principe selon lequel il est interdit de traiter des données à caractère personnel concernant la santé, à l'exception des conditions prévues par le 2 de l'article 9 du RGPD dont notamment :
- la personne concernée a donné son consentement explicite au traitement de ces données à caractère personnel ;
- le traitement est nécessaire aux fins de l'exécution des obligations et de l'exercice des droits propres au responsable du traitement ou à la personne concernée en matière de droit du travail, de la sécurité sociale et de la protection sociale ;
- le traitement est nécessaire pour des motifs d'intérêt public dans le domaine de la santé publique.
L'autorisation d'exploitation des données de santé, en raison de leur caractère sensible, fait l'objet d'un contrôle en amont exercé principalement par la commission nationale de l'informatique et des libertés (Cnil).
Échappent à ce contrôle plusieurs traitements énumérés à l'article 65 de la loi du 6 janvier 1978 dans sa version à venir, ayant pour trait commun d'être mis en oeuvre par l'autorité publique dans un objectif de suivi des politiques de santé publique.
La loi prend soin de distinguer , parmi les traitements des données de santé à caractère personnel en-dehors de ceux mis en oeuvre par l'autorité publique :
- en général , tous les traitements de données de santé mis en oeuvre par des responsables de traitement publics ou privés, à la condition stricte d'une finalité d'intérêt public (notamment la garantie de normes élevées de qualité et de sécurité des soins de santé et des médicaments ou des dispositifs médicaux). Ces traitements ne sont possibles que s'ils respectent les référentiels et les règlements types établis par la Cnil destinés à garantir leur sécurité ou, dans le cas contraire, si cette dernière leur a attribué une autorisation de traitement (article 66 de la loi du 6 janvier 1978 dans sa version à venir) ;
- en particulier , les traitements de données de santé dont la finalité est limitée à la « recherche, l'étude ou l'évaluation dans le domaine de la santé ». Ces traitements sont dispensés de l'autorisation de la Cnil, à condition toutefois que le responsable du traitement ait préalablement transmis à cette dernière une déclaration de conformité à une méthodologie de référence (article 73 de la loi du 6 janvier 1978 dans sa version à venir).
|
Le contrôle de la Cnil sur les traitements de données de santé : de l' a priori à l' a posteriori La loi du 26 janvier 2016 avait précisé les modalités d'intervention de la Cnil pour le seul cas des traitements de données à caractère personnel à des fins de recherche, d'étude ou d'évaluation . Ces traitements faisaient alors l'objet d'une autorisation délivrée a priori par la Cnil , à l'issue d'un processus décisionnel complexe : - le dépôt de la demande devait être obligatoirement fait auprès de l'institut national des données de santé (INDS), qui dispose de la faculté de rendre un avis sur l'intérêt public de la recherche ou de l'étude ; - dans les cas où ces traitements portaient sur des recherches impliquant la personne humaine, l'avis préalable du comité de protection des personnes (CPP) compétent était requis ; - dans tous les autres cas, l'avis du comité d'expertise pour les recherches, les études et les évaluations dans le domaine de la santé (Cerees) devait être recueilli. La transposition du RGPD dans le droit interne français, opéré par la loi du 20 juin 2018 83 ( * ) , a permis de considérablement assouplir ce régime d'autorisation . Il est notamment prévu que la Cnil établisse des référentiels et des règlements types ; le responsable de traitement est réputé autorisé à effectuer le traitement s'il a préalablement adressé à la Cnil une déclaration attestant de la conformité de sa méthode de traitement auxdits référentiels . Le contrôle de la Cnil ne s'effectue donc potentiellement qu' a posteriori , en vérification de la conformité déclarée par le responsable. Le régime de l'autorisation a priori n'est maintenu qu'en cas de déclaration de non-conformité par le responsable. Par ailleurs, le RGPD assouplit davantage le régime d'autorisation pour deux cas particuliers : - les traitements de données à finalité de recherche, d'étude ou d'évaluation : la déclaration préalable de conformité n'a pas pour objet un « référentiel type » ou un « règlement type », mais une simple méthodologie de référence homologuée par la Cnil ; - les traitements de données ayant pour seule finalité de répondre en cas d' urgence à une alerte sanitaire : dans ce cas, le responsable de traitement n'est astreint qu'à une analyse de l'impact du traitement et, selon les résultats de cette analyse, à la seule consultation de la Cnil. Pour autant , en cas d'absence de déclaration préalable de conformité pour tout type de traitement, la délivrance d'une autorisation de la Cnil reste soumise aux mêmes conditions que celles définies par le droit antérieur (avis préalable du CPP ou du Cerees). |
b) L'accès aux données
• La protection de l'identité des personnes
L'article L. 1461-4 du CSP dispose explicitement que le SNDS ne contient ni les noms et prénoms des personnes, ni leur numéro d'inscription au répertoire national d'identification des personnes physiques (NIR), ni leur adresse . Par ailleurs, la loi du 6 janvier 1978 précise que « toute personne a le droit de s'opposer à ce que des données à caractère personnel la concernant fassent l'objet de la levée du secret professionnel rendue nécessaire par un traitement » de données de santé.
Pour autant, la possibilité de ré-identifier les données de santé pseudonymisées par les responsables de traitement qui alimentent le SNDS a été laissée ouverte par le même article qui dispose qu'un « organisme distinct » du responsable du SNDS peut se voir confier les données à caractère personnel concernées par un risque d'identification directe. Cet organisme distinct, appelé « tiers de confiance », n'a pour l'heure jamais été désigné.
La loi du 6 janvier 1978 tient par ailleurs spécifiquement compte des traitements de données de santé comportant des informations identifiantes, notamment le NIR . Pour ces traitements particuliers, la loi prévoit qu'un décret en Conseil d'État , pris après avis motivé de la Cnil, détermine précisément les responsables de traitement et les finalités des traitements habilités (article 30 de la loi du 6 janvier 1978 dans sa version à venir). On peut toutefois noter qu'un traitement mettant en oeuvre le NIR, pourvu qu'il obéisse à une finalité de recherche , échappe au cadre spécifique de l'article 30 et s'inscrit dans le cadre général de l'article 73.
• La régulation des accès
Depuis la loi du 26 janvier 2016, l'article L. 1461-3 du CSP définit soigneusement le régime d'accès aux données personnelles de santé contenues dans le SNDS . Il n'est en principe autorisé que :
- de manière permanente , pour permettre l'accomplissement des missions des services de l'État, des établissements publics ou des organismes chargés d'une mission de service public compétents . Dans ce cas, l'accès aux données ne peut être accordé qu'aux personnes nommément désignées et habilitées à cet effet par la Cnam, dans des conditions précisées par décret en Conseil d'État 84 ( * ) ;
- de manière ponctuelle et sur demande , pour permettre des traitements à des fins de recherche, d'étude ou d'évaluation contribuant à une finalité répondant à un motif d'intérêt public.
Pour ce cas particulier, l'article L. 1461-3 prévoit explicitement la situation où la recherche, l'étude ou l'évaluation pourrait être menée par une personne morale de droit privé produisant ou commercialisant des médicaments ou des produits de santé .
Cette dernière est alors tenue, outre l'homologation obligatoire de sa méthode de traitement à la méthodologie de référence élaborée par la Cnil :
- soit de démontrer l'incompatibilité du traitement qu'elle envisage avec un objectif promotionnel en direction des professionnels de santé ou un objectif de redéfinition de la cible et des conditions contractuelles de compagnies d'assurance ;
- soit de faire réaliser l'étude par un laboratoire de recherche ou un bureau d'étude indépendant, à qui incombera également l'obligation de déclaration de conformité.
c) Le contenu des traitements fait l'objet d'un contrôle en opportunité approfondi mené par l'institut national des données de santé
L'élaboration de ces recherches, études ou évaluations a donné lieu à des débats particulièrement vifs eu égard au caractère extrêmement sensible des données de santé à caractère personnel et à la finalité des traitements. La création, par la loi du 9 août 2004 85 ( * ) , de l' institut des données de santé (IDS) a constitué une première étape décisive dans le contrôle de leur contenu .
En parallèle de la réaffirmation du rôle déterminant de la Cnil en matière d'autorisation ou d'homologation des méthodes de traitement, l'IDS apporte une expertise spécifique destinée à accompagner et à vérifier la validité d'un traitement des données à des fins de recherche ou d'étude. S'y est substitué en 2016 l' institut national des données de santé (INDS) qui, en plus de ces missions, est chargé d' émettre un avis sur le caractère d'intérêt public que présente une recherche, une étude ou une évaluation, une fois cette dernière autorisée.
|
Les missions de l'INDS (article L. 1462-1 du CSP) 1) Veiller à la qualité des données de santé et aux conditions générales de leur mise à disposition, garantissant leur sécurité et facilitant leur utilisation dans le respect de la loi du 6 janvier 1978 ; 2) Assurer le secrétariat unique auprès duquel sont déposées les demandes d'autorisation de traitement de données de santé ; 3) Émettre un avis sur le caractère d'intérêt public que présente une recherche, une étude ou une évaluation ; 4) Faciliter la mise à disposition d'échantillons ou de jeux de données agrégées présentant un faible risque d'impact sur la vie privée, dans des conditions préalablement homologuées par la Cnil ; 5) Contribuer à l'expression des besoins en matière de données anonymes et de résultats statistiques, en vue de leur mise à la disposition du public. |
L'action de l'INDS se situe en amont et en aval de la réalisation du traitement (article L. 1461-3 du CSP).
En amont du traitement , l'INDS est :
- avant l'autorisation d'accès, qualifié pour déterminer la finalité d'intérêt public de la recherche, de l'étude ou de l'évaluation. Cette mission est assuré par un comité d'expertise sur l'intérêt public (CEIP) ;
- une fois l'autorisation d'accès délivrée, destinataire, le cas échéant, de l'autorisation délivrée par la Cnil, dont il assure la publication, mais aussi de la déclaration des intérêts du demandeur du traitement ainsi que d'un protocole d'analyse précisant les moyens d'en évaluer la validité et les résultats.
Là où la Cnil se limite à la vérification ponctuelle et a posteriori de la conformité technique du traitement aux référentiels qu'elle établit, l'INDS assure un contrôle d'opportunité sur la finalité de l'étude .
En aval du traitement , l'INDS est récipiendaire, dans un délai raisonnable, de la méthode, des résultats de l'analyse et des moyens d'en évaluer la validité. Il en assure également la publication.
|
Le droit existant en matière de traitement des données de santé à des fins de recherche, d'étude ou d'évaluation a donc subi une double évolution favorisant : |
|
- l' assouplissement des conditions d'accès aux données , fondé sur une responsabilisation accrue des responsables de traitements et un contrôle a posteriori de la Cnil ; |
|
- en parallèle, un renforcement du contrôle en opportunité exercé par l'INDS sur les conditions et les résultats du traitement . |
B. Le droit proposé
1. Une architecture globale des données de santé élargie aux données cliniques
L'article 11 procède à une redéfinition en profondeur de l'architecture globale des données de santé. En plus des cinq grandes bases de données qui alimentent le SNDS, le projet de loi y ajoute ( 1° du II, 2° du VI et 4° du VII ) les données recueillies à l'occasion d'activités de prévention, de diagnostic, de soins ou de suivi médico-social .
Le SNDS était jusqu'alors composé exclusivement de données médico-administratives , uniquement obtenues par la liquidation d'une prestation de soins livrée à un assuré. Les données visées par l'article 11 du projet de loi sont pour leur part des données cliniques , de nature qualitative, renseignées par le professionnel de santé à l'occasion d'une consultation ou d'un suivi. Les données médico-administratives sont recueillies par leurs collecteurs à titre obligatoire ; les données cliniques recueillies par les praticiens dans le cadre de la consultation ou du suivi ne revêtant pas un tel caractère, le a) du 1° du I supprime le critère obligatoire afin de permettre leur intégration au SNDS.
Aux termes de l'étude d'impact, cet élargissement du SNDS a pour objectif de « démultiplier l'utilisation du SNDS aussi bien en recherche clinique qu'en termes de nouveaux usages notamment ceux liés au développement des méthodes d'intelligence artificielle ». Cette initiative s'inscrit dans l'objectif plus large annoncé par le Gouvernement d'une exploitation plus performante des données de santé, à des fins de performance de la recherche, de l'appui au personnel de santé et du pilotage du système de santé. Le croisement des données médico-administratives, dont le contenu se « limite » aux parcours de soins des individus concernés, et des données cliniques, qui renseignent sur leurs profils de soins , a vocation à satisfaire cet objectif.
Comme relevé par le Conseil d'État, cet ajout, même s'il « modifie significativement le champ du SNDS », ne pose pas de difficulté juridique particulière dans la mesure où ces données cliniques, qui revêtent la nature de données de santé, s'inscrivent dans la cohérence de sa mission originelle.
2. Une gestion largement redéfinie
a) Une gestion décentralisée favorisant la création d'entrepôts de données multiples
L'étude d'impact souligne que « compte tenu de l'élargissement du périmètre du SNDS, il n'est plus envisageable que la Cnam, qui a la charge de la maîtrise d'ouvrage de l'applicatif, demeure l'unique responsable du traitement et centralisateur ». En conséquence, l'article 11 du projet de loi ( 2° du II, 3° du VII et 6° du XI ) prévoit une mise en oeuvre décentralisée et opérée par plusieurs organismes responsables, qui seront désignés par décret en Conseil d'État après avis de la Cnil .
Il s'agit là d'une modification importante : l'accès au SNDS ne pouvait jusqu'alors être réalisé que par l'unique biais de l'entrepôt de données national géré par la Cnam. Lui seront substitués plusieurs entrepôts de données (tous alimentés par l'ensemble des données du SNDS) gérés par différents organismes. L'objectif de cette mesure est notamment de limiter la constitution d'entrepôts de données « secondaires » et spécifiques à certains fournisseurs de données (notamment les établissements de santé). En effet, malgré l'intérêt de ces initiatives, elles présentaient le triple risque :
- d'une approche nécessairement limitée à une certaine patientèle, une aire géographique, ou un type de prestation ;
- de l'émergence de bases de données concurrentes ;
- du développement d'un réflexe « propriétaire » de l'initiateur de la base de données et de réticences à en verser certains éléments au SNDS.
b) Un élargissement des organismes collecteurs
Outre les organismes collecteurs actuellement habilités à alimenter le SNDS, le projet de loi y ajoute les « professionnels de santé » ( b) du 1° du I ), en cohérence avec l'intégration des données cliniques. Comme l'a souligné notre collègue député et rapporteur Thomas Mesnier, « viser les professionnels de santé accroît considérablement la capacité de collecte, indépendamment de la structure d'emploi. [...] Tous les acteurs de soins sont autorisés à effectuer des collectes de données de santé ».
c) Des destinataires inchangés
Les destinataires des données de santé, ainsi que les conditions sous lesquelles elles sont mises à disposition auprès du public, ne sont pas modifiés par le projet de loi.
d) Des finalités assouplies
Le projet de loi maintient les deux finalités actuelles de mise à disposition pour consultation et de traitement pour les données de santé à caractère personnel. Néanmoins, pour cette seconde finalité, comme le souligne le Conseil d'État, il « modifie l'accès aux données contenues dans le SNDS en supprimant la condition tenant à la poursuite d'une finalité de recherche, d'étude ou d'évaluation ».
Le projet de loi procède, par conséquent, à une réécriture globale des dispositifs régissant les motifs d'accès au SNDS. Les articles L. 1460-1 ( c) et d) du 1° et 2° du I ), L. 1461-3 ( a) et b) du 1° et a), b) et c) du 2° du III ), L. 1461-5 ( V ) et L. 1461-7 ( 1° du VI ) du CSP ne mentionnent donc plus la finalité de recherche, d'étude ou d'évaluation et font désormais référence à la notion plus large de « traitement de données concernant la santé ». À noter néanmoins qu'est conservée, à l'article L. 1461-3, la condition de respect d'un motif d'intérêt public pour qu'un traitement soit autorisé .
Aux termes de l'étude d'impact, la suppression de la finalité de recherche permettra « la constitution d'entrepôts de données ou l'implémentation automatique des données du système national des données de santé dans les registres de suivi de certains dispositifs médicaux ». Il va sans dire qu'un pareil assouplissement des usages autorisés des données de santé à caractère personnel ne peut que s'accompagner d'un renforcement de leur protection.
3. Une modification profonde du régime de protection des données de santé
L'article 11 du projet de loi apporte plusieurs modifications à la loi du 6 janvier 1978, dans sa rédaction issue de l'ordonnance du 12 décembre 2018 86 ( * ) , elle-même assurant la transposition du RGPD ( 3° du II , 2° du VII et XII ).
a) Un assouplissement du régime d'accès
Les différents régimes définissant les conditions d'accès aux données pour les responsables de traitement selon la finalité du traitement (articles 66 et 73 de la loi du 6 janvier 1978 dans sa version à venir) ne sont pas substantiellement modifiés. Les nouveaux traitements de données de santé devront donc se conformer aux conditions inchangées soit de l'article 66 (déclaration de conformité à un référentiel de la Cnil ou, à défaut, autorisation de cette dernière) dans le cas général d'un traitement, soit de l'article 73 (déclaration de conformité à une méthodologie de référence de la Cnil) dans le cas d'un traitement ayant une finalité de recherche.
L'article 11 procède toutefois à deux assouplissements significatifs.
Le premier concerne le régime d'accès concernant les traitements mettant en oeuvre le NIR . Jusqu'alors, ces traitements relevaient du régime restrictif de l'article 30 de la loi du 6 janvier 1978 dans sa version à venir, qui n'autorisait ces traitements que pour un nombre limité de responsables définis par décret en Conseil d'État, à l'exception des traitements ayant des finalités de recherche, qui eux relevaient de l'article 73. L'article 11 élargit cette exception aux traitements mettant en oeuvre le NIR et « servant à constituer des bases de données à des fins ultérieures de recherche » ( 1° du XI ).
Le second ( a) du 5° du XI ) concerne les accès aux données de santé dans le cas d'une absence de déclaration de conformité préalable et d'une nécessité d'une autorisation délivrée par la Cnil . Cette autorisation sera désormais délivrée après l'avis d'un « comité éthique et scientifique pour les recherches, les études et les évaluations dans le domaine de la santé », qui a vocation à se substituer au Cerees ainsi qu'au CEIP (cf. infra sur la disparition de l'INDS). Ainsi que le souligne l'étude d'impact, « actuellement, les demandes d'autorisation [...] sont potentiellement expertisées par deux comités : le Cerees et le CEIP. Cette double expertise introduit d'une part un niveau de complexité élevé pour les demandeurs et d'autre part un partage de l'expertise parfois complexe entre les deux comités ».
b) Un renforcement de la pseudonymisation
La contrepartie de cet assouplissement du régime d'accès réside dans le renforcement de la pseudonymisation des données . Le Conseil d'État a effectivement noté que « le projet de loi prévoit de rendre irréversible la pseudonymisation en supprimant les dispositions du code de la santé publique autorisant la conservation séparée des données permettant une réidentification des personnes ». Deux dispositions de l'article 11 remplissent cet objectif :
- l'impossibilité irréfragable de l'identification directe ou indirecte des personnes concernées par les données de santé à caractère personnel, alors que le droit existant en maintenait la possibilité à la faveur d'une disposition législative spécifique ( e) du 1° du I ) ;
- la suppression de l'organisme distinct « tiers de confiance » habilité à détenir, en dehors du responsable du SNDS, des données de santé potentiellement réidentifiantes ( IV et 1° du VII ).
c) La création d'une plateforme des données de santé (PDS) en substitution de l'INDS
L'article 11 procède à la création d'un groupement d'intérêt public appelé « plateforme des données de santé » ( 1° du VIII ), destiné à succéder à l'INDS ( IX ), au plus tard le 31 décembre 2019 ( XIII ). Ses parties constitutives sont identiques. Ses missions sont néanmoins, pour certaines, substantiellement modifiées ( 2° du VIII ) ; il sera désormais chargé de :
- réunir, organiser et mettre à disposition les données du SNDS et de promouvoir l'innovation dans leur utilisation ;
- d'assurer le secrétariat unique des demandes de traitement ( b) du 5° du XI , par coordination) ;
- d'assurer le secrétariat du nouveau comité éthique et scientifique pour les recherches, les études et les évaluations dans le domaine de la santé ;
- de contribuer à l'élaboration des référentiels et des méthodologies de référence auxquels les responsables de traitement doivent déclarer leur conformité ( a) du 2° et 4° du XI , par coordination) ;
- de procéder, pour le compte d'un tiers et à la demande de ce dernier, à des opérations nécessaires et à la réalisation d'un traitement de données issues du SNDS .
À ce stade, deux modifications principales méritent d'être soulignées : la possibilité ouverte à la PDS d'agir comme sous-traitant d'un responsable de traitement, sur simple demande de ce dernier et la disparition de l'avis sur l'intérêt public d'une recherche .
Concernant ce dernier aspect, il convient toutefois de noter qu'est maintenue la possibilité pour le nouveau comité éthique et scientifique, en substitution de l'INDS, de se saisir ou d'être saisi sur le caractère d'intérêt public que présente une recherche ( b) du 2° et 3° du XI ).
L'article 11 du projet de loi crée par ailleurs un article L. 1462-2 du CSP ( 3° du VIII ) qui précise que la PDS pourra recruter, outre des agents des trois fonctions publiques, des personnels dont les contrats relèvent du droit privé .
Enfin, il doit être souligné que le contrôle d'opportunité exercé par l'INDS (déclaration d'intérêts et communication des résultats et de la méthode une fois le traitement réalisé) est maintenu pour la PDS, à une exception près : l'article 11 prévoit que « les résultats de l'analyse et les moyens d'en évaluer la validité » ne seront désormais communiqués à la PDS que pour les seuls traitements réalisés à des fins de recherche ( c) du 2° du III ). La PDS n'aura donc plus à connaître des résultats des traitements de données de santé qui ne s'inscrivent pas dans cette finalité.
II - Les modifications adoptées par l'Assemblée nationale
A. En commission des affaires sociales
Outre quatorze amendements rédactionnels, la commission des affaires sociales a adopté quatre amendements visant à :
- sur l'initiative des membres du groupe La République En Marche, enrichir le SNDS d'une nouvelle catégorie de données de santé , à savoir les « données à caractère personnel des enquêtes dans le domaine de la santé », lorsque ces dernières sont appariées avec les autres données du SNDS ;
- sur l'initiative du rapporteur, préciser le champ des missions de la nouvelle PDS , en y ajoutant l'information des patients, la promotion de leurs droits, notamment leur droit d'opposition à la levée du secret médical ;
- sur l'initiative du Gouvernement, étendre le champ des traitements de données de santé à caractère personnel mis en oeuvre par l'autorité publique (et échappant de ce fait au cadre des articles 66 et 73 de la loi du 6 janvier 1978 dans sa version à venir) aux traitements dont la finalité est la conception, le suivi ou l'évaluation des politiques publiques dans le domaine de la santé ;
- sur l'initiative du rapporteur, préciser la composition du nouveau comité éthique et scientifique , dont le secrétariat sera assuré par la nouvelle PDS et qui aura pour tâches de donner un avis sur l'intérêt public d'une recherche et de donner un avis préalable à l'autorisation donnée par la Cnil en cas de non-conformité d'une déclaration préalable par un demandeur. Cet amendement précise notamment que ne pourront participer à une délibération du comité « les personnes qui ne sont pas indépendantes du promoteur et de l'investigateur de la recherche, de l'étude ou de l'évaluation examinée ».
B. En séance publique
L'Assemblée nationale a approfondi en séance publique, sur l'initiative du groupe Modem, le champ du SNDS en y ajoutant les données recueillies lors des visites médicales et de dépistage obligatoires en milieu éducatif, les données recueillies par les services de protection maternelle et infantile et les données de santé recueillies lors des visites d'information et de prévention dans un cadre professionnel.
Elle a par ailleurs élargi les missions de la future PDS , sur l'initiative du groupe La République En Marche, à la diffusion de normes de standardisation pour l'échange et l'exploitation des données de santé, en tenant compte de standards européens et internationaux, et, sur l'initiative du Gouvernement, à l'accompagnement financier des porteurs de projets sélectionnés dans le cadre d'appels à projets lancés à son initiative.
Elle a également adopté un amendement, sur l'initiative du groupe La République En Marche, visant à assurer une parité hommes-femmes au sein du nouveau comité éthique et scientifique .
Elle a enfin adopté, sur l'initiative de notre collègue Albane Gaillot, un amendement prévoyant la remise d'un rapport au Parlement sur la nouvelle PDS .
L'Assemblée nationale a adopté cet article ainsi modifié.
III - La position de la commission
A. Une approbation d'ensemble du dispositif
Outre l'intérêt scientifique présenté par l'élargissement du contenu du SNDS, votre commission en souligne également le caractère nécessaire compte tenu de la complexification des profils pathologiques .
Les traitements statistiques traditionnels, appuyés jusqu'ici sur les données médico-administratives, empruntaient une méthode d'analyse dite « hypothético-déductive », qui consistait à réfléchir en amont aux données à utiliser et aux variables qui permettraient de les exploiter. Cette méthode, en définissant des modèles préalables, présentait le risque de biais humains liés à la définition de cadres d'analyse a priori . A contrario , la méthode statistique du « big data » permet de brasser largement des données sans modèle préalable et sans postulat scientifique, laissant les algorithmes extraire des régularités ou des incongruités de la masse de données en présence 87 ( * ) .
La complexification du contexte clinique et l'importance accrue des profils polypathologiques nécessitent de plus en plus de recourir à des méthodes statistiques qui limitent les biais préalables mais qui, par conséquent, requièrent des bases de données les plus exhaustives possible.
Si votre commission reconnaît le caractère sensible du sujet traité par l'article 11, elle estime que les modifications apportées par ce dernier ne sont pas de nature à menacer l'usage et la sécurité des données de santé à caractère personnel, pour trois raisons :
- la fin du monopole de gestion du SNDS par la Cnam et l'attribution de la compétence gestionnaire à plusieurs organismes seront encadrées par un décret en Conseil d'État pris après avis de la Cnil ;
- l'enrichissement des données du SNDS n'a pas vocation à compromettre leur pseudonymisation , dont l' impératif est par ailleurs renforcé ;
- enfin, l'introduction potentielle d'acteurs privés au sein de la PDS, chargée de se prononcer sur l'intérêt public des demandes d'accès aux données de santé, a été régulée de façon bienvenue par la disposition introduite à l'Assemblée nationale selon laquelle la demande d'accès devra être examinée par des personnes strictement indépendantes du promoteur ou de l'instigateur de la demande .
Votre commission tient toutefois à souligner qu'avec la disparition de la finalité d'étude, d'évaluation ou de recherche, l'examen du caractère d'intérêt public deviendra le seul critère de définition de la légalité d'un traitement de données de santé (en dehors, bien entendu, du maintien des finalités interdites). Cette évolution rend particulièrement urgentes la clarification et la circonscription de la notion d'intérêt public, dont l'appréciation est à ce jour entièrement laissée aux comités de l'INDS.
Pour l'heure, l'une des seules mentions explicites de la notion d'intérêt public figure à l'article 66 de la loi du 6 janvier 1978, dans sa version ultérieure au 1 er juin 2019, qui en donne une occurrence possible : « la garantie de normes élevées de qualité et de sécurité des soins de santé et des médicaments ou des dispositifs médicaux constitue une finalité d'intérêt public ».
Le rapporteur de la commission des affaires sociales de l'Assemblée nationale, ayant identifié les risques liés à cette définition encore lacunaire, indique que, pour l'heure, l'INDS (future PDS) intègre dans l'intérêt public la clarté et la sincérité des finalités, ainsi que la garantie de l'intégrité scientifique du traitement.
B. Les modifications apportées par votre commission
Outre cinq amendements rédactionnels (amendements COM-317, COM-318, COM-319, COM-320 et COM-321 du rapporteur), votre commission a souhaité intégrer les informations relatives à la perte d'autonomie des personnes âgées aux données recueillies dans le cadre du SNDS. La collecte de cette donnée particulière présente un intérêt majeur à deux égards :
- outre son intérêt strictement thérapeutique, elle se révèlera déterminante pour la conduite d'une véritable politique de la prévention de la perte d'autonomie ;
- par ailleurs, elle permettra un pilotage plus fin des dépenses de santé des personnes dépendantes accueillies en établissement (Ehpad), qui bénéficient en même temps du forfait versé à l'établissement et des dépenses de soins de ville qu'elles peuvent encore solliciter.
Votre commission a donc adopté un amendement COM-316 de votre rapporteur dans ce sens.
La commission a adopté cet article ainsi modifié.
Article 11 bis A
(art. L. 1413-3 du code de la santé
publique)
Désignation de l'État comme titulaire des droits
sur les bases de données anonymisées et sur le
matériel biologique transmis en cas de risque grave pour la santé
humaine
Objet : Cet article, inséré par l'Assemblée nationale, propose d'attribuer à l'État l'exercice des droits sur les bases de données anonymisées transmises à l'Agence nationale de santé publique dans l'exercice de ses missions et de lui reconnaître la propriété du matériel biologique transmis aux centres nationaux de référence en cas de risque grave pour la santé humaine.
I - Le dispositif adopté par l'Assemblée nationale
L' Agence nationale de santé publique (ANSP), créée par la loi du 26 janvier 2016 portant modernisation de notre système de santé, est un établissement public administratif de l'État ayant pour missions :
- l'observation épidémiologique et la surveillance de l'état de santé des populations ;
- la veille sur les risques sanitaires menaçant les populations ;
- la promotion de la santé et la réduction des risques pour la santé ;
- le développement de la prévention et de l'éducation pour la santé ;
- la préparation et la réponse aux menaces, alertes et crises sanitaires ;
- le lancement de l'alerte sanitaire.
Pour l'exercice de ces missions, l'article L. 1413-3 du code de la santé publique (CSP) prévoit que l'ANSP s'appuie sur un réseau national de santé publique qu'elle organise et qu'elle anime . La coopération des membres de ce réseau s'effectue par voie de convention ou par participation à des groupements d'intérêt public dont l'ANSP est membre. Elle peut par ailleurs s'appuyer sur un réseau de centres nationaux de référence pour la lutte contre les maladies transmissibles.
En outre, lorsqu'il s'avère nécessaire de prévenir ou de maîtriser des risques graves pour la santé humaine, l'article L. 1413-8 du CSP prévoit que tout laboratoire de biologie médicale public ou privé est tenu de transmettre aux centres nationaux de référence le matériel biologique en sa possession en rapport avec de tels risques. Ce matériel est conservé dans une collection nationale de ressources biologiques d'intérêt national pour la santé publique .
Un amendement déposé en séance publique à l'Assemblée nationale par les membres du groupe La République En Marche précise le régime applicable à l'utilisation des données et matériels transmis par les différentes parties aux réseaux coordonnés et organisés par l'ANSP. Cet amendement prévoit notamment que :
- lorsque les réseaux de santé publique animés par l'ANSP ont à connaître de bases de données anonymisées, les droits exercés sur ces dernières restent exercés par l'État . En conséquence, les conventions ou groupements d'intérêt public initiés par l'ANSP ne peuvent soustraire à l'État la maîtrise des données enregistrées dans des bases données, publiques ou privées ;
- le matériel biologique transmis aux centres nationaux de référence en cas de risque grave pour la santé humaine reste propriété de l'État .
II - La position de la commission
Sur proposition de son rapporteur, la commission a adopté l' amendement COM-322 de coordination.
La commission a adopté cet article ainsi modifié.
Article 11 bis
(art. L. 161-28-1 du code de la
sécurité sociale, art. 65 de la loi n° 78-17 du
6 janvier 1978 relative à l'informatique, aux fichiers et aux
libertés)
Permettre à l'assurance maladie d'utiliser le
SNIIRAM
pour l'ensemble de ses missions
Objet : Cet article, inséré par l'Assemblée nationale, propose de modifier la nature des missions du Sniiram en cohérence avec la redéfinition du système national des données de santé (SNDS) prévue par l'article 11 du projet de loi.
I - Le dispositif adopté par l'Assemblée nationale
Les missions du système national d'information interrégimes d'assurance maladie (Sniiram), désigné par le code de la santé publique comme l'un des contributeurs du système national des données de santé (SNDS), sont définies à l'article L. 161-28-1 du code de la sécurité sociale. Ces missions sont :
- la connaissance des dépenses de l'ensemble des régimes d'assurance maladie par circonscription géographique, par nature de dépenses, par catégorie de professionnels responsables de ces dépenses et par professionnel ou établissement ;
- la transmission en retour aux prestataires de soins d'informations pertinentes relatives à leur activité et leurs recettes, et s'il y a lieu à leurs prescriptions ;
- la définition, à la mise en oeuvre et à l'évaluation de politiques de santé publique ;
- la constitution du SNDS.
Jugées trop restrictives, notamment au regard de l'évolution des missions du SNDS définies à l'article 11 du projet de loi, les trois premières missions ont été remplacées , par un amendement adopté en commission des affaires sociales à l'initiative du Gouvernement, par une mission plus large d'accompagnement des missions des organismes chargés de la gestion d'un régime de base d'assurance maladie ( I ).
Par coordination, la même modification est apportée à la loi du 6 janvier 1978 relative à l'informatique, aux fichiers et aux libertés ( II ).
II - La position de la commission
La commission a adopté cet article sans modification.
* 80 Loi n° 2016-41 du 26 janvier 2016 de modernisation de notre système de santé.
* 81 Loi n° 78-17 du 6 janvier 1978 relative à l'informatique, aux fichiers et aux libertés.
* 82 Règlement (UE) 2016/679 du 27 avril 2016.
* 83 Loi n° 2018-493 du 20 juin 2018 relative à la protection des données personnelles.
* 84 Ces personnes sont énumérées à l'article R. 1461-12 du CSP.
* 85 Loi n° 2004-806 du 9 août 2004 relative à la politique de santé publique.
* 86 Ordonnance n° 2018-1125 du 12 décembre 2018 prise en application de l'article 32 de la loi n° 2018-493 du 20 juin 2018 relative à la protection des données personnelles et portant modification de la loi n° 78-17 du 6 janvier 1978 relative à l'informatique, aux fichiers et aux libertés et diverses dispositions concernant la protection des données à caractère personnel.
* 87 A. CHEVALLIER et G. TAUBER, « Big data et protection sociale : au-delà de la lutte contre la fraude, des opportunités à saisir pour améliorer l'accès aux droits », Regards , 2017/2, p. 205-215.