Rapport n° 128 (2002-2003) de M. Francis GIRAUD , fait au nom de la commission des affaires sociales, déposé le 15 janvier 2003
Disponible au format Acrobat (1,4 Moctet)
Tableau comparatif au format Acrobat (445 Koctets)
-
AVANT-PROPOS
-
I. LE CONTEXTE
-
A. UNE ÉVALUATION DU DROIT EN VIGUEUR :
LE RAPPORT D'ÉVALUATION DE LA LOI N° 94-654 PAR L'OFFICE
PARLEMENTAIRE D'ÉVALUATION DES CHOIX SCIENTIFIQUES ET
TECHNOLOGIQUES
-
B. UNE RÉFLEXION PRÉPARATOIRE :
L'ÉTUDE DU CONSEIL D'ÉTAT SUR LES LOIS BIOÉTHIQUES
-
C. UNE CONTRAINTE CROISSANTE :
L'ENVIRONNEMENT INTERNATIONAL
-
A. UNE ÉVALUATION DU DROIT EN VIGUEUR :
LE RAPPORT D'ÉVALUATION DE LA LOI N° 94-654 PAR L'OFFICE
PARLEMENTAIRE D'ÉVALUATION DES CHOIX SCIENTIFIQUES ET
TECHNOLOGIQUES
-
II. LE PROJET DE LOI
-
A. LE CONTENU DU PROJET DE LOI INITIAL : LA
CONSÉCRATION DES RÉFLEXIONS PRÉLIMINAIRES
-
B. LES MODIFICATIONS ADOPTÉES PAR
L'ASSEMBLÉE NATIONALE : OUVERTURE OU AVENTURE ?
-
1. La proclamation de quelques principes :
paix des morts et reconnaissance de la Nation aux donneurs
-
2. Le sort de l'embryon : création
possible d'embryons à des fins de recherche et autorisation de leur
transfert post mortem
-
3. L'extension des pouvoirs de l'Agence de la
procréation, de l'embryologie et de la génétique
humaine
-
4. L'affirmation de la non-brevetabilité du
vivant
-
1. La proclamation de quelques principes :
paix des morts et reconnaissance de la Nation aux donneurs
-
A. LE CONTENU DU PROJET DE LOI INITIAL : LA
CONSÉCRATION DES RÉFLEXIONS PRÉLIMINAIRES
-
III. LES PROPOSITIONS DE VOTRE COMMISSION
-
A. DON ET PRÉLÈVEMENT
D'ORGANES : FAVORISER LE PRÉLÈVEMENT POST MORTEM POUR
PRÉSERVER LES VIVANTS
-
B. ASSISTANCE MÉDICALE À LA
PROCRÉATION ET STATUT DE L'EMBRYON : DÉCLINER LE PRINCIPE DE
PRÉCAUTION
-
C. LA TUTELLE DES POUVOIRS PUBLICS SUR LE CHAMP
BIOÉTHIQUE : RECHERCHER L'EFFICACITÉ
-
A. DON ET PRÉLÈVEMENT
D'ORGANES : FAVORISER LE PRÉLÈVEMENT POST MORTEM POUR
PRÉSERVER LES VIVANTS
-
I. LE CONTEXTE
-
EXAMEN DES ARTICLES
-
CHAPITRE II
Examen des caractéristiques génétiques et identification
d'une personne par ses empreintes génétiques
-
TITRE II
-
DON ET UTILISATION DES ÉLÉMENTS
ET PRODUITS DU CORPS HUMAIN
-
Article 5
(art. L. 1211-1, L. 1211-2 , L. 1211-4, L 1211-6, L. 1211-7, L. 1211-8, L. 1211-9 du code de la santé publique)
Principes généraux du don et de l'utilisation des éléments
et produits du corps humain
-
Article 6
(art. L. 1221-5, L. 1221-8, L. 1221-12 du code de la santé publique)
Collecte, préparation et conservation du sang, de ses composants
et des produits sanguins labiles
-
Article 7
Prélèvements d'organes
-
Article 8
Principes généraux applicables aux prélèvements de tissus ou de cellules ou à la collecte de produits issus du corps humain
-
Article 9
Conditions d'élaboration des règles de bonnes pratiques
-
Article 10
(art. L 1263-1, L. 1263-2, L. 1263-3 et L. 1263-4
du code de la santé publique)
Coordination
-
Article 11
Dispositions pénales
-
Article 12
Dispositions pénales
-
Article 12 bis
Non-brevetabilité des éléments du corps humain
-
Article 5
-
TITRE III
-
PRODUITS DE SANTÉ
-
TITRE IV
-
PROCRÉATION ET EMBRYOLOGIE
-
CHAPITRE II
AGENCE DE LA PROCRÉATION, DE L'EMBRYOLOGIE ET DE LA GÉNÉTIQUE HUMAINES
-
CHAPITRE III
Diagnostic prénatal et assistance médicale à la procréation
-
Article 17
(art. L. 2131-1, L. 2131-3 à L. 2131-5 du code de la santé publique)
Diagnostics prénatal et préimplantatoire
-
Article 18
Assistance médicale à la procréation
-
Article 18 bis
Dispositions permettant d'assurer la filiation et les droits successoraux
de l'enfant né d'un transfert d'embryon réalisé après le décès du père
-
Article 17
-
CHAPITRE IV
-
RECHERCHE SUR L'EMBRYON ET LES CELLULES EMBRYONNAIRES ET FoeTALES
-
CHAPITRE V
-
DISPOSITIONS PÉNALES
-
TITRE V
-
DISPOSITIONS DIVERSES ET TRANSITOIRES
-
Article 23
Prorogation des mandats des membres
des comités d'experts
-
Article 24
Prorogation d'autorisations de prélèvements de moelle osseuse
et de cellules de la moelle hématopoïétique
-
Article 25
Dispositions transitoires relatives aux préparations de thérapie génique
et cellulaire xénogénique
-
Article 26
Dispositions transitoires relatives aux activités de conservation
et cession d'éléments du corps humain
-
Article 27
Entrée en vigueur des dispositions relatives
à la recherche sur l'embryon
-
Article 28
Dispositions applicables à Mayotte, au territoire des îles Wallis-et-Futuna, des terres australes et antarctiques françaises, en Polynésie française
et en Nouvelle-Calédonie
-
Article 29 (nouveau)
Révision de la loi et évaluation de son application
-
Article 23
-
TRAVAUX DE LA COMMISSION
-
LISTE DES PERSONNES
AUDITIONNÉES
-
I. AUDITION DE M. JEAN-FRANÇOIS MATTEI,
MINISTRE DE LA SANTÉ, DE LA FAMILLE ET DES PERSONNES HANDICAPÉES
SUR LE PROJET DE LOI RELATIF À LA BIOÉTHIQUE
(JEUDI 12 DÉCEMBRE 2002)
-
II. AUDITIONS DU MERCREDI 4 DÉCEMBRE
2002
-
A. AUDITION DU PROFESSEUR CLAUDE HURIET,
PRÉSIDENT DE L'INSTITUT CURIE
-
B. AUDITION DU PROFESSEUR AXEL KAHN, DIRECTEUR DE
L'INSTITUT COCHIN, DIRECTEUR DE RECHERCHE À L'INSTITUT NATIONAL DE LA
SANTÉ ET DE LA RECHERCHE MÉDICALE (INSERM)
-
C. AUDITION DU PROFESSEUR ARNOLD MUNNICH, CHEF DU
SERVICE GÉNÉTIQUE MÉDICALE DE L'HÔPITAL
NECKER-ENFANTS MALADES, DIRECTEUR DE RECHERCHE À L'INSTITUT NATIONAL DE
LA SANTÉ ET DE LA RECHERCHE MÉDICALE (INSERM)
-
D. AUDITION DU PROFESSEUR ISRAËL NISAND, CHEF
DE SERVICE DE GYNÉCOLOGIE-OBSTÉTRIQUE AU SIHCUS-CMCO DE
STRASBOURG
-
E. AUDITION DU PROFESSEUR LAURENT DEGOS, CHEF DU
SERVICE D'HÉMATOLOGIE DE L'HÔPITAL SAINT-LOUIS, DIRECTEUR DE
L'INSTITUT UNIVERSITAIRE D'HÉMATOLOGIE
-
F. AUDITION DU PROFESSEUR DIDIER SICARD,
PRÉSIDENT DU COMITÉ CONSULTATIF NATIONAL D'ÉTHIQUE POUR
LES SCIENCES DE LA VIE ET DE LA SANTÉ
-
G. AUDITION DE M. SADEK BELOUCIF, PROFESSEUR
D'ANESTHÉSIE-RÉANIMATION AU CHU D'AMIENS, M. MICHEL GUGENHEIM,
GRAND RABBIN, DIRECTEUR DU SÉMINAIRE ISRAÉLITE DE FRANCE,
M. PATRICK VERSPIEREN, THÉOLOGIEN, DIRECTEUR DU DÉPARTEMENT
D'ÉTHIQUE BIOMÉDICALE DU CENTRE SÈVRES, M. GEOFFROY
DE TURCKHEIM, PRÉSIDENT DE LA COMMISSION oeCUMÉNIQUE DE LA
FÉDÉRATION PROTESTANTE DE FRANCE, M. STÉPHANE MEYER,
MÉDECIN, CONSEILLER DE L'ORDRE DU GRAND ORIENT DE FRANCE
-
A. AUDITION DU PROFESSEUR CLAUDE HURIET,
PRÉSIDENT DE L'INSTITUT CURIE
-
I. AUDITION DE M. JEAN-FRANÇOIS MATTEI,
MINISTRE DE LA SANTÉ, DE LA FAMILLE ET DES PERSONNES HANDICAPÉES
SUR LE PROJET DE LOI RELATIF À LA BIOÉTHIQUE
(JEUDI 12 DÉCEMBRE 2002)
-
TABLEAU COMPARATIF
N° 128
SÉNAT
SESSION ORDINAIRE DE 2002-2003
|
Annexe au procès-verbal de la séance du 15 janvier 2003 |
RAPPORT
FAIT
au nom de la commission des Affaires sociales (1) sur le projet de loi, ADOPTÉ PAR L'ASSEMBLÉE NATIONALE, relatif à la bioéthique ,
Par M. Francis GIRAUD,
Sénateur.
(1) Cette commission est composée de : M. Nicolas About, président ; MM. Alain Gournac, Louis Souvet, Gilbert Chabroux, Jean-Louis Lorrain, Roland Muzeau, Georges Mouly, vice-présidents ; M. Paul Blanc, Mmes Annick Bocandé, Claire-Lise Campion, M. Jean-Marc Juilhard, secrétaires ; MM. Henri d'Attilio, Gilbert Barbier, Christian Bergelin, Joël Billard, Mme Brigitte Bout, MM. Jean-Pierre Cantegrit, Bernard Cazeau, Jean Chérioux, Mme Michelle Demessine, M. Gérard Dériot, Mme Sylvie Desmarescaux, MM. Claude Domeizel, Michel Esneu, Jean-Claude Étienne, Guy Fischer, Jean-Pierre Fourcade, Serge Franchis, André Geoffroy, Francis Giraud, Jean-Pierre Godefroy, Mme Françoise Henneron, MM. Philippe Labeyrie, Roger Lagorsse, André Lardeux, Dominique Larifla, Dominique Leclerc, Marcel Lesbros, Mmes Valérie Létard, Nelly Olin, Anne-Marie Payet, M. André Pourny, Mme Gisèle Printz, MM. Henri de Raincourt, Gérard Roujas, Mmes Janine Rozier, Michèle San Vicente, MM. Bernard Seillier, André Vantomme, Alain Vasselle, Paul Vergès, André Vézinhet.
Voir les numéros :
Assemblée nationale ( 11 ème législ.) : 3166 , 3528 et T.A. 763
Sénat : 189 (2001-2002)
|
Vie, médecine et biologie. |
AVANT-PROPOS
Mesdames, Messieurs,
En 1994, après plusieurs années de réflexions, encouragé par les avancées considérables réalisées dans les domaines de la génétique et de la médecine de la reproduction, le Parlement s'est résolu à doter la France d'un cadre législatif. Il s'agit des trois lois de juillet 1994 dites de bioéthique.
Aujourd'hui, l'apport bénéfique de ces premières lois n'est plus guère contesté : le législateur avait défini le droit sans apparaître comme le porte-parole d'aucune partie, qu'elle soit scientifique, philosophique ou religieuse.
Mieux informés, les citoyens s'interrogent sur les questions essentielles qui touchent à la personne humaine, sa dignité, le respect qu'on lui doit, le bien-fondé et la sincérité des exigences de la recherche et de l'industrie.
Les professionnels concernés ont admis, dans leur immense majorité, la nécessité d'une régulation de leur pratique et reviennent aujourd'hui d'eux-mêmes vers le législateur témoignant de leur attente, voire de leur impatience, à ce que la révision alors prévue des lois de bioéthique précise mieux aujourd'hui les limites de leur action.
Dans l'attente de cette révision, les travaux se sont poursuivis et de nombreuses institutions, compétentes dans le domaine du droit ou de l'éthique, se sont interrogées sur les modifications qu'il serait nécessaire d'apporter au corpus juridique voté en 1994.
Le Parlement, pour sa part, n'est pas resté inactif. Plusieurs rapports de l'Office public d'évaluation des choix scientifiques et technologiques rendent compte de cette attention. En vue de l'examen du présent projet de loi, l'Assemblée nationale a conduit une importante mission d'information dont les conclusions ont été rendues publiques à la fin du mois de juin 2001.
Rarement, donc, un tel projet ne fut précédé d'une réflexion préalable aussi complète. Mais c'est in fine avec un retard certain que celui-ci a été déposé par le Gouvernement sur le bureau de l'Assemblée nationale le 20 juin 2001.
Ce retard initial de deux ans aurait pu être compensé par une gestion plus dynamique de l'ordre du jour parlementaire mais, l'encombrement de ce dernier et les échéances électorales importantes de l'année 2002 n'ont pas permis que l'ancien gouvernement, non plus que le nouveau, n'inscrive l'examen de ce texte à l'ordre du jour du Sénat avant le 28 janvier prochain.
Transmis par l'Assemblée nationale le 22 janvier 2001 et renvoyé pour examen à la commission des Affaires sociales, le délai laissé avant l'examen du texte a permis à cette dernière de se livrer à un examen approfondi de ses dispositions et à l'ensemble des consultations nécessaires en deux étapes.
Votre rapporteur a, d'une part, procédé de manière précoce à une série d'auditions auxquelles ses collègues étaient invités à se joindre. Votre commission a, d'autre part, lors de deux séances d'auditions publiques, entendu un certain nombre de personnalités qualifiées ainsi que le nouveau ministre en charge de la santé.
Le nouveau Gouvernement a pris la sage décision de ne pas interrompre la procédure législative pour présenter un texte qui serait le sien. En effet, le présent projet comporte beaucoup de mesures consensuelles, ou d'autres qui traversent les clivages partisans. Pour la deuxième fois, le projet de loi relatif à la bioéthique sera examiné à cheval sur deux législatures séparées par une alternance politique. Cette situation, qui fut déjà celle des lois de 1994, n'a porté aucun préjudice à ces dernières.
En sus de l'examen détaillé au sein de ce rapport de l'ensemble de ses dispositions, certains aspects du texte doivent faire l'objet ici d'un bref développement.
Il s'agit en premier lieu des risques du clonage reproductif dont l'actualité récente a démontré qu'il incarnait à lui seul la meilleure illustration des dérives que peuvent engendrer les sciences du vivant. L'indignation quasi générale soulevée par les allégations de certains, qui auraient procédé à la reproduction par clonage d'un être humain, est un encouragement puissant à l'interdiction et à la condamnation de cette pratique.
Mais les dispositions prévues par le présent projet ne valent que pour notre pays. C'est donc à l'échelon européen et mondial qu'il convient d'oeuvrer afin que cette pratique soit proscrite. Lors de son audition par votre commission, M. Jean-François Mattei, ministre de la santé, de la famille et des personnes handicapées, a fait part de sa volonté ferme que soit adopté, au niveau mondial, un corpus juridique contraignant. Les événements récents ne peuvent qu'encourager cette démarche.
Dans son avant-projet de loi, le précédent gouvernement avait envisagé d'autoriser la pratique du clonage à des fins thérapeutiques, arguant des perspectives médicales que celui-ci pourrait ouvrir.
De nombreux avis négatifs, en particulier celui du Conseil d'Etat, l'ont incité à ne pas faire figurer une telle possibilité. L'actualité montre la sagesse d'un tel retrait. Fondé sur une technique identique à celle du clonage reproductif qu'elle banaliserait, le clonage thérapeutique conduirait tôt ou tard quelques scientifiques ayant appris à la maîtriser, à la tentation de devenir des « apprentis sorciers ». Il doit être expressément interdit.
La question de l'embryon est sans nul doute le point le plus délicat abordé par le projet de loi : tel fut-il en 1994, tel reste-t-il aujourd'hui.
Lors de l'examen des premières lois de bioéthique, le législateur avait renoncé à définir son statut juridique, se tenant ainsi prudemment à l'écart d'un débat philosophique et biologique que nul ne saurait prétendre trancher d'autorité. Cette position n'est d'ailleurs pas modifiée par le projet de loi tel que l'a adopté l'Assemblée nationale.
En revanche, à défaut de définir son statut juridique, il est possible et même nécessaire de décider de son sort. En 1994, le législateur avait strictement interdit que des recherches soient menées sur l'embryon, mais avait admis qu'à titre dérogatoire, des études qui ne porteraient pas atteinte à son intégrité soient réalisées. De fait, ces études ont abouti à la possibilité du diagnostic préimplantatoire.
Mais fort peu de choses avaient alors été prévues pour décider du sort des embryons créés dans le cadre d'un projet parental et qui, pour des raisons diverses, n'avaient finalement pu être implantés. Or aujourd'hui, le nombre de ces derniers, qui se chiffre à plusieurs dizaines de milliers, soulève un grave dilemme.
Pour les uns, aucune recherche ou prélèvement ne saurait être admis par respect pour cette « personne humaine potentielle » , telle que définie par le Comité national consultatif d'éthique. Pour d'autres, avec l'assentiment explicite du couple qui a accompli ou renoncé à son projet parental et qui n'a plus de projet pour les embryons restants, il pourrait être envisagé des prélèvements de cellules embryonnaires à des fins de recherche.
Cette dernière, qui se ferait sur des cellules souches embryonnaires et non sur des embryons, n'est sans doute pas conforme au principe de protection de la vie tel qu'il figure dans le code civil. C'est donc la proscription de cette recherche qu'il convient d'inscrire dans nos principes.
Toutefois, peut-on et doit-on fermer à jamais une porte à la recherche sans rien connaître de sa potentialité et de son innocuité ? Le législateur doit, en 2003, conserver la même modestie qu'en 1994, et reconnaître lui-même la possibilité d'une dérogation transitoire et strictement encadrée aux principes fondamentaux qu'il a consacrés, en permettant que des recherches soient menées uniquement sur des embryons qui ne font plus l'objet d'un accord parental après accord des membres du couple.
Ces quelques réflexions sur l'ouverture ou la fermeture de la recherche sur l'embryon doivent nécessairement s'accompagner d'une mise en garde solennelle quant à la présentation qui est faite à nos concitoyens des espoirs que font naître les thérapies cellulaires, qu'elles recourent aux cellules embryonnaires ou aux cellules souches adultes.
De manière quelque peu irresponsable, on a pu prénommer ces dernières « les cellules de l'espoir », accréditant dans l'esprit du public l'espérance de voir surgir à court ou moyen terme des thérapies efficaces en réponse aux nombreuses pathologies contre lesquelles la science reste aujourd'hui impuissante.
Menées de front avec les recherches sur les cellules d'origine embryonnaire, les recherches sur les cellules souches adultes doivent sans nul doute être développées et soutenues, leur utilisation ne posant en effet pas de difficultés éthiques. Mais il doit être clairement affirmé que des années de recherches seront nécessaires avant qu'apparaissent les premiers espoirs thérapeutiques concrets.
La compétition scientifique qu'évoque ce processus invite votre rapporteur à conclure son avant-propos par un mot relatif à la brevetabilité du vivant.
Les quelques années qui séparent le présent projet de loi des lois de 1994 ont été marquées par la formidable course au séquençage du génome humain. Là encore, la science bouscule le droit et le législateur doit s'interroger s'il est possible ou non que des éléments du corps humain, et notamment ses gènes, fassent l'objet d'une quelconque protection intellectuelle.
L'Assemblée nationale a adopté une position de principe forte qui a le mérite de réaffirmer son opposition ferme à la brevetabilité du vivant mais qui prend l'exact contre-pied des dispositions prévues par l'article 5 de la directive européenne relative à la protection des inventions biotechnologiques.
Cette disposition a-t-elle vocation à affirmer un soutien ferme au Gouvernement dans l'optique d'une renégociation de la directive ou appelle-t-elle une rédaction de compromis entre le principe qu'elle défend et les dispositions du droit européen ?
C'est avec une certaine impatience que votre rapporteur attend, dans sa traduction juridique, la proposition médiane évoquée par M. Jean-François Mattei devant votre commission, car c'est au Gouvernement qu'il appartiendra in fine de défendre au niveau européen le contenu de cette rédaction nouvelle.
|
Loi n° 94-548 du 1 er juillet 1994 relative au traitement de données nominatives ayant pour fin la recherche dans le domaine de la santé et modifiant la loi n° 78-17 du 6 janvier 1978 relative à l'informatique, aux fichiers et aux libertés Première lecture - Assemblée nationale : Projet de loi n° 2601 ; Rapport de M. Bioulac, au nom de la commission spéciale, n° 2871 ; Discussion les 19, 20 et 23 novembre 1992 et adoption le 25 novembre 1992. - Sénat : Projet de loi, adopté par l'Assemblée nationale, n° 68 (1992-1993) ; Rapport de M. Alex Türk, au nom de la commission des lois, n° 209 (1993-1994) ; Discussion les 13, 14, 17, 18, 19, 20 et 21 janvier 1994 et adoption le 21 janvier 1994. Deuxième lecture - Assemblée nationale : Projet de loi, modifié par le Sénat, n° 962 ; Rapport de M. Jean-François Mattei, au nom de la commission spéciale, n° 1057 ; Discussion le 19 avril 1994 et adoption le 20 avril 1994. - Sénat : Projet de loi, adopté avec modifications par l'Assemblée nationale en deuxième lecture, n° 355 (1993-1994) ; Rapport de M. Alex Türk, au nom de la commission des lois, n° 397 (1993-1994) ; Discussion et adoption le 19 mai 1994. Nouvelle lecture - Assemblée nationale : Projet de loi, modifié par le Sénat en deuxième lecture, n° 1268 ;Rapport de M. Jean-François Mattei, au nom de la commission spéciale, n° 1338 ; Discussion et adoption le 20 juin 1994. Loi n° 94-653 du 29 juillet 1994 relative au respect du corps humain Première lecture - Assemblée nationale : Projet de loi n° 2599 ; Rapport de M. Bioulac, au nom de la commission spéciale, n° 2871 ; Discussion les 19, 20, 23 novembre 1992 et adoption le 25 novembre 1992. - Sénat : Projet de loi, adopté par l'Assemblée nationale en première lecture, n° 66 (1992-1993) ; Rapport de M. Guy Cabanel, au nom de la commission des lois, n° 230 (1993-1994) ; Discussion les 13, 14, 17, 18, 19 et 20 janvier 1994 et adoption le 20 janvier 1994, n° 77. Deuxième lecture - Assemblée nationale : Projet de loi, modifié par le Sénat, n° 961 ; Rapport de M. Jérôme Bignon, au nom de la commission des lois, n° 1062 ; Discussion le 19 avril 1994 et adoption le 20 avril 1994. - Sénat : Projet de loi, adopté avec modification par l'Assemblée nationale en deuxième lecture, n° 356 (1993-1994) ; Rapport de M. Guy Cabanel, au nom de la commission des lois, n° 398 (1993-1994) ; Discussion et adoption le 19 mai 1994. Nouvelle lecture Assemblée nationale : Projet de loi, modifié par le Sénat, n° 1267 ; Rapport de M. Jérôme Bignon, au nom de la commission mixte paritaire, n° 1386 ; Discussion et adoption le 21 juin 1994. - Sénat : Rapport de M. Guy Cabanel, au nom de la commission mixte paritaire, n° 515 (1993-1994) ; Discussion et adoption le 23 juin 1994. Conseil constitutionnel : Décision n° 94-343/344 DC du 27 juillet 1994 publiée au Journal officiel du 29 juillet 1994. Loi n° 94-654 du 29 juillet 1994 relative au don et à l'utilisation des éléments et produits du corps humain, à l'assistance médicale à la procréation et au diagnostic prénatal dite de bioéthique Première lecture - Assemblée nationale : Projet de loi n° 2600 ; Rapport de M. Bioulac, au nom de la commission spéciale, n° 2871 ; Discussion les 19, 20, 24 et 25 novembre 1992 et adoption le 25 novembre 1992. - Sénat : Projet de loi, adopté par l'Assemblée nationale en première lecture, n° 67 (1992-1993) ; Rapport de M. Jean Chérioux, au nom de la commission des affaires sociales, n° 236 (1993-1994) ; Avis de la commission des affaires culturelles n° 234 (1993-1994) ; Discussion les 13, 14, 17, 18, 19 janvier 1994 et adoption le 19 janvier 1994. Deuxième lecture - Assemblée nationale : Projet de loi, modifié par le Sénat, n° 957 ; Rapport de M. Jean-François Mattei, au nom de la commission spéciale, n° 1057 ; Discussion les 14 et 15 avril 1994 et adoption le 20 avril 1994. - Sénat : Projet de loi, adopté avec modifications par l'Assemblée nationale en deuxième lecture, n° 354 (1993-1994) ; Rapport de M. Jean Chérioux, au nom de la commission des affaires sociales, n° 395 (1993-1994) ; Discussion les 17 et 18 mai 1994 et adoption le 18 mai 1994. Commission mixte paritaire - Assemblée nationale : Projet de loi, modifié par le Sénat en deuxième lecture, n° 1264 ; Rapport de M. Jean-François Mattei, au nom de la commission mixte paritaire, n° 1369 ; Discussion et adoption le 15 juin 1994. - Sénat : Rapport, au nom de la commission mixte paritaire, n° 497 (1993-1994) ; Discussion et adoption le 23 juin 1994. Conseil constitutionnel : Décision n° 94-343/344 DC du 27 juillet 1994 publiée au Journal officiel du 29 juillet 1994. |
|
LISTE DES PRINCIPAUX AVIS ET ÉTUDES RÉALISÉS EN VUE DE LA RÉVISION DES LOIS DE BIOÉTHIQUE 18 février 1999 : Office parlementaire d'évaluation des choix scientifiques et technologiques (OPECST) , rapport de M. Alain Claeys, député, et de M. Claude Huriet, sénateur, sur l'application de la loi n° 94-654 du 29 juillet 1994 relative au don et à l'utilisation des éléments et produits du corps humain, à l'assistance médicale, à la procréation et au diagnostic prénatal. Février 1999 : Institut de droit comparé , rapport de synthèse de Mme Myriam Blumberg-Mokri, Vers un droit européen de la bioéthique ? Les institutions productrices en matière de reproduction humaine. 13 octobre 1999 : OPECST , rapport de M. Franck Sérusclat, sénateur : Génomique et informatique : l'impact sur les thérapies et sur l'industrie pharmaceutique. 25 novembre 1999 : Conseil d'Etat, étude : Les lois de la bioéthique : cinq ans après. 24 février 2000 : OPECST, rapport de M. Alain Claeys, député, et de M. Claude Huriet, sénateur : Clonage, thérapie cellulaire et utilisation thérapeutique des cellules embryonnaires. 29 juin 2000 : Commission nationale consultative des droits de l'homme ( CNCDH) avis : révision des lois de 1994 sur la bioéthique . Novembre 2000 : Ministère de la recherche , rapport de M. François Gros sur les cellules souches adultes et leurs potentialités d'utilisation en recherche et en thérapeutique : comparaison avec les cellules souches embryonnaires. 18 janvier 2001 : Comité national consultatif d'éthique pour les sciences de la vie et de la santé (CNCE) , avis n° 67 : avant-projet de révision des lois de bioéthique. 25 janvier 2001 : CNCDH , avis : avant-projet de loi tendant à la révision des lois relatives à l'éthique biomédicale. Avril 2001 : Commission des Affaires sociales du Sénat , rapport de M. Claude Huriet : fonctionnement des comités consultatifs de protection des personnes dans la recherche biomédicale. 27 juin 2001 : Assemblée nationale , rapport d'information n° 3208 de M. Alain Claeys : mission d'information commune préparatoire au projet de loi de révision des « lois bioéthiques » de juillet 1994. 20 décembre 2001 : OPECST , rapport de M. Alain Claeys, député : la brevetabilité du vivant. Mars 2002 : Inspection générale des affaires sociales , rapport de Françoise Lalande, Valérie Delahaye-Guillocheau, Marc Ollivier, Elisabeth Dufourcq : la conservation d'éléments du corps humain en milieu hospitalier. 4 juillet 2002 : CNCE, avis n° 72 : l'extension du diagnostic préimplantatoire . Novembre 2002 : CNCE , avis n° 73 : questions éthiques soulevées par les essais de phase I chez les malades atteints de cancer. |
I. LE CONTEXTE
Rarement un projet de loi n'aura été précédé d'une telle réflexion préparatoire. Le législateur de 1994, qui avait invité son successeur à réviser les dispositions qu'il s'apprêtait à adopter, n'avait pas laissé ce dernier dépourvu. En effet, il s'était confié à lui-même, par le truchement d'une mission confiée à son Office parlementaire d'évaluation des choix scientifiques et technologiques, le soin de préparer le chemin.
Ce travail fut le point de départ d'une série de travaux de qualité.
Comme il en avait déjà été le cas pour la préparation des projets de loi adoptés en 1994, le précédent gouvernement a jugé utile de disposer de l'analyse complémentaire du Conseil d'Etat.
L'Assemblée nationale a, pour sa part, formé une mission spéciale d'évaluation et préparatoire à la révision des lois de bioéthique dont les conclusions ont été rendues publiques concomitamment au dépôt du projet de loi sur le bureau de cette Assemblée.
Enfin, votre rapporteur ne saurait ignorer l'influence croissante des travaux qui ont été menés au niveau international -notamment européens- et dont le législateur doit, dès à présent, sur de nombreux aspects du texte, tenir compte.
A. UNE ÉVALUATION DU DROIT EN VIGUEUR : LE RAPPORT D'ÉVALUATION DE LA LOI N° 94-654 PAR L'OFFICE PARLEMENTAIRE D'ÉVALUATION DES CHOIX SCIENTIFIQUES ET TECHNOLOGIQUES
L'article 21 de la loi n° 94-654 du 29 juillet 1994 relative au don et à l'utilisation des éléments et produits du corps humain, à l'assistance médicale, à la procréation et au diagnostic prénatal avait confié à l'Office parlementaire d'évaluation des choix scientifiques et technologiques le soin de procéder à l'évaluation de son application dans le délai de cinq ans prévu pour la révision des dispositions de cette loi.
Le champ de l'évaluation devait être circonscrit aux dispositions de ladite loi. Cela étant, ainsi que le justifient MM. Claude Huriet et Alain Claeys auteurs de ce rapport d'évaluation 1 ( * ) , « la démarche globale adoptée par le législateur lui-même en 1994 et les évidentes complémentarités unissant le texte dont nous étions saisis et la loi n° 94-653 relative au respect du corps humain conduisaient à s'écarter d'une appréciation trop " sectorielle " » .
En préambule à leur évaluation, les auteurs ont tenu à souligner deux perspectives importantes :
- la nécessité de replacer les normes juridiques dans l'évolution des connaissances et des techniques ;
- la nécessité de replacer la loi dans son environnement international.
C'est en s'appuyant sur un grand nombre d'auditions que l'Office parlementaire d'évaluation des choix scientifiques et technologiques a rendu public, le 18 février 1998, son rapport articulé autour d'une triple évaluation : la première est consacrée à des considérations générales notamment relatives au délai de mise en oeuvre de la loi, la deuxième est consacrée au don et à l'utilisation des éléments et produits du corps humain, et la troisième aux questions entourant l'assistance médicale à la procréation et au diagnostic prénatal.
1. Les difficultés de mise en oeuvre de la loi
Les auteurs du rapport dressent un bilan sévère de la mise en oeuvre de la loi, du fait de délais trop importants pour la parution des textes d'application.
Sur la partie relative aux greffes, la publication de certains décrets essentiels a été différée de trois années. A titre d'exemple, « l'installation du registre des refus n'a été effective qu'au début de l'été 1998 » 2 ( * ) .
Concernant les dispositions relatives à l'assistance médicale à la procréation (AMP), c'est davantage le retard dans la délivrance des autorisations et agréments qui est responsable des délais dans la mise en application des dispositions de la loi. Ainsi que le notent les auteurs, les conditions d'autorisation des études menées sur l'embryon ont été fixées par un décret du 27 mai 1997 et la pratique du diagnostic préimplantatoire (DPI) ne débutera qu'en 1999.
Quelles que soient les difficultés invoquées, dont certaines sont bien évidemment justifiées 3 ( * ) , le retard pris dans l'application effective des dispositions affaiblissait la portée de l'évaluation, ce que reconnaissent fort justement les auteurs qui remarquent « que ces effets dilatoires sont particulièrement préjudiciables lorsqu'ils s'appliquent à un texte dont la longévité a été volontairement réduite afin que son efficacité puisse être appréciée au terme de cinq années d'application et avant une remise sur le métier. Sur certains points, comme on le verra, tout véritable travail d'évaluation s'avère impossible, soit que la loi vienne tout juste d'être effectivement mise en oeuvre, soit qu'elle n'ait encore trouvé aucun commencement d'exécution » 4 ( * ) .
2. Sur le don et l'utilisation des produits du corps humain
Après avoir rappelé les objectifs que s'était assigné le législateur de 1994, les auteurs du rapport ont formulé plusieurs propositions.
En premier lieu adapter la loi à l'évolution des techniques notamment celle « qui n'avait pu être prise en compte au moment de son élaboration (greffes en domino, prélèvement de cellules souches hématopoïétiques) » 5 ( * ) .
En second lieu remédier aux omissions de la loi « qui créent des difficultés pratiques ou compromettent le respect du principe du consentement (régime des tissus et des résidus opératoires, organisation des prélèvements sur mineurs) » 6 ( * ) .
En troisième lieu élargir le cercle des donneurs. A cet égard, les auteurs du rapport rappellent que la limitation au cercle familial était justifiée par le principe de non-patrimonialité et les règles de compatibilité. Les travaux les plus récents, dont fait part le rapport, amènent ses auteurs à relativiser les justifications d'une restriction de ce cercle.
Reste la question du lien affectif. « Le critère affectif sur lequel repose le don entre époux ne doit-il pas conduire à admettre les concubins au rang des donneurs ? Le législateur les avait écartés faute de pouvoir définir combien de temps le donneur doit avoir vécu maritalement avec le receveur. Mais il n'avait pas par ailleurs imposé aux époux une durée minimale de vie conjugale pour justifier un don d'organes. On aboutit alors, comme le relève le CCNE, à des situations paradoxales où un conjoint de fraîche date peut être admis au don alors que le compagnon ou la compagne de plusieurs années doit être écarté. On doit enfin noter qu'en d'autres domaines de l'éthique biomédicale, spécialement en matière d'assistance médicale à la procréation, la loi met sur le même plan époux et concubins . La profession médicale semble majoritairement favorable à un assouplissement mesuré des règles en vigueur » 7 ( * ) .
Sur le consentement au don d'organe, les auteurs constatent que les dispositions législatives prévoient une information du donneur sur les risques encourus mais non sur les résultats escomptés de la greffe. Certes ils constatent 8 ( * ) que « cette lacune a été comblée par la voie réglementaire (article R. 671-3-1 résultant du décret n° 96-375 du 29 avril 1996) mais il serait sans doute souhaitable que cette exigence figure dans la loi elle-même. L'information pourrait au demeurant être plus complète et porter également, pour les greffes de moelle entre donneurs non apparentés, sur les résultats effectifs du don ».
Sur la base des constats qu'ils dressent de la situation des prélèvements sur les personnes décédées, les auteurs font part d'un certain nombre de solutions qui leur ont été suggérées.
En premier lieu un aménagement du « témoignage de la famille » dans la recherche de la volonté du défunt semble « souhaitable » , « car « l'inscription au registre ne constituant qu'un mode d'expression parmi d'autres , il demeure fréquemment nécessaire de solliciter le témoignage de la famille qui s'apparente en fait, dans bon nombre de cas, à un véritable pouvoir de décision » . Sont ainsi évoqués le caractère trop restrictif de la notion « de famille », l'opportunité d'une information préalable et complète de cette dernière sur la pratique des greffes ou la possibilité évoquée par une personnalité auditionnée « d'associer aux médecins des représentants des associations qui se consacrent à la défense des droits des patients » , voire d'introduire « dans le dispositif actuel, un médiateur chargé de représenter les donneurs » 9 ( * ) .
Le régime juridique de l'autopsie appelle pour sa part une plus grande transparence « en séparant clairement l'autopsie, dont les finalités sont très spécifiques, des prélèvements à fin thérapeutique » .
3. L'assistance médicale à la procréation et la recherche sur l'embryon
Les auteurs du rapport auscultent les difficultés soulevées par l'AMP et la question de l'embryon d'une manière très complète. La présentation faite ici par votre rapporteur ne prétend pas en rendre compte dans son intégralité mais simplement souligner quelques points importants.
Une première difficulté soulevée est relative à la stimulation ovarienne . Les risques associés à une telle pratique sont connus et rappelés par les auteurs : aggravation des risques d'affections iatrogènes, augmentation de la fréquence des grossesses multiples, risques accrus de naissance de grands prématurés. Le recours sans doute trop fréquent à cette technique s'explique en partie par un accès relativement facile à cette technique qui suscite une multiplication des prescriptions. Listant l'ensemble des avis remis par les autorités compétentes, les auteurs du rapport concluent 10 ( * ) « qu'on y procède par la voie législative ou réglementaire, la soumission de ces actes médicaux pratiqués hors fécondation in vitro (FIV) à un encadrement plus rigoureux s'impose de toute évidence, même si la mise en oeuvre d'un contrôle s'avère difficile compte tenu du nombre de praticiens impliqués (8.000 gynécologues exerçant actuellement en France) ».
Une seconde difficulté soulevée est relative à la fécondation in vitro par micro-injection d'un spermatozoïde (ICSI 11 ( * ) ), méthode d'assistance médicale à la procréation qui suscite un large débat. Des dérapages inquiétants sont décrits par les auteurs du rapport. « Dès 1994, le Comité consultatif national d'éthique, dans son avis n° 42 sur l'évolution des pratiques d'AMP, avait recommandé la plus grande vigilance à propos de l'ICSI dont il relevait les dangers potentiels. Des efforts devaient être faits pour trouver un modèle animal et respecter les règles applicables à la recherche médicale. Les couples devaient être informés du caractère expérimental de la méthode. Les protocoles expérimentaux devaient être de nature à permettre une évaluation rigoureuse de celle-ci. L'ICSI ne devait pas être associée à d'autres techniques susceptibles de faciliter la pénétration dans l'ovocyte d'éléments étrangers. Il est rien moins que sûr que ces recommandations aient guidé les pratiques suivies depuis quatre ans . » 12 ( * )
Une troisième question posée est celle de l'efficacité des dispositions juridiques adoptées en 1994 contre le clonage reproductif. Les auteurs rappellent la doctrine « officielle » établie depuis le rapport public du Conseil d'Etat de 1998 à savoir qu'il 13 ( * ) « ne fait guère de doute que l'article 16-4 du code civil contient déjà, dans sa rédaction actuelle, une interdiction de jure du clonage reproductif car celui-ci porte évidemment atteinte à l'intégrité de l'espèce humaine et constitue une transformation des gènes dans le but de modifier la descendance de la personne, toutes choses formellement prohibées » . Ne tranchant pas ce point, les auteurs formulent néanmoins un double constat fondamental :
- le législateur ne doit pas oublier « la portée limitée de la norme juridique interne face à un environnement international instable où les pressions économiques, sociales et culturelles ne se heurtent, pour l'heure, qu'à des barrières morales dépourvues de force contraignante » 14 ( * ) ;
- la distinction établie entre clonage reproductif, condamnable, et thérapeutique, admissible, « fait bon marché des problèmes éthiques que peut soulever ce dernier s'il conduit à une instrumentalisation de l'embryon, utilisé comme banque de cellules, hors de tout projet parental » 15 ( * ) ;
Concernant la recherche sur l'embryon, et fort du constat que le compromis élaboré en 1994 est aujourd'hui l'objet de nombreuses critiques, les auteurs du rapport tracent 16 ( * ) deux alternatives pour le législateur.
- « La première consiste à refuser toute transaction avec le principe du respect de la vie dès son origine. Dans cette optique, la recherche, à condition qu'elle se conforme à l'ensemble des règles protectrices de la personne, peut s'appliquer aux gamètes. Aucune étude invasive et sans bénéfice direct pour l'enfant à naître ne saurait, en revanche, être menée sur un ovocyte fécondé » ;
- « La seconde conduit à rechercher une traduction juridique de la " personnalité différée " qui permette de concilier, dans sa finalité, l'intérêt de la personne à naître et celui de la personne déjà née. La notion de bénéfice indirect admise par le Comité consultatif national d'éthique en 1986 ouvrait la voie en ce domaine et son avis de juin 1998 qui se réfère à l'utilité thérapeutique des cellules embryonnaires élargit encore la perspective » ;
Mais dans ce dernier cas, MM. Claude Huriet et Alain Claeys précisent qu'il convient d'établir une distinction entre deux catégories d'embryons, distinction que le législateur avait refusé d'effectuer : ceux qui sont destinés à être transférés dans le cadre d'un projet parental, et ne sauraient de la sorte être affectés, et ceux qui ne s'inscrivent plus dans un tel projet et sur lesquels il serait possible, jusqu'à un certain stade de développement, de conduire des « expérimentations visant, soit à améliorer les techniques d'AMP, soit à mettre en oeuvre les cultures de cellules souches promises à un grand avenir thérapeutique. Toute création d'embryon à des fins exclusives de recherche demeurant proscrite, ces expérimentations et prélèvements ne pourraient s'appliquer qu'aux embryons surnuméraires existants, après accord de leurs géniteurs » 17 ( * ) .
Les auteurs du rapport insistent enfin sur la nécessité de mieux encadrer les activités d'assistance médicale à la procréation, tant dans l'agrément des praticiens que dans l'autorisation des établissements et des laboratoires.
B. UNE RÉFLEXION PRÉPARATOIRE : L'ÉTUDE DU CONSEIL D'ÉTAT SUR LES LOIS BIOÉTHIQUES
A peine les résultats de cette évaluation connus, par une lettre en date du 22 avril 1999, M. Lionel Jospin, alors Premier ministre, a confié au Conseil d'Etat le soin de réaliser une étude dans le domaine de la bioéthique, prolongeant les travaux de l'OPECST.
La démarche du Premier ministre d'alors s'inscrivait dans un choix clair : élargir les questions de bioéthique et se placer, pour l'élaboration d'un projet de loi, sous l'autorité du Conseil d'Etat, comme cela fut le cas lors de la préparation des projets de loi adoptés en 1994.
Rappelant que le Conseil avait déjà abordé les questions de bioéthique dans son rapport public de 1998, il a laissé à ce dernier une grande latitude pour se pencher sur « tout autre sujet en lien avec la bioéthique » . Néanmoins il lui fut confié la tâche expresse d'examiner cinq questions :
- l'usage des tests génétiques et leurs applications ;
- le don d'organes et les greffes en général ;
- les divers problèmes liés au consentement des personnes, tant pour les dons d'organes que pour les dons de tissus et cellules ;
- les questions touchant à l'assistance médicale à la procréation, du double point de vue de l'évolution des techniques de l'accueil et de la conservation des embryons ;
- les problèmes posés par le clonage et sa pratique, en distinguant selon qu'il a ou non un objet reproductif .
Ces cinq thèmes, sur lesquels le Conseil d'Etat a construit son étude, constituent en conséquence la trame du projet de loi aujourd'hui examiné par le Parlement. Une grande partie des propositions formulées par le Conseil y figurent.
Sans détailler de manière exhaustive les différentes analyses du Conseil d'Etat, qui seront exposées, le cas échéant, lors de l'examen des articles auxquels elles se rapportent, votre rapporteur proposera ici un bref rappel des principaux enseignements et propositions de l'étude remise par le Conseil.
1. L'interdiction formelle du clonage reproductif
Rappelant l'émoi international causé par la révélation du clonage de la brebis Dolly en 1997, le Conseil d'Etat constate le caractère finalement nouveau de la question du clonage et la célérité avec laquelle les institutions internationales se sont saisies de cette question : adoption, le 12 mars 1997, d'une résolution le condamnant par le Parlement européen, adoption, le 12 janvier 1998, d'un protocole additionnel à la Convention d'Oviedo interdisant « toute intervention ayant pour but de créer un être humain génétiquement identique à un autre être humain vivant ou mort » par le Conseil de l'Europe, condamnation ferme de cette pratique par l'Organisation mondiale de la santé, le 14 mai 1997 ainsi que par l'UNESCO, dont l'article 11 de la Déclaration universelle sur le génome humain et les droits de l'Homme déclare solennellement que « des pratiques qui sont contraires à la dignité humaine, telles que le clonage à des fins de reproduction d'êtres humains, ne doivent pas être permises » .
Fort du constat que les dispositions du code civil ne permettent vraisemblablement pas de s'adonner à une telle pratique, - « il ne fait guère de doute que l'article 16-4 du code civil contient déjà, dans sa rédaction actuelle une interdiction de jure du clonage reproductif, car celui-ci porte évidemment atteinte à l'intégrité de l'espèce humaine et constitue une transformation des gènes dans le but de modifier la descendance de la personne, toutes choses formellement prohibées 18 ( * ) » , le Conseil s'interroge sur l'opportunité de prévoir une interdiction expresse dans la révision des lois bioéthiques.
Toutefois, observant 19 ( * ) que « les lois du 29 juillet 1994 ont fait le choix d'interdire explicitement les pratiques qu'elles estiment contraires au principe du respect de la personne humaine ; c'est le cas par exemple du recours à une mère porteuse. Dans le cadre d'une telle architecture, il semble donc plus cohérent de prévoir l'introduction, par exemple, dans l'article 16-4 du code civil, d'une interdiction de « toute intervention ayant pour but de faire naître un enfant ou de faire se développer un embryon humain dont le génome serait identique à celui d'un autre être humain vivant ou décédé » .
2. L'autorisation d'une recherche strictement encadrée sur l'embryon
Les difficultés posées par le statut de l'embryon sont antérieures à l'adoption des lois de 1994 ; il s'agit d'une question éthique, philosophique, culturelle et scientifique qui reste sous l'empire des convictions de chacun.
Ainsi que le rappelle le Conseil 20 ( * ) , « la loi du 17 janvier 1975 relative à l'interruption volontaire de grossesse a largement fixé la position française dans ce débat. Elle a d'abord affirmé le principe de l'assimilation du foetus à un être humain. Son article premier dispose ainsi que « la loi garantit le respect de tout être humain dès le commencement de la vie ». Toutefois, elle s'est placée dans une logique de mise en balance de ce droit avec la prise en compte de la situation de détresse de la mère et des dangers que celle-ci peut courir. La loi a aussi veillé à ce que la mère fasse son choix en étant éclairée sur les conséquences de cet acte et a posé une limite au recours à l'avortement non thérapeutique en fixant à dix semaines de grossesse le seuil au-delà duquel est demeurée l'interruption volontaire de grossesse » .
Mais, les évolutions scientifiques et de la médecine procréative posent cette difficulté sous un jour nouveau, celui de l'embryon in vitro . A défaut de définir un statut juridique, le législateur de 1994 a fixé son sort en prévoyant expressément qu'aucune recherche ne pourrait être menée sur celui-ci à son détriment.
Rappelant 21 ( * ) que « le pouvoir réglementaire a fait une stricte interprétation de ces dispositions (...) en prévoyant « qu'aucune étude ne peut être entreprise si elle a pour objet ou risque d'avoir pour effet de modifier le patrimoine génétique de l'embryon, ou est susceptible d'altérer ses capacités de développement » , le Conseil d'Etat appelle de ses voeux un réexamen de la question de l'interdiction des recherches sur l'embryon au regard des perspectives thérapeutiques nouvelles.
Et de rappeler 22 ( * ) que « pour beaucoup d'équipes et de scientifiques, il est nécessaire d'autoriser les recherches sur l'embryon en vue de mieux connaître le processus de développement embryonnaire et d'améliorer l'AMP au même titre que les recherches portant sur les cellules embryonnaires » .
A ces perspectives, le Conseil d'Etat ajoute le constat d'une évolution de la société qui, au travers de ses différentes instances, a, au cours des années précédentes, fait connaître son souhait de voir évoluer la position prise par le législateur de 1994. Le Conseil cite notamment les avis d'organismes aussi divers que le Comité consultatif national d'éthique pour les sciences de la vie et la santé, l'Académie de médecine, la Commission nationale de médecine et de biologie de la reproduction et du diagnostic prénatal (CNMBRDP), la Commission nationale consultative des droits de l'homme ou l'Union nationale des associations familiales.
Pour autant, fort du constat que « ni le maintien de l'interdiction des recherches sur l'embryon, ni le basculement dans un système très ouvert d'autorisation ne paraissent aujourd'hui souhaitables » 23 ( * ) , le Conseil d'Etat propose d'encadrer très strictement la possibilité de mener des recherches sur l'embryon autour de cinq principes essentiels :
- interdiction de création d'embryons à des fins de recherche : une telle pratique « marquerait, en effet, un changement radical par rapport aux fondements de la loi française qui l'interdit explicitement et serait contraire à l'article 18 de la Convention d'Oviedo » 24 ( * ) ;
- recherches menées uniquement sur des embryons qui ne font plus l'objet d'un projet parental et dont le couple a consenti qu'ils fassent l'objet de telles recherches ainsi que les embryons jugés d'emblée non viables ;
- impossibilité d'implantation des embryons sur lesquels la recherche a été réalisée ;
- caractère transitoire de cette ouverture, le Conseil d'Etat proposant que 25 ( * ) « ce régime pourrait avoir une durée limitée de cinq ans, afin de bien témoigner de son caractère expérimental. Au terme de cette période, soit ce régime deviendrait caduc, soit le législateur devrait le reconduire pour une période limitée, soit encore le pérenniser en fonction des résultats obtenus par ces recherches » ;
- le strict environnement scientifique de ces recherches par le recours à un régime d'autorisation préalable.
Le Conseil d'Etat rappelle enfin que, par ricochets, l'interdiction de création d'embryons à des fins de recherche rend impossibles certaines évaluations de techniques d'AMP car « les recherches qui portent sur la fécondation de l'ovocyte par le spermatozoïde et qui sont nécessaires à l'amélioration de l'AMP peuvent conduire à la constitution d'embryons. Actuellement, de telles recherches doivent être regardées comme interdites, en application de l'article L. 152-2 du code de la santé publique car la fécondation in vitro n'est autorisée que dans le cadre d'une AMP et la création d'embryons pour la recherche est également interdite. » 26 ( * )
3. L'élargissement du recours à l'assistance médicale à la procréation
A l'égard des conditions de recours et d'exercice de l'AMP, le Conseil d'Etat formule plusieurs propositions, soit pour renforcer les garanties sanitaires des dispositifs existants, soit pour inscrire dans la loi des pratiques ayant cours, soit pour inscrire certaines dispositions visant des publics particuliers. Il propose ainsi de prévoir dans la loi :
- le recueil des gamètes à des fins conservatoires avant un traitement médical stérilisant ;
- l'élargissement des cas de recours à l'AMP aux couples au sein desquels le risque de transmission d'une maladie particulièrement grave existe ;
- l'autorisation du transfert post mortem d'embryons sous deux conditions : accord préalable et exprès du père, et inscription d'un délai de réflexion minimal pour la mère.
Le Conseil d'Etat propose en outre de « renforcer l'organisation administrative et les conditions de fonctionnement du secteur de l'AMP » 27 ( * ) , en harmonisant la formation des acteurs de l'AMP, en durcissant les contrôles des établissements où l'AMP est pratiquée et en proposant un suivi pédiatrique facultatif des enfants issus d'une fécondation in vitro . Le Conseil d'Etat rappelle la proposition formulée par l'Office parlementaire de faire évoluer la CNMBRDP vers une agence conçue sur le modèle de la Human Fertilisation and Embryology Authority (HFEA), en adossant la Commission à l'Etablissement français des greffes.
Tirant les conclusions du corpus juridique international de plus en plus précis et contraignant, le Conseil formule en outre un nombre important de propositions relatives au don et à l'utilisation des produits du corps humain ou sur la brevetabilité du vivant. Votre rapporteur les rappellera, le cas échéant, dans le commentaire des articles du présent projet de loi.
C. UNE CONTRAINTE CROISSANTE : L'ENVIRONNEMENT INTERNATIONAL
1. Des structures nombreuses et actives
Dès le début des années 1970, l'Europe s'est préoccupée de mener une réflexion sur les risques des avancées scientifiques. C'est d'abord autour de l'Europe des droits de l'Homme, le Conseil de l'Europe, puis auprès des instances communautaires que s'est peu à peu institutionnalisée cette réflexion.
Au sein du Conseil de l'Europe, s'est d'abord mis en place un comité directeur de bioéthique (CDBI) en charge de l'appréciation éthique et de l'élaboration normative en matière de bioéthique. Cette instance a notamment joué un rôle déterminant dans la préparation de la Convention d'Oviedo de 1997.
De son côté, l'Assemblée parlementaire du Conseil de l'Europe adopte régulièrement des recommandations sur les sujets touchant à la bioéthique qui, rédigées à l'intention du comité des ministres, ont vocation à inciter les états membres à légiférer.
Au sein de la Communauté européenne, un pôle de compétence autour de la bioéthique s'est d'abord organisé autour de la 12 e Direction générale de la commission, la DG XII. Cette dernière anime plusieurs groupes de propositions et de réflexion sur tous les sujets relatifs à la bioéthique et, notamment, travaille sur les implications juridiques, sociales et éthiques du programme de recherche européen relatif au génome.
Depuis 1998, la commission a institutionnalisé un groupe de travail s'apparentant, à bien des égards, à un comité d'éthique communautaire : le groupe européen d'éthique des sciences et des nouvelles technologies -le GEE- qui examine non seulement les difficultés que soulève le développement de la médecine et de la biologie, mais également certaines questions liées à l'évolution des technologies de l'information et des implications éthiques que celles-ci comportent.
L'ensemble de ces institutions produit un grand nombre de travaux et résolutions dont la chronologie ci-jointe fournit un aperçu non exhaustif. Mais la multiplication des résolutions demeure encore souvent tempérée par le caractère peu normatif de ces dernières.
2. Des textes dont la contrainte s'affirme progressivement
Beaucoup des textes juridiques produits par les autorités précitées demeurent largement incitatifs, puisqu'ils émanent la plupart du temps d'autorités dépourvues de compétence juridique de plein exercice : recommandations du Conseil de l'Europe -qu'elles soient de nature ministérielle ou parlementaire- mais également les conclusions du groupe de conseillers de la Commission européenne ou les résolutions adoptées par les parlementaires européens.
Toutefois, ce foisonnement incitatif s'accompagne de plus en plus souvent de textes dont la portée normative est pleine ou potentielle.
Il s'agit en tout premier lieu de la Convention d'Oviedo, adoptée en 1997 dans le cadre du Conseil de l'Europe, relative à la protection des droits de l'homme et de la dignité de l'être humain à l'égard des applications de la biologie et de la médecine .
Cette Convention, que la France a signée le 4 mai 1997 s'accompagne de trois protocoles relatifs au clonage, à la recherche biomédicale et à la transplantation d'organes et de tissus d'origine humaine. Si la France ne l'a pas encore ratifiée, elle s'efforce néanmoins de tenir compte de ses dispositions. En s'inspirant de plusieurs des principes qui y figurent, le présent projet de loi traduit cette poussée du droit européen.
Il s'agit également des trois directives européennes intervenues dans le domaine de la bioéthique, la directive 2001/20/CE du 4 avril 2001 concernant le rapprochement des dispositions législatives, réglementaires et administratives des Etats membres relatives à l'application de bonnes pratiques cliniques dans la conduite d'essais cliniques de médicaments à usage humain , la directive 98/44/CE du 6 juillet 1998 relative à la protection juridique des inventions biotechnologiques , ou la directive 95/46/CE du 24 octobre 1995, relative à la protection des personnes physiques à l'égard du traitement des données à caractère personnel et à la libre circulation de ces données .
Ces textes doivent être incorporés en droit interne dans un délai fixé et, à défaut, deviennent directement applicables. Or, le débat soulevé par l'article 12 nouveau, introduit par l'Assemblée nationale dans le présent projet de loi, souligne la contrainte nouvelle dans laquelle s'exerce la compétence du législateur national. Est-il tenable d'affirmer expressément dans la loi la non-brevetabilité du vivant dans une rédaction qui contrevient en tous points l'article 5 de la directive de 1998 ? Votre rapporteur ne le pense pas.
Reste encore aujourd'hui posée la question de l'adoption d'un corpus juridique mondial, notamment au niveau de l'ONU.
L'UNESCO a, pour sa part, pris des initiatives lors de l'adoption d'une déclaration universelle sur le génome humain en 1997.
Les récentes annonces relatives au clonage reproductif témoignent de la pertinence et de la nécessité d'une telle action mais cette démarche mondiale sera d'autant plus difficile à mettre en oeuvre qu'elle devra prendre en compte des sensibilités parfois très divergentes pour aboutir.
|
M. CHRISTIAN MUCH ( Allemagne ), s'exprimant également au nom de la France , a présenté des amendements au projet de résolution franco-allemand qui figure dans le rapport du Groupe de travail chargé du projet de convention internationale contre le clonage à des fins de reproduction. Ces amendements ont été acceptés par les coauteurs de ce texte et d'autres pays partageant la même position. Il a exprimé son souhait de voir ce projet de résolution, tel qu'amendé, adopté par la Sixième Commission. Soulignant qu'il existe une autre initiative concurrente, sous l'égide de l'Espagne, des Etats-Unis et des Philippines, M. Much a déclaré que cette initiative tend à vouloir associer des questions consensuelles et des questions sur lesquelles il n'existe pas de consensus dans un même processus de négociation, ce qui signifie qu'on risque de manquer l'opportunité actuelle d'interdire le clonage à des fins de reproduction. L'avantage de cette approche est que dans de nombreux pays, y compris l'Allemagne, les préoccupations relatives au clonage vont au-delà du clonage à des fins de reproduction. La France et l'Allemagne ne remettent pas en question ces préoccupations ; toutefois elles se posent des questions sur la sagesse et l'efficacité d'une approche « tout ou rien » qui n'aboutit à rien dans l'immédiat. Cette approche aura tendance à rendre service au mauvais côté, à savoir aux chercheurs irresponsables, aux médecins frauduleux et à des sectes obscures. Les défenseurs de cette approche expliquent qu'en raison des abus possibles, on ne peut pas interdire une forme de clonage sans aborder la question des autres formes, et qu'il faut clarifier la terminologie. Face à cette position, M. Much s'est interrogé sur ce qu'en pensera la Sixième Commission, qui est après tout la Commission juridique, si elle devait consacrer un temps indéfini à l'élaboration d'instruments sur des questions comme les signatures électroniques, et ne ferait preuve d'aucun sens de l'urgence en ce qui concerne la question du clonage à des fins de reproduction, question qui a été reconnue par tous comme étant une violation flagrante de la dignité humaine. Dans une perspective nationale, la France et l'Allemagne pourraient se demander pourquoi elles devraient déployer tant d'efforts dans la mesure où nos deux pays sont déjà dotés d'une législation sur cette question, a déclaré M. Much, ajoutant que cette attitude pourrait être celle des autres pays qui disposent de lois nationales sur le clonage. Il a estimé que ce serait là une démarche dangereuse pour trois raisons : les chercheurs rencontrant des problèmes pour mener leurs expériences de clonage dans leurs propres pays pourraient trouver asile dans d'autres pays dont la législation serait plus souple ; il faut faire passer un message strict pour couper les financements, surtout privés, des expériences de clonage ; l'approche « tout ou rien » est d'autant plus dangereuse que dans certains pays, les recherches en clonage ont atteint des niveaux de sophistication considérables, et qu'il n'y existe pas de cadre juridique national sur le clonage. Il est inquiétant de savoir qu'en absence d'instruments juridiques nationaux et internationaux, ces pays pourront offrir des environnements permissifs, ce qui se ferait au détriment de la dignité de la race humaine. M. Much s'est déclaré convaincu que les Nations-Unies, par le biais de la Sixième Commission, pourront s'acquitter de leurs responsabilités vis-à-vis de l'humanité et prouver qu'elle est en mesure de prendre une action préventive face à un danger imminent. Source : ONU, communiqué de presse - AG/S/381 - 17 octobre 2002 |
|
14 avril 1994, Conseil de l'Europe , Assemblée parlementaire, Recommandation 1240 relative à la protection et à la brevetabilité des produits d'origine humaine 10 octobre 1994, Conseil de l'Europe , Comité des Ministres, Recommandation sur le dépistage comme instrument de médecine préventive 24 octobre 1995, Union Européenne, Directive 95/46/CE relative à la protection des personnes physiques à l'égard du traitement des données à caractère personnel et à la libre circulation de ces données. 13 février 1997, Conseil de l'Europe , Comité des Ministres, Recommandation relative à la protection des données médicales 4 avril 1997, Conseil de l'Europe, Convention d'Oviedo pour la protection des droits de l'homme et de la dignité de l'être humain à l'égard des applications de la biologie et de la médecine (sur les droits de l'homme et la biomédecine) 25 juillet 1997, Conseil de l'Europe , Recommandation du Comité des Ministres aux Etats membres sur la xénotransplantation 30 septembre 1997, UNESCO Déclaration universelle sur le génome humain 12 janvier 1998, Conseil de l'Europe, Protocole additionnel à la Convention d'Oviedo sur l'interdiction du clonage des êtres humains 6 juillet 1998, Union Européenne, Directive 98/44/CE relative à la protection juridique des inventions biotechnologiques. 29 janvier 1999, Conseil de l'Europe , Assemblée parlementaire Recommandation 1399 relative à la xénotransplantation 23 septembre 1999, Conseil de l'Europe , Assemblée parlementaire Recommandation 1418 relative à la protection des droits de l'homme et de la dignité des malades incurables et des mourants 23 septembre 1999, Conseil de l'Europe , Assemblée parlementaire Recommandation 1425 relative à la biotechnologie et propriété intellectuelle 18 février 2000, Union européenne, signature de la Charte des droits fondamentaux 29 juin 2000, Conseil de l'Europe , Assemblée parlementaire Recommandation 1468 relative aux biotechnologies 7 septembre 2000, Union Européenne, résolution du Parlement sur le clonage des êtres humains . 14 novembre 2000, Groupe européen d'éthique des sciences et des nouvelles technologies auprès de la commission européenne, avis n° 15 : Les aspects éthiques de la recherche sur les cellules souches humaines et leur utilisation " 16 janvier 2001 , Union Européenne, Parlement , début des travaux de la Commission temporaire sur la génétique humaine et les autres technologies nouvelles de la médecine moderne 7 mars 2001, Conseil de l'Europe , Comité des Ministres Recommandation sur la gestion des listes d'attente et des délais d'attente en matière de transplantation d'organe 4 avril 2001, Union Européenne Directive 2001/20/CE concernant le rapprochement des dispositions législatives, réglementaires et administratives des États membres relatives à l'application de bonnes pratiques cliniques dans la conduite d'essais cliniques de médicaments à usage humain . 25 avril 2001, Conseil de l'Europe , Assemblée parlementaire Recommandation 1512 relative à la protection du génome humain par le Conseil de l'Europe 24 janvier 2002, Conseil de l'Europe, Protocole additionnel à la Convention d'Oviedo relatif à la transplantation d'organes et de tissus d'origine humaine 7 mai 2002, Groupe européen d'éthique des sciences et des nouvelles technologies auprès de la commission européenne, Avis n° 16 : les aspects éthiques de la brevetabilité des inventions impliquant des cellules souches humaines; 18 septembre 2002, Conseil de l'Europe , Comité des Ministres Recommandation sur la protection des données à caractère personnel collectées et traitées à des fins d'assurance |
II. LE PROJET DE LOI
Le contenu du projet de loi déposé à l'Assemblée nationale est très largement charpenté autour des propositions formulées par le Conseil d'Etat dont l'un des aspects de la mission consistait précisément à proposer des rédactions susceptibles de constituer un pré-projet de loi.
Pour l'essentiel donc, le projet de loi initial consacre les propositions d'amélioration et d'ouverture formulées par cette institution, non sans tenir compte, par ailleurs, de l'évaluation réalisée par l'OPECST.
L'Assemblée nationale n'a pas bouleversé les grandes lignes de ce projet mais a néanmoins pris un certain nombre d'initiatives. Certaines des modifications qu'elle a introduites posent toutefois de sérieuses difficultés, tantôt de forme, tantôt de fond, tantôt pour ces deux raisons cumulées et contribuent à ce qu' in fine , elles apparaissent à certains égards aventureuses.
A. LE CONTENU DU PROJET DE LOI INITIAL : LA CONSÉCRATION DES RÉFLEXIONS PRÉLIMINAIRES
Le projet de loi, préalablement à son dépôt sur le bureau de l'Assemblée nationale, a fait l'objet d'un examen par le Conseil d'Etat et par deux organes particulièrement qualifiés en matière d'éthique : le Comité consultatif national d'éthique et la Commission nationale consultative des droits de l'Homme .
Ces institutions ont rendu des avis motivés sur le projet de loi qui leur était soumis, le 18 janvier 2001 pour le comité consultatif national d'éthique et le 25 janvier 2001, pour la Commission nationale consultative des droits de l'Homme.
Reprenant un grand nombre des propositions formulées par le Conseil d'Etat dans son étude de 1999 ainsi que des divers rapports de l'OPECST, le projet de loi déposé s'articule autour de cinq titres : quatre thématiques et un consacré aux mesures transitoires. Sont abordés successivement les droits des personnes et les caractéristiques génétiques , le don et l'utilisation des éléments et produits du corps humain , les produits de santé , et enfin, la procréation et l'embryologie .
1. Sécuriser le régime juridique des examens et identifications génétiques
Le principe de non-discrimination en raison des caractéristiques génétiques est réaffirmé par l'article premier du texte.
Ce principe figure dans la plupart des textes internationaux consacrés à ce sujet, la Convention d'Oviedo , la déclaration universelle sur le génome humain ainsi que la charte des droits fondamentaux de l'Union européenne .
Conscient des dérives pouvant potentiellement apparaître dans le domaine de l'emploi ou de l'assurance, du fait d'un accès plus aisé aux caractéristiques génétiques des personnes, le Gouvernement a prévu d'inscrire ce principe de non-discrimination au sein des codes civil, pénal et du code du travail.
Le projet de loi prévoit, par ailleurs, d'harmoniser les terminologies relatives à « l'examen des caractéristiques génétiques », cette dernière formule, qui figure déjà au sein du code de la santé publique, étant substituée à la notion d'étude génétique inscrite dans les codes civil et pénal.
Il est en outre précisé le régime de consentement des personnes à la réalisation d'une identification par empreinte génétique au cours d'une procédure civile d'établissement de filiation. Lorsque la personne est vivante, le consentement préalable et exprès à l'identification est requis alors qu'au contraire il est présumé dans le cas de l'identification post mortem . Il faut en effet que la personne ait fait connaître, de son vivant, son opposition à un tel examen pour que ce dernier ne puisse être réalisé après son décès.
2. Conforter et préciser les principes régissant les dons et utilisations des éléments du corps humain
Les principes généraux régissant les dons et utilisations d'éléments du corps humain ne sont pas fondamentalement modifiés par le projet de loi mais sont toutefois précisés sur quatre points :
- leur champ d'application est étendu aux activités d'exportation et d'importation, ce qui n'était jusque-là pas le cas ;
- la présomption du consentement est généralisée, qu'il s'agisse de la réutilisation, à des fins scientifiques ou diagnostiques, de produits ou tissus prélevés à des fins thérapeutiques, ou des autopsies médicales. Toutefois, dans les deux cas, le principe d'une faculté d'opposition est conservé selon des modalités différentes ;
- les règles de sécurité sanitaire sont renforcées. Les manipulations effectuées sur des éléments du corps humain, lorsqu'elles entrent dans une finalité thérapeutique, seront soumises à ces règles, et feront notamment l'objet d'un dépistage du risque de transmission des pathologies infectieuses. Les produits thérapeutiques annexes sont, pour leur part, soumis à la biovigilance exercée par l'Agence française de sécurité sanitaire des produits de santé (AFSSAPS) ;
- l'introduction du principe préconisé par le Conseil d'Etat de la « balance risque-gain » 28 ( * ) en matière d'utilisation des produits du corps humain à des fins thérapeutiques.
Plusieurs articles prévoient en outre, dans le détail, les dispositions relatives au prélèvement et à l'utilisation des organes, du sang, et des autres tissus issus du corps humain.
Concernant les dons d'organes, le projet de loi commence par élargir considérablement le cercle des donneurs vivants en prévoyant que, par dérogation, des personnes ayant des liens étroits et stables avec le receveur puissent procéder à un don.
Une telle extension justifie à elle seule que les règles entourant l'expression du consentement soient renforcées : comme dans le droit existant, le consentement est exprimé au Tribunal de grande instance, non sans que le donneur n'ait au préalable reçu une information relative aux risques et conséquences du prélèvement. Le projet prévoit, en outre, le recours à un comité d'experts qui délivre une autorisation dans le cas du don dérogatoire, c'est-à-dire entre personnes n'étant pas de la même famille. Sauf sur l'initiative du magistrat précité, l'autorisation de ce comité n'est toutefois pas nécessaire dans le don intra-familial.
Quelle que soit la finalité du don scientifique ou thérapeutique, le consentement présumé est généralisé dans le cadre du prélèvement post mortem . Si le sujet décédé n'a pas exprimé, par tout moyen, son opposition au prélèvement -et le médecin doit, le cas échéant, recueillir le témoignage des proches- ce prélèvement est donc la règle. Cette présomption ne s'applique toutefois pas pour les personnes sous tutelle. Cette réaffirmation de la présomption est la contrepartie d'une amélioration de l'information à destination du public.
Afin de renforcer le contexte de protection entourant l'utilisation du corps humain, il est prévu que tout prélèvement fasse préalablement l'objet d'une information de l'Etablissement français des greffes (EFG), et que toute recherche scientifique fasse l'objet d'un protocole préalablement transmis à ce dernier.
Le projet de loi assouplit les règles relatives au prélèvement de sang sur mineurs. Les deux conditions, aujourd'hui cumulatives, -compatibilité cellulaire et urgence thérapeutique- deviennent alternatives. Sont en outre autorisés les prélèvements à des fins de recherche sous la protection des dispositions relatives à la recherche biomédicale sur personnes mineures. En outre, le projet de loi complète et précise la liste des produits dérivés du sang ainsi que le régime des importations et exportations de ces produits.
Il est enfin rappelé que le prélèvement ou la collecte des cellules, tissus et produits du corps humain ne peuvent être effectués qu'à des fins scientifiques ou thérapeutiques. Le régime du consentement du premier cas (scientifique) n'est guère détaillé tandis que le second cas (thérapeutique) prévoit une règle de principe et plusieurs exceptions.
Cette règle est que le consentement est formulé par écrit, après information complète et détaillée sur la finalité et les conséquences du prélèvement.
Toutefois, lorsque le don d'organes est effectué par un mineur ou une personne protégée apte à consentir, le consentement doit être formulé devant un magistrat et, parfois, un comité d'experts.
La règle du consentement présumé prévaut également pour le prélèvement ou la collecte post mortem .
Enfin, les règles régissant l'utilisation de ces tissus sont revues et simplifiées. La distinction entre thérapie cellulaire et autre utilisation est supprimée. Les produits cellulaires thérapeutiques relèvent, à présent, soit de la pharmacie -et sont régis par les dispositions relatives aux médicaments humains-, soit de la catégorie des préparations de thérapie cellulaire. Les établissements autorisés à travailler sur ces produits sont étendus à des établissements à caractère lucratif, sous réserve de l'autorisation de l'AFSSAPS après avis de l'EFG.
3. Elargir l'accès de l'assistance médicale à la procréation
Sans être modifiés en profondeur, les principes généraux de l'assistance médicale à la procréation (AMP) sont précisés sur divers points. La stimulation ovarienne, lorsqu'elle est réalisée dans le cadre d'une AMP, est incluse dans cette dernière et bénéficie, de ce fait, des dispositions légales afférentes.
Le projet de loi propose, en outre, d'inscrire dans la loi un certain nombre de pratiques ayant fait l'objet de tolérance, voire de dispositions infra-législatives : il s'agit essentiellement de l'élargissement de l'indication d'AMP aux couples sous le risque d'une infection par une maladie grave -notamment le VIH- ainsi que le recueil et la conservation de gamètes à titre conservatoire pour des personnes, même mineures, bénéficiant d'un traitement médical potentiellement attentatoire à leur fertilité.
Enfin, le projet de loi rappelle que la dissolution du couple fait obstacle au transfert de l'embryon ainsi qu'à l'insémination. La porte du transfert post mortem d'embryon n'est donc pas ouverte.
La fécondation in vitro est mise en oeuvre dans le cadre d'un « projet parental », qui se substitue, en partie, à l'ancienne expression « demande parentale ». Le projet de loi prévoit deux séries de mesures restrictives à la manipulation des embryons conçus in vitro . D'une part, ses déplacements sont réglementés par un régime d'autorisation préalable assorti de dispositions pénales pour les contrevenants. D'autre part, il est prévu que, pour pouvoir procéder à une nouvelle tentative de fécondation in vitro, les couples doivent d'abord utiliser la totalité des embryons congelés disponibles.
Les conditions de recours à un tiers donneur sont, pour leur part, considérablement élargies puisque le couple peut lui-même, en renonçant simplement à l'AMP au sein du couple, obtenir le bénéfice du tiers donneur. Sont également inscrites, dans le texte du projet de loi, des mesures destinées à améliorer l'approvisionnement des banques de gamètes : le donneur devra seulement « avoir procréé » et non plus « être en couple », et il serait en outre possible de doubler le nombre de naissances par donneur, en passant de cinq à dix enfants chacun.
Le sort de l'embryon conçu in vitro repose sur le projet parental. Tant que celui-ci est maintenu, la conservation de l'embryon est assurée dans les conditions habituelles de l'AMP. Lorsque le projet parental prend fin, les embryons n'ayant plus d'objet peuvent se trouver, selon la volonté du couple, soit accueillis par un autre couple, soit faire l'objet de recherches scientifiques ou voir leur conservation arrêtée. Au bout de cinq années, dans tous les cas de figure, cette conservation n'est plus assurée.
4. Ouvrir la recherche sur l'embryon
Le projet interdit explicitement, tant dans le code civil que dans le code pénal, le clonage humain reproductif, mais ne proscrit pas explicitement le clonage humain thérapeutique. En effet, l'autorisation de cette pratique figurait dans l'avant-projet de loi mais, à l'invitation du Conseil d'Etat, le précédent gouvernement l'aurait retirée. Dans le présent texte ne figurent désormais ni autorisation ni interdiction du clonage thérapeutique.
Les recherches scientifiques sont autorisées sur les seuls embryons qui ne font plus l'objet d'un projet parental et pour lesquels les couples ont consenti à ce que de telles recherches soient menées. Ces dernières doivent faire l'objet d'un protocole autorisé par le ministre de la santé après avis d'une nouvelle Agence de la procréation, de l'embryologie et de la génétique humaine (APEGH).
En effet, le projet de loi prévoit le remplacement de la Commission nationale de médecine et de biologie de la reproduction et du diagnostic prénatal (CNMBRDP) par une Agence de la procréation de l'embryologie et de la génétique humaine (APEGH). Cette dernière devrait à la fois renforcer le contrôle sur les activités de recherche, que le projet de loi propose d'élargir, ainsi que rassembler diverses personnalités -médecins, chercheurs etc.- en vue d'effectuer une veille scientifique et de formuler des propositions aux pouvoirs publics dans les domaines de sa compétence. Cette Agence est dotée d'un Haut Conseil à la composition pluridisciplinaire qui peut saisir le Comité consultatif national d'éthique et établit un rapport annuel rendu public et transmis au Gouvernement et au Parlement.
Le projet de loi prévoit, en outre, que des recherches puissent être menées sur les tissus ou cellules issus d'une interruption de grossesse, embryon ou foetus sous la réserve d'un nihil obstat de la femme ayant subi cette interruption. Ces recherches, sauf lorsqu'elles sont menées afin de découvrir la cause de l'interruption de la grossesse, doivent toutefois faire l'objet d'un protocole transmis à l'APEGH.
B. LES MODIFICATIONS ADOPTÉES PAR L'ASSEMBLÉE NATIONALE : OUVERTURE OU AVENTURE ?
Le texte adopté par l'Assemblée nationale le 22 janvier 2001 respecte, dans ses grandes lignes, l'équilibre du projet déposé par le Gouvernement. L'Assemblée a néanmoins adopté un certain nombre de dispositions qui infléchissent certains aspects du texte.
1. La proclamation de quelques principes : paix des morts et reconnaissance de la Nation aux donneurs
Après avoir formellement supprimé l'article premier du texte pour le réinscrire dans le projet de loi relatif aux droits des malades promulgué le 4 mars 2002, l'Assemblée nationale a renversé les principes régissant le consentement des personnes décédées à leur identification par empreinte génétique dans le cadre d'une procédure civile. Alors que le projet de loi prévoyait le principe de consentement présumé, le texte adopté par l'Assemblée nationale prévoit que l'identification post mortem n'est possible qu'en cas d'accord exprès de la personne exprimé de son vivant.
Les principes relatifs au don et à l'utilisation des organes ne connaissent qu'une innovation majeure. Il est prévu que la Reconnaissance de la Nation soit accordée aux personnes réalisant ces dons.
Il faut noter en outre quelques autres dispositions qui ont, sur ce sujet, fait l'objet d'aménagements : une extension des finalités du prélèvement des tissus ou de cellules sur personne vivante, l'assimilation des greffes de tissus vascularisés aux greffes d'organes et donc au régime juridique qui les régit, ainsi qu'un renforcement de l'information des femmes réalisant un don d'ovocytes.
2. Le sort de l'embryon : création possible d'embryons à des fins de recherche et autorisation de leur transfert post mortem
Le statut de l'embryon se trouve profondément modifié car, par ricochets, l'Assemblée nationale a autorisé le principe de création d'embryons à des fins de recherche.
En effet, en prévoyant que toute nouvelle technique d'AMP devrait systématiquement faire l'objet d'une évaluation ex-ante , l'Assemblée nationale pose implicitement que, dans certains cas, des embryons seront créés dans le cadre d'un projet de recherche. Ces recherches devront néanmoins être au préalable autorisées par le ministre de la santé, après avis de l'APEGH.
L'Assemblée nationale a en outre ouvert la possibilité d'un transfert post mortem d'embryons, entre le sixième et le dix-huitième mois suivant le décès d'un des deux membres du couple, et a en conséquence prévu un régime juridique, civil et successoral, spécifique pour cette éventualité.
3. L'extension des pouvoirs de l'Agence de la procréation, de l'embryologie et de la génétique humaine
L'Assemblée a amendé la composition du Haut Conseil de l'APEGH, mais a surtout revu l'étendue de ses pouvoirs en prévoyant que celui-ci devra non seulement évaluer, mais également autoriser les protocoles de recherches sur l'embryon in vitro et les cellules en dérivant.
4. L'affirmation de la non-brevetabilité du vivant
Enfin, l'Assemblée nationale a introduit, au moyen d'un article additionnel, le principe de non-brevetabilité de l'humain dans une rédaction qui prend le contre-pied de l'article 5 de la Convention d'Oviedo.
Cette initiative, que votre rapporteur a déjà évoquée dans son avant-propos, sera présentée plus longuement lors de l'examen de l'article 12 bis nouveau .
III. LES PROPOSITIONS DE VOTRE COMMISSION
Par sagesse, mais également par pragmatisme, le nouveau Gouvernement a préféré saisir le Sénat du projet voté par l'Assemblée nationale l'an passé plutôt que de proposer un projet dont il revendiquerait la paternité.
Ainsi qu'il a été exprimé à de nombreuses reprises, les dispositions contenues par le présent projet transcendent les clivages partisans ou idéologiques.
En examinant les dispositions proposées, votre commission a cherché avant tout à réaffirmer la prééminence d'un regard éthique, mais également à permettre, lorsqu'elles lui semblaient justifiées, les évolutions que les nombreuses institutions saisies de cette question avaient préconisées.
Schématiquement, votre commission propose trois grands axes pour les grands thèmes proposés par ce projet.
Concernant le don d'organes, elle a en premier lieu souhaité ne solliciter qu'avec prudence les donneurs vivants ce qui, en conséquence, la conduit à la fois à favoriser les dons post mortem et à entourer le don entre vifs de garanties renforcées.
Concernant l'assistance médicale à la procréation et le statut de l'embryon, elle a cherché à décliner le principe de précaution : précaution sanitaire afin que ces techniques soient mises en oeuvre dans un contexte optimal de sécurité mais également précaution éthique en ne permettant pas, au-delà du strict nécessaire, tel qu'il peut être évalué aujourd'hui, les manipulations sur l'embryon.
Concernant les activités s'exerçant dans le champ de la bioéthique, elle a souhaité que la tutelle des pouvoirs publics puisse s'exercer dans les meilleures conditions possibles.
A. DON ET PRÉLÈVEMENT D'ORGANES : FAVORISER LE PRÉLÈVEMENT POST MORTEM POUR PRÉSERVER LES VIVANTS
1. Favoriser le don post mortem en améliorant l'information du jeune public sur le don d'organes
Au grave problème posé par le déficit en greffons, le projet de loi choisit de répondre par l'élargissement du champ des donneurs vivants aux personnes ayant « un lien étroit et stable » avec le receveur. Cette situation s'inspire d'une certaine générosité mais également d'une certaine facilité : parce que le prélèvement post mortem est encore accueilli avec méfiance par nos concitoyens, et notamment les familles dans la douleur d'un deuil, les pouvoirs publics choisissent d'encourager les prélèvements sur des personnes vivantes volontaires.
Or, ces prélèvements ne sont pas anodins. Ils comportent des risques sérieux : risque de mort, risque de complications post-opératoires. Si les statistiques ne sont pas nombreuses sur le sujet, on évalue néanmoins, pour le don d'une partie de foie, la mortalité à 0,2 % et la morbidité à 12 %, et pour le don d'un rein, la mortalité à 1 cas sur 600.
En conséquence, votre commission estime qu'il convient de favoriser le développement du don post mortem , notamment par une politique d'information plus active sur la finalité du don d'organes après le décès et sur le régime du consentement auquel il est soumis. L'objectif est de rendre pleinement effectif le régime actuel de consentement présumé.
Votre commission propose en conséquence de prévoir que tout médecin devra s'assurer auprès de ses patients âgés de 16 à 25 ans qu'ils ont bien reçu une telle information et, dans le cas contraire, de la délivrer le plus rapidement possible. La définition des modalités de cette information et du support durable la retraçant est renvoyée à un décret en Conseil d'Etat.
2. Encadrer très strictement le recours au don entre vifs
a) Limiter le cercle des donneurs potentiels
Le projet de loi élargit le cercle potentiel des donneurs vivants à toute personne ayant avec le receveur un lien « étroit et stable ».
Cet élargissement est contestable à plusieurs chefs.
En effet, le concept de lien « étroit et stable » demeure particulièrement vague, cette notion pourrait viser les personnes vivant avec le bénéficiaire, mais également d'autres catégories de proches, voisins et amis connus de longue date.
Il s'agit in fine d'un recours au seul lien affectif sur lequel le Conseil d'Etat a exprimé des réserves dans son étude de 1999 29 ( * ) , considérant qu'il était « possible d'étendre le cercle des donneurs au-delà de la parenté du premier degré (un cousin peut être le seul donneur compatible), de poursuivre cette extension en dépassant la notion de parenté mais en limitant cet élargissement aux seuls conjoints après avoir levé la condition d'urgence qui s'impose aujourd'hui à eux, de procéder à un élargissement mesuré en englobant dans la notion de conjoint les concubins ou, d'ouvrir au maximum le cercle potentiel des donneurs majeurs non apparentés en retenant la catégorie de « personnes affectivement liées » qui permet d'inclure les concubins et les amis et d'élargir le cercle des donneurs apparentés au-delà de la parenté de premier degré.
« Dans ce dernier cas, il faudrait sans conteste soumettre cet élargissement à des contrôles et prévoir des garde-fous afin d'éviter qu'un commerce d'organes ne se crée. Pour s'assurer de la sincérité du don et protéger les donneurs contre toutes formes de pressions, certaines instances envisagent la mise en place d'un comité ad hoc qui devrait examiner tous les cas de dons émanant de personnes majeures apparentées ou non.
« Si une définition élargie de la famille ne pose pas de problèmes juridiques majeurs, tel n'est pas le cas d'une extension maximale de la catégorie des donneurs sur le fondement du seul lien affectif. Le risque induit par un tel choix est de consacrer un critère dont l'interprétation est totalement ouverte, et donc nécessairement subjective et arbitraire, et dont le contrôle est, par voie de conséquence, fort peu aisé. Accepter le don au titre des seuls liens affectifs augmente le risque de tractations commerciales. »
Généreux dans son inspiration, un tel élargissement porte donc potentiellement deux graves dangers :
- le risque d'une dérive mercantile que comporte la possibilité ainsi largement ouverte de prélever des organes ;
- le risque de pressions morales fortes sur des tiers qui, sans être des proches du receveur, constitueraient néanmoins son entourage habituel et deviendraient par conséquent des donneurs potentiels.
C'est la raison pour laquelle votre commission, avec prudence et pragmatisme, vous proposera de limiter l'élargissement du cercle des donneurs potentiels au cercle familial élargi : petits-enfants, neveux, nièces, cousins germains, enfants du conjoint du receveur et à la personne apportant la preuve de deux ans de vie commune.
b) Simplifier et encadrer le don de moelle osseuse par les mineurs et les majeurs protégés
Votre commission vous propose d'harmoniser ce régime dérogatoire qui intervient à titre exceptionnel et en l'absence d'autres solutions thérapeutiques tout en élargissant le cercle des bénéficiaires de prélèvements de moelle osseuse aux oncles et tantes, neveux et nièces des mineurs (en sus donc des frères et soeurs et cousins germains) et aux cousins germains, oncles et tantes, neveux et nièces (en sus donc des frères et soeurs) des majeurs sous curatelle ou sauvegarde de justice dès lors qu'ils se seront vu reconnaître la faculté de consentir par le juge des tutelles.
En l'état actuel du droit, la loi prévoit une dérogation à l'interdiction de prélever des cellules de la moelle osseuse sur un mineur pour les seuls prélèvements effectués au bénéfice de ses frères et soeurs. Le projet de loi élargit quant à lui la dérogation à la possibilité de prélèvement sur un mineur qui est le cousin ou la cousine germaine du receveur.
Les règles de la comptabilité tissulaire, impératives pour la réussite des greffes de moelle osseuse, font que parfois cette comptabilité ne peut être trouvée ni chez un donneur majeur, ni même auprès d'un mineur, frère ou soeur, cousin ou cousine du receveur. En revanche, dans certains cas rares, les hasards de la consanguinité font que d'autres parents proches comme les neveux ou nièces, oncles ou tantes se révèlent HLA 30 ( * ) identiques au receveur.
Plusieurs raisons conduisent ainsi votre commission à proposer d'élargir le champ des donneurs mineurs de moelle osseuse à cette dernière catégorie :
- la rareté des cas concernés fait que cette extension ne peut en aucun cas conduire à une banalisation des prélèvements sur personne mineure ;
- les personnes en attente d'une greffe de moelle osseuse souffrent de pathologies graves et la greffe représente la seule solution thérapeutique ; l'enjeu vital pour ces personnes doit être mis en regard avec le caractère relativement bénin et sans complexité technique particulière du prélèvement opéré sur le donneur ;
- en ce qui concerne les donneurs, le projet de loi offre d'ores et déjà un niveau de protection important se traduisant par l'information des parents du mineur avant le consentement et par une autorisation délivrée par un comité d'experts dont la composition a été renforcée.
En contrepartie, elle vous propose d'exiger pour tout prélèvement de moelle sur personne mineure ou majeure protégée, que le comité d'experts n'autorise le prélèvement ou formule son avis au juge des tutelles qu'après s'être assuré que tous les moyens ont été mis en oeuvre pour trouver un donneur majeur histocompatible.
B. ASSISTANCE MÉDICALE À LA PROCRÉATION ET STATUT DE L'EMBRYON : DÉCLINER LE PRINCIPE DE PRÉCAUTION
1. Garantir l'environnement éthique et sanitaire du recours à l'assistance médicale à la procréation
a) Limiter par l'édiction de règles de bonne pratique les risques suscités par la stimulation ovarienne.
La stimulation ovarienne permet, en agissant sur l'ovaire, d'obtenir la maturation de plusieurs ovocytes au cours d'un seul cycle d'ovulation. Cette pratique, dans la fécondation in vitro (FIV) , permet de réduire le nombre de prélèvements ovocytaires en créant plusieurs embryons qui, conservés par congélation, permettront le cas échéant plusieurs transferts.
Cette pratique a d'ailleurs dépassé la seule stimulation ovarienne dans le cadre d'une FIV, les femmes recourant, hors de cette technique d'AMP, à une consommation d'inducteurs d'ovulation, dont l'aboutissement a été une forte augmentation de la fréquence des grossesses multiples.
Des inquiétudes se font donc jour depuis quelques années devant la croissance rapide de l'utilisation de ces inducteurs et les risques qui en découlent pour les femmes.
La mission d'information conduite par l'Assemblée nationale 31 ( * ) avait à ce titre rappelé que « ce traitement hormonal n'est pas sans danger. Il comporte en effet des risques immédiats, à moyen et à long terme dont les plus importants sont le syndrome d'hyperstimulation ovarienne et les grossesses multiples. Le premier correspond au développement d'un nombre trop grand de follicules ; sous sa forme bénigne, il donne des douleurs abdominales, des ballonnements et dans 2 % des cas des troubles de la vision. S'y ajoutent, sous sa forme modérée, des nausées, des vomissements et diarrhées avec prise de poids de moins de 6 kg. Enfin, sous sa forme sévère, le syndrome se manifeste par de fortes douleurs abdominopelviennes, l'augmentation de volume des ovaires avec apparition de kystes susceptibles de se rompre ou de se tordre, l'apparition de troubles biologiques « dont les conséquences peuvent être redoutables» et une prise de poids qui atteint ou dépasse les 10 kg. Lorsqu'il y a grossesse, ces symptômes sont aggravés et peuvent nécessiter l'hospitalisation ».
Chacun s'accorde donc à reconnaître que les diverses pratiques de stimulation ovarienne méritent aujourd'hui d'être mieux encadrées.
L'Assemblée nationale a souhaité que cet encadrement soit à la fois légal et réglementaire, ce qui soulève des difficultés de mise en oeuvre compte tenu des formes très diverses de prescription d'inducteurs de stimulation.
Le rapporteur, lui même, M. Alain Claeys, se montrait réservé sur l'opportunité de cette démarche puisqu'il écrit dans son rapport 32 ( * ) qu'il est possible de « s'interroger sur la nécessité de prévoir expressément l'édiction de règles encadrant les traitements de stimulation ovarienne dans la mesure où le champ de compétences de l'ANAES, décrit précédemment, les inclut d'ores et déjà. Il aurait en effet suffi que le ministre de la santé demande à l'Agence d'établir ces règles avant de les édicter par voie d'arrêté. Toutefois, l'inscription dans la loi permet de donner un caractère obligatoire, et prioritaire, à l'édiction de ces règles. Il conviendrait cependant parallèlement, pour leur donner plus d'efficacité, de les inclure prioritairement dans les thèmes de formation médicale professionnelle continue et de s'assurer qu'elles seront incluses dans la formation initiale de tous les futurs médecins. A défaut , votre rapporteur craint que ces règles aient peu d'effet sur la pratique médicale dans la mesure où leur non-respect n'est pas sanctionné, sauf dans le cas d'une faute grave ou d'un contrôle médical. Une autre solution aurait consisté à considérer la stimulation ovarienne comme une technique d'AMP afin que ces traitements soient exclusivement prescrits dans les centres d'AMP autorisés. Toutefois, une telle limitation de l'exercice médical, aurait l'inconvénient de restreindre la compétence des médecins généralistes, des gynécologues et des médecins spécialisés dans le traitement de la stérilité. Il semble préférable, dans un premier temps tout au moins, d'en appeler à la responsabilité de chaque médecin en mettant à sa disposition les règles de bonne pratique qui doivent l'aider à mieux prescrire et à mieux suivre ces traitements ».
Cet avis fut également celui de M. Bernard Kouchner, alors ministre délégué à la santé qui, lors du débat en séance 33 ( * ) , s'est déclaré assez « perplexe » : « j'aurais tendance à penser qu'un tel encadrement est bien difficile à mettre en oeuvre . Je comprends le souci de Mmes Roudy et Boisseau d'encadrer, d'informer les couples des risques encourus. Mais s'il s'agit d'encadrer les bonnes pratiques, il y a le code de déontologie et toutes les réglementations de bonnes pratiques cliniques qui pèsent sur les médecins».
Il paraît préférable en effet -et plus efficace- de renvoyer l'encadrement des pratiques de stimulation ovarienne à des recommandations de bonnes pratiques homologuées par le ministre chargé de la santé. C'est la proposition qu'a retenue votre commission.
b) Le rétablissement d'une durée de vie commune préalable pour recourir à l'assistance médicale à la procréation
Le texte du projet de loi prévoyait la nécessité de faire la preuve d'un délai de deux années de vie commune pour que les couples non mariés puissent recourir à l'AMP.
Contre l'avis du Gouvernement 34 ( * ) , l'Assemblée nationale a supprimé cette disposition protectrice pour l'enfant à naître.
Or, cette exigence n'apparaît pas excessive si l'on souhaite que seuls des couples stables se lancent dans l'aventure souvent difficile de la procréation assistée et que les embryons conçus artificiellement et congelés le soient dans le cadre d'un projet parental solide. En conséquence, votre commission vous proposera de rétablir cette disposition.
c) L'interdiction du transfert post mortem d'embryons
L'Assemblée nationale a ouvert la possibilité d'un transfert d'embryon post mortem . Cette position, qui contredit les dispositions prises par le législateur de 1994, est le fruit d'un débat sur lequel un consensus ne peut, en l'état, être trouvé.
Plusieurs grandes institutions, compétentes tant sur le plan du droit que de l'éthique, se sont, sur cet aspect tout à fait particulier de l'AMP, prononcées 35 ( * ) dans des sens différents, sans pour autant prétendre à une autorité déterminante sur ce sujet.
Il faut avant tout garder en mémoire que le transfert d'embryon post mortem , qui soulève des débats juridiques et éthiques complexes, ne concerne qu'un nombre extraordinairement faible de cas par an, les dispositions adoptées par l'Assemblée nationale relevant véritablement de la « loi individuelle ».
La douleur des veuves, il s'agit uniquement de ce cas, est bien légitime. Toutefois, les interrogations éthiques et psychologiques que peut susciter la mise au monde consciente d'un orphelin ne sont pas mineures.
En 1994, le législateur, soucieux de donner à l'enfant à naître un cadre familial traditionnel, a voulu l'interdire ; c'est pourquoi, aujourd'hui, la loi précise que les deux membres du couple qui engagent une AMP doivent être vivants, ce qui prohibe aussi bien le transfert d'embryons que l'insémination post mortem .
Et c'est cette position que votre commission, en toute connaissance de cause, souhaite voir confirmée.
En effet, la légalisation du transfert d'embryons post mortem , introduite par l'Assemblée nationale, ne laisserait vraisemblablement pas intacte la conception commune du couple et du projet parental ni celle du rapport entre la volonté des géniteurs et l'intérêt de l'enfant. La souffrance de la mère justifie-t-elle que l'on donne naissance à un enfant orphelin ? L'intérêt de l'enfant autorise-t-il un tel transfert ? Il ne serait pas acceptable de considérer ce dernier, ainsi que le font certains, comme une aide à laquelle la veuve pourrait faire appel pour « faire son deuil », car l'enfant ne peut être ainsi « instrumentalisé ». Comment, en outre, cet enfant construira-t-il son identité ?
Cette législation conduit enfin à une grande inégalité entre les couples bénéficiant d'une AMP et les autres. Beaucoup de couples sont séparés par la mort, précocement et prématurément, laissant un projet d'enfant qu'ils portaient peut-être depuis longtemps. Il n'est pas possible de contourner, en leur faveur, cette réalité que constitue le décès de l'homme, qui lui, dans le cas inverse du décès de sa conjointe, ne pourrait, sauf autorisation de recours à une mère porteuse, bénéficier d'une telle faculté.
Au delà de ces obstacles, qui sont à eux seuls déterminants, les difficultés juridiques que soulève une telle autorisation sont également importantes. En effet, la naissance d'un enfant issu d'un tel transfert bouscule profondément le droit des successions et génère des problèmes innombrables, dont témoigne d'ailleurs le dispositif imparfait de l'article 18 bis. Cet article a en effet été introduit précisément par l'Assemblée nationale pour tirer les conséquences dans le code civil de la possibilité ainsi offerte de faire naître un enfant plus d'un an après le décès de son géniteur. Il semble en réalité qu'aucune solution juridique ne soit pleinement satisfaisante et ne parvienne à rétablir l'égalité entre les différents enfants héritiers.
Pour l'ensemble de ces raisons, votre commission vous proposera de supprimer la possibilité d'un transfert d'embryons post mortem .
2. Réaffirmer le respect dû à l'embryon sans entraver la recherche
a) Poser le principe d'interdiction de recherche sur l'embryon tout en permettant une dérogation transitoire et strictement encadrée
Votre commission demeure très attachée au principe du respect de l'être humain dès le commencement de sa vie, défini à l'article 16-4 du code civil, et à la protection de l'embryon. Elle souhaite par conséquent réaffirmer le principe de l'interdit de toute atteinte à l'embryon.
Toutefois , afin d'évaluer l'intérêt que présentent les recherches sur les cellules embryonnaires pour développer la médecine de l'embryon ainsi que de nouvelles thérapies cellulaires susceptibles d'entraîner des progrès décisifs dans le traitement de maladies pour lesquelles l'arsenal thérapeutique actuel est impuissant, il est proposé une dérogation autorisant la recherche dans un cadre strictement délimité et pour une période transitoire.
La possibilité qui serait ouverte de mener des recherches sur l'embryon et les cellules embryonnaires aurait en effet un caractère dérogatoire et transitoire et ses conditions de mise en oeuvre seraient très précisément circonscrites. Ces recherches ne pourraient être effectuées que sur des embryons surnuméraires et après l'accord des membres du couple.
Le but de ces recherches sera uniquement d'évaluer les potentialités respectives des différents types de cellules souches humaines susceptibles d'entrer dans des stratégies thérapeutiques.
La possibilité de la recherche sur l'embryon et les cellules souches embryonnaires aura un caractère transitoire afin que son bien-fondé soit réexaminé au bout de cinq ans, notamment parce qu'il n'est pas exclu que les progrès de la science conduisent à vider le débat de son contenu ou du moins à en atténuer la vivacité. Au terme de ces cinq ans, les recherches autorisées qui n'auront pu être achevées pourront être poursuivies sous réserve de l'autorisation de l'APEGH qui évaluera le bien-fondé de la demande.
b) Affirmer une interdiction générale de toute création d'embryon à des fins de recherche scientifiques
L'Assemblée nationale a introduit la possibilité d'une évaluation préalable de toute nouvelle technique d'assistance médicale à la procréation avant sa mise en oeuvre.
Cette initiative part d'une bonne intention, à savoir éviter que ne se reproduise ce qui s'est passé dans le cas de l'injection intracytoplasmique de sperme (ICSI).
Le Conseil d'Etat, dans son étude précitée, rappelle les difficultés posées par cette technique d'assistance médicale à la procréation et en conclut à la nécessité de prévoir une évaluation préalable de toute technique d'AMP avant sa mise en oeuvre.
|
« Malgré ses succès, l'ICSI est en effet considérée comme une technique dont l'absence de danger est loin d'être garantie . Elle est très différente de la FIV classique qui calque largement le processus procréatif naturel. D'une part, elle passe outre la sélection naturelle du spermatozoïde. De l'autre, sa réalisation est plus délicate, puisque l'injection d'un seul spermatozoïde directement dans le cytoplasme de l'ovule se fait par pénétration de sa membrane. C'est donc au moyen de gestes de plus en plus invasifs que l'on parvient à une efficacité bien plus importante en termes de fécondations, de grossesses ainsi que de difficultés des cas de stérilité pris en charge. L'ICSI a même été réalisée avec des spermatides prélevés directement dans les testicules d'hommes azoospermiques dont la stérilité est due à l'absence de transformation de ces spermatides en spermatozoïdes. Or les risques liés à ces pratiques ne font l'objet que d'une évaluation a posteriori et peu approfondie . (...) « Au-delà des progrès qui pourront être faits en termes de qualité et de jugement des contrôles, la loi pourrait prévoir pour l'avenir que toute nouvelle technique d'AMP devra faire l'objet d'une autorisation préalable à son éventuelle application clinique. » Etude du Conseil d'Etat précitée, p. 48 |
Or, le principe d'évaluation a priori de toute nouvelle technique d'AMP se heurte à une difficulté de mise en oeuvre pratique. M. Alain Claeys, rapporteur de la mission d'information précitée constate 36 ( * ) d'ailleurs la nécessité de « reconnaître cependant qu'aucun système d'évaluation ne pourra être totalement efficace . On ne saurait préconiser, en effet, de tester une technique en autorisant l'implantation d'embryons in vivo et encore moins de détruire l'embryon implanté issu de la technique évaluée si le danger de cette dernière devait être prouvé. Les évaluations ne pourront donc porter que sur les embryons in vitro. Dans ces conditions, on ne peut qu'accepter le caractère partiel de l'évaluation puisqu'il faudrait implanter l'embryon, le laisser se développer voire attendre la naissance de l'enfant sans être certain de l'innocuité totale de la technique évaluée. Il faut donc concilier différents principes. Votre rapporteur considère en l'espèce que la nécessité d'évaluer toutes les nouvelles techniques d'AMP, poussée à l'extrême, pourrait apparaître éthiquement inacceptable » .
Cette préoccupation débouche nécessairement sur l'autorisation de concevoir des embryons par ou pour cette évaluation, ce qui constituerait une exception forte au principe selon lequel la conception in vitro d'embryons humains à des fins de recherche est interdite, prinicpe que votre commission, de concert avec le Gouvernement, souhaite réaffirmer.
La réponse apportée par l'Assemblée nationale à la difficulté d'évaluation des techniques d'AMP porte en elle un risque de dérive inacceptable.
c) L'interdiction du clonage thérapeutique
Le présent projet de loi interdit formellement toute tentative de faire un être humain par le procédé de clonage.
Néanmoins, ce texte ne dit mot du clonage qualifié de thérapeutique. Une telle pratique est-elle possible ? L'article 8 du présent projet de loi précise que les gamètes humains sont réservés à des fins d'AMP, or la pratique du clonage thérapeutique nécessite de recourir à un ovocyte. On pourrait estimer que, par incidence, le clonage thérapeutique est impossible pour ce motif. A l'inverse, l'interdiction formelle du clonage reproductif pourrait laisser entendre qu' a contrario le clonage thérapeutique serait licite.
Votre commission estime en conséquence qu'il est préférable de faire figurer explicitement l'interdiction du clonage thérapeutique qui, en l'état représente, ainsi qu'il est détaillé à l'article 19, un triple danger : éthique, technique et médical.
C. LA TUTELLE DES POUVOIRS PUBLICS SUR LE CHAMP BIOÉTHIQUE : RECHERCHER L'EFFICACITÉ
1. L'APEGH : clarifier la composition et la mission de ses organes
a) Remplacer le Haut Conseil par un Conseil d'orientation médical et scientifique
Le dispositif prévu par le projet de loi concernant le Haut Conseil de l'APEGH est une source potentielle de confusion avec les compétences du Comité consultatif national d'éthique et de dysfonctionnements au sein même de l'Agence du fait de l'absence de définition claire des attributions de cet organe.
Votre commission propose en conséquence de substituer au Haut conseil un Conseil d'orientation médical et scientifique dont les attributions sont précisées et la composition revue en conséquence.
Il reviendrait tout d'abord au conseil médical et scientifique de contribuer par ses avis, recommandations et rapports à assurer la qualité de l'expertise médicale et scientifique de l'Agence. La prise en considération de la dimension éthique des questions traitées fait partie intégrante de cette exigence de qualité, et elle est d'ailleurs expressément prévue par le projet de loi pour ce qui concerne les autorisations temporaires de recherche sur les embryons et les cellules embryonnaires.
En conséquence, le Conseil d'orientation médical et scientifique dont la composition ferait une plus grande place aux institutions scientifiques ainsi qu'aux experts médicaux et scientifiques.
Toutefois, ce Conseil comporterait également des membres des hautes juridictions, le Conseil d'Etat et la Cour de Cassation, qui seront en mesure d'éclairer notamment sur le plan juridique les problématiques éthiques soulevées à l'occasion des expertises médicales ou scientifiques.
Le Comité consultatif national d'éthique (CCNE) y serait également représenté ainsi que la Commission nationale consultative des droits de l'Homme (CNDH).
En outre, parce que la présence du législateur est indispensable au sein de ce Conseil, il est prévu que chaque assemblée désigne l'un de ses membres pour y siéger.
Il convient enfin de préciser que des représentants d'associations d'usagers et de malades concernés par les activités de l'Agence pourraient par ailleurs être nommés membres du conseil d'orientation au titre des personnes qualifiées.
Votre commission propose en outre que le Conseil d'orientation médical et scientifique soit consulté sur les demandes d'autorisation concernant les recherches sur l'embryon et plus généralement sur toute décision de l'Agence intéressant la recherche médicale ou scientifique, telle que par exemple le soutien à des projets de recherche. Il lui reviendrait également d'assurer une veille scientifique sur les avancées dans ses domaines de compétences en vue d'assurer l'information permanente du Gouvernement et du Parlement.
Cette révision de la composition du Conseil d'orientation médical et scientifique par rapport à celle initialement prévue pour le Haut Conseil, vise avant tout à ne pas limiter, de fait, sa compétence à l'exercice solennel d'une magistrature morale mais plutôt à la situer dans une posture « opérationnelle » dans sa mission d'appréciation des travaux de l'Agence.
Il est enfin proposé que le contenu des avis du Conseil d'orientation médical et scientifique soit annexé au rapport public de l'Agence, afin d'assurer une large publicité à ces dernières.
b) Préciser la composition du conseil d'administration de l'Agence
Le présent projet de loi prévoit que le conseil d'administration soit composé pour moitié de représentants de l'Etat et pour moitié de personnalités qualifiées.
Votre commission propose de préciser :
- la notion de « représentant de l'Etat » à laquelle est substitué, des représentants des trois ministères concernés -santé, recherche, justice- et de l'élargir à des représentants de la caisse primaire d'assurance maladie ;
- que l'autre moitié est composée à la fois de personnalités qualifiées et de représentants du personnel.
2. Clarifier le régime juridique d'exercice des recherches scientifiques
Le présent texte prévoit, à plusieurs reprises, des dispositions censées préserver la poursuite de recherches menées sur des tissus ou produits issus du corps humain de toutes dérives. Si l'ensemble de ces dispositions sont utiles et nécessaires, votre commission est en mesure de proposer quelques simplifications procédurales d'appoint :
- elle propose en premier lieu, en accord avec le ministre de la santé, de limiter au ministre de la recherche deux procédures d'autorisations : celle relative à l'importation et à l'exportation de sang à des fins de recherche scientifique, et celle relative à l'importation ou l'exportation de tissus et cellules à ces mêmes fins. Dans ces deux cas, en effet, la double autorisation du ministre chargé de la recherche et du ministre chargé de la santé prévue par le projet de loi n'apparaît pas nécessaire et alourdit considérablement la procédure ;
- elle propose en second lieu de ne pas soumettre les recherches biomédicales portant sur des tissus aux dispositions de l'article L. 1241-1 qui limite la possibilité de prélèvement de tissus sur une personne vivante en vue de don à des fins thérapeutiques aux seuls tissus inscrits sur une liste fixée par décret en Conseil d'Etat ;
- elle propose enfin de prendre en compte la spécificité des recherches biomédicales portant sur les produits cellulaires à finalité thérapeutique, sur les produits de thérapie génique et sur les produits cellulaires d'origine animale en prévoyant une équivalence entre l'autorisation de recherche biomédicale et l'autorisation du lieu dans lequel s'effectuent le prélèvement, la conservation, la préparation et l'administration des cellules.
Sur le sujet des recherches biomédicales, votre commission propose, en outre, de préciser que les déclarations relatives aux collections d'échantillons biologiques doivent être accompagnées de l'avis d'un comité consultatif de protection des personnes dans la recherche biomédicale (CCPPRB) sur la pertinence générale du projet et les conditions d'information et de recueil du consentement des personnes.
Outre un certain nombre d'amendements apportant au texte davantage de lisibilité et de sécurité juridique, telles sont les principales orientations que vous propose votre commission.
Elles seront complétées, comme il a été dit, par un certain nombre d'initiatives fortes d'ores et déjà annoncées par le Gouvernement concernant l'incrimination du clonage reproductif, la création d'une agence de biomédecine et la brevetabilité du vivant auquel votre commission apportera son soutien
EXAMEN
DES ARTICLES
TITRE
PREMIER
-
DROITS DE LA PERSONNE
ET CARACTÉRISTIQUES
GÉNÉTIQUES
CHAPITRE
PREMIER
Prohibition des discriminations
Votre commission vous propose d'adopter l'intitulé du présent titre tel que retenu par l'Assemblée nationale et de maintenir la suppression de la division et de l'intitulé du présent chapitre premier (cf. commentaire ci-dessous de l'article premier).
Article premier
Prohibition des discriminations en raison
des
caractéristiques génétiques
Objet : Cet article unique du présent chapitre tendait, dans le texte initial du projet de loi, à interdire toute discrimination en raison des caractéristiques génétiques.
I - Le dispositif proposé
Le présent article pose le principe de non-discrimination en raison des caractéristiques génétiques. Son dispositif a été repris à l'identique dans le projet de loi relatif aux droits des malades et à la qualité du système de santé devenu la loi n° 2002-303 du 4 mars 2002.
Dans son commentaire de l'article premier bis de ce projet de loi (article 4 de la loi du 4 mars 2002), votre rapporteur avait présenté le contenu de la rédaction proposée par cet article pour l'article 16-13 du code civil en ces termes :
« Cet article se propose de combler une lacune de la législation relative à l'interdiction des discriminations en modifiant tout à la fois le code civil, le code pénal et le code du travail.
« Un principe d'interdiction des discriminations est actuellement édicté par les articles 225-1 à 225-4 du code pénal ainsi que par l'article L. 122-45 du code du travail, mais ces dispositions ne prennent pas en compte le nouveau facteur de discrimination à l'égard des personnes que peut constituer la connaissance de leurs caractéristiques génétiques.
« Or, les risques potentiels liés à une utilisation discriminatoire des résultats des examens génétiques tendent à croître, dans des domaines tels que ceux du contrat d'assurance ou du contrat de travail. En effet, en raison des progrès intervenus en matière de tests génétiques, les prédispositions à des pathologies susceptibles d'être révélées sont de plus en plus nombreuses. En outre, on assiste à l'apparition d'une offre de dispositifs de tests dont la nature n'exclut pas qu'ils puissent échapper à l'avenir au cadre de la prescription et de la mise en oeuvre par des professionnels de santé.
« Il convient de rappeler qu'un principe de prohibition des discriminations fondées sur les caractéristiques génétiques des personnes a été énoncé par des instruments internationaux récents tels que la convention du Conseil de l'Europe sur les droits de l'Homme et la biomédecine, dans son article 11, et la Déclaration universelle sur le génome humain et les droits de l'Homme, dans son article 6.
« De même, les caractéristiques génétiques sont expressément mentionnées, en tant que source possible de discrimination, dans le principe de non-discrimination figurant à l'article 21 de la Charte des droits fondamentaux de l'Union européenne.
« Le I du présent article insère au chapitre III du titre I er du livre I er du code civil, qui contient les garanties de protection en matière d'examen des caractéristiques génétiques d'une personne, un article 16-13 stipulant que nul ne peut faire l'objet de discriminations en raison de ses caractéristiques génétiques.
« Le II étend le délit de discrimination défini aux articles 225-1 et 225-2 du code pénal aux discriminations opérées à raison des caractéristiques génétiques des personnes et précise la portée de la dérogation prévue au 1° de l'article 225-3 en ce qui concerne les discriminations fondées sur l'état de santé. La répression de telles discriminations, lorsqu'il s'agit de prendre en compte les résultats des test prédictifs d'une maladie future ou d'une prédisposition génétique à une maladie, est maintenue.
« Enfin, le III complète l'article L. 122-45 du code du travail en étendant l'interdiction des discriminations en matière de recrutement, de sanction et de licenciement qui y figure aux discriminations fondées sur les caractéristiques génétiques. » 37 ( * )
II - Les modifications adoptées par l'Assemblée nationale
Ayant introduit, le 3 octobre 2001, la teneur du présent article dans le projet de loi relatif aux droits des malades et à la qualité du système de santé , l'Assemblée nationale en a, en conséquence, adopté la suppression dans le présent projet de loi relatif à la bioéthique , le 16 janvier 2002, lors de son examen en première lecture. Votre rapporteur observe que cette « coordination », en quelque sorte interne aux délibérations de l'Assemblée nationale, a été opérée avant même que le Sénat ait confirmé cette procédure et ce changement de support législatif. La Haute Assemblée n'a en effet adopté, en première lecture, le projet de loi « droits des malades » que le 6 février 2002.
III - La position de votre commission
Sur le fond, votre commission qui réitère son avis favorable sur ce dispositif, formulera cependant deux remarques.
La première est relative aux interrogations que suscite la multiplication des dispositions de principe relatives à l'interdiction des discriminations. Ces dispositions sont, dans leur intention, éminemment louables mais leur application reste toujours l'objet de difficultés, sauf à admettre que leur finalité est circonscrite à l'affirmation de grands principes.
A titre d'exemple, elle rappellera la difficulté formulée par l'un de ses anciens membres les plus éminents, M. Claude Huriet lors de son audition devant la commission 38 ( * ) , à propos des « kits génétiques » :
« On peut disposer de puces à ADN et de kits de diagnostics déjà largement accessibles aux Etats-Unis. Nous devons nous interroger, non pas sur le bien fondé des dispositions législatives encadrant l'utilisation et l'accès aux données génétiques, mais sur la question de savoir si la diffusion de ces procédés ne va pas changer fondamentalement l'application de la loi ». A juste titre, il conclut que « rien n'empêchera des personnes ayant réalisé leur propre diagnostic génétique et disposant d'un « profil idéal », de le faire valoir auprès des assureurs, pour bénéficier d'un bonus, ou des employeurs, pour obtenir une priorité à l'embauche. Il est nécessaire, dans le cadre de l'évaluation et de la révision de la loi, de tenir compte de ces nouvelles possibilités de diagnostic » .
Comment donc l'affirmation posée par cet article trouvera-t-elle à s'appliquer dans ce cas de discrimination à son profit suscitée par celui-là même que le législateur a souhaité protéger ?
Ce point renforce le grief alors formulé par votre rapporteur lors de l'examen de cette disposition dans le projet de loi relatif aux droits des malades à savoir qu'elle « partage naturellement les objectifs poursuivis par cet article. Elle regrette cependant que l'Assemblée nationale ait souhaité dissocier cet article du projet de loi relatif à la bioéthique, anticipant de la sorte sur un débat plus global. Cet article avait, à l'évidence, davantage vocation à être examiné à la lumière des autres dispositions dudit projet de loi ». C'est en effet lorsque l'ensemble des dispositions sont examinées que les possibilités de mieux encadrer les principes qu'elles viennent réglementer apparaissent plus cohérentes.
La seconde remarque vient, une nouvelle fois, déplorer le retard pris par l'examen du présent projet de loi, du fait de la gestion de l'ordre du jour par le précédent gouvernement. Aux yeux des auteurs de l'amendement, il était manifeste que le texte relatif aux droits des malades constituait un véhicule législatif rapide -il était de fait assorti d'une procédure d'urgence- tandis que le texte relatif à la bioéthique faisait figure « d'omnibus ». Sans doute, puisqu'on l'avait attendu déjà trois ans, son adoption était-elle susceptible d'être à nouveau différée.
Sous le bénéfice de ces observations, votre commission vous propose, par cohérence, de maintenir la suppression de cet article .
CHAPITRE II
Examen des caractéristiques génétiques
et identification
d'une personne par ses empreintes
génétiques
Article 2
Examen génétique des caractéristiques d'une
personne
Objet : Cet article fixe les conditions dans lesquelles il peut être procédé à l'examen des caractéristiques génétiques d'une personne.
I - Le dispositif proposé
Le I du présent article propose de modifier le chapitre III du titre premier du livre premier du code civil relatif à « l'étude génétique des caractéristiques d'une personne et de l'identification d'une personne par ses empreintes génétiques » afin :
- dans son intitulé, de remplacer les termes « études génétiques des caractéristiques » par les termes « examens des caractéristiques génétiques » ( 1° ) ;
- de mettre en conformité partielle la rédaction de l'article 16-10 du code civil avec l'article 16 de la Convention d'Oviedo qui prévoit que « pour la protection des personnes se prêtant à une recherche », le consentement est « consigné par écrit » , précision que ne comportait pas cet article. Est en outre harmonisée, conformément à l'intitulé du chapitre, la rédaction relative à l' examen des caractéristiques génétiques qui est substitué à l' étude génétique des caractéristiques . La disposition essentielle de l'article 16-10, précisant que ces recherches ne peuvent être menées que dans une finalité thérapeutique ou scientifique, demeure inchangée ( 2° ).
Le II modifie la terminologie figurant dans le code de la santé publique en substituant, pour l'intitulé du titre III du livre premier de sa première partie, les mots « examens des caractéristiques génétiques, identification et recherche génétique » à la notion de médecine prédictive , cette dernière étant trop étroite car elle n'autorise pas le diagnostic d'une maladie déjà déclarée. Son remplacement par la notion indiquée ci-dessus permet de recouvrir une notion plus large.
Le III propose cette même harmonisation pour le code pénal :
- le 1° modifie l'intitulé de la section VI du chapitre VI du titre II du livre II du code pénal qui réprime les atteintes aux personnes résultant de l'examen génétique de leurs caractéristiques qui deviendrait « Des atteintes à la personne résultant de l'examen de ses caractéristiques génétiques ou de l'identification par ses empreintes génétiques » ;
- le 2° propose deux modifications pour l'article 226-25 du même code. La première est l'harmonisation terminologique décrite ci-dessus, c'est-à-dire le remplacement du terme « étude » par le terme « examen ». La seconde prévoit la modification du renvoi initialement prévu à l'article L. 1131-1 du code de la santé publique : il est proposé que le code pénal fasse une référence directe à l'article 16-10 du code civil ;
- le 3° prévoit le remplacement du mot « étude » par le mot « examen » au sein de l'article 226-26 du code pénal.
II - Les modifications adoptées par l'Assemblée nationale
Sur proposition de sa commission spéciale, l'Assemblée nationale a adopté quatre amendements :
- le premier prévoit que le consentement est « exprès » ;
- le deuxième prévoit que la personne qui se prête à un examen est préalablement informée sur la finalité de ce dernier ;
- le troisième vise à inscrire dans le code civil que le consentement écrit comporte la finalité de l'examen ;
- le dernier propose une nouvelle rédaction pour l'article 226-25 du code pénal qui punit le fait de se livrer à un examen des caractéristiques génétiques à des fins de recherches scientifiques hors des conditions prévues par les textes en vigueur, ou à d'autre fins quelles que soient les conditions. Aux termes de cet article dans sa rédaction précédente, seuls les examens réalisés à des fins médicales, lorsqu'elles ne respectaient pas le régime juridique qui les régit, étaient incriminés.
III - La position de votre commission
Le débat terminologique
L'origine de l'harmonisation proposée par cet article tient à la grande diversité des rédactions figurant dans les trois codes traitant du régime juridique de l'examen -ou des recherches- des caractéristiques génétiques d'un individu.
Le code de la santé publique fait, pour sa part, référence à trois notions : la médecine prédictive , l'examen des caractéristiques génétiques , qui figure déjà à l'article L. 1131-1 et est pris pour pivot de l'harmonisation, et l'étude des caractéristiques génétiques qui figure au troisième alinéa de ce même article et qui sera, pour sa part, harmonisée à l'article 3 du présent projet de loi.
Le code civil retient, quant à lui, l'expression « étude des caractéristiques d'une personne » dans son article 16-10, expression qui figure également à l'article 226-25 du code pénal.
Cette harmonisation a suscité un véritable débat lors de l'examen du projet de loi en première lecture par l'Assemblée nationale, la commission spéciale proposant la rédaction « examen génétique des caractéristiques de la personne » à laquelle le Gouvernement préférait la rédaction « examen des caractéristiques génétiques de la personne » .
En effet, M. Bernard Kouchner, alors ministre délégué à la santé, estimait 39 ( * ) :
« Le terme « examen génétique des caractéristiques de la personne » apparaît trop restrictif. Il ne permet pas de garantir la protection de la personne à l'égard d'une éventuelle utilisation abusive d'informations génétiques obtenues à l'occasion d'investigations médicales diverses non spécifiquement génétiques, comme par exemple une biopsie musculaire chez un myopathe de Duchêne, l'électroforèse de l'hémoglobine pour le diagnostic de la drépanocytose ou des thalassémies, ou encore de l'HLA 27. Le terme utilisé dans le projet de loi vise à encadrer l'ensemble des examens de caractère génétique. Ce terme est plus large et plus adapté à l'objectif de l'encadrement fixé » .
Au contraire, pour l'actuel ministre de la santé, alors député, M. Jean-François Mattei, c'est la rédaction proposée par le Gouvernement qui était trop restrictive :
« Je ne crois pas qu'on puisse s'en tenir à l'expression : « caractéristiques génétiques ». Un simple examen clinique ou biologique permet de distinguer des caractères génétiques. Lors d'une numération sanguine, vous savez, par la forme des globules rouges, s'il y a ou non une anomalie de l'hémoglobine. Je pourrais multiplier les exemples. Un groupage sanguin, un groupage HLA ne sont pas des études génétiques mais peuvent aboutir à observer et apprécier des données génétiques. Ce sur quoi je croyais que nous voulions légiférer, c'était sur l'utilisation des examens génétiques, et notamment la génétique moléculaire. Or, avec l'expression : « caractéristiques génétiques », nous incluons à la fois les caractéristiques génétiques par l'examen clinique, par l'examen biologique traditionnel et par les études moléculaires. Voilà pourquoi j'ai souhaité que nous précisions: « examen génétique ». Ce sont les techniques génétiques qui vont nous permettre d'étudier les caractères de la personne ».
Finalement, le débat entre les membres de l'Assemblée nationale et le Gouvernement a convergé afin que la protection la plus large des personnes soit assurée.
« M. Jean-François Mattei. Je ne crois pas que le débat soit tranché. A « examen des caractéristiques génétiques », on devait substituer « examen génétique des caractéristiques ». Vous reviendriez donc à l'expression « examen des caractéristiques génétiques » ?
« M. le ministre délégué à la santé. Oui !
« M. Jean-François Mattei. En sous-entendant : clinique, biologique et, spécifiquement, par les techniques de la génétique ? C'est bien cela ?
« M le ministre délégué à la santé. Absolument !
« M. Jean-François Mattei. Je n'entends pas, en insistant ainsi, vous mettre en difficulté. Je veux simplement que cela figure au Journal officiel pour éclairer une éventuelle interprétation devant la justice et pour que nous soyons bien d'accord : lorsque nous parlons de caractéristiques génétiques, nous entendons, d'abord et avant tout, la mise en oeuvre des nouvelles techniques...
« M. le ministre délégué à la santé. Sur le noyau !
« M. Jean-François Mattei.... mais, naturellement, cela n'exclut pas totalement les analyses génétiques par le biais des examens conventionnels, y compris l'étude clinique.
« M. Bernard Charles, président de la commission spéciale . Tout à fait !
« Mme la présidente. Les choses me semblent claires. »
Cette convergence méritait d'être rappelée afin d'éclairer l'interprétation du présent article.
La protection des personnes se prêtant à l'examen de leurs caractéristiques génétiques
Dès 1995, dans son avis n° 46, le Comité consultatif national d'éthique rappelait que « tout autant et même plus qu'un autre examen médical, un test génétique comporte une entrée dans l'intimité d'une personne, à savoir son intimité corporelle et les significations qu'elle y attache en rapport à son identité psychique » . Aussi préconisait-il, dans sa première recommandation, que la conduite de ces tests s'insère dans une démarche susceptible de garantir le respect de la personne qui s'y est livrée.
|
L'examen des caractéristiques génétiques d'un individu peut avoir, quel que soit son résultat, de profondes répercussions sur la vie du sujet qui s'y prête. Le respect de son autonomie exige qu'il ait une compréhension aussi complète que possible des conséquences de sa décision de se soumettre ou non à cet examen. Cette compréhension implique une information sur la nature de l'examen, la signification des résultats, l'existence éventuelle d'une prévention et d'une thérapie ainsi que leurs contraintes. Cette information doit être donnée par un professionnel ayant une bonne connaissance de la génétique médicale et être directe et orale pour permettre un dialogue, puis consignée dans un document écrit. Toute détermination de caractères du génotype d'un individu ne doit être entreprise qu'à des fins médicales sur prescription ou à des fins scientifiques et que si le sujet a donné spécifiquement son consentement écrit. Les résultats de l'examen doivent être communiqués directement par un médecin, qui, de par sa compétence, pourra expliquer aux sujets testés la signification de ces résultats. Un suivi du sujet testé devra être assuré, pour pallier les éventuelles répercussions psychologiques du résultat, que celui-ci soit positif ou négatif.
Certaines informations peuvent avoir un effet potentiellement
néfaste pour l'individu. Celui-ci peut donc refuser de connaître
les résultats de l'examen et son droit de ne pas savoir doit toujours
être respecté.
|
La Convention d'Oviedo 40 ( * ) prévoit, pour sa part, à ses articles 5 et 16 une série de protections en faveur de la personne humaine.
L'article 5 prévoit en effet qu'aucune intervention ne peut avoir lieu dans le domaine de la santé sans que la personne ait donné son « consentement libre et éclairé » , qu'elle ait reçu une information claire au sujet de cette information et qu'elle peut « à tout moment, librement retirer son consentement » .
L'article 16, relatif à la protection des personnes se prêtant à une recherche prévoit expressément l'application des dispositions prévues par l'article 5.
L'Assemblée nationale a complété les dispositions prévues par cet article pour l'article 16-10 du code civil, en prévoyant que le consentement à la recherche des caractéristiques génétiques est exprès et que la personne reçoit préalablement une information claire et détaillée.
Toutefois, ne figure pas le principe prévu par la Convention d'Oviedo du retrait possible, à tout moment, de ce consentement. Aussi votre commission vous propose-telle d'adopter un amendement prévoyant cette précision.
La question d'un changement de finalité des tests réalisés n'est guère abordée. La personne s'étant livrée à un test à finalité médicale doit-elle consentir expressément et préalablement à ce que ces tests soient, le cas échéant, utilisés à des fins de recherches scientifiques ? Votre commission ne l'envisage pas autrement.
Ces principes et précautions rappelés, votre rapporteur formulera deux interrogations.
Ainsi qu'il a été dit précédemment (cf. commentaire ci-dessus de l'article premier) , M. Claude Huriet a mis en lumière, lors de son audition par notre commission, la difficulté soulevée par la généralisation des tests génétiques. Peut-on et doit-on organiser l'émergence d'un marché libre des tests génétiques en France, rendu possible par l'amélioration des techniques qui d'ailleurs permettent déjà, via un simple test sanguin, de faire réaliser sa carte génétique à l'étranger ?
Le Conseil d'Etat propose, pour sa part, que ce développement s'inscrive dans une politique de prévention cohérente dans le cadre duquel pourrait être amélioré le dépistage de maladies génétiques ou de certains cancers. « Les professionnels de santé, au coeur de ce dispositif, seraient en mesure de garantir les conditions de prescription et d'utilisation des tests, qui, en tant que produits de santé, devraient obtenir une autorisation de mise sur le marché » 41 ( * ) .
Ce meilleur encadrement est également réclamé par les praticiens les plus éminents, à l'instar du professeur Arnold Munnich qui déclarait devant votre commission que « des décrets encadrent effectivement les tests génétiques, mais cinq ans après leur promulgation, ils n'ont pas été accompagnés des circulaires devant mettre en application les règles de bonnes pratiques. Ce problème concerne, non la poignée de couples concernés par les maladies dont nous avons discuté, mais des centaines de milliers de Français. Les conditions réglementaires des tests génétiques restent d'un flou total et nous sommes à la veille d'une dérive retentissante . Nous ne savons pas qui prescrit le test, comment il est pratiqué, rendu, et si une consultation génétique intervient préalablement à la prescription. Des catastrophes arrivent dans la mesure où, en France, des résultats d'examens prescrits à la légère, parfois par téléphone, sont rendus par courrier sans être accompagnés de la moindre explication . Ils sont transmis par le médecin généraliste, qui n'y connaît rien, à des patients qui comprennent encore moins. S'agissant d'un grand nombre de Français, j'appelle votre attention sur la nécessité de l'adoption de circulaires d'application des dispositions réglementaires 42 ( * ) » .
Un tel développement traduit bien l'inquiétude que suscite la potentielle dérive issue de la mise à disposition de chacun de sa carte génétique et de l'insuffisance de l'encadrement en vigueur. C'est à juste titre que le Conseil d'Etat note que :
- le principe général de non-discrimination figurant à l'article 225-1 du code pénal ne mentionnait pas les caractéristiques génétiques d'une personne parmi les sources de discrimination qu'il énumère -cet oubli a été corrigé par l'article premier du présent projet de loi repris par la loi relative aux droits des malades ;
- rien n'interdirait un assureur -ou un employeur- de solliciter des tests réalisés à des fins médicales ou scientifiques afin de « discriminer » les bons et les mauvais risques car « la communication spontanée par un individu des données génétiques le concernant au médecin de l'assureur pourrait être analysée par les tribunaux comme ne constituant ni une dérogation au secret médical -l'assureur n'ayant communication par son service médical que d'une barémisation du risque, et non d'une information couverte par le secret médical- ni le détournement de finalité sanctionné par l'article 226-26 du code pénal » 43 ( * ) .
Ces difficultés sont sans doute appelées à se poser, dans les années qui viennent, avec une acuité accrue.
Sous réserve de l'amendement sus-mentionné, et d'un amendement de précision à la rédaction qu'il propose pour l'article 226-25 du code pénal, votre commission vous propose d'adopter cet article ainsi amendé.
Article 3
Identification d'une personne par ses empreintes
génétiques
Objet : Cet article précise le régime juridique de l'identification des personnes par empreintes génétiques.
I - Le dispositif proposé
Le I du présent article propose deux modifications pour l'article 16-11 du code civil qui prévoit le régime juridique de l'identification par empreintes génétiques.
Le 1 ° complète cet article pour préciser le régime d'identification post mortem dans le cadre d'une procédure civile. La position de principe qu'il est proposé de retenir est que seule l'opposition expresse exprimée du vivant de la personne fait obstacle à une telle identification.
Le 2° prévoit que le consentement à l'identification génétique réalisée à des fins médicales ou de recherche scientifique est exprimé par écrit.
Le II procède à une réécriture de l'article L. 1131-1 du code de la santé publique.
Tel qu'en vigueur aujourd'hui, cet article prévoit :
- au premier alinéa , les règles régissant les examens des caractéristiques génétiques ou leur identification. Seuls les examens ou identifications dans le cadre d'une procédure judiciaire dispensent du consentement de la personne ;
- au deuxième alinéa , la nécessité du consentement écrit, et la mise sous la protection des dispositions de la loi Huriet de 1988, pour les recherches et identifications effectuées à des fins médicales ou thérapeutiques ;
- au troisième alinéa , le cas de dispense de consentement lorsque, exceptionnellement, celui-ci ne peut être recueilli. Il fallait pour cela que l'étude envisagée soit réalisée dans le respect de la confiance de la personne , et bien sûr dans son intérêt .
Le texte proposé pour cet article L. 1131-1 vise à simplifier la rédaction en vigueur , en renvoyant aux dispositions du code civil et du titre III du code de la santé publique les conditions de réalisation des examens des caractéristiques génétiques d'une personne ou son identification. Il est, en outre prévu, que, désormais, seul l'intérêt du patient permettra de recueillir le consentement de la personne.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a tout d'abord adopté, à l'initiative de MM. Jean-François Mattei et plusieurs de ses collègues, un amendement au 1° du I du présent article renversant le régime de l'identification post mortem prévue par le projet de loi. Cette identification ne sera désormais possible que si la personne décédée y avait consenti expressément de son vivant.
Elle a ensuite adopté trois amendements à l'initiative de sa commission spéciale :
- elle a, en premier lieu, inséré un 3° nouveau dans la rédaction proposée pour l'article 16-11 du code civil. Cet article aligne les conditions du recueil du consentement d'une personne à son identification à des fins médicales ou scientifiques par empreintes sur celles prévues pour l'examen des caractéristiques génétiques ;
- elle a, en second lieu, au II de cet article, adopté deux amendements à la rédaction proposée pour l'article L. 1131-1 du code de la santé publique. Le premier rappelle que l'examen ou l'identification précités demeurent soumis aux dispositions de la loi du 20 décembre 1988, figurant dans le titre II du même code. Le second prévoit la consultation d'un proche ou de la personne de confiance si la personne qui doit subir cet examen dans son intérêt n'est pas en état d'exprimer son consentement.
III - La position de votre commission
1°) L'identification d'une personne dans le cadre d'une procédure civile
Le droit fait appel à la science pour l'identification par utilisation des empreintes génétiques dans deux domaines particuliers : la procédure pénale et la procédure civile, la première n'étant pas soumise au consentement de la personne identifiée tandis que la seconde l'est. En matière civile, l'article 16-11 de ce code ne prévoit que deux cas de recours à cette identification : l'établissement de la filiation et l'obtention ou la suppression de subsides. Or, cette rédaction prévoit expressément le consentement de la personne sur laquelle l'identification est conduite. Cette règle du consentement s'applique-t-elle aussi lorsque la personne à identifier est décédée ?
La question de l'identification post mortem en matière civile
Est-il possible de recourir à l'exhumation d'un corps, dans une procédure civile de recherche en paternité, dès lors que la personne décédée n'a pas clairement fait connaître son opposition à un tel test, voire même lorsqu'elle l'a fait connaître de son vivant ?
La rédaction de l'article 16-11 du code civil ne le permettrait a priori pas, le consentement devant être à la fois préalable et exprès. Pour autant, dans le contentieux entre vifs, le juge peut tirer « les conséquences » du refus d'une personne qui refuserait de se soumettre à un tel test et, déclarer d'office la paternité, ce qu'il ne peut pas faire pour un mort.
En 1996, la Cour d'appel d'Aix a autorisé une personne à faire procéder à une mesure d'expertise par empreintes génétiques sur un individu décédé, bien que ce dernier n'ait pas expressément consenti à cet examen de son vivant. Pour écarter l'application de l'article 16-11 du code civil, la Cour d'appel avait alors fait référence au « silence de la loi » .
Le Conseil d'Etat, pour sa part, appelait de ses voeux un encadrement plus strict de l'identification d'une personne dans le cadre d'une enquête judiciaire.
« Saisie d'une action en établissement de paternité d'Yves Montand, la Cour d'appel de Paris a cependant cru pouvoir écarter ces dispositions (art. 16-11 du code civil), au motif qu'il n'était plus possible de recueillir le consentement de l'artiste qui était décédé, alors même que l'intéressé avait manifesté de son vivant une opposition à une telle mesure.
« Si elle devait être renouvelée par un juge, cette interprétation volontariste fragiliserait le texte et le choix qu'il traduit de donner le pas à la liberté de garder le secret sur une filiation sur le droit ou l'aspiration d'un enfant à connaître ses origines. En effet, la reconnaissance à la personne, de son vivant, d'une possibilité de refus de consentement à l'expertise de filiation irait de pair avec le fait que cette mesure pourrait être imposée sans restriction après le décès de l'intéressé. Ce risque d'incohérence pourrait être prévenu par l'adjonction à la fin du second alinéa de l'article 16-11 du Code civil de la phrase suivante : « L'opposition clairement manifestée de son vivant par une personne à une telle mesure d'instruction fait obstacle à la mise en oeuvre de celle-ci après le décès de l'intéressé. ». Une telle mesure assurerait le respect du principe du consentement par-delà le décès de la personne.
« Il convient néanmoins de souligner qu'elle sera à l'origine d'une dissymétrie entre les morts et les vivants. Lorsque la personne qui refuse de se soumettre à une expertise de filiation est vivante, en effet, le juge peut tirer les conséquences de ce refus et procéder à une affirmation judiciaire de la paternité sur la base de présomptions. Cette faculté résulte notamment de l'article 11 du nouveau code de la procédure civile, aux termes duquel « les parties sont tenues d'apporter leur concours aux mesures d'instruction sauf au juge à tirer toute conséquence d'une abstention ou d'un refus ».
« Certains ont pu souligner en outre que si la mort écarte toute appréciation du juge civil, l'équilibre qui sera consacré entre le principe de l'intégrité du corps humain et le principe du droit de l'enfant à connaître sa filiation ne va pas de soi 44 ( * ) . »
Pour sa part, votre rapporteur prend acte de la position prise par l'Assemblée nationale qui a renversé la rédaction prévue initialement par le présent projet de loi pour affirmer la nécessité d'un consentement exprès de la personne décédée, formulé de son vivant.
Certes, on pourrait arguer, en s'appuyant sur l'analyse du Conseil d'Etat, qu'une telle précision induit une inégalité entre les requérants, entre ceux qui auront eu la possibilité de formuler leur requête du vivant de leur parent putatif, et qui in fine bénéficieront d'une réponse au moins présumée 45 ( * ) , et ceux qui seront confrontés à la barrière de la mort.
Cela étant, le législateur devait trouver une conciliation entre deux principes également respectables : celui des vivants à connaître leurs origines et la paix des morts . La position retenue par le texte tel qu'issu des travaux de l'Assemblée nationale rend en définitive raison au poète pour qui « le silence est le meilleur avocat des morts » 46 ( * ) .
Le cantonnement de l'identification génétique à la procédure civile de filiation
L'identification par empreintes génétiques ne peut être conduite, dans le cadre d'une procédure civile, qu'en matière de filiation. Cette restriction est-elle pertinente ?
Elle pourrait, en effet, être développée afin de permettre d'éclairer le juge au cours de litiges divers. Sur proposition de M. Jean François Mattei, député, l'Assemblée nationale a examiné un amendement visant à étendre le champ du premier alinéa de l'article 16-11 du code civil.
Le rapporteur de la commission spéciale, M. Alain Claeys 47 ( * ) , a éclairé cette proposition d'un exemple concret : « Il y a quelques années, une jeune femme dont le mari était décédé dans un accident de voiture s'est vu refuser le bénéfice de l'assurance au motif que les examens sanguins pratiqués sur le mort montraient des traces d'alcool. La jeune femme les a contestés en faisant valoir que son mari ne buvait pas d'alcool. Elle pensait qu'il y avait eu confusion de flacons. Elle demandait au juge des référés d'ordonner une mesure d'identification par empreintes génétiques pour établir la comparaison des sangs des flacons, mesure que le juge des référés refusa, décision confirmée en appel sur le fondement de l'article 16-11 du code civil » .
Le Gouvernement 48 ( * ) a, pour sa part, souhaité que ne soit pas étendue la faculté prévue pour la seule recherche en filiation au motif « qu'il ne faut pas rompre cet équilibre en autorisant le juge à prescrire cette mesure, quelle que soit la nature de l'action dont il est saisi. Une expertise génétique pourrait ainsi être demandée, par exemple, dans le cas d'un litige successoral, lors d'une contestation devant le juge de l'identité des bénéficiaires d'une assurance sur la vie, voire lors de procédures qui ne présentent pas un caractère contradictoire. Au surplus, cette extension comporterait sans nul doute des risques de contrariété de jurisprudence. De surcroît, un tel élargissement des possibilités de mise en oeuvre des mesures civiles d'empreintes génétiques serait contraire à l'orientation d'ensemble d'un texte qui, dans un souci de protection des droits fondamentaux, tend à restreindre les conditions dans lesquelles peut être autorisée une mesure d'empreintes génétiques sur une personne décédée ».
La question reste, là encore, ouverte.
2°) La réécriture de l'article L 1131-1 du code de la santé publique
L'amélioration des garanties
La réécriture de l'article L. 1131-1 du code de la santé publique se justifie par le souci de simplifier le régime des garanties entourant la réalisation d'examens ou d'identification génétique.
Le droit en vigueur prévoit en effet qu'à titre exceptionnel, le consentement de la personne peut ne pas être recueilli lorsque cet examen ou identification est réalisé à des fins médicales, qu'il est dans l'intérêt du patient et est effectué dans le respect de sa confiance.
La rédaction proposée par le présent projet de loi est plus protectrice puisque cette dérogation sera désormais limitée aux seuls cas où les personnes ne peuvent matériellement manifester leur consentement. Deux conditions expresses sont prévues : l'examen est à finalité médicale et est mené dans l'intérêt du patient.
L'Assemblée nationale est allée plus loin en prévoyant, c'est heureux, la consultation obligatoire de la « personne de confiance » , notion introduite en droit positif par la loi du 4 mars 2002 relatif au droits des malades.
Votre commission souscrit à cette nouvelle rédaction proposée pour l'article L. 1131-1 du code de la santé publique, sous une double réserve justifiant deux amendements :
- elle vous propose de corriger une erreur matérielle, car la personne de confiance visée par l'Assemblée nationale est mentionnée à l'article L. 1111-6 du présent code et non à l'article L. 1111-5 ;
- elle vous propose d'apporter une précision en remplaçant, au troisième alinéa le terme « patient » par le terme « personne » . Il est manifeste que dans l'esprit de l'article, la personne constitue le patient mais il peut se trouver certains cas où cette identité n'est pas vérifiée. Puisque l'article prévoit expressément que la recherche ou l'identification ne peuvent être faits en l'absence de consentement, que dans l'intérêt de la personne sur laquelle elles sont pratiquées, il ne faudrait pas qu'elles puissent être pratiquées dans l'intérêt d'un tiers lui-même « patient » .
La difficile conciliation du secret médical et des tests ou examens génétiques
Lors de son audition par votre commission, le professeur Arnold Munnich 49 ( * ) a soulevé les difficultés posées par le secret médical au regard du statut génétique des sujets :
« Nous avons, encore tout récemment, été confrontés à des difficultés liées à ce secret . Ces maladies ne sont pas seulement celle d'un individu, elles éclaboussent toute la famille. Au regard du droit, le respect de la vie privée des gens l'emporte sur l'assistance à personne en danger . Il n'est malheureusement pas exceptionnel, j'en ai fait la douloureuse expérience samedi dernier, qu'une mésentente intrafamiliale aboutisse à la maladie et à la mort de plusieurs enfants apparentés éloignés. Lorsque nous nous retournons vers les personnes qui auraient pu, ou dû, prévenir leurs apparentés, elles se retranchent derrière le respect de la vie privée et du secret médical . J'attire donc votre attention sur le fait -nous y avons été confrontés avec la contamination intraconjugale dans le SIDA- que ce problème réglementaire est extraordinairement douloureux. Le législateur pourrait envisager une disposition selon laquelle, lorsque la vie des apparentés est en danger, une obligation est formulée d'aller au-devant des personnes à risques » .
Cette difficulté a déjà été évoquée par le Comité consultatif national d'éthique qui, dans la deuxième recommandation jointe à son avis n° 46 du 30 octobre 1995, ne pouvait se résoudre à proposer cette exception au secret médical :
« Le secret médical doit être respecté vis-à-vis des tiers, y compris les autres membres de la famille . Lorsque la découverte d'une anomalie génétique de caractère familial conduit à envisager un prélèvement biologique sur l'ensemble des membres de la famille, ceux-ci devront être sollicités directement par le sujet demandeur et non par le médecin. Si le sujet refuse de faire connaître aux membres de sa famille le risque révélé par l'examen génétique qu'il a subi, le médecin sera dans l'impossibilité de les prévenir du risque éventuel qu'ils ont de développer une maladie ou de la transmettre à leur descendance. Le médecin devra informer le sujet testé de sa responsabilité et tout faire pour le convaincre d'informer ses proches. En cas d'échec, le devoir de confidentialité et le secret médical seront en contradiction avec le devoir d'informer les sujets et les familles, d'un risque qui peut être l'objet d'une prévention. Le médecin sera confronté à un grave conflit éthique sur lequel la société devra se prononcer, en tenant compte du caractère inacceptable de la non-assistance à personne en danger, particulièrement lorsque des enfants sont concernés. »
Votre commission ne saurait purement et simplement écarter l'application du secret médical.
Pour autant, l'existence d'une affection génétique grave, non décelée et inconnue de la personne qui en est atteinte peut avoir une incidence importante sur la conduite de soins prodigués à cette personne.
Convaincue de l'intérêt potentiel qu'il existerait à ce qu'une personne, se sachant atteinte d'une telle affection génétique grave, soit sensibilisée par son médecin à la nécessité d'en informer sa parentèle, lorsque cette information permettrait des mesures efficaces de prévention ou de soins, votre commission vous proposera d'adopter un amendement prévoyant la faculté pour le médecin d'informer le patient de la nécessité de prévenir les membres de sa famille potentiellement concernés.
Votre commission vous propose d'adopter cet article ainsi amendé.
Article 4
(art. L. 1131-4, L. 1131-6 et art. L. 1131-7
et L. 1132-6
nouveaux du code de la santé publique)
Echantillons biologiques
humains
Objet : Cet article précise les conditions auxquelles sont soumises la constitution et l'utilisation de collections d'échantillons biologiques humains à des fins de recherche.
I - Le dispositif proposé
Le 1° du présent article propose une nouvelle rédaction de l'article L. 1131-4 du code de la santé publique en soumettant la constitution et l'utilisation de collections d'échantillons biologiques humains à des fins de recherche génétique au régime d'encadrement de droit commun prévu pour la conservation et l'utilisation des tissus et cellules. Ce régime est prévu notamment aux articles L. 1243-3 et L. 1243-4 du code de la santé publique, que l'article 8 du présent projet de loi modifie substantiellement.
En effet, dans leur rédaction nouvelle, ces deux articles définissent un régime juridique unique pour les établissements qui manipulent les tissus, cellules et leurs dérivés, régime comportant le principe d'une obligation de déclaration et d'une autorisation préalable du ministre de la recherche qui dispose d'une faculté d'opposition. Le ministre recueille l'avis du comité consultatif sur le traitement de l'information en matière de recherche dans le domaine de la santé . Ces dispositions s'appliqueront aux collections d'échantillons biologiques humains prévues par le nouvel article L. 1131-4.
Le 2° prévoit de supprimer le 3° du L. 1131-6 du code de la santé publique, devenu superfétatoire du fait des modifications prévues par le 1°. La disparition d'un régime spécifique pour les collections d'échantillons rend inutile le maintien d'un dispositif réglementaire ad hoc .
Le 3° introduit une dérogation. Les examens visant à vérifier la compatibilité avant le don, qui seront soumis aux dispositions du livre II, première partie, relative « aux don et utilisation des éléments et produits du corps humain » ne relèvent pas du régime décrit ci-dessus. S'appliquent à ces examens les conditions relatives au recueil du consentement appliquées au prélèvement.
Le 4° introduit en la reproduisant dans le code de la santé publique une disposition du code pénal qui concerne la responsabilité des personnes morales en matière d'infraction à la législation relative à l'examen et identification par les caractéristiques génétiques.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a adopté un amendement remplaçant dans le 3° de cet article les mots « préalablement en vue du don » par les mots « dans le contexte du don ».
La nécessité d'utiliser des échantillons à tout moment antérieurement au don mais également postérieurement pour faciliter le suivi justifiait cette modification.
III - La position de votre commission
Votre rapporteur souhaite formuler un certain nombre de considérations sur le 1° du présent article.
La genèse de l'article L. 1131-4 du code de la santé publique
Cet article a été introduit dans la loi n° 96-452 du 28 mai 1996, par un amendement déposé à l'Assemblée nationale à l'initiative de M. Jean-François Mattei.
Examinant cette disposition, M. Claude Huriet, rapporteur de votre commission, avait préconisé de ne pas l'adopter au motif que la superposition des régimes juridiques applicable à la collection d'échantillons biologiques rendrait difficile, voire impossible, leur application.
|
Dans son rapport n° 285 du 26 mars 1996 relatif au projet de loi portant diverses mesures d'ordre sanitaire, social et statutaire, M. Claude Huriet justifiait la proposition de la commission des Affaires sociales de ne pas retenir cette rédaction en ces termes. « L'article proposé indique clairement qu'il se superpose à la législation relative aux recherches biomédicales et à la loi dite « Fillon » de juillet 1994 ; « - il laisse la possibilité, soit à une personne, soit à un organisme, de constituer une collection (...) ; « - il fait référence, sans les définir, à l'« utilisation » des prélèvements et à l'« exploitation » de la collection (...) ; « - il introduit des notions nouvelles (...). Ainsi, la notion de « bon usage » des données recueillies, sans autre précision ; « - sa méconnaissance n'est pas assortie de sanctions pénales. « La portée de ces changements est difficile à apprécier, les notions nouvelles n'étant pas plus définies que les précédentes. « Si votre commission approuve la nécessité d'un texte législatif pour certaines collections qui n'en sont pas pourvues aujourd'hui, elle ne peut, en l'état, accepter cet article additionnel. Une législation concernant les collections d'échantillons doit répondre aux questions suivantes : « - qui peut constituer une collection ? « - que peut-on faire avec une telle collection ? « - quelles données peut-on recueillir et à quelles fins ? « En l'état, le dispositif proposé répond surtout à la troisième question. « Il se superpose à des législations existantes : « - le livre II bis sur les recherches biomédicales, dont l'article premier A ne reprend pas les catégories (investigateur-promoteur) comme l'avait fait l'article 8 undecies ; « - la loi dite Fillon du 1 er juillet 1994 relative au traitement de données nominatives ayant pour fin la recherche dans le domaine de la santé, dont le mécanisme de contrôle s'appliquerait en addition de celui prévu par l'article premier A (...) ; « - l'article L. 145-16 du code de la santé publique qui prévoit que « sont seules habilitées à procéder à des identifications par empreintes génétiques à des fins médicales ou de recherche les personnes ayant fait l'objet d'un agrément dans des conditions fixées par décret en Conseil d'Etat » ; « - l'article L. 672-10 du code de la santé publique qui prévoit que seuls des établissements de santé publics et des organismes à but non lucratif peuvent être autorisés à conserver des cellules et tissus.
« Considérant que la coordination des
législations pourrait être mieux assurée et que des
questions importantes sont malgré tout laissées sans
réponse,
votre commission
, s'engageant à mener
une réflexion active sur ce sujet qui le mérite,
vous
propose de supprimer cet article. »
|
Le Gouvernement avait invité le Parlement, au cours de la navette, à mieux définir l'articulation de ces régimes. La commission mixte paritaire avait in fine retenu cet article non sans avoir préalablement cherché à préciser certains points de son contenu.
|
« M. Jean-François Mattei, député, a rappelé que l'objectif de cet article, introduit à l'Assemblée nationale, était d'empêcher d'éventuelles dérives, notamment commerciales, susceptibles de se manifester dans le cadre de certaines recherches génétiques nécessitant la constitution de collections d'échantillons biologiques. Il a indiqué que grâce à cet article, un contrôle pourrait être institué, non seulement à l'occasion de la constitution initiale de la collection, mais aussi en cas de modification de l'objet de la recherche. « M. Claude Huriet, rapporteur pour le Sénat, a estimé que les propos tenus par M. Jean-François Mattei, député, répondaient en large partie aux interrogations qui s'étaient exprimées au Sénat au cours de l'examen du projet de loi en deuxième lecture. Il lui a cependant demandé de préciser les termes « exploitation » et « autorité administrative compétente ». « M. Jean-François Mattei, député, a indiqué que le terme exploitation devait être compris comme n'ayant aucun caractère industriel ou commercial et que l'autorité administrative compétente en matière de contrôle des collections d'échantillons biologiques devait être le ministre chargé de la santé, le ministre chargé de la recherche devant être invité à donner son avis. « Sous le bénéfice de ces explications, la commission mixte paritaire a adopté cet article dans le texte de l'Assemblée nationale. »
Rapport de commission mixte paritaire sur le projet de loi
portant diverses mesures
|
Un dispositif à bien des égards insatisfaisant
La complexité du dispositif, dénoncée alors par M. Claude Huriet est clairement établie par le Conseil d'Etat qui, lors de son étude de 1999, s'est interrogé sur le statut des collections d'échantillons biologiques humains constituées à des fins scientifiques 50 ( * ) .
« Afin de concilier le respect de l'individu et l'efficacité scientifique, le législateur a mis en place un régime dont la complexité a pu être soulignée . L'intérêt des donneurs est préservé de deux manières. Tout d'abord, les personnes dont proviennent les échantillons doivent dans tous les cas consentir explicitement à participer à une étude, dont elles ont le droit de connaître les résultats, comme de les ignorer, et l'utilisation d'une collection doit, en outre, être limitée à ce à quoi ont initialement consenti les donneurs. D'autre part, la constitution de collections informatisées et l'utilisation des échantillons sont soumises à des procédures d'autorisation strictes. La loi du 1 er juillet 1994 relative au traitement de données nominatives ayant pour fin la recherche dans le domaine de la santé, a tout d'abord complété la loi « informatique et liberté » du 6 janvier 1978 en soumettant à autorisation de la CNIL le traitement automatisé de données génétiques -fichiers constitués dans le cadre de consultations d'onco-génétique, sérothèques ou cellulothèques. Deux textes prévoient ensuite des dispositifs différents selon que les échantillons sont destinés à une recherche génétique ou non. L'article L. 145-16-1 du code de la santé publique, issu de la loi du 28 mai 1996, instaure un régime de déclaration auprès de « l'autorité administrative » pour les collections d'échantillons biologiques humains constituées dans le cas de recherches génétiques. Pour celles qui sont utilisées à des fins de recherche non génétique, un système analogue de déclaration au ministre chargé de la recherche a été prévu par l'article 19 de la loi du 1 er juillet 1998 relative à la veille sanitaire, afin de ne pas les soumettre au régime d'autorisation prévu à l'article L. 672-10 du code de la santé publique.
« La CNIL et les organismes de recherche font valoir que la multiplicité de ces procédures administratives est difficile à gérer pour les chercheurs. Il n'est pas toujours aisé, en effet, de distinguer entre une recherche à fin génétique et une recherche à fin scientifique, et tout élément biologique est potentiellement génétique. Aussi une harmonisation des deux dispositifs est-elle souhaitable pour garantir le développement de la recherche dans les sciences de la vie, mais aussi sa transparence et sa légitimité. »
Devant ces difficultés, le Conseil d'Etat proposait une alternative.
La première solution avancée par la Haute juridiction était une simplification drastique du régime juridique de ces collections.
« Elle consisterait à supprimer toute déclaration auprès du ministre chargé de la recherche ou de la santé et à se contenter de soumettre à une autorisation de la CNIL la constitution, l'utilisation et la conservation de toutes les collections d'échantillons biologiques humains quel que soit le caractère de la recherche à laquelle ils sont destinés.
« Cette première solution souffrirait cependant de certaines insuffisances. En effet, s'il est souhaitable d'unifier le régime juridique des collections d'échantillons biologiques humains à des fins de recherche génétique et à des fins scientifiques, le maintien d'une déclaration de toutes les collections au ministre chargé de la recherche paraît nécessaire compte tenu de la diversité des enjeux en cause. »
En effet, le Conseil d'Etat constate que l'encadrement juridique de ces collections vise non seulement un premier but, la protection des personnes concernées, ce qui revient à la CNIL, mais également à s'assurer de la pertinence scientifique du projet et du respect des règles d'hygiène et de sécurité. Pour votre rapporteur, ces deux derniers rôles ne relèvent pas de la CNIL, mais bien des deux ministres en charge de ces secteurs.
Une seconde solution avait donc davantage la faveur du Conseil d'Etat.
« Aussi, afin de préserver les exigences scientifiques de transparence et d'évaluation, l'unification des régimes définis par les articles L. 145-16-1 (devenu l'article L.1131-4) et L. 672-11 (devenu l'article L. 1243-2) du code de la santé publique devra-t-elle s'accompagner du maintien d'une déclaration préalable de toutes les collections d'échantillons biologiques humains auprès du ministre chargé de la recherche. Celui-ci, après avis du comité consultatif des traitements de données dans le domaine de la recherche en santé, conserverait le pouvoir de s'opposer dans un délai de trois mois à l'exploitation d'une collection.
« L'adoption de cet encadrement juridique à la lisibilité plus grande serait de nature à permettre un contrôle plus efficace du développement de ces collections du point de vue du droit des personnes comme celui de la recherche scientifique. »
Le régime proposé, qui reprend la deuxième option présentée par le Conseil d'Etat, laisse subsister une interrogation.
La nouvelle rédaction proposée pour l'article L. 1131-4 du code de la santé publique vise à soumettre les collections d'échantillons biologiques aux règles régissant la conservation et la transformation d'éléments du corps humain à des fins de recherche scientifique.
Ces règles définies à l'article 8 du présent projet de loi comprennent la faculté d'opposition du ministre de la recherche. Le souhait du Conseil d'Etat, rappelé ci-dessus, que subsiste une obligation générale de déclaration lors de la constitution de ces collections subsiste ainsi que la compétence du ministre de la recherche.
Si l'unification de ce régime était souhaitable, elle laisse subsister une interrogation qui était un point d'achoppement en 1996. En effet la commission mixte paritaire s'était interrogée sur la notion de « autorité administrative » qu'elle avait définie comme étant les ministres en charge de la recherche et de la santé. La nouvelle rédaction unifie le dispositif au bénéfice du ministre en charge de la recherche, le ministre de la santé n'étant désormais plus consulté.
Sous le bénéfice de ces observations, votre commission vous propose d'adopter cet article sans modification .
TITRE
II
-
DON ET UTILISATION DES ÉLÉMENTS
ET PRODUITS DU
CORPS HUMAIN
Article 5
(art. L. 1211-1, L. 1211-2 , L. 1211-4, L
1211-6, L. 1211-7, L. 1211-8, L. 1211-9 du code de la
santé publique)
Principes généraux du don et de
l'utilisation des éléments
et produits du corps humain
Objet : Cet article vise à renforcer, en précisant leur portée, les principes généraux applicables au don et à l'utilisation des éléments et produits du corps humain.
I - Le dispositif proposé
Le présent article vise à préciser les principes généraux applicables au don et à l'utilisation des éléments et parties du corps humain.
Pour cela, il modifie l'ensemble des articles L. 1211-1 à L. 1211-9 du code de la santé publique, à l'exception des articles L. 1211-3 et L. 1211-5.
Article L. 1211-1 du code de la santé publique
Le 1° du présent article remplace les deux derniers alinéas de l'article L. 1211-1 par un alinéa unique qui affirme une position de principe : toutes les activités relatives aux éléments et produits du corps humain, y compris en vue de leur importation ou exportation, doivent poursuivre une finalité médicale, scientifique ou être menées dans le cadre d'une procédure judiciaire.
Les dispositions des deux alinéas remplacés ne sont toutefois pas abrogées :
- celles du deuxième alinéa relatives à la sécurité sanitaire sont renvoyées à l'article L. 1211-6 du code de la santé publique, lui-même amendé en ce sens ;
- celles du troisième alinéa définissant la thérapie cellulaire sont reportées au titre IV du code de la santé publique.
Article L. 1211-2 du code de la santé publique
Le 2° du présent article complète l'article L. 1211-2 par deux alinéas.
Le premier dispose que, sauf opposition de la personne concernée, il sera possible de changer la finalité de l'utilisation des éléments prévue au moment du prélèvement.
Le second précise la réglementation applicable aux autopsies médicales qui ne figure pas aujourd'hui dans la loi. Ces dernières doivent avoir pour but la recherche des causes du décès. Elles sont soumises à la règle du consentement présumé. Toutefois, un danger pour la santé publique ou une nécessité impérieuse de suivi épidémiologique ainsi que l'absence d'autres procédés permettant d'établir avec certitude la cause du décès pourront justifier la conduite de telles autopsies malgré l'opposition du défunt.
Article L. 1211-4 du code de la santé publique
L'article L. 1211-4 pose le principe qu'aucun paiement ne peut être alloué à celui qui se prête au prélèvement d'éléments de son corps ou à la collecte de ses produits. Seul peut intervenir, « le cas échéant, le remboursement des frais engagés » selon les modalités arrêtées par le décret n° 2000-401 du 11 mai 2000.
Le 3° du présent article assouplit cette règle en prévoyant que « les frais (...) sont intégralement pris en charge » . Le principe de gratuité ne doit pas en effet conduire les donneurs à devoir faire l'avance de leurs frais.
Article L. 1211-6 du code de la santé publique
Le 4° du présent article modifie l'article L. 1211-6 :
- en inscrivant dans la loi le principe de non-utilisation des produits issus du corps humain si, en l'état actuel des techniques, le risque prévisible encouru par le receveur est très supérieur à l'avantage escompté pour celui-ci. Il s'agit là du principe de la « balance bénéfice-risque » prôné par le Conseil d'Etat ;
- en réécrivant dans un second alinéa le principe de soumission des prélèvements à des fins thérapeutiques -et des activités ayant les mêmes fins- à des règles de sécurité sanitaire comprenant notamment des tests de dépistages.
Ces règles sont actuellement édictées par le décret n° 97-928 du 9 octobre 1997.
Article L. 1211-7 du code de la santé publique
Le 5° du présent article modifie l'article L. 1211-7 pour inclure les produits thérapeutiques annexes dans le champ de la biovigilance. Cette activité, qui relève de l'AFSSAPS, concerne les produits énumérés à l'article L. 5311-1 du code de la santé publique.
Articles L. 1211-8 et L. 1211-9 du code de la santé publique
Les 6° et 7° du présent article procèdent à un certain nombre de coordinations aux articles L. 1211-8 et L. 1211-9.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a adopté sept amendements au présent article.
Au premier alinéa du texte proposé par le 2° pour compléter l'article L. 1211-2, elle a, sur proposition de sa commission spéciale, adopté un amendement rédactionnel prévoyant que l'opposition à l'utilisation d'un élément ou d'un produit du corps humain à une fin différente de celle prévue initialement est exercée conjointement par les deux titulaires de l'autorité parentale lorsque la personne sur laquelle est opéré le prélèvement ou la collecte est mineure. Elle a, en outre, adopté un amendement proposé par le Gouvernement prévoyant qu'il soit dérogé de droit à l'obligation d'information préalable en cas d'impossibilité de retrouver la personne concernée, ou en cas de décès de cette dernière.
Au second alinéa de ce texte, elle a adopté deux amendements :
- le premier, à l'initiative de la commission spéciale, est de nature rédactionnelle. Il remplace, pour les autopsies médicales, le terme « réalisées » par celui de « pratiquées » ;
- le second, à l'initiative du Gouvernement, réserve la possibilité d'autopsie, malgré l'opposition de la personne décédée, au cas de « nécessité impérieuse pour la santé publique » et non plus au cas de « danger pour la santé publique ou de nécessité impérieuse de suivi épidémiologique ». Cette nouvelle rédaction réalise une synthèse des deux possibilités prévues par la précédente rédaction. Le Gouvernement, par la voix de M. Bernard Kouchner, en a précisé la portée rédactionnelle en ces termes :
« L'amendement vise à clarifier les intentions du Gouvernement qui entend limiter l'exception au principe du consentement présumé requis pour la pratique des autopsies médicales en cas de danger immédiat pour la santé publique ou de nécessité impérieuse de suivi épidémiologique dans un souci de santé publique, qu'il s'agisse, par exemple, de méningite ou d'encéphalopathie spongiforme bovine. La rédaction proposée fait la synthèse de ces deux critères.
« Cette exception vise à permettre la pratique des autopsies afin de suivre, par exemple, l'épidémiologie de la maladie de Creutzfeldt-Jacob. Elle pourra aussi être utilisée exceptionnellement en face d'un syndrome émergent que l'on ne comprend pas et pour lequel ces investigations sont absolument nécessaires pour protéger le reste de la population, notamment en présence de cas groupés de décès dans un tableau clinique comparable et non rattachable à une cause connue. »
Cet amendement prévoit en outre qu'il revient au ministre de la santé de préciser, par arrêté, les pathologies et situations pouvant justifier de cette dérogation.
A l'initiative de la commission spéciale et du Gouvernement, l'Assemblée nationale a complété l'article L. 1211-3 du code de la santé publique en prévoyant que l'information en faveur du don d'éléments ou de produits du corps humain serait menée en collaboration avec le ministre chargé de l'éducation nationale (2° bis nouveau du présent article) .
A l'initiative de la commission spéciale et de M. Jean-François Mattei, l'Assemblée nationale a adopté, à l'article L. 1211-6, un amendement précisant que les prélèvements et collectes de produits du corps humain à des fins thérapeutiques seraient soumis aux règles de sécurité sanitaire en vigueur (4° du présent article) .
Elle a enfin, à l'initiative de sa commission spéciale, adopté un amendement prévoyant le principe de la reconnaissance de la Nation aux personnes ayant fait don, à des fins médicales ou scientifiques, d'éléments ou produits de leur corps (5° bis nouveau du présent article) .
III - La position de votre commission
L'encadrement juridique de l'utilisation des éléments et produits du corps humain
L'article L. 1211-1 du code de la santé publique, dans sa rédaction actuelle, prévoit que l'interdiction de céder ou d'utiliser des éléments et produits du corps humain ne s'applique qu'au prélèvement.
Le Conseil d'Etat 51 ( * ) avait estimé que « cette limitation est contestable car elle ne met pas les éléments et produits du corps humain totalement à l'abri des pratiques commerciales . Ainsi, leur importation et leur utilisation pour des buts qui ne sont ni scientifiques et médicaux ni judiciaires n'est pas interdite. Il semble donc souhaitable d'introduire un principe général d'interdiction de l'utilisation des éléments ou produits du corps humain (vivant ou mort) à des fins autres que médicales, scientifiques ou judiciaires et d'insérer ce principe au titre premier du livre VI » .
La réponse proposée par le texte répond de manière satisfaisante au souhait formulé par la Haute Juridiction.
L'amélioration de l'information du public
Dans son rapport d'information en vue de la révision de cette loi, l'Assemblée nationale relève le caractère éminemment symbolique du prélèvement et de la greffe. A ce titre, son rapporteur 52 ( * ) , M. Alain Claeys note que « évoqué comme manifestation de cohésion sociale, le don d'organes fait référence à la nécessité d'un gisement d'organes où puiser pour sauver des malades. Cette référence heurte la représentation que l'homme garde de lui-même, de son corps comme siège de l'expérience primordiale de la vie, comme totalité rebelle à une approche analytique. Or, il est désormais confronté à une médecine qui recourt de plus en plus à la science laquelle, par définition, analyse, segmente et parcellise son champ d'investigation. La prescription d'une greffe pour un malade revient, en dernier ressort, à attendre la mort d'une personne inconnue. Mort violente, puisque le prélèvement ne peut avoir lieu que sur une personne en état de mort encéphalique, laquelle n'est pas encore très connue du public et dont les fondements scientifiques, définis par quelques savants, ne sont pas partagés par l'ensemble des sociétés ».
Cette symbolique n'est pas sans éclairer le déficit en greffons que connaît notre pays. Certes, depuis la loi Caillavet, le principe du consentement présumé est consacré. Mais, depuis une simple circulaire du 3 avril 1978, la famille intervient dans le processus de prélèvement par le biais de son témoignage.
Or, la situation tragique dans laquelle intervient ce prélèvement -la disparition d'un proche, dans neuf cas sur dix, de mort violente 53 ( * ) - explique la réticence des proches à témoigner dans les limites que leur pose la législation : le sujet décédé a-t-il formulé son opposition au prélèvement d'organes ?
En conséquence, une moitié des personnes en état de mort cérébrale ne fait pas l'objet de prélèvement et dans un tiers des cas cette situation est due à une opposition, le plus souvent des proches.
Devenir des sujets en état de mort encéphalique recensés en 2000
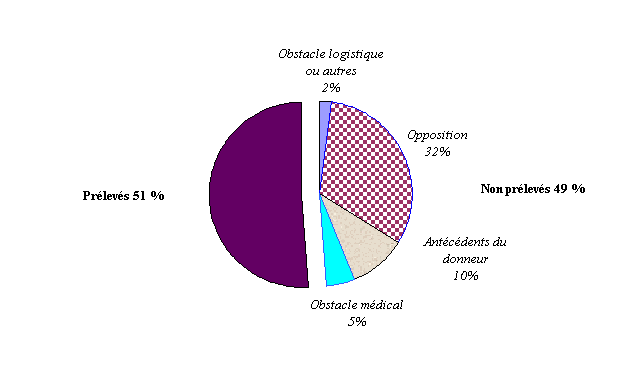 Source : Etablissement
français des greffes, Information presse du 30 janvier
2001.
Source : Etablissement
français des greffes, Information presse du 30 janvier
2001.
Alors même que le praticien serait en droit de prélever, il ne le fera généralement pas contre l'assentiment de la famille. C'est donc par une meilleure information qu'il convient de lever ces réticences.
Le présent article prévoit la nécessité de campagnes auprès des jeunes. Ces dernières pourront associer les ministères de la santé et de l'éducation nationale.
Votre commission vous propose d'aller plus loin et de prévoir, par un amendement, que tout médecin devra s'assurer auprès de ses patients âgés de 16 à 25 ans qu'ils ont bien reçu une telle information et, dans le cas contraire, la délivrer le plus rapidement possible.
Cette mesure d'information, d'ordre éthique et sanitaire, permet en outre de rendre la règle du prélèvement présumé plus équitable. Ce ne sera en effet plus dans l'ignorance de la loi que les personnes « subiront » cette règle encore parfois perçue comme illégitime.
L'introduction du principe de la balance « avantage-coût »
Plusieurs drames ont gravement affecté la crédibilité de la santé publique dans notre pays notamment, la contamination des produits sanguins par le virus du Sida et le développement de la maladie de Creutzfeldt-Jacob chez des enfants traités avec de l'hormone de croissance. Ces drames ont renforcé la nécessité de voir des règles de sécurité sanitaire stricte régir l'utilisation des produits et éléments du corps humain à des fins thérapeutiques.
La loi de 1994 posait des principes importants, notamment le dépistage et la vigilance, en renvoyant au décret leur mise en oeuvre. Ces dispositions ont été renforcées par la loi du 28 mai 1996 qui confère une sorte de pouvoir « conservatoire » au ministre de la santé à l'égard de la transformation, cession ou utilisation de ces produits.
Néanmoins, vis-à-vis de ces produits, une difficulté se posait, rappelée par MM. Claude Huriet et Alain Claeys 54 ( * ) : « S'agissant des prélèvements de tissus ou cellules post mortem, il (le législateur) n'a pas cru devoir les interdire en dépit des risques de contamination difficiles à prévenir mais a confié, là encore, au pouvoir réglementaire le soin de fixer les situations médicales où ils pourraient être autorisés ».
Le présent article va plus loin, puisqu'il propose d'écrire dans la loi que ces produits ne peuvent être utilisés à des fins thérapeutiques si, en l'état des connaissances scientifiques, leur utilisation présente pour le receveur plus de risques que d'avantages.
La paternité de ce concept de « balance avantages/risques » revient sans nul doute au Conseil d'Etat. Ce dernier avait, en effet, formulé des réserves quant à l'articulation entre le domaine de la loi et le domaine réglementaire sur cet aspect de la sécurité sanitaire. Ces dispositions devaient-elles continuer à figurer en intégralité dans la loi, ou seuls leurs aspect éthiques ? A ce stade, le Conseil ne tranchait pas mais formulait une proposition « Si le choix est fait de ne pas dissocier ces dispositions et de les maintenir dans la loi de 1994 révisée, il paraîtrait possible et souhaitable de préciser, à cette étape du texte, la notion de sécurité sanitaire en introduisant la notion de balance avantages/risques. La modification ici suggérée consiste à expliciter cette notion de sécurité sanitaire et à affirmer un principe qui doit s'imposer tant aux autorités sanitaires, dans leur rôle de régulation et de réglementation, qu'au praticien à qui il revient, dans chaque cas particulier, d'apprécier le rapport avantages/risques ».
Le Conseil définissait ce dernier précisément : « La balance avantages/risques conduit à renoncer à un prélèvement si les avantages attendus pour la personne concernée sont inférieurs aux risques encourus . Cependant, cette formulation négative consacre, en sens inverse, la nécessité de la prise de risque. La décision consiste également, en effet, à prendre un risque si celui-ci est acceptable , c'est-à-dire s'il n'est pas hors de proportion avec les bénéfices escomptés de l'intervention envisagée. Un éventuel receveur ne saurait encourir une grave perte de chance, celle de bénéficier d'un don d'organe, au nom d'un risque infime pour sa santé. La recherche de sécurité ne doit donc pas être assimilée à une exigence de risque zéro, qui n'existe pas dans la pratique, mais procéder d'une évaluation portant sur l'acceptabilité du risque » .
Ce type de raisonnement n'est pas étranger à la jurisprudence du Conseil qui, pour apprécier la légalité de certains actes administratifs, avait déjà construit une « théorie du bilan ».
Votre rapporteur n'est pas opposé à cette introduction qui est en effet utile. Elle se heurte cependant à des limites fortes que le Conseil reconnaît lui-même. Il est en effet nécessaire que « soient estimées la potentielle gravité du risque et sa probabilité de se réaliser au regard du nombre et de la nature des bénéfices thérapeutiques attendus de l'opération envisagée ».
Ce sont donc les autorités sanitaires qui sont confrontées à la nécessité d'évaluer un risque pour le patient, et de lui proposer de le prendre au regard des bénéfices escomptés de l'opération.
Il est nécessaire de s'interroger en conséquence sur le régime de responsabilité des praticiens étant conduits à évaluer ce risque. En cas de réalisation de ce dernier, la personne qui aura consenti au traitement ne devrait pouvoir, si l'autorité sanitaire n'a pas commis de faute manifeste dans l'évaluation de ce risque, se retourner contre cette dernière. En conséquence, c'est le régime de responsabilité prévu au titre III de la loi du 4 mars 2002 relatif aux droits des malades qui devrait s'appliquer avec, le cas échéant, indemnisation du patient par l'Office national d'indemnisation des accidents médicaux, des affections iatrogènes et des infections nosocomiales (ONIAM), qui trouve ici toute sa justification.
La reconnaissance de la Nation aux donneurs
Cette possibilité, introduite par l'Assemblée nationale, est controversée. Pour le rapporteur de la mission d'information de l'Assemblée nationale, M. Alain Claeys, il est évident 55 ( * ) que « cette reconnaissance (...) devrait s'exprimer en faveur des donneurs seuls car exprimer de la reconnaissance aux familles « de ceux qui donnent » mettrait à bas tout l'édifice du consentement présumé reposant sur l'intégrité du donneur et le respect de son libre arbitre. Même si la réalité des faits tend à le laisser croire, ce ne sont pas les familles qui donnent, elles ne sont que porteuses, selon la loi, de la parole du défunt » .
Il s'agit donc de réserver cette reconnaissance aux donneurs vivants des éléments et produits du corps humain.
Cette proposition présente deux difficultés : l'une pratique et l'autre éthique.
La difficulté pratique a été formulée devant votre commission par M. Claude Huriet. Tout en agréant cette proposition, celui-ci s'interrogeait sur les modalités d'expression de ce don 56 ( * ) . « Il reste à voir comment s'exprimera cette reconnaissance de la Nation pour ceux qui font don généreusement d'une partie de leur corps, de leurs tissus ou de leur sang ».
La difficulté éthique a été précisée 57 ( * ) par M. Didier Sicard, président du Comité national consultatif d'étique, qui, devant votre commission, a estimé que « la notion de reconnaissance de la Nation à celui qui donnerait son corps ne me paraît pas forcément à encourager. En effet, il s'agit ici du domaine du privé et de l'intime et de donner un gage de reconnaissance de la Nation ne me paraît pas nécessaire. Enfin, ce point de vue est marginal. Aucun autre pays ne me semble avoir inscrit une telle disposition et cette spécificité française peut, paradoxalement, sembler ambiguë ».
M. Didier Sicard réitérait ainsi le scepticisme formulé par le Comité d'éthique, qu'il préside, dans son avis sur l'avant-projet de révision des lois de bioéthique.
|
Article L. 1211-8 « La reconnaissance de la Nation est acquise aux personnes qui font don à des fins thérapeutiques ou scientifiques d'éléments ou produits de leur corps. » Supprimer
Cette disposition relève d'une
rhétorique dépassée et mal accordée avec
l'éthique individuelle du don. Le CCNE rappelle que la valorisation
excessive du don a, dans un passé récent, été
désignée comme l'une des causes du dysfonctionnement du
dispositif français de don du sang. Au surplus, si cette disposition
devait se traduire par des manifestations concrètes de reconnaissance
(diplôme, décoration, médaille...),
elle serait contraire au principe fondamental qui inspire la loi, et
qui est celui de l'anonymat du don
.
|
Votre commission demeure sceptique sur la proposition formulée par l'Assemblée nationale et s'interroge sur sa mise en oeuvre pratique.
En l'état, tout en comprenant les motivations de cette initiative de l'Assemblée nationale, elle observe que « la reconnaissance de la Nation » est un acte d'une forte portée symbolique que l'on ne peut décerner de manière indifférenciée. Donner un élément du corps humain, un tissu ou du sang, est un geste noble mais qui peut difficilement être comparé avec le don de sa vie par un sapeur-pompier ou un militaire tué dans l'exercice de son devoir. Aussi vous propose-t-elle, par amendement, de supprimer cet ajout de l'Assemblée nationale.
Votre commission vous propose d'adopter cet article ainsi amendé.
Article 6
(art. L. 1221-5, L. 1221-8, L. 1221-12 du code de
la santé publique)
Collecte, préparation et conservation du
sang, de ses composants
et des produits sanguins labiles
Objet : Cet article vise à clarifier les dispositions législatives en matière de recherche scientifique sur le sang.
I - Le dispositif proposé
Le I du présent article assouplit les conditions de prélèvement de sang sur les mineurs. Les deux conditions complémentaires actuellement prévues par l'article L. 1221-5 du code de la santé publique -urgence thérapeutique et compatibilité cellulaire- deviennent alternatives.
Les b) et c) du II complètent la liste des produits pouvant être préparés à base de sang pour l'actualiser au regard, tant des dispositions de la loi du 1 er juillet 1998 relative au renforcement de la veille sanitaire que de la simplification du régime juridique encadrant les cellules. Cette liste est donc complétée par :
- les pâtes plasmatiques,
- les produits thérapeutiques annexes,
- les « produits cellulaires à finalité thérapeutique » . Cette terminologie se substitue, par ailleurs, aux anciennes appellations « préparations cellulaires » et « produits de thérapie cellulaire » .
Cette clarification doit beaucoup aux considérations du Conseil d'Etat qui, dans son rapport, critiquait la complexité excessive de la dualité du régime des cellules.
|
Les cellules peuvent être d'origine sanguine ou provenir d'une autre origine. En l'état actuel des textes, les cellules issues du sang sont soumises à des règles distinctes selon qu'elles sont utilisées pour obtenir des produits sanguins labiles, qu'elles ne sont pas destinées à des produits de thérapie cellulaire. Toutes les autres cellules, hors la moelle osseuse, obéissent à des règles différentes selon qu'elles sont destinées à entrer dans la composition de produits de thérapie cellulaire ou qu'elles ne sont pas destinées à des thérapies cellulaires. Cette distinction entre les cellules qui sont destinées à des thérapies cellulaire et celles qui ne le sont pas a été rajoutée par la loi portant DMOS du 28 mai 1996. Cet ajout complexifie le dispositif, comme en témoigne la rédaction de l'article L. 672-9 qui dispose que : « les conditions techniques, sanitaires et médicales et les conditions propres à garantir un fonctionnement conforme aux principes généraux énoncés au titre I du présent livre, que doivent remplir les établissements de santé pouvoir être autorisés à effectuer des prélèvements de tissus ou de cellules qui ne sont pas destinés à des thérapies géniques ou cellulaires sont déterminées par décret en Conseil d'Etat ». Or cette différenciation paraît peu pertinente tant il s'avère difficile de la fonder sur des critères objectifs et de cerner la catégorie des produits cellulaires qui ne seraient pas des produits de thérapie cellulaire et ceux qui en seraient. Il semble donc préférable, dans un souci de cohérence, de simplifier le statut trop obscur des cellules et de prévoir des règles communes applicables à ces dernières. L'intérêt de cette simplification est de rendre la loi plus claire et plus conforme aux évolutions techniques. Les décrets d'application concernant l'AFSSAPS anticipent d'ailleurs cette évolution. C'est, en effet, l'agence qui va gérer l'ensemble des autorisations concernant les produits et les établissements où ils sont préparés et qui va, de facto , soumettre les cellules à des règles communes. Il conviendra donc, sur le plan rédactionnel, de supprimer cette distinction dans les articles où elle apparaît et de considérer que si les cellules sanguines peuvent être distinguées suivant leur utilisation (produits sanguins labiles ou produits de thérapie cellulaire), les autres cellules doivent être considérées comme destinées à des thérapies cellulaires. Cette unité de finalité permettra d'unifier les régimes d'autorisation de prélèvement. Il conviendra ainsi à l'article L. 672-9 de prévoir que « les cellules utilisées à des fins thérapeutiques, à l'exception des produits sanguins labiles, sont des produits de thérapie cellulaire soumis aux dispositions du titre IV du présent livre ». Il faudrait également tirer les conséquences rédactionnelles du choix de ranger la moelle osseuse dans la catégorie des cellules. Dans les dispositions communes, l'insertion d'un nouvel article précisant que les dispositions du présent chapitre s'appliquent à la moelle osseuse s'impose. Il serait également opportun de privilégier, pour l'ensemble des raisons qui ont invité à ranger la moelle dans les cellules, l'expression « utilisation de cellules souches hématopoïétiques d'origine médullaire » à celle de « greffe de moelle osseuse » . Etude du précité Conseil d'Etat, p. 80-81 |
Le d) du II précise les règles relatives au prélèvement sur mineur et, par extension, au majeur protégé en supprimant à la dernière phrase de l'article L. 1221-8 du code de la santé publique le renvoie aux principes fixés à l'article L. 1221-5. Ce dernier interdit tout prélèvement de sang sur mineur ou majeur protégé avec l'exception, pour les mineurs, de la double condition susmentionnée (urgence thérapeutique et compatibilité cellulaire).
Le prélèvement de sang à visée de recherche sur mineur ou majeur protégé sera soumis aux dispositions de l'article L. 1211-2 du code de la santé publique relatif à la réalisation d'une recherche biomédicale : le consentement est donné, selon le cas, par le titulaire de l'autorité parentale ou le tuteur, le consentement du mineur ou majeur protégé doit être en outre recherché s'il est apte à le formuler. Son refus ne peut être surmonté, à la différence du prélèvement de moelle osseuse prévu au dernier alinéa de l'article L. 1241-3 (cf. article 8) .
Le a) du II prévoit un nouveau référencement du fait du décalage suscité par l'insertion d'un nouvel alinéa.
Le a) du III soumet à l'autorisation de l'AFSSAPS l'importation de produits sanguins à seul usage thérapeutique direct ou destiné à la fabrication de produits de santé.
Le b) prévoit, pour sa part, la soumission de ces mêmes produits destinés à des fins scientifiques à l'autorisation du ministre de la recherche figurant à l'article L. 1245-5 du code de la santé publique tel que modifié par l'article 8.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a adopté deux amendements :
- le premier, de nature rédactionnelle, complète le travail de renumérotation entamé par le texte initial pour l'énumération des produits dérivés du sang ;
- le second prévoit d'associer le ministre en charge de la santé à la décision d'importation ou d'exportation de sang à des fins scientifiques.
III - La position de votre commission
Votre commission vous propose un amendement élaboré en accord avec le ministre chargé de la santé, qui vise à rétablir la seule compétence du ministre de la recherche pour les autorisations d'importations ou d'exportations de sang à des fins de recherche scientifique.
Dans ce cas précis, en effet, l'autorisation du ministre chargé de la santé n'apparaît pas nécessaire et alourdirait inutilement la procédure.
|
Examinant la proposition de loi portant création d'une Agence française de sécurité sanitaire environnementale [rapport n° 476 (1999-2000)], M. Claude Huriet, rapporteur pour votre commission, s'était élevé contre la dénumérotation dans les codes législatifs des articles ou paragraphes d'articles. Cette démarche retenue par le présent article 6 du projet de loi consiste, lorsque l'on souhaite introduire un paragraphe additionnel après un paragraphe 1°, non pas d'insérer un paragraphe « 1° bis », mais à dénuméroter les 2°, 3°, 4° et 5° (etc.) qui deviennent des 3°, 4°, 5° et 6° (etc.) pour faire place audit paragraphe additionnel baptisé dès lors « 2° ». S'élevant contre cette technique qui s'applique tout aussi bien aux articles du code eux-mêmes (cf. articles 7 (B, IV, 3°), 10 (I, 3°), 18 (I, 2°) etc. du présent projet de loi), M. Claude Huriet avait souligné qu'elle était « contraire à toute lisibilité de la loi » puisque l'usager du code est amené en permanence à s'interroger, à l'occasion notamment de référence dans les autres textes de loi, sur le contenu effectif des paragraphes et articles ainsi dénumérotés et renumérotés. Cette vision de la codification lui avait semblé relever « d'une sorte de syndrome du pont de la rivière Kwaï : la perfection formelle de l'ouvrage l'emporte sur l'usage qui en est fait ». Votre rapporteur constate que ce syndrome demeure. Il le regrette. Il souhaite vivement que les projets de loi du Gouvernement en soient désormais préservés. Il renonce toutefois à bouleverser le présent projet de loi à ce stade de la navette par un nombre considérable d'amendements de pure codification. |
Votre commission vous propose d'adopter cet article ainsi amendé.
Article 7
Prélèvements d'organes
Objet : Cet article propose une réforme substantielle des dispositions relatives aux prélèvements et au don d'organes tant post mortem qu'entre vifs.
I - Le dispositif proposé
Le présent article propose une série de modifications pour le titre III du livre premier de la première partie du code de la santé publique, relatif aux organes humains.
Le I de cet article modifie le chapitre premier de ce titre, qui rassemble les dispositions relatives au « prélèvement sur une personne vivante » .
Le 1° du I propose trois modifications essentielles au régime du don d'organes entre vifs prévu par l'article L. 1231-1 du code de la santé publique :
- le cercle des donneurs potentiels est élargi. Si le texte proposé pour cet article prévoit toujours que la règle est le don dans le cadre familial (premier alinéa) , ce dernier est élargi « par dérogation » à toute personne ayant un « lien étroit et stable » avec le receveur (deuxième alinéa) ;
- les conjoints regagnent le cercle des donneurs familiaux (père, mère, fils, fille, frères et soeurs) sans qu'il soit exigé une urgence pour recourir à eux ;
- il n'est plus fait mention du don de moelle osseuse qui n'est plus considérée comme un organe et dont le régime est désormais fixé par les articles L. 1241-1, L. 1241-3 et L. 1241-4 (cf. commentaire ci-après de l'article 8) ;
- le régime d'expression du consentement est conservé dans ses grandes lignes avec néanmoins plusieurs aménagements. Celui-ci est toujours exprimé devant un magistrat, le Président du tribunal de grande instance ou tout autre magistrat désigné par lui, ou en cas d'urgence devant le procureur de la République (troisième alinéa) . En revanche, il est prévu l'autorisation d'un comité d'experts pour les donneurs non issus du cercle familial, et même pour ceux issus de ce cercle lorsque le magistrat chargé de recueillir le consentement l'estime nécessaire (quatrième et cinquième alinéas) .
Le présent article maintient en outre l'obligation préalable d'information du donneur sur les risques et les conséquences possibles de son don (troisième alinéa) . Il est également prévu que l'Etablissement français des greffes (EFG) est préalablement informé de tout prélèvement d'organe à des fins thérapeutiques (dernier alinéa) .
Les autres modifications prévues pour les articles de ce chapitre sont de conséquence.
Le 2° propose une nouvelle rédaction pour l'article L. 1231-3 du code de la santé publique , les dispositions prévues par la rédaction précédente étant devenues sans objet. En effet, celles-ci définissaient les règles relatives au prélèvement de moelle osseuse sur mineur. Cette dernière n'étant plus considérée comme un organe, les dispositions relatives à son prélèvement sont transférées par le présent projet de loi à l'article L. 1241-3 du même code.
Ces dispositions sont remplacées par celles régissant la composition et le fonctionnement des comités d'experts prévus à l'article précédent et aux articles L. 1241-3 et L. 1241-4 du code de la santé publique. Il est ainsi prévu que ces comités :
- siègent en deux formations de cinq membres, dont trois sont communs aux deux formations (deux médecins et un spécialiste dans le domaine des sciences humaines et sociales) , ; lorsque le comité se prononce sur les prélèvements sur personne majeure , il comporte un troisième médecin et un psychologue ; lorsqu'il se prononce sur les prélèvements sur personne mineure , il comporte un pédiatre et « une personne qualifiée dans le domaine de la psychologie de l'enfant » ; le comité se « prononce » stricto sensu :
. sur les prélèvements d'organes sur personne majeure n'appartenant pas au cercle familial ou sur les personnes majeures appartenant à ce cercle dès lors que le magistrat chargé de recueillir le consentement l'estime nécessaire (article L. 1231-1) ;
. sur les prélèvements de moelle osseuse sur personne mineure ou sur personne majeure faisant l'objet d'une mesure de curatelle ou de sauvegarde de justice dès lors qu'elle a la faculté d'exprimer son consentement (articles L. 1241-3 et L. 1241-4) ;
. et, pour avis , sur les prélèvements de moelle osseuse autorisés par le juge des tutelles (article L. 1241-4) ;
- se prononcent dans le respect des principes énoncés au titre premier, qui sont les principes généraux prévus pour le don d'organes par le code de la santé publique et le code civil : gratuité, consentement éclairé, vigilance sanitaire et, le cas échéant, anonymat (deuxième alinéa) ;
- ont accès aux informations médicales concernant le donneur et le receveur, et sont soumis à l'obligation de secret médical qu'un tel accès impose (troisième alinéa) ;
- ne motivent pas leurs décisions de refus (quatrième alinéa) .
Le 3° modifie la rédaction de l'article L. 1231-4 du code de la santé publique , devenu lui aussi sans objet. Cet article prévoyait les dispositions régissant les comités d'experts chargés d'autoriser le prélèvement de moelle sur mineurs. Ces comités sont à présent prévus à l'article L. 1231-3 (cf. ci-dessus) . Le présent article prévoit dans sa nouvelle rédaction que les modalités d'application de ces articles sont prises par décret en Conseil d'Etat.
Le 4° abroge l'ancien article L. 1231-5 du code de la santé publique qui prévoyait ce même renvoi au pouvoir réglementaire.
Le II modifie le chapitre II qui contient les dispositions relatives « au prélèvement sur les personnes décédées » .
Le 1° modifie les articles L. 1232-1 à L. 1232-3 du code de la santé publique .
La rédaction proposée pour l'article L. 1232-1 prévoit cinq modifications principales :
- une précision sur le régime juridique de la mort autorisant le prélèvement. La rédaction initiale, disposant que le prélèvement est effectué « après que le constat de la mort a été établi » est remplacée par celle disposant que « la mort a été dûment constatée » . Ce constat renvoie aux trois critères cliniques du constat de la mort prévus par le décret n° 96-1041 : absence totale de conscience et d'activité motrice cérébrale, abolition de tous réflexes du tronc cérébral et absence totale de ventilation spontanée (premier alinéa) ;
- la confirmation du principe de consentement présumé au prélèvement qui ne peut avoir lieu qu'à des fins thérapeutiques ou scientifiques. Ce consentement peut être « exprimé par tout moyen » , dont l'inscription sur le registre national des greffes (fusion des deuxième et troisième alinéas anciens dans un deuxième alinéa) ;
- l'élargissement du cercle des « témoins » potentiels. La volonté du défunt n'étant plus recherchée auprès de la seule « famille » mais « des proches » (troisième alinéa) ;
- l'amélioration de l'information des proches à la fois sur l'objet du prélèvement (troisième alinéa) et la nature des prélèvements effectués (quatrième alinéa) ;
- l'information préalable de l'EFG lors de tout prélèvement (dernier alinéa) .
La rédaction proposée pour l'article L. 1232-2 conserve les grandes lignes des règles régissant le prélèvement sur mineur en introduisant néanmoins :
- une précision : en remplaçant, pour les majeurs protégés décédés, le consentement du « représentant légal » par celui du « tuteur » , et ce pour permettre aux majeurs faisant l'objet d'une protection légale qui n'est pas la tutelle (sauvegarde de justice ou curatelle) d'exprimer par eux-mêmes leur volonté lorsqu'ils en sont aptes (premier alinéa) ;
- une harmonisation : en mettant fin à la différence d'expression du consentement des titulaires de l'autorité parentale selon la finalité du prélèvement. Les dispositions en vigueur du code de la santé publique prévoient en effet que, pour le prélèvement thérapeutique, le double consentement soit nécessaire alors que le consentement d'un seul titulaire de l'autorité parentale suffit à autoriser le prélèvement à des fins scientifiques. Le texte proposé par cet article prévoit une harmonisation du régime de consentement quelles que soient les finalités du prélèvement (premier alinéa) ;
- une innovation : en permettant que le consentement exprès et formulé par écrit d'un seul des titulaires de l'autorité parentale permette le prélèvement, lorsque le second n'a pu être consulté (second alinéa) ;
La rédaction proposée pour l'article L. 1232-3 remplace les dispositions existantes relatives au prélèvement à finalité scientifique sur les mineurs, reprises dans l'article précédent, par l'obligation d'établir un protocole de recherche transmis préalablement à l'EFG pour tout prélèvement à des fins scientifiques. En cas de non-pertinence de la recherche ou de l'inutilité du prélèvement, le ministre chargé de la recherche peut suspendre ou interdire leur mise en oeuvre.
Le 2° modifie l'article L. 1232-4 du code de la santé publique pour substituer au premier alinéa le terme « greffe » à celui de « transplantation » ( a ) et, par coordination, supprimer l'obligation d'information de l'EFG prévue par cet article dans la rédaction proposée pour l'article L. 1232-1 du même code ( b ).
Le 3° modifie l'article L. 1232-5 du code de la santé publique pour étendre l'obligation de « restauration décente du corps » au cas où celui-ci a subi une autopsie médicale, le droit en vigueur limitant cette obligation aux activités de prélèvement.
Le 4° modifie les 1° et 2° de l'article L. 1232-6 du code de la santé publique, qui prévoit le renvoi à un décret en Conseil d'Etat de la rédaction des modalités de prélèvement sur les personnes décédées :
- le ( a ) modifie le premier alinéa pour y inscrire que les conditions dans lesquelles est établi le constat de la mort sont prévues au L. 1232-1 ;
- le ( b ) complète cet article par un troisième alinéa qui prévoit que seront fixées par décret en Conseil d'Etat les modalités d'interdiction de suspension par le ministre de la recherche des protocoles relatifs au prélèvement à des fins scientifiques ainsi que la transmission par l'EFG des informations dont il dispose sur ces protocoles.
Le III modifie le chapitre III où figurent les dispositions relatives au régime juridique des établissements autorisés à prélever des organes.
Le 1° introduit dans l'article L. 1233-1 du code de la santé publique qui traite de ces établissements deux précisions :
- les dispositions de cet article visent les prélèvements d'organes « en vue de don à des fins thérapeutiques » , formulation reprise de l'article R. 671-9 du code de la santé publique ;
- l'EFG formule un avis sur l'autorisation délivrée par l'autorité administrative.
La rédaction proposée par le 1° déclasse certaines dispositions relatives à l'autorisation qui figuraient précédemment dans un second alinéa de cet article, et notamment, que cette autorisation est délivrée pour cinq ans et est renouvelable. En effet, ces dispositions figurent dans l'article R. 671-9 précité. Elles ne seront donc plus de nature législative.
Par coordination , le 2° prévoit la même précision - « prélèvements d'organes en vue de don » - dans l'article L. 1233-2 du code de la santé publique qui prévoit le principe de non-rémunération des prélèvements.
Le 3° prévoit une modification rédactionnelle en complétant l'article L. 1233-3 du code de la santé publique , pour ajouter « à des fins de greffe » à la notion de « prélèvements d'organes » qui y figure.
Le IV prévoit deux séries de modifications au chapitre IV de ce titre:
- rédactionnelles, en remplaçant dans l'intitulé du chapitre ainsi qu'aux articles L. 1234-2 et L. 1234-3 les mots « transplantations » par « greffes d'organes » et « greffe » ( 1° et 3° ) ;
- de coordination en mettant à jour les références du code ( 2° ).
Le V propose pour le chapitre V relatif aux dispositions communes trois séries de mesures :
- le « nettoyage » des dispositions relatives aux produits du corps humain qui ne sont pas des organes et qui n'ont plus vocation à figurer dans les dispositions relatives à ces derniers. Ainsi le 1° prévoit la suppression dans l'article L. 1235-1 de la référence aux produits issus du sang humain (article L. 1221-12) et le 2° prévoit la suppression de la référence à la moelle osseuse qui y figure ;
- la précision du régime du consentement applicable aux organes prélevés à l'occasion d'une intervention médicale pratiquée dans l'intérêt de la personne opérée. L'autorisation d'utilisation est présumée, la personne conservant une faculté d'opposition. Elle doit avoir bénéficié d'une information sur l'objet de cette utilisation. Pour les personnes mineures ou majeures sous tutelle, l'opposition est exprimée par les titulaires de l'autorité parentale ou le tuteur ;
- l'introduction de deux dispositions nouvelles prévoyant pour l'article L. 1235-3 une nouvelle rédaction et créant un article L. 1235-4 nouveau.
Le premier de ces articles dispose que tout prélèvement d'organes réalisé conformément aux dispositions prévues par le chapitre III est une activité médicale. Cette reconnaissance est « destinée à valoriser cette activité » qui pourra ainsi figurer dans le cursus des études de médecine et être répertoriée au PMSI.
Le second prévoit que les prélèvements effectués dans le cadre des recherches biomédicales sont regardés comme des prélèvements thérapeutiques et bénéficient en conséquence des garanties de sécurité sanitaire afférentes prévues par les dispositions figurant aux articles L. 1211-6 et L. 1211-7 du code de la santé publique.
Le 3°, en numérotant l'article L. 1235-3 en L. 1235-5 nouveau transfère dans ce dernier les dispositions figurant dans le premier. Le principe d'une application des dispositions du présent chapitre par le biais d'un décret en Conseil d'Etat est donc conservé.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a modifié cet article à neuf reprises, en adoptant sept amendements à l'initiative de sa commission spéciale et deux à l'initiative de MM. Jean-François Mattei et plusieurs de ses collègues.
A l'initiative de ces derniers, elle a adopté :
- avec l'avis favorable de la commission spéciale et du Gouvernement, un amendement visant à introduire en tête de cet article, une modification de l'article 16-3 du code civil précisant qu'il peut être porté atteinte à l'intégrité du corps humain, à titre exceptionnel, dans l'intérêt thérapeutique d'autrui et ce afin d'y traduire le principe du don d'organes entre vifs ;
- contre l'avis de la commission spéciale, le Gouvernement s'en remettant à la sagesse de l'Assemblée nationale, un amendement prévoyant au troisième alinéa de l'article L. 1231-1 que l'information préalable du donneur d'organe est assurée par le comité d'experts prévu au L. 1231-3 ;
- il est en outre notable que, contre l'avis de la commission spéciale et du Gouvernement, elle a adopté dans un premier temps un amendement prévoyant au troisième alinéa de l'article proposé pour le L. 1231-1 du code de la santé publique le consentement du conjoint au don lorsque le donneur est marié, ou de l'autre parent, lorsque celui-ci a charge d'enfant ; cette modification a ensuite été supprimée lors d'une seconde délibération.
A l'initiative de sa commission spéciale et avec l'avis favorable du Gouvernement, l'Assemblée nationale a adopté :
- un amendement complétant l'article L. 1231-1 par un alinéa prévoyant un rapport quadriennal d'évaluation de la pratique des prélèvements ;
- un amendement prévoyant au premier alinéa de l'article L. 1231-3 que les membres des comités d'experts sont nommés pour trois ans par le ministre de la santé ;
- un amendement prévoyant au dernier alinéa de l'article L. 1231-3 que l'ensemble des décisions des comités d'experts ne seront pas motivées et non les seules décisions de refus ;
- un amendement de précision au troisième alinéa de l'article L. 1232-3 qui remplace le terme « objet » par celui de « finalité » ;
- avec l'avis favorable du Gouvernement, un amendement rétablissant le second alinéa de l'article L. 1233-3 du code de la santé publique, qui prévoit d'inscrire dans la loi la durée et le caractère renouvelable de l'autorisation délivrée aux établissements de santé pour le prélèvement d'organes ;
- un amendement prévoyant au dernier alinéa de l'article L. 1235-3 que l'autorisation d'exporter et d'importer des organes à des fins scientifiques est délivrée après consultation de l'EFG ;
- un amendement introduisant au deuxième alinéa de l'article L. 1235-2 le principe de l'absence d'opposition du mineur ou du majeur sous tutelle pour l'utilisation des organes prélevés sur ces derniers au cours d'une intervention médicale pratiquée dans leur intérêt.
III - La position de votre commission
La pénurie des greffons
Les besoins d'organes sont précisément recensés par l'EFG. Son rapport d'activités pour 2001 rappelle qu'au 31 décembre 2000, 6.033 patients restaient en attente de greffe d'organes.
Ce nombre s'accroît d'ailleurs au cours de l'année, les patients s'inscrivant en liste d'attente : 4.326 inscriptions pour l'année 2001.
Patients restant inscrits en attente de greffe d'organes
|
1997 |
1998 |
1999 |
2000 |
2001 |
|
|
Coeur |
247 |
270 |
339 |
337 |
345 |
|
Coeur-poumons |
69 |
69 |
66 |
59 |
70 |
|
Poumons |
113 |
108 |
115 |
115 |
128 |
|
Foie |
238 |
261 |
346 |
404 |
457 |
|
Reins |
4.428 |
4.504 |
4.852 |
4.903 |
5.124 |
|
Pancréas |
119 |
132 |
176 |
197 |
195 |
|
Intestin |
10 |
9 |
13 |
18 |
13 |
|
Total |
5.224 |
5.353 |
5.907 |
6.033 |
6.332 |
Source EFG 2002
Evolution de l'activité de greffe d'organes
|
1997 |
1998 |
1999 |
2000 |
2001 |
|
|
Coeur |
366 |
370 |
321 |
328 |
316 |
|
Coeur-poumons |
25 |
26 |
28 |
25 |
26 |
|
Poumons |
65 |
88 |
71 |
70 |
91 |
|
Foie |
621 |
693 |
699 |
806 |
803 |
|
Reins |
1.690 |
1.882 |
1.842 |
1.924 |
2.022 |
|
Pancréas total |
63 |
47 |
48 |
54 |
60 |
|
Intestin |
10 |
9 |
7 |
4 |
7 |
|
Total |
2.840 |
3.115 |
3.016 |
3.211 |
3.325 |
Source EFG 2002
Cette situation implique nécessairement que les pouvoirs publics améliorent les mécanismes de prélèvement.
Pour autant doit-on considérer les deux sources de greffons, prélèvements post mortem et donneurs vivants, comme susceptibles d'être sollicitées avec la même insistance ?
Votre rapporteur ne le pense pas.
Les limites et les risques du recours aux donneurs vivants
Votre rapporteur a déjà détaillé, dans son exposé général, ainsi qu'à l'article 5, les difficultés rencontrées aujourd'hui par la pratique du prélèvement post mortem . Près de 50 % des décès pouvant donner lieu à prélèvement n'y donnent pas lieu, malgré la règle du consentement présumé.
|
- Lorsque l'intéressé a fait connaître son refus de son vivant : un rôle essentiel mais non exclusif est dévolu à cet effet au registre national automatisé . Il remplace le registre spécial dont la loi Caillavet avait prévu le dépôt dans chaque établissement hospitalier concerné et qui n'était que très rarement utilisé. A défaut d'une volonté exprimée par l'inscription sur ce registre (ou par tout autre moyen), le médecin « doit s'efforcer de recueillir le témoignage de la famille » ; - lorsque le prélèvement en vue d'une greffe s'applique à une personne décédée qui était mineure ou majeure incapable : le consentement écrit et exprès de chacun des titulaires de l'autorité parentale ou du représentant légal est alors nécessaire ; - lorsque le prélèvement a lieu à des fins exclusivement scientifiques : la loi distingue ici les autopsies cliniques (en vue de rechercher les causes de la mort) dont la famille est simplement informée, et les autopsies scientifiques pour lesquelles le consentement doit avoir été exprimé, soit directement par le défunt, soit par le témoignage de la famille qui peut donc jouer ici un rôle plus déterminant que pour les prélèvements à des fins thérapeutiques. On verra plus loin les critiques adressées par les anatomopathologistes à cette distinction qu'ils jugent artificielle et préjudiciable à la pratique des autopsies. Rapport de l'OPECST, p. 59 |
L'autre source potentielle de greffons est constituée des dons en provenance de personnes vivantes, dons que la législation en vigueur réglemente strictement : seuls peuvent donner un organe les personnes majeures, au bénéfice de leurs père, mère, frère, soeur, fils et fille.
Certes la pratique du don entre vifs est répandue, notamment dans les pays du Nord de l'Europe, pour les dons de reins.
Nombre de prélèvements rénaux par million d'habitants
|
Donneurs vivants |
Donneurs cadavériques |
|
|
Norvège |
16 |
26 |
|
Suède |
14 |
24 |
|
Danemark |
9 |
22 |
|
Suisse |
8 |
26 |
|
Pays-Bas |
6 |
27 |
|
Allemagne |
4 |
23 |
|
Grande-Bretagne |
3 |
26 |
|
France |
1 |
27 |
Source EFG 2002
Toutefois, les complications parfois mortelles, que peut entraîner le don entre vif, doivent conduire à y recourir avec modération.
La transplantation rénale est une pratique maîtrisée, qui donne de bons résultats.
Les autres types de transplantations : hépatique, pulmonaire ou en domino, doivent être envisagées avec la plus grande prudence. Le rapport de l'OPECST rappelle 58 ( * ) que, pour les donneurs de foie, la mortalité atteint 0,2 % et la morbidité 12 %.
Pour votre commission, il est nécessaire de mieux encadrer ce type de prélèvement. Le présent article propose un élargissement du cercle des donneurs. Outre la levée du caractère « d'urgence » qui subordonnait le prélèvement au profit du conjoint, le présent article propose d'élargir « par dérogation » la liste des donneurs au cercle affectif, c'est-à-dire à toute « personne pouvant justifier de liens étroits et stables » avec le receveur.
Votre commission ne s'oppose pas à l'idée qu'un deuxième cercle de donneurs vivants puisse être proposé, mais estime que celui-ci doit être défini précisément.
En effet, la pratique du don entre vifs peut donner lieu à deux dérives que ne saurait connaître le don post mortem , le chantage psychologique et la négociation commerciale.
Certes le présent projet de loi prévoit (cf. tableau ci-après) , que le consentement est formulé devant un magistrat et l'autorisation délivrée par un comité d'experts.
|
Les comités d'experts ont été créés par la loi du 29 juillet 1994 et sont chargés d'autoriser les prélèvements de moelle osseuse sur les personnes mineures. Le décret n° 96-375 du 29 avril 1996 les a mis en place. Au nombre de sept, les comités d'experts sont répartis en centres interrégionaux. Ils sont composés de trois membres titulaires et trois membres suppléants. Ils sont bénévoles et désignés pour trois ans par le ministre de la santé. Ils comportent un médecin non-pédiatre désigné sur proposition du directeur général de l'EFG, et choisi au sein du personnel de cet établissement, un pédiatre et une personnalité non médicale choisie en fonction de sa compétence et de son expérience dans le domaine de la psychologie de l'enfant.
Le présent projet de loi renforce les missions des
comités d'experts du fait de l'extension du cercle du don entre vifs, et
l'introduction de la faculté de don de moelle par les majeurs
protégés. Ils comporteront désormais cinq membres et
seront appelés à siéger sous deux formations
différentes selon qu'ils autorisent un prélèvement sur une
personne mineure ou majeure.
|
Toutefois, ces deux réserves ne permettent pas de lever tous les risques. Ainsi votre commission vous propose, par amendement, de définir précisément le cercle élargi des donneurs qui comprendrait outre le premier cercle familial, les grands-parents, les oncles et tantes, les cousins germains , ainsi que les conjoints des parents du receveur . Elle vous propose, en sus, d'autoriser le prélèvement sur la personne susceptible d'apporter la preuve d'une vie commune d'au moins deux ans avec le receveur.
Votre commission vous propose, en conséquence, de préciser, par amendement, que le rapport quadriennal d'évaluation remis au Parlement par le Gouvernement et consacré à « l'élargissement du cercle du donneur à toute personne ayant des liens étroits et stables avec le receveur » , soit, par cohérence, puisqu'elle vous propose de ne pas conserver cette notion, étendu à l'ensemble de la question du don d'organes entre vifs.
Elle vous propose en outre trois amendements de précision rédactionnelle à l'article L. 1231-1 :
- le premier précise la mission du magistrat chargé de recueillir le consentement de la personne qui fait un don d'organe ; le texte dispose en effet que le magistrat s'assure que « (le consentement)... est donné dans les conditions prévues, selon le cas, par le premier ou le deuxième alinéa » de cet article ; or, ces alinéas ne prévoient pas de conditions dans lesquelles le consentement pourrait être donné, mais la finalité thérapeutique du prélèvement et la qualité du donneur (lien avec le receveur). Aussi, votre commission vous propose-t-elle de prévoir que le magistrat « s'assure que le don est conforme aux conditions prévues » par ces alinéas. Il appartiendra au magistrat de s'assurer de l'identité de la personne consentante et de la nature de ses liens avec le receveur -notamment les preuves d'une vie commune de deux ans- ainsi que, le cas échéant, la finalité du prélèvement. Il reste qu'il n'appartient pas au juge d'autoriser le prélèvement mais simplement de recueillir le consentement du donneur qui doit être « libre et éclairé » ;
- le deuxième amendement écarte une ambiguïté s'agissant de la révocabilité sans forme et à tout moment du consentement. Cette révocabilité doit être générale. Or, la rédaction actuelle retenant un article démonstratif (ce consentement) semble ne s'appliquer qu'au consentement recueilli en urgence par le procureur de la République. Aussi est-il proposé de lui substituer un article défini (le consentement) ;
- le troisième amendement est de même nature. Le quatrième alinéa de cet article prévoit que le don d'organes, quand le donneur fait partie du « cercle élargi », doit être autorisé par « l'un des comités d'experts chargés d'autoriser le prélèvement sur une personne vivante, mentionnés à l'article L. 1231-3 » . Cette formule apparaît inutilement lourde par rapport à celle retenue dans l'alinéa précédent ( « le comité d'experts mentionné à l'article L. 1231-3 » ) et, de ce fait, pourrait laisser entendre que serait visée l'une ou l'autre formation du comité d'experts selon qu'il se prononce sur des prélèvements sur majeur ou sur mineur. Or, il ne saurait y avoir d'ambiguïté sur ce point : le prélèvement d'organes sur un mineur vivant est proscrite.
Votre commission vous propose d'adopter cet article ainsi amendé.
Don d'organes et moelle osseuse par personne vivante
|
DROIT EN VIGUEUR |
PROJET DE LOI |
PROPOSITIONS DE VOTRE COMMISSION |
||||||||||||||||
|
Personne majeure |
Mineur |
Personne majeure |
Mineur ou majeur sous tutelle (moelle) (3) |
Curatelle et sauvegarde
|
Personne majeure |
Mineur ou majeur sous tutelle
|
Curatelle et sauvegarde
|
|||||||||||
|
Organes |
Moelle osseuse |
Moelle osseuse (3) |
Organes |
Moelle osseuse |
Mineur |
Majeur sous tutelle |
Apte à consentir |
Inapte à consentir |
Organes |
Moelle osseuse |
Mineur |
Majeur sous tutelle |
Apte à consentir |
Inapte à consentir |
||||
|
Qualité du receveur par rapport au donneur |
Père, mère, fils, filles, frères, soeurs
;
|
Toute personne |
Frères, soeurs
|
Père, mère, fils, filles frères, soeurs, conjoint, toute personne ayant des liens étroits et stables |
Toute personne |
Frères, soeurs, cousins germains |
Frères, soeurs
|
Père, mère, fils, filles, frères soeurs,
conjoint,
|
Toute personne |
Frères, soeurs, cousins germains, oncles, tantes, neveux, nièces |
Frères, soeurs |
Frères, soeurs, cousins germains, oncles, tantes, neveux, nièces |
- 101 - Frères, soeurs |
|||||
|
Information sur le risque |
Praticien |
Comité d'experts |
Praticien |
Praticien |
Comité d'experts |
Praticien |
Praticien |
|||||||||||
|
Expression du consentement |
TGI (1) |
TGI (2) |
TGI (1) |
TGI (2) |
TGI (1) |
TGI (1) |
TGI (2) |
TGI (1) |
||||||||||
|
Autorisation |
Non |
Non |
Comité d'experts |
Père, mère, fils, filles frères, soeurs, conjoint : comité d'experts si le juge l'estime nécessaire. Les autres : comité d'experts |
Non |
Comité d'experts |
Juge des tutelles après avis du comité d'experts |
Comité d'experts |
Juge des tutelles après avis du comité d'experts |
Père, mère, fils, filles, frères, soeurs,
conjoint : comité d'experts si le juge l'estime
nécessaire.
|
Non |
Comité d'experts |
Juge des tutelle après avis du comité d'experts |
Comité d'experts |
Juge des tutelles après avis du comité d'experts |
|||
( 1) Président du Tribunal de Grande Instance ou tout magistrat désigné par lui, ou, en cas d'urgence, procureur de la République.
(2) Consentement des parents dans les conditions prévues au (1) ci-dessus.
(3) Le prélèvement d'organes n'est pas autorisé sur les mineurs et majeurs protégés
Article 8
Principes généraux applicables aux
prélèvements de tissus ou de cellules ou à la collecte de
produits issus du corps humain
Objet : Cet article procède à une redéfinition et à une reclassification des différents régimes juridiques applicables aux cellules, s'agissant de leur prélèvement, de leur préparation ou de leur administration.
I - Le dispositif proposé
Le I du présent article propose un nouvel intitulé pour le titre IV du livre II de la première partie du code de la santé publique « tissus, cellules, produits du corps humain et leurs dérivés » .
Le II modifie le chapitre premier du titre IV du livre II de la première partie du code de la santé publique susmentionné.
Article L. 1241-1 du code de la santé publique
Cet article vise à redéfinir les conditions de prélèvement de tissus et cellules sur une personne vivante.
Le premier alinéa rappelle les deux finalités à un tel prélèvement : scientifique ou thérapeutique. Pour des motifs de sécurité sanitaire, seuls les tissus inscrits sur une liste fixée par décret en Conseil d'Etat (cf. article L. 1241-7 ci-après) peuvent donner lieu à un tel prélèvement.
Le deuxième alinéa dispose que les prélèvements à des fins thérapeutiques de cellules ou tissus -hors moelle osseuse- doivent faire l'objet d'un consentement écrit, après information sur les conséquences et les risques du prélèvement. Dans le silence de la loi, il appartiendrait au praticien d'assurer cette information. Sa dernière phrase prévoit toutefois que « lorsque la nature du prélèvement et ses conséquences pour le donneur le justifient » les « conditions d'expression du consentement et d'obtention d'une autorisation prévues à l'article L. 1231-1 s'appliquent ».
L'article L. 1241-7 ( cf. ci-après) dans son 2° renvoie à un décret en Conseil d'Etat le soin de fixer la liste des tissus et cellules dont le prélèvement est soumis à ce régime particulier. « Les conditions d'expression du consentement (...) prévues à l'article L. 1231-1 » renvoient notamment ( cf. commentaire ci-dessus de l'article 7 ) au recueil du consentement « libre et éclairé » par un magistrat, à l'information préalable non plus par le praticien mais par le comité d'experts prévu à l'article L. 1231-3 et la révocabilité du consentement « sans forme et à tout moment ». « Les conditions (...) d'obtention d'une autorisation prévue à l'article L. 1231-1 » visent les cas où le magistrat estime nécessaire que le prélèvement soit autorisé par le comité d'experts.
Le troisième alinéa précise le régime du don de moelle hématopoïétique. Ce régime est démarqué partiellement de celui précité de l'article L. 1231-1. La personne doit être informée des risques et conséquences du prélèvement mais, dans le silence de la loi, cette information reviendrait au praticien et non au comité d'experts. Le consentement est recueilli par un magistrat selon une procédure identique à celle de l'article L. 1231-1, à la seule exception qu'il n'est pas précisé que le magistrat s'assure du caractère « libre et éclairé » du consentement.
Article L. 1241-3 du code de la santé publique
Cet article précise le régime juridique applicable au prélèvement de moelle osseuse sur mineur :
- le premier alinéa confirme le régime en vigueur, à savoir que le don de moelle par un mineur n'est possible qu'en l'absence d'une autre solution thérapeutique et réservé aux frères et soeurs ;
- toutefois, le deuxième alinéa prévoit, en cas d'impossibilité du prélèvement ci-dessus, la possibilité à « titre exceptionnel » du prélèvement de moelle au bénéfice des cousines et cousins germains ;
- le troisième alinéa confirme le régime juridique existant pour ce type de prélèvement sur mineur : consentement des deux titulaires de l'autorité parentale et expression de ce consentement devant un magistrat ;
- le quatrième alinéa prévoit que le consentement, en cas d'urgence, est recueilli par le procureur de la République ;
- le dernier alinéa prévoit que l'autorisation est donnée par le comité d'experts prévu à l'article L. 1231-3. Il s'agit en l'espèce du comité d'experts réuni dans la formation qu'il adopte lorsqu'il est saisi d'une demande de prélèvement sur une personne mineure (présence d'un pédiatre et d'une « personne qualifiée dans le domaine de la psychologie de l'enfant »). Il appartient au comité de s'assurer que le mineur a été informé du prélèvement « en vue d'exprimer sa volonté s'il y est apte ». Si le mineur est jugé apte par le comité à exprimer sa volonté, son refus fait obstacle au prélèvement. Ainsi, comme pour le cas des majeurs protégés ( cf. ci-après ), une personne peut ne pas avoir la faculté de consentir (dans le cas des mineurs, le consentement relève des parents), mais être apte à refuser.
Votre rapporteur formulera trois remarques sur cet alinéa :
le contenu de l'information reçue par le mineur est minimale : il est informé qu'il va y avoir prélèvement, mais ne reçoit pas d'informations sur le risque encouru. Cette information est délivrée par le praticien aux parents ;
le mineur n'exprime pas un consentement mais une simple volonté. De fait, le consentement doit, en principe, être « libre et éclairé » et le mineur ne l'est pas puisqu'il ne reçoit pas d'informations sur la nature et le risque du prélèvement envisagé. Lui est-il néanmoins possible « d'exprimer sa volonté » , en l'espèce son refus, dans l'ignorance des tenants et des aboutissants du prélèvement ?
seul le mineur reconnu en état d'exprimer sa volonté a la capacité de faire obstacle au prélèvement. Selon le rapporteur de l'Assemblée nationale 59 ( * ) , « cela devrait être la règle pour les mineurs de 13 ans puisqu'ils ont la possibilité de s'inscrire sur le registre des refus » . Il est sans doute souhaitable que la limite de 13 ans ne soit pas considérée comme une présomption mécanique de la faculté du mineur d'exprimer sa volonté. L'intérêt du recours au comité d'experts, dans sa formation spécifiquement prévue pour l'examen des prélèvements sur personne mineure, repose avant tout sur la souplesse d'un examen au cas par cas des situations. Une interprétation mécanique de l'« aptitude » des mineurs rendrait, sur ce point, l'utilité des comités toute relative.
Article L. 1241-4 du code de la santé publique
Cet article introduit la possibilité d'un prélèvement de moelle osseuse sur une personne majeure protégée et, en conséquence, précise le régime juridique de ce prélèvement.
Ce régime juridique prévoit :
- qu'il peut être réalisé au profit des frères et soeurs ( ( cf. article L. 1241-3 ci-dessus premier alinéa) . Cette qualité du receveur présente un caractère restrictif -il s'agit du droit en vigueur pour les mineurs- alors que le régime de ces derniers prévoit désormais, en cas de besoin, la possibilité de prélever en faveur des cousins germains ;
- que le prélèvement sur la personne sous tutelle est autorisé par le juge des tutelles après avis du comité d'experts (deuxième alinéa) . La compétence du juge des tutelles est pleine et entière : elle ne prévoit pas de recueillir l'avis du tuteur, ni son accord, le juge n'est en outre pas lié par le contenu de l'avis du comité d'experts qui doit recueillir ;
- que la personne sous curatelle ou sauvegarde de justice peut consentir par elle-même au prélèvement, si cette faculté de consentir lui a été reconnue par le juge des tutelles. Dans ce cas, il appartient au comité d'experts d'autoriser le prélèvement « après recueil du consentement de l'intéressé dans les conditions prévues par (l'article L. 1231-3) ». Cette référence apparaît erronée car ledit article L. 1231-3 ne concerne pas les conditions de recueil du consentement. Il est probable que les auteurs du projet de loi aient entendu viser le consentement « libre et éclairé » recueilli par un magistrat. Dans le cas contraire, il appartient, comme pour les majeurs sous tutelle, au juge de tutelle compétent d'autoriser le prélèvement après avis du comité d'experts.
Dans tous les cas, le refus de la personne protégée fait obstacle au prélèvement.
Article L. 1241-6 du code de la santé publique
Cet article prévoit de soumettre les tissus et cellules prélevés à des fins thérapeutiques sur une personne décédée aux règles relatives au prélèvement d'organes post mortem :
- présomption du consentement avec application pour les cellules et tissus du principe de refus posé par l'inscription au registre national desdits refus (article R. 676-6-2 du code de la santé publique) ;
- les modalités de recueil pour les mineurs ou majeurs protégés décrites ci-dessus s'appliquent avec néanmoins l'accord des titulaires de l'autorité parentale ou du tuteur ;
- présence d'un protocole pour les prélèvements à des fins scientifiques ;
- restauration décente du corps.
Article L. 1241-7 du code de la santé publique
Cet article renvoie à des dispositions prises par décret en Conseil d'Etat :
1°) la liste des tissus mentionnée au premier alinéa de l'article L. 1241-1 qui peuvent être prélevés en vue de don à des fins thérapeutiques ;
2°) les tissus et cellules mentionnés au deuxième alinéa du même article dont le prélèvement doit relever du régime prévu à l'article L. 1231-1 ;
3°) les « situations médicales et les conditions » dans lesquelles le prélèvement de tissus et cellules sur un cadavre doit être réalisé. Ce régime est actuellement fixé par le décret n° 97-306 du 1 er avril 1997.
Le III du présent article modifie le chapitre II du titre IV du livre II de la première partie du code de la santé publique relatif aux autorisations des établissements effectuant des prélèvements.
Le 1° propose une nouvelle rédaction pour l'article L. 1242-1 édictant le régime des autorisations pour les établissements et organismes prélevant des tissus et cellules.
Le régime d'autorisation en vigueur, avec l'avis de l'EFG, des établissements de santé préleveurs, est maintenu pour les tissus et cellules prélevés à des fins d'allogreffe (premier alinéa) .
En revanche, il est modifié et unifié pour les prélèvements destinés à un usage autologue ou allogénique qui suivront les dispositions prévues ci-dessus (deuxième alinéa) .
Est en revanche prévue une dérogation pour certains prélèvements autologues réalisés en médecine de ville par des médecins et chirurgiens dentistes (troisième alinéa) . La liste des cellules susceptibles d'être prélevées est déterminée par arrêté du ministre de la santé après avis de l'EFG et sur proposition de l'AFSSAPS.
Le dernier alinéa du texte proposé pour cet article prévoit que les autorisations susmentionnées sont valables pour un délai de cinq ans.
Le 2° propose d'ajouter la notion de cellule à l'article L. 1242- 2 qui prévoit l'interdiction de rémunération de l'activité de préleveur.
Le 3° précise le contenu du décret en Conseil d'Etat devant permettre l'application du chapitre afin de prendre en compte les modifications du 2° ci-dessus.
Le IV du présent article a pour objet d'encadrer les activités de préparation, conservation et utilisation des cellules et de leurs dérivés, d'origine humaine, en modifiant les dispositions contenues au chapitre III du titre IV du livre II de la première partie du code de la santé publique relatif à l'encadrement des établissements se livrant à ces activités.
Le régime juridique de ces établissements avait été fixé par la loi du 29 juillet 1994 modifiée par la loi du 28 mai 1996 et par celle du 1 er juillet 1998.
L'intitulé du chapitre III est modifié et inclut les notions de « conservation », « utilisation » et « préparation » des tissus, cellules et aussi « leurs dérivés ».
Article L. 1243-1 du code de la santé publique
Le premier alinéa prévoit que l'ensemble des cellules humaines, à l'exception des produits sanguins labiles, utilisées à des fins thérapeutiques autologues ou allogènes, reçoivent l'appellation de produits cellulaires à finalité thérapeutique. Les produits non directement issus du corps humain -produits de thérapie génique et cellulaire d'origine animale- se trouvent par cohérence transférés dans un titre séparé (cf. article 13) . L'un des apports essentiels de ce projet de loi est de proposer cette séparation.
Le second alinéa prévoit deux statuts possibles pour les produits à finalité thérapeutique, ils relèvent soit :
- de la catégorie des spécialités pharmaceutiques ou des médicaments fabriqués industriellement et sont régis par les dispositions relatives aux médicaments humains ;
- de la catégorie des préparations de thérapie cellulaire régies par les dispositions du IV du présent article.
L'unification du régime des cellules humaines -destinées ou non aux thérapies cellulaires- supposait une redéfinition du régime juridique des établissements se livrant à des activités sur ces dernières.
Article L. 1243-2 du code de la santé publique
Cet article prévoit l'extension de la catégorie des établissements pouvant se livrer à des activités de conservation, distribution et cession de ces cellules, cette activité n'étant plus réservée au seul secteur non lucratif. L'autorisation est délivrée par l'AFSSAPS après avis de l'EFG (premier alinéa) .
Le deuxième alinéa prévoit que toute modification des éléments figurant initialement dans l'autorisation doit faire l'objet d'une autorisation nouvelle.
Article L. 1243-3 du code de la santé publique
Cet article propose la création d'un régime unique de déclaration préalable auprès du ministre chargé de la recherche pour :
- les activités de conservation et préparation des tissus et cellules issus du corps humain à des fins scientifiques ;
- la conservation d'organes, de sang et produits qui en sont issus, à des fins scientifiques ;
- la constitution de collections d'échantillons biologiques à des fins scientifiques.
Cette unification avait été préconisée par le Conseil d'Etat (cf. article 4) .
Le premier alinéa précise que cette activité est ouverte à tout organisme qui fait la déclaration préalable auprès du ministre de la recherche.
Le deuxième alinéa définit la collection d'échantillons biologiques humains comme la réunion, à des fins scientifiques, de prélèvements effectués sur un groupe de personnes identifiées et sélectionnées en fonction des caractéristiques cliniques ou biologiques d'un ou plusieurs membres du groupe ainsi que des dérivés de ces prélèvements.
Le troisième alinéa prévoit pour le ministre de la recherche une faculté d'opposition dans un délai de trois mois suivant la déclaration si les conditions de conduite de l'activité ne semblent pas en mesure d'assurer le respect des dispositions du titre premier du présent livre du code de la santé publique.
Le quatrième alinéa prévoit la possibilité pour le ministre de la recherche de suspendre ces activités quand les exigences posées ne sont plus remplies.
Le cinquième alinéa prévoit, dans l'hypothèse mentionnée à l'alinéa ci-dessus, l'avis préalable du comité consultatif sur le traitement de l'information en matière de recherche dans le domaine de la santé.
Le sixième alinéa prévoit l'information de l'AFSSAPS lorsque des activités à des fins scientifiques sont menées sur les mêmes sites que des activités à des fins thérapeutiques. En ce cas, cette Agence peut suspendre à tout moment l'activité en cas de risque pour la sécurité sanitaire.
Le dernier alinéa dispose que les tissus et cellules conservés ou préparés ne peuvent être cédés qu'à un établissement qui a déclaré des activités similaires.
Article L. 1243-4 du code de la santé publique
Cet article propose d'instituer un régime d'autorisation préalable pour la conservation et la préparation de tissus et cellules du corps humain à des fins de cessions pour un usage scientifique. L'autorisation est obtenue auprès du ministre chargé de la recherche après avis du comité consultatif cité à l'article précédent (premier alinéa) .
Le deuxième alinéa prévoit que ces dispositions sont applicables aux activités de conservation et de préparation des organes, du sang, de ses composants et de ses produits dérivés.
Article L. 1243-5 du code de la santé publique
Cet article prévoit que l'utilisation des tissus et des préparations de thérapie cellulaire est autorisée par l'AFSSAPS qui évalue l'environnement technique de constitution et les indications thérapeutiques de ces produits (premier alinéa).
Les deuxième et troisième alinéas prévoient respectivement que toute modification des éléments de l'autorisation initiale doit être autorisée et que l'EFG est informé des autorisations délivrées.
Article L. 1243-6 du code de la santé publique
Cet article précise que seuls des établissements de santé peuvent pratiquer des greffes au moyen de ces tissus, cellules ou préparations. Il prévoit en outre que, lorsque l'intérêt de la santé publique l'impose ou que le coût de l'opération est élevé, ces établissements doivent être autorisés par l'EFG (premier alinéa) .
Le deuxième alinéa prévoit une dérogation comme pour les établissements préleveurs (cf. III ci-dessus) au profit de certains cabinets libéraux pour certains tissus et préparations de thérapie cellulaire figurant sur une liste établie par arrêté ministériel, sur proposition de l'AFSSAPS après avis de l'EFG.
Le troisième alinéa prévoit un régime spécifique pour les allogreffes de cellules souches hématopoiétiques en raison de la technicité que requiert cette activité. Cette dernière est donc réservée aux CHU et établissements de santé qui leur sont liés par convention.
Article L. 1243-7 du code de la santé publique
Cet article prévoit les conditions de délivrance des autorisations prévues précédemment (articles L. 1243-2, L. 1243-5 et L. 1243-6) . Cette autorisation est subordonnée :
- au respect des conditions techniques, sanitaires, médicales et, le cas échéant, financières ;
- au respect des principes généraux du titre premier du livre II de la première partie du code de la santé publique (cf. article 5 du présent projet).
Article L. 1243-8 du code de la santé publique
Cet article prévoit que les modalités d'application des dispositions du présent chapitre seront fixées par décret en Conseil d'Etat.
Ce décret devra fixer notamment :
- les activités d'un coût élevé ou relevant de « l'intérêt de la santé publique » ;
- les conditions de délivrance, de suspension et de retrait des autorisations ;
- les règles permettant d'assurer le respect des principes généraux applicables aux produits dont il est question dans ce chapitre.
Le V du présent article modifie le chapitre IV du titre IV du livre II de la première partie du code de la santé publique .
Le 1° modifie l'intitulé du chapitre IV qui devient « Don et utilisation des gamètes en vue d'une AMP » .
Le 2° modifie l'article L. 1244-2 pour ouvrir aux célibataires, ayant procréé, la faculté de donner leurs gamètes en vue d'une AMP avec tiers donneur. Si ce donneur est en couple, le consentement de l'autre membre est requis (premier alinéa) . Le deuxième alinéa prévoit en outre le double consentement des membres du couple receveur.
Le 3° prévoit, à l'article L. 1244-4 , le doublement (de cinq à dix) du nombre maximum de naissances qui peut être réalisé à partir des gamètes d'un même donneur.
Le 4° prévoit, à l'article L. 1244- 5, la suppression de la consultation préalable de la CNMBRDP et du CNOSS en vue de la délivrance de l'autorisation des organismes ou établissements de santé qui recueillent, traitent, conservent et cèdent des gamètes.
Le VI du présent article propose de modifier le chapitre V du titre IV du livre II de la première partie du code de la santé publique consacré aux dispositions communes.
Article L. 1245-1 du code de la santé publique
Cet article est consacré aux modalités de retrait des autorisations des établissements autorisés à prélever et greffer des organes, des tissus et cellules, conserver, préparer des tissus, greffer des tissus ou administrer des préparations de thérapie cellulaire ainsi que des organismes chargés du recueil et de la conservation des gamètes (premier alinéa) .
Le deuxième alinéa prévoit, sauf urgence quant à la sécurité des personnes, un délai d'un mois après mise en demeure avant que le retrait ne soit effectif.
Article L. 1245-2 du code de la santé publique
Cet article prévoit le régime juridique des résidus opératoires. Ces derniers ne peuvent être prélevés qu'à l'occasion d'une intervention réalisée dans l'intérêt des personnes (premier alinéa) :
- les personnes majeures doivent être informées et disposer d'une faculté d'opposition ;
- pour les mineurs ou majeurs protégés, l'opposition des titulaires parents ou tuteurs fait obstacle au prélèvement, de même que le refus du mineur ou du majeur protégé (deuxième alinéa).
Le dernier alinéa précise les principes généraux auxquels sont soumis les tissus, cellules et produits du corps humain de même que le placenta. Ces principes sont ceux énoncés au titre premier du livre II de la première partie du code de la santé publique.
Article L. 1245-3 du code de la santé publique
Cet article prévoit que tout prélèvement de produits ou éléments du corps humain a le statut d'activité médicale, de même que le prélèvement d'organes (cf. article 7) .
Article L. 1245-4 du code de la santé publique
Cet article prévoit que les prélèvements réalisés dans le cadre d'une recherche biomédicale sont assimilés à des prélèvements à des fins thérapeutiques et notamment soumis aux règles de sécurité sanitaire et vigilance mentionnées aux articles L. 1211-6 et L. 1211-7 (cf. article 5).
Article L. 1245-5 du code de la santé publique
Cet article prévoit le régime juridique des exportations et importations des éléments et produits du corps humain. Ces dernières doivent être réalisées par des organismes autorisés par l'AFSSAPS (premier alinéa) .
Par dérogation, les établissements de santé autorisés à prélever de la moelle osseuse peuvent l'exporter à des fins thérapeutiques, de même que ceux autorisés à procéder à des greffes peuvent importer cette moelle à des fins thérapeutiques (deuxième alinéa) .
Les trois derniers alinéas reprennent les dispositions du droit en vigueur pour :
- l'importation et l'exportation des produits thérapeutiques annexes (troisième alinéa) ;
- l'importation et l'exportation des échantillons biologiques ;
- l'autorisation délivrée par le ministre chargé de la recherche d'importer ou exporter des tissus et cellules à des fins scientifiques
Article L. 1245-6 du code de la santé publique
Cet article renvoie à un décret en Conseil d'Etat l'édiction des modalités d'application du présent article.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a adopté vingt amendements modifiant cet article :
- à l'initiative de sa commission spéciale et de M. Jean-François Mattei et plusieurs de ses collègues, elle a adopté un amendement précisant que les prélèvements d'éléments du corps humain peuvent être réalisés en vue « de réalisation de dispositif in vitro » (article L. 1241-1) ;
- à l'initiative du Gouvernement, elle a adopté un amendement prévoyant de renforcer le contenu de l'information fournie au donneur avant un prélèvement en précisant à celui-ci les risques associés audit prélèvement (article L. 1241-1) ;
- à l'initiative de sa commission spéciale, elle a adopté un amendement séparant les dispositions prévues par la dernière phrase du troisième alinéa « ce consentement est révocable sans forme et à tout moment » pour en faire un quatrième alinéa ;
- à l'initiative du Gouvernement, elle a adopté un amendement prévoyant que le consentement des parents ou du représentant légal du mineur faisant l'objet d'un prélèvement de moelle osseuse dispose d'une information délivrée par le praticien sur les risques et conséquences éventuels du prélèvement ; il est explicitement précisé que l'obligation d'information repose sur « le praticien qui a posé l'indication de greffe » mais il est également prévu qu'elle peut relever d'un praticien choisi par les parents ( article L. 1241-3 ) ;
- à l'initiative de sa commission spéciale, elle a adopté un amendement prévoyant que le juge des tutelles entend le majeur protégé susceptible de donner sa moelle osseuse, afin de déterminer s'il a la faculté de consentir à un tel prélèvement ( article L. 1241-4 ) ;
- sur proposition de sa commission spéciale, elle a adopté un amendement de précision prévoyant, à l'article L. 1241-6 que la mort doit être « dûment constatée » ;
- à l'initiative de sa commission spéciale, elle a adopté un amendement proposant d'étendre la veille à la protection exercée par le ministre chargé de la recherche à toute personne travaillant sur les sites prévus à l'article L. 1243-3 ;
- à l'initiative du Gouvernement, elle a adopté un amendement proposant que lorsque l'organisme prévu à l'article L. 1243-4 est un établissement de santé, l'autorisation du ministre de la santé soit ajoutée à celle du ministre de la recherche ;
- à l'initiative de sa commission spéciale, elle a adopté un amendement précisant que les dispositions du dernier alinéa de l'article L. 1243-4 du code de la santé publique s'appliquent aux organismes exerçant des activités de préparation et conservation des produits et éléments du corps humain, et non aux produits eux-mêmes ;
- à l'initiative de sa commission spéciale et de M. Jean-Michel Dubernard, elle a adopté un amendement prévoyant l'assimilation des greffes composites de tissus vascularisés aux greffes d'organes ;
- à l'initiative de sa commission spéciale, elle a adopté un amendement supprimant le 1° du V du présent article afin de maintenir la rédaction actuelle du chapitre IV du livre II de la première partie du code de la santé publique : le don et l'utilisation des gamètes humains restent réservés à l'AMP. Votre rapporteur note à ce titre que cet usage unique permet de rendre difficile la pratique du clonage thérapeutique, puisque le don de gamètes à des fins d'un transfert nucléaire ne serait pas possible ;
- à l'initiative de sa commission spéciale, elle a adopté un amendement prévoyant la consultation préalable de l'APEGH avant d'autoriser les activités d'AMP ( 4° du V du présent article ) ;
- à l'initiative du Gouvernement, elle a adopté un amendement prévoyant qu'un avis préalable du CNOSS n'est pas nécessaire avant la mise en oeuvre des procédures d'autorisation des activités d'AMP ( 5° nouveau du V du présent article ) ;
- à l'initiative de Mme Yvette Roudy, elle a adopté un amendement prévoyant une information de la donneuse d'ovocytes relative aux conditions de ce don ( 6° nouveau du V du présent article) ;
- à l'initiative de sa commission spéciale, le Gouvernement s'en remettant à sa sagesse, elle a adopté un amendement prévoyant que le retrait temporaire ou définitif des autorisations mentionnées aux articles L. 1233-1, L. 1242-1 et L. 1243-4 est de droit lorsqu'il est demandé par l'AFSSAPS ( article L. 1245-1 ) ;
- à l'initiative du Gouvernement, elle a adopté un amendement prévoyant que les titulaires de l'autorité parentale ou le tuteur d'un mineur ou majeur protégé concernés par le prélèvement de déchet opératoire, peuvent exprimer leur absence d'opposition par tout moyen. Votre rapporteur s'interroge sur la portée de cette précision. S'il est logique d'exprimer son opposition ou son consentement par tout moyen, l'absence d'opposition semble davantage relever du consentement présumé. En conséquence, seul le silence exprime cette absence d'opposition. Dans le cas où la personne l'exprime par un autre moyen, elle consent ( article L. 1245-2 ) ;
- à l'initiative de sa commission spéciale, elle a adopté un amendement précisant que les produits visés au dernier alinéa de l'article L. 1245-2 sont bien les produits du corps humain ;
- à l'initiative de sa commission spéciale, elle a adopté deux amendements, l'un de rectification, substituant à l'article L. 1245-3 les mots « chapitre II » à « chapitre III », l'autre rectifiant une référence erronée ;
- à l'initiative de commission spéciale et de M. Jean-François Mattei et plusieurs de ses collègues, elle a adopté un amendement prévoyant le double accord du ministre de la recherche et du ministre de la santé pour les dispositions prévues par l'article L. 1245-5 ;
- elle a, enfin, adopté un amendement créant un B nouveau qui sanctionne, par l'ajout à l'article L. 1425-1 du code de la santé publique de la référence à l'article L. 5313-1 du même code, le fait de faire obstacle à l'action des inspecteurs de l'AFSSAPS.
III - La position de votre commission
Ainsi qu'il a été annoncé dans l'exposé général, votre commission vous proposera d'étendre le cercle des receveurs potentiels de moelle osseuse prélevée sur des mineurs ou majeurs protégés.
Par dérogation à l'interdiction générale posée à l'article L. 1241-2, le droit en vigueur n'ouvre une faculté de prélèvement de moelle osseuse qu'en faveur des frères et soeurs pour les mineurs et l'interdit pour les majeurs protégés. Le présent article ouvre davantage le dispositif en étendant « à titre exceptionnel » la possibilité de prélèvement sur les mineurs au bénéfice des cousins germains. Pour les majeurs protégés, il ouvre la possibilité d'une dérogation pour les prélèvements en faveur des frères et soeurs.
Votre commission vous propose d'élargir et d'unifier ce régime dérogatoire qui intervient à titre exceptionnel et en l'absence d'autre solution thérapeutique.
Par deux amendements , elle vous propose d'élargir le cercle des bénéficiaires de prélèvements de moelle osseuse aux :
- oncles et tantes, neveux et nièces des mineurs (en sus donc des frères et soeurs et cousines et cousins germains) ;
- cousines et cousins germains, oncles et tantes, neveux et nièces (en sus donc des frères et soeurs) des majeurs sous curatelle ou sauvegarde de justice dès lors qu'ils se seront vu reconnaître la faculté de consentir par le juge des tutelles.
En contrepartie, par deux amendements , votre commission vous propose d'exiger, pour tout prélèvement de moelle sur personne mineure ou majeure protégée, que le comité d'experts n'autorise le prélèvement ou formule son avis au juge de tutelle qu'après s'être assuré que tous les moyens ont été mis en oeuvre pour trouver un donneur majeur compatible.
Votre commission, par quatre amendements , vous propose en outre de clarifier et de renforcer le régime du consentement en l'alignant sur celui prévu pour le don d'organes. Elle vous propose de prévoir expressément :
- pour les prélèvements sur personnes mineures, que le magistrat doit s'assurer que le consentement des titulaires de l'autorité parentale est « libre et éclairé » et que ce consentement est révocable sans forme et à tout moment ;
- pour les prélèvements sur personnes majeures sous curatelle ou sauvegarde de justice, qui ont la faculté de consentir, que le consentement doit être recueilli par un magistrat, qu'il est « libre et éclairé », qu'il est précédé d'une information sur les risques et les conséquences du prélèvement, et qu'il est révocable sans forme et à tout moment.
Votre commission vous propose, par ailleurs, d'apporter, par trois amendements , des précisions au régime des tissus et cellules issus du corps humain proposé par cet article.
Au premier alinéa de l'article L. 1241-1, elle vous propose de ne pas soustraire, dans un souci de simplification, à la liste limitative, fixée en Conseil d'Etat, des tissus du corps humain pouvant donner lieu à un don thérapeutique les tissus prélevés dans le cadre d'une recherche biomédicale.
A l'article L. 1245-4, elle vous propose, là encore dans un souci de simplification, de prendre en compte la spécificité des recherches biomédicales portant sur les produits cellulaires à finalité thérapeutique, sur les produits de thérapie génique et sur les produits cellulaires d'origine animale en prévoyant une équivalence entre l'autorisation de recherche biomédicale et l'autorisation du lieu dans lequel s'effectuent le prélèvement, la conservation, la préparation et l'administration des cellules.
Elle vous propose, enfin, en plein accord avec le ministre de la santé, de rétablir la compétence unique du ministre de la recherche pour les autorisations d'importation ou d'exportation de tissus et cellules à des fins de recherche.
Votre commission vous propose d'adopter cet article ainsi amendé.
Article 9
Conditions d'élaboration des règles de bonnes
pratiques
Objet : Cet article a pour objet de fixer les conditions d'élaboration des règles de bonnes pratiques s'appliquant au cycle d'utilisation des éléments et produits du corps humain.
I - Le dispositif proposé
Le présent article modifie les deux premiers alinéas de l'article L. 1251-2 du code de la santé publique.
Le premier alinéa de l'article L. 1251-2 renvoie à l'Etablissement français des greffes (EFG), après avis de l'Agence française pour la sécurité sanitaire des produits de santé (AFSSAPS), la mission d'élaborer les règles de bonnes pratiques s'appliquant à l'ensemble du cycle d'utilisation des organes du corps humain .
Le présent article modifie à la marge la rédaction figurant actuellement dans le code de la santé publique en ajoutant le terme « préparation » et en retranchant celui de « transformation » à la liste des opérations composant le cycle d'utilisation des organes et des tissus issus du corps humain. La notion de « bonnes pratiques » est, pour sa part, mise au pluriel. En outre, le texte proposé substitue le terme « élaborer » à celui de « préparer » pour les préparations de thérapie génique visées par cet article.
Le second alinéa de l'article L. 1251-2 prévoit que la compétence d'élaboration des règles de bonnes pratiques applicables aux tissus, cellules et produits du corps humain soit confiée à l'AFSSAPS après avis de l'Etablissement français des greffes.
Outre des modifications identiques à celles apportées au premier alinéa, le présent article met en conformité les dispositions du droit existant avec le cadre juridique nouveau applicable aux cellules. Ces règles de bonnes pratiques s'appliqueront désormais « aux préparations de thérapie cellulaire » alors que le droit existant prévoyait l'exclusion des produits, tissus ou cellules destinés à des fins de thérapie cellulaire ou génique.
II - Les modifications adoptées par l'Assemblée nationale
A l'initiative du Gouvernement, l'Assemblée nationale a adopté un amendement prévoyant une extension des missions de l'Etablissement français des greffes (EFG). Ce dernier se voit confier le soin de constituer et gérer un fichier des personnes vivantes ayant subi un prélèvement d'organe et ce, afin de renforcer l'évaluation des conséquences des prélèvements sur les vivants.
III - La position de votre commission
Votre commission vous propose d'adopter cet article sans modification .
Article 10
(art. L 1263-1, L. 1263-2, L. 1263-3 et
L. 1263-4
du code de la santé publique)
Coordination
Objet : Cet article a pour objet de coordonner un certain nombre de dispositions du code de la santé publique.
I - Le dispositif proposé
Le présent article propose une série de modifications rédactionnelles et de coordination du titre VI du livre II du code de la santé publique.
Le 1° en modifie l'intitulé. Ce dernier, actuellement « Produits de thérapie génique et cellulaire et produits thérapeutiques annexes » deviendrait « Dispositions relatives aux produits thérapeutiques annexes », intégrant ainsi la modification du régime juridique applicable aux produits de thérapie génique et l'unification du régime des produits cellulaires à finalité thérapeutique décrits au chapitre III du titre VI.
Le 2° supprime deux chapitres du titre VI : les premier et deuxième.
Le 3° prévoit par conséquence que le chapitre III devient le chapitre unique de ce titre.
Par coordination avec les dispositions prévues à l'article 5 du présent projet qui en reprend le contenu, le 4° abroge l'article L. 1263-4 du code de la santé publique qui prévoit l'obligation de déclaration auprès de l'Association française de sécurité sanitaire et des produits de santé (AFSSAPS) des effets inattendus ou indésirables des produits thérapeutiques par leurs utilisateurs, fabricants, importateurs ou distributeurs.
II - Les modifications adoptées par l'Assemblée nationale
A l'initiative de sa commission spéciale, l'Assemblée nationale a adopté un amendement de coordination qui :
- prévoit la modification des références du code figurant au chapitre premier du titre VI du fait de sa suppression ;
- abroge, dans les compétences de l'AFSSAPS, le fonctionnement de la commission actuellement prévue au troisième alinéa de l'article L. 1261-2 et qui est supprimé.
III - La position de votre commission
Votre commission vous propose d'adopter cet article sans modification.
Article 11
Dispositions pénales
Objet : Cet article prévoit le régime des peines pour les infractions régissant les éléments et produits du corps humain.
I - Le dispositif proposé
Le présent article propose une série de modifications des dispositions de la deuxième section du chapitre premier du titre premier du livre V du code pénal relatif à la protection du corps humain.
Le 1° modifie l'article 511-3 du code pénal.
Concernant le prélèvement d'organes sur personnes vivantes et majeures, le premier alinéa introduit la pénalisation du non-respect des conditions de prélèvement prévues à l'article L. 1231-1 du code de la santé publique, et modifié par le présent projet de loi à l'article 7 (recueil du consentement et délivrance des autorisations nécessaires). L'alinéa prévoit en outre la conversion de la peine d'amende applicable qui passe de 700.000 francs à 100.000 euros.
Concernant les personnes mineures ou protégées, le second alinéa prévoit les mêmes peines en cas de prélèvement d'organes mais également de tissus ou de cellules.
Une nouvelle rédaction de cet article qui avait été introduit par la loi du 29 juillet 1994 était en effet rendue nécessaire par la modification du statut juridique de la moelle osseuse. Elle prend en outre en considération les dispositions dérogatoires prévues pour le prélèvement de cellules hématopoïétiques sur les personnes mineures ou protégées figurant aux articles L. 1241-3 et L. 1241.4 du code de la santé publique tels que modifiés par l'article 8 du présent projet.
Le 2° modifie l'article 511-5 du code pénal . Cet article, introduit par la loi du 29 juillet 1994 précitée, précise les peines applicables pour avoir prélevé des tissus, des cellules, ou collecté des produits sur des personnes majeures hors de leur consentement, ou sur une personne mineure ou majeure protégée sans respecter les conditions entourant ces prélèvements.
La modification apportée par cette nouvelle rédaction est triple :
- préciser que les conditions d'expression du consentement pour les personnes majeures sont celles prévues par l'article L. 1241-1 du code de la santé publique nouvellement rédigé au 1° du II de l'article 8 prévu par le présent projet de loi ;
- préciser les peines applicables en cas de prélèvement de cellules de moelle hématopoïétique sur une personne vivante mineure ou majeure protégée ;
- aménager les peines : celles prévues dans le premier cas sont maintenues, le seul montant de l'amende étant converti en euros, les 500.000 francs initiaux étant remplacés par 75.000 euros ; la peine d'emprisonnement prévue dans le second cas est relevée de cinq à sept ans.
Le 3° introduit deux articles nouveaux dans cette section du code pénal, les articles 511-5-1 et 511-5-2 .
Le premier prévoit une peine d'emprisonnement de deux ans assortie d'une amende de 30.000 euros pour toute personne ayant réalisé un prélèvement sur une personne décédée en dehors d'un protocole de recherche prévu à l'article L. 1232-3 du code de la santé publique, dont la rédaction est prévue à l'article 7 du présent projet de loi.
Le I du second de ces articles punit de la même peine la conservation ou la transformation à des fins scientifiques de produits issus ou dérivés du corps humain sans en avoir fait la déclaration préalable ou lorsque cette dernière a suscité l'opposition du ministre de la recherche.
Le II prévoit une peine identique pour les mêmes infractions lorsque la conservation ou la transformation est entreprise en vue de la cession de ces produits.
Le 4° modifie l'article 511-7 du code pénal , introduit par la loi du 29 juillet précitée afin de prendre en compte les modifications introduites par le présent projet de loi au régime des différentes autorisations nécessaires à la manipulation des produits du corps humain et de prendre en compte l'incidence de l'introduction de l'euro. La peine sanctionnant la pratique des activités de prélèvements ou de greffes d'organes, de tissus ou de cellules ainsi que la conservation, la transformation ou l'administration de tissus ou thérapies cellulaires dans des établissements n'étant pas autorisés à cet effet est de deux années d'emprisonnement et de 30.000 euros d'amende.
Le 5° modifie l'article 511-8 du code pénal , non pour en modifier le régime des peines mais pour substituer aux mots « de cellules et produits » les mots de « produits cellulaires à finalité thérapeutique ».
Le 6° modifie l'article 511-8-1 du code pénal , introduit par la loi du 1 er juillet 1998. Cet article prévoit que le fait de procéder à la conservation, la préparation ou la transformation de produits du corps humain en violation des règles prévues à l'article L. 1243-6 du code de la santé publique (agrément des établissements et autorisation préalable de l'AFSSAPS) est puni de deux ans d'emprisonnement et 200.000 francs d'amende. La modification qui n'affecte pas le régime des peines a été rendue nécessaire par la suppression de cette autorisation préalable (cf. article 8) , remplacée par une procédure d'autorisation de produit après évaluation précisée à l'article L. 1243-5 du code de la santé publique, ainsi que par les modifications apportées au régime juridique des cellules.
Le 7° modifie l'article 511-8-2 du code pénal qui punit de deux années de prison et 200.000 francs d'amende l'importation et l'exportation de produits du corps humain qui ne sont pas destinés à des thérapies cellulaires ou géniques en violation des règles prévues pour ces activités. En effet, le V de l'article 7 du présent projet réserve l'importation et l'exportation d'organes aux établissements dûment habilités à cet effet (modification de l'article L. 1235-1) . Le VI de l'article 8 fixe le régime juridique applicable à l'exportation et l'importation des tissus et cellules (modification de l'article L. 1245-2) . Ainsi, les contrevenants aux dispositions édictées par les articles cités ci-dessus s'exposent à la peine prévue initialement, l'amende étant convertie en euros (30.000 euros).
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a adopté huit amendements au présent article.
A l'initiative de sa commission spéciale et de M. Jean-François Mattei et plusieurs de ses collègues, elle a adopté un amendement visant à préciser que les peines prévues par le 1° de cet article s'appliquent aussi au prélèvement thérapeutique.
A l'initiative de sa commission spéciale, elle a adopté deux amendements rédactionnels visant à préciser les alinéas de l'article L. 1241-1 dont le non-respect entraîne l'application des pénalités prévues au 2° de cet article.
Au 3° de cet article, elle a adopté deux amendements de même origine. Le premier alourdit le régime de la peine prévue pour l'article 511-5-2 du code pénal en prévoyant cinq années d'emprisonnement plutôt que deux et 75.000 euros d'amende plutôt que 30.000. Le second, d'ordre rédactionnel, supprime le « ou » prévu au commencement du troisième alinéa prévu par cet article pour l'article 511-5-2 du code pénal.
Aux 4° et 5° , à l'initiative de sa commission spéciale, elle a adopté deux amendements, le premier prévoyant que la peine prévue par l'article 511-7 du code pénal pour les infractions qui y sont décrites s'applique également en cas de retrait ou de suspension de l'autorisation qui y est mentionnée, le second procédant à une modification rédactionnelle de l'article 511-8 du code pénal, prévoyant notamment l'actualisation de la référence au code de la santé publique et la conversion en euros de l'amende prévue.
Au 7° , à l'initiative de sa commission spéciale, elle a adopté un amendement de coordination avec l'amendement adopté au 3° et tendant à alourdir les peines prévues par cet article.
Au 8° , à l'initiative de sa commission spéciale, elle a adopté un amendement rédactionnel.
III - La position de votre commission
Votre commission vous propose d'adopter cet article sans modification.
Article 12
Dispositions pénales
Objet : Cet article a pour objet de reproduire, au sein du code de la santé publique, le contenu des rédactions pour les infractions relatives à l'utilisation de produits et éléments du corps humain.
I - Le dispositif proposé
Le présent article vise à insérer deux articles dans le code de la santé publique :
- un article L. 1272-4-1 qui reproduit le contenu de l'article 511-5-1 du code pénal, tel que modifié par l'article 11 du présent projet de loi ;
- un article L. 1272-4-2 qui reproduit le contenu de l'article 511-5-2 du code pénal, tel que modifié également par ledit article 11.
II - Les modifications adoptées par l'Assemblée nationale
A l'initiative de sa commission spéciale, l'Assemblée nationale a adopté un amendement de coordination, modifiant le présent article compte tenu des modifications à l'article 11 qu'elle avait apportées aux deux articles du code pénal reproduits au présent article.
III - La position de votre commission
Votre commission vous propose d'adopter cet article sans modification.
Article 12 bis
Non-brevetabilité des éléments du corps
humain
Objet : Cet article, introduit par l'Assemblée nationale, vise à affirmer le principe de la non-brevetabilité des éléments du corps humain.
I - Le dispositif proposé
Sur proposition de M. Leroy d'une part, et MM. Lefort et Mei d'autre part, avec l'avis favorable de la commission spéciale, le Gouvernement s'en remettant à sa sagesse, l'Assemblée nationale a introduit le présent article disposant qu'un élément du corps humain, qu'il soit isolé ou produit par un procédé technique ne peut constituer une invention brevetable.
Cette disposition vise également, d'une manière expresse, la séquence d'un gène.
II - La position de votre commission
Cet article pose la question de la brevetabilité éventuelle du vivant.
La législation nationale bousculée par la directive 98/44/CE
L'article 7 de la loi n° 94-653 du 29 janvier 1994 avait prévu l'insertion au sein du code de la propriété intellectuelle d'un article énumérant une liste de sujets non brevetables. Aux termes de cette disposition, devenue l'article L. 611-17 du code de la propriété intellectuelle « (...) le corps humain, ses éléments et ses produits, ainsi que la connaissance de la structure totale ou partielle d'un gène humain ne peuvent, en tant que tels, faire l'objet de brevet (...) » .
La disposition alors adoptée a suscité un grand nombre de commentaires dont le Conseil d'Etat s'est, dans son rapport, fait l'écho, en notant le caractère équivoque de la notion « en tant que tels » appliqué au gène. En effet, il n'apparaît pas clairement si les gènes sont pris en compte une fois « en tant que connus par leur structure » ou deux fois « par le biais de cette connaissance et par le fait qu'ils sont les éléments constitutifs du corps humain ».
Selon le Conseil d'Etat, trois interprétations différentes de l'intention du législateur seraient possibles :
- la première interprétation est qu'il aurait posé comme règle de principe l'interdiction de breveter tous les éléments et produits du corps humain ;
- la deuxième interprétation est qu'il aurait posé comme règle la non-brevetabilité des éléments du corps humain en « l'état de leur structure naturelle ». Dans ce cas, «ces éléments pourraient toutefois être brevetables quand ils sont dupliqués et copiés dans le cadre d'une invention technique » ;
- enfin la troisième interprétation est qu'il aurait seulement cherché à exclure du champ du brevetable les gènes dont « on aurait procédé à la caractérisation, sans avoir déterminé leur fonction codante » ;
Il reste que, pour le Conseil d'Etat, « l'état du droit européen ne permet pas, en tout état de cause et même si les ambiguïtés générées par cette rédaction sont levées, de conserver le « en tant que tels » , dès lors que le niveau biologique où peut s'exercer la revendication du brevet ne peut plus être « le corps humain, ses éléments et ses produits... en tant que tels » car celui-ci, en l'état, n'est pas compatible avec les dispositions de la directive 98/44 CE » .
|
1. Le corps humain, aux différents stades de sa constitution et de son développement, ainsi que la simple découverte d'un de ses éléments, y compris la séquence ou la séquence partielle d'un gène, ne peuvent constituer des inventions brevetables. 2. Un élément isolé du corps humain ou autrement produit par un procédé technique, y compris la séquence ou la séquence partielle d'un gène, peut constituer une invention brevetable, même si la structure de cet élément est identique à celle d'un élément naturel. 3. L'application industrielle d'une séquence ou d'une séquence partielle d'un gène doit être concrètement exposée dans la demande de brevet. |
L'article 5 de cette directive prévoit ainsi un domaine brevetable et un domaine non brevetable. Pour M. Alain Claeys, auteur du rapport de l'OPECST sur la brevetabilité du vivant la présence du « peut » au deuxième aliéna ne saurait être interprétée comme « une sorte de choix d'accepter ou de refuser le brevet. Cette expression doit être interprétée dans le contexte du droit des brevets et indique que, si les conditions de brevetabilité sont remplies, le brevet doit être délivré » 60 ( * ) .
Aux termes de cette disposition, un gène est donc brevetable s'il est isolé par un procédé technique et susceptible d'une application industrielle.
Les difficultés éthiques soulevées par les dispositions de cet article ne sont pas minces. Peut-on en effet considérer que les gènes de l'homme et leur combinaison ne sont pas davantage que des molécules ?
Le Comité consultatif national d'éthique, dans son avis n° 64 du 8 juin 2000 affirmait avec force que « le gène humain porte inscrits dans sa séquence des déterminants élémentaires fondamentaux de l'être humain ; son rapport au corps humain est, de ce fait, d'une tout autre signification que pour d'autres molécules ; décrypter l'information que porte le gène, c'est ouvrir la compréhension du vivant et si ce vivant est humain, cette compréhension est fondamentale pour les êtres humains que nous sommes. Comment imaginer, si l'on décidait de traiter le gène comme un produit banal, que cette conception ne s'étendrait pas à une cellule, à un organe ou à des transactions concernant la reproduction ? Le CCNE persiste donc à penser que ce qui serait dit du gène, à propos de la propriété intellectuelle, pourrait si l'on n'y prend garde, fragiliser la règle qui met le corps humain hors commerce et qu'il faut éviter d'en arriver là ».
Cette position témoigne de l'émoi suscité par la possibilité ouverte par les dispositions de la directive dont la transposition a rencontré un nombre croissant d'opposition notamment celle d'une pétition lancée par MM. Jean François Mattei et Wolfgang Wodarg 61 ( * ) et celle du Comité consultatif national d'éthique qui a formulé, dans son avis mentionné ci-dessus, de strictes réserves.
Telle que conçue, la directive ne permet pas de conserver la position jusqu'ici inscrite dans la loi française et consistant à soustraire du champ de la brevetabilité les éléments du corps humain.
Doit-on et peut-on contrer les dispositions prévues par cette directive ?
Devant ce sujet éminemment complexe, votre rapporteur s'attachera à isoler les problèmes pour mieux en présenter les enjeux.
La première question posée est celle de l'opportunité de remettre en cause les principes posés par la directive en les considérant comme dénués de toute légitimité.
Interrogé sur ce point lors de son audition par votre commission, M. Axel Kahn a exprimé 62 ( * ) une position nuancée.
« L'article 12 bis voté en première lecture, si vous me permettez d'être un peu brutal, ne convient pas. Il dit : « Un élément isolé du corps humain ou autrement produit par un procédé technique, y compris la séquence ou la séquence partielle d'un gène ne peut constituer une invention brevetable. » Cet article ne me choque pas mais il est un peu dangereux . En effet, dans l'histoire des biotechnologies, une des premières grandes innovations ayant nécessité une très grande créativité intellectuelle a été de reconnaître l'érythropoïétine, de cloner son gène, de le fabriquer par un procédé technique utilisant l'ADN recombinant et de l'utiliser en thérapeutique. Est-il anormal de demander, suivant la logique des brevets que je ne veux pas employer ici, de remettre en cause, à ce titre, un brevet sur l'erythropoïétine recombinante ? Je ne le crois pas et si jamais nous devions en arriver à rendre impossible cela, ce serait un obstacle très important à l'évolution des biotechnologies. En revanche, le texte de la loi antérieure me semblait tout à fait correct. Il disait qu'en tant que telle, la connaissance totale ou partielle d'un gène ne pouvait faire l'objet d'un brevet.
« J'en arrive aux contradictions entre le nouvel article 12 bis et l'article 5 de la directive 98/44 CE. Selon cette dernière, lorsqu'on a trouvé la fonction d'un gène et qu'il se trouve hors de sa situation naturelle, il peut faire l'objet d'un brevet. De plus, il est ajouté que la revendication d'un brevet sur la séquence du gène en tant que telle est légitime. La loi française, quant à elle, déclarait qu'un brevet dérivé de la séquence du gène peut être légitime, en revanche en tant que telle la connaissance du gène doit rester libre pour pouvoir réaliser tout ce qui n'a pas été prévu par le premier breveté. Cette position est scientifiquement juste . En effet, l'idée selon laquelle un gène n'a qu'une fonction est scientifiquement fausse : un gène a une très grande quantité de fonctions. Un inventeur peut isoler un gène, en trouver une fonction importante, fabriquer un médicament, par exemple une protéine recombinante et demander, à mon avis légitimement, une propriété industrielle sur cette invention. En revanche, qu'il en arrive à considérer que le gène en lui-même, ou la séquence du gène, est un objet brevetable pour toute utilisation possible, même celle dont la plausibilité n'a pas été établie par le premier brevet, n'est pas légitime et me semble contraire à l'intérêt bien compris des biotechnologies » .
Le choix se porte aujourd'hui sur trois rédactions : celle du droit en vigueur, celle proposée par le présent article 12 bis et celle de la directive européenne qui in fine l'emporte aujourd'hui puisque cette directive, le délai de ratification ayant expiré, peut faire valoir ses effets en droit interne. Il conviendrait donc a priori d'adopter une rédaction qui ne prenne pas son exact contre-pied.
Votre rapporteur s'attachera donc à démontrer, en second lieu, la marge de manoeuvre offerte aujourd'hui au législateur.
La rédaction proposée par l'Assemblée nationale n'a pas pris la voie de la conciliation. Sans doute vise-t-elle à donner un mandat fort au Gouvernement pour renégocier le contenu de l'article 5 avec les autorités européennes. Cette voie, pose néanmoins un problème de légitimité car, ainsi que le rappelle M. Axel Kahn, « la situation est difficile, parce qu'en 1998, cette directive a été votée notamment avec l'appui soutenu de la France. Cela ne la met, d'ailleurs, pas dans une position facile lors de ces discussions avec la Commission de Bruxelles pour la renégociation de cette directive ».
Toutefois, et M. Kahn le rappelle fort bien, « aujourd'hui, elle n'a été transposée que par six pays et donc pas par les neuf autres, ce qui montre l'extraordinaire réticence des Etats. Parmi ceux n'ayant pas procédé à la transposition, au moins deux sont sur la même longueur d'onde, à savoir l'Allemagne et la France. L'idée selon laquelle cette directive n'est pas bonne me semble aujourd'hui gagner du terrain. Tout travail législatif laissant ouverte la possibilité de préciser la signification ou de réviser la directive me semble extrêmement bénéfique ».
La tentation d'une voie intermédiaire existe, et se trouve, à certains égards légitime car, comme le rappelait M. Axel Kahn ci-dessus, certaines activités scientifiques devraient pouvoir faire l'objet d'un brevet.
Nombreux sont les intervenants de la table ronde organisée par votre commission qui ont rappelé la distinction possible et reconnue dans le droit des brevets, entre découverte et invention 63 ( * ) .
« M. Michel GUGENHEIM - (...) La difficulté, ici, réside, en fait, dans la tension entre deux intérêts, entre le risque, en brevetant, de brider l'accueil aux soins, et ne le faisant pas, de manquer de moyens commerciaux pour la recherche. Sur ce point, il n'y a pas véritablement de point de vue religieux pouvant, à mon sens, s'exprimer. Simplement, d'une certaine manière, on pourrait demander un brevet sur une découverte sur le corps humain même si ce n'est pas une invention. »
« Dr. Stéphane MEYER - En fait, la grande différence classique entre découvrir et inventer existe. Les découvertes, au niveau du génome, doivent rester dans le patrimoine planétaire et, en aucun cas, une appropriation ne doit être possible . Là-dessus, la France, avec votre aide, conserve une position très ferme, contre l'avis de la majorité de l'Europe, qu'il faudra maintenir pour contrer tous les projets mercantilistes de rachat du corps humain sous toutes ses formes. (...) Vous, législateurs, devez trouver le juste milieu entre ces deux extrêmes pour les uns exceptionnels et pour les autres intolérables. »
« M. Patrick VERSPIEREN - (...) La principale question me paraît être une question de justice sociale et internationale, plus encore que du respect du corps. Au nom de quoi un découvreur, parce qu'il dispose d'une petite avance, va accaparer les connaissances ? Nous devons réfléchir sur cette question difficile. Personnellement, il me paraît sage de bien marquer la différence entre découverte et invention . »
« M. Geoffroy de TURCKHEIM - Cette distinction (entre découverte et invention) reste tout à fait pertinente. Elle était très chère à France Quéré qui nous disait souvent, en comité d'éthique, qu'une découverte n'est pas brevetable, contrairement à une invention. Je suis sensible à certains arguments, développés ce matin, selon lesquels certains procédés découlant de découvertes devraient, hélas, dans la logique du système, être brevetés. Le législateur ne pourra pas éviter, ici, une certaine ouverture mais dans le domaine des inventions et surtout des applications. »
« Pr. Sadek BELOUCIF - Au sujet des brevets, je reste touché par la différence entre invention et découverte. Nous pourrions, par rapport au gène, opposer de façon binaire deux conceptions, l'une considérant qu'il constitue un nouveau Far West ou une nouvelle frontière, et l'autre prenant en compte une inspiration plus rousseauiste. La proposition du professeur Axel Kahn de revenir à la formulation ancienne : « en tant que telle, la connaissance totale ou partielle d'un gène ne peut faire l'objet d'un brevet » permet pleinement de différencier le travail mécanique d'un séquenceur automatique par rapport à la valeur ajoutée intellectuelle qui doit mériter salaire ». »
Ce dernier rappel aux réflexions de M. Kahn fait par M. Beloucif reste une des clefs du problème. Devant la mécanisation des moyens de recherche, la distinction entre découverte et invention en matière de génétique garde-t-elle toute sa pertinence ? Est-elle suffisamment robuste pour être traduite en droit positif ? Certains en doutent.
|
Une invention doit satisfaire à trois critères pour être susceptible d'être protégée par un brevet : nouveauté, utilité et inventivité. La nouveauté ne semble pas devoir poser de problèmes dans ce domaine puisque, par exemple, une séquence génétique clonée est bien mise à disposition sous une forme sous laquelle on ne la trouvait pas auparavant. L'utilité rejoint l'exigence de décrire une application pratique, de démontrer que la séquence génétique en l'occurrence peut servir à quelque chose. Il n'est pas niable que ce critère peut être rempli en envisageant par exemple les tests diagnostiques qui permettent et permettront certainement de plus en plus de mettre en évidence les origines génétiques d'un certain nombre d'affections. Reste le problème de l'inventivité. C'est un problème crucial car en droit des brevets une invention s'oppose à une découverte et il est établi que celle-là est brevetable mais que celle-ci ne l'est pas. La définition de l'invention est donc essentielle. Le dictionnaire enseigne qu'une invention est à la fois la création de quelque chose de nouveau et la découverte de choses cachées. Le code de la propriété industrielle dans son article L. 611-10-2 ne donne pas de définition positive de l'invention, se contentant d'en exclure certaines choses comme par exemple, entre autres, les méthodes mathématiques ou les théories scientifiques. On peut par contre retenir la distinction faite par M. Jean-Marc Mousseron dans son « Traité des brevets » entre invention et découverte : « La découverte se distingue en ce qu'elle est la perception par voie d'observation d'un phénomène naturel préexistant à toute intervention de l'homme, alors que l'invention se caractérise en ce qu'elle est la coordination volontaire par l'homme de moyens matériels. L'aspect naturel d'un objet distingue la découverte de l'invention industrielle nécessairement marquée par une intervention artificielle de l'homme ». Comme l'ont noté de nombreux chercheurs, l'inventivité en matière d'isolement de gènes a considérablement changé depuis un certain nombre d'années. En effet il y a quelques années, lorsqu'on isolait un gène, c'était le plus souvent après avoir lancé une recherche biologique dans un but particulier. On travaillait ainsi sur une hormone, une enzyme, un récepteur ou un phénomène biologique quelconque et on essayait de trouver le gène responsable. Pour arriver à ce résultat, on mettait en oeuvre une recherche souvent fortement inventive qui permettait d'aboutir au gène. Isoler un gène constituait à cette époque un tour de force expérimental et résultait d'une approche pouvant à juste titre être assimilée à une démarche inventive. Mais depuis une dizaine ou une quinzaine d'années l'isolement de gènes humains et la détermination de leur structure chimique a considérablement changé grâce à l'apport des puissantes capacités de calcul de l'informatique. Cette contribution de l'informatique à la biologie a d'ailleurs donné lieu au développement d'une nouvelle branche de celle-ci : la bio-informatique. Celle-ci a révélé toute son efficacité et son caractère irremplaçable dans le développement du projet « Génome humain » ; sans elle celui-ci n'aurait sans doute pu être envisageable. (...) Le rôle irremplaçable joué dans cette recherche par la bio-informatique conduit de très nombreux chercheurs à estimer abusif de parler d'invention puisque l'essentiel du travail est effectué par des programmes informatiques, certes sophistiqués, qu'il suffit simplement de savoir faire marcher. Beaucoup de ces chercheurs estiment aussi que les prédictions d'activité biologique qui peuvent être faites au vu des résultats donnés par ces programmes informatiques peuvent rester très souvent assez vagues et les applications potentielles proposées génériques. (...) Il semble donc que la frontière entre la découverte et l'invention devienne, dans ce domaine, de plus en plus floue. La tendance semble bien s'être établie de ne plus chercher, dans ce domaine des biotechnologies, à faire réellement la séparation entre découverte et invention au profit de cette dernière. Cette attitude serait-elle due à la volonté de faciliter l'appropriation privée du génome ?
Source Alain Clayes, rapport précité de
l'OPESCT
|
Devant cette difficulté, les administrations françaises ne sont pas restées sans formuler des propositions.
L'Institut national de la propriété intellectuelle (INPI) a formulé une proposition de rédaction reprenant le texte même de la directive mais en modifiant sa structure.
|
Le corps humain, aux différents stades de sa constitution et de son développement, ainsi que la simple découverte de l'un de ses éléments, y compris la séquence ou la séquence partielle d'un gène, ne peuvent constituer des inventions brevetables. Un élément isolé du corps humain ou autrement produit par un procédé technique, y compris la séquence ou la séquence partielle d'un gène, peut constituer une invention brevetable, même si la structure de cet élément est identique à celle d'un élément naturel . |
Le Conseil d'Etat a critiqué 64 ( * ) cette proposition au motif que « les marges de manoeuvre du législateur national pourraient toutefois être davantage utilisées à propos de la notion « d'élément isolé du corps humain » : un prélèvement est bien une manière d'isoler un tel élément et le terme d'isoler n'a pas le même sens selon le niveau biologique auquel il s'applique : molécule, gène, cellules, organes ».
Et de formuler sa proposition de « spécifier la notion d'isolement des éléments du corps humain pour exclure les organes de la brevetabilité et dire à quels procédés techniques il est fait allusion , afin de protéger le prélèvement de velléités brevetaires. On peut également se demander s'il ne conviendrait pas a minima de subordonner explicitement la brevetabilité d'une séquence d'un gène à la précision de sa fonction au sens de l'application trouvée (production d'une protéine ayant une activité thérapeutique par exemple). En effet, le brevet doit porter sur une invention avec une application déterminée et l'alinéa 3 de l'article 5 de la directive prévoyait que : "L'application industrielle d'une séquence ou d'une séquence partielle d'un gène doit être concrètement exposée dans la demande de brevet». Entendu dans ce sens strict, un brevet n'interdit pas aux chercheurs de chercher des applications nouvelles sur des molécules déjà brevetées . Un nouveau brevet portera alors sur la nouvelle application à partir du même gène (un gène ayant plusieurs fonctions), le brevet précédent n'interdisant pas la recherche sur ce gène initial) dès lors que son adoption consacre des choix qui sont directement contraires à ceux effectués par le législateur en 1994 » .
Pour sa part, M. Jean François Mattei, s'exprimant devant votre commission, a exprimé l'intention du Gouvernement de déposer un amendement qui permette d'aller « vers une transposition partielle, à condition d'avoir prévu dans notre texte une disposition que nous pourrions faire accepter à la Commission comme notre interprétation du texte ».
Sous le bénéfice de ces observations, et dans cette attente, votre commission vous propose d'adopter cet article sans modification.
TITRE
III
-
PRODUITS DE SANTÉ
Article 13
Produits de thérapie génique et produits
cellulaires
d'origine animale à finalité
thérapeutique
Objet : Cet article prévoit le régime juridique des produits de thérapie génique et produits cellulaires d'origine animale à finalité thérapeutique.
I - Le dispositif proposé
Le présent article propose la création d'un titre V nouveau, au sein du livre premier de la cinquième partie du code de la santé publique, intitulé « Produits de thérapie génique et produits cellulaires d'origine animale à finalité thérapeutique » .
Il comprend six articles nouveaux répartis dans deux chapitres, le premier consacré aux « définitions » (articles L. 5151-1 et L. 5151-2 nouveaux) et le second, aux « dispositions communes » (articles L. 5152-1, 5152-2, 5152-3 et 5152-4 nouveaux) .
La création de ce titre nouveau doit permettre de rassembler les dispositions relatives aux produits de thérapie génique et cellulaire non issus du corps humain, c'est-à-dire essentiellement d'origine animale, disjointes du livre relatif aux éléments et produits du corps humain dans lequel elles figuraient précédemment. Ce transfert est justifié par le fait que ces produits 65 ( * ) , pour la plupart, n'incorporent aucune cellule d'origine humaine.
L'article L. 5151-1 du code la santé publique est consacré à la définition des produits de thérapie génique qui sont « les produits servant à transférer du matériel génétique et ne consistant pas en des cellules d'origine humaine ou animale » .
Il existe deux catégories de ces produits précisés par cet article : soit des médicaments, soit des « préparations de thérapie génique préparées à l'avance et dispensées sur prescription médicale à un ou plusieurs patients » . Dans le premier de ces deux cas, ils sont régis par les dispositions relatives au médicaments à usage humain. Dans le second de ces cas, leur statut juridique est défini au chapitre II nouveau de ce titre (cf. ci après) .
L'article L. 5151-2 de code de la santé publique définit les produits cellulaires d'origine animale à finalité thérapeutique toutes cellules ou dérivés de ces dernières d'origine animale et utilisés à cette fin. Ces produits sont soit des médicaments régis par les mêmes dispositions que ceux prévus à l'article précédent, soit des « préparations de thérapie cellulaire xénogénique» .
Premier article du second chapitre, l'article L. 5152-1 du code de la santé publique édicte le régime d'autorisation prévu pour les préparations de thérapie génique et de thérapie cellulaire xénogénique. Cette autorisation, qui n'est valable que pour une indication thérapeutique donnée, est délivrée par l'AFSSAPS (premier alinéa) , l'EFG étant pour sa part informé des décisions prises concernant les produits xénogéniques (second alinéa) .
L'article L. 5152-2 du code de la santé publique soumet les activités d'importation et d'exportation des préparations visées à l'article précédent à une autorisation délivrée par l'AFSSAPS (premier alinéa) , cette dernière n'étant pas nécessaire lorsque l'établissement, qui réalise ces opérations, dispose de l'autorisation prévue à l'article L. 5152-1 nouveau (second alinéa) .
L'article L. 5152-3 du code de la santé publique prévoit un second régime d'autorisation spécifique aux établissements réalisant les opérations sur ces produits (préparation, conservation, cession, distribution, importation, exportation). Cette autorisation est délivrée par l'AFSSAPS après avis de l'EFG pour les produits xénogéniques (premier alinéa) . Cette autorisation vaut pour une durée de cinq ans. Elle est renouvelable, modifiable et peut être suspendue ou retirée (deuxième alinéa) . Ces établissements sont, pour ces activités, soumis à des règles de bonnes pratiques (troisième alinéa) . Ces règles, édictées par arrêté du ministre de la santé, doivent garantir la qualité du traitement de ces produits (locaux, personnels, traçabilité, assurance qualité).
L'article L. 5152-4 du code de la santé publique renvoie à un décret en Conseil d'Etat les modalités d'application de ces articles.
II - Les modifications adoptées par l'Assemblée nationale
Sur proposition de M. Jean-François Mattei, contre l'avis de sa commission spéciale, le Gouvernement s'en remettant à la sagesse de l'Assemblée nationale, cette dernière a adopté un amendement rédactionnel substituant dans la dernière phrase de l'article L. 5151-1 du code de la santé publique prévu par cet article le mot « élaboré » à celui de « préparé ».
III - La position de votre commission
Votre commission vous propose d'adopter un amendement d'harmonisation des rédactions des articles L. 5151-1 et L. 5151-2 du code de la santé publique, par la suppression de la référence à une « élaboration à l'avance » ou à une « préparation à l'avance », précision superfétatoire pour des préparations tant de thérapie génique que de thérapie cellulaire xénogénique.
Votre commission vous propose d'adopter cet article ainsi amendé.
Article 14
Dispositions pénales
Objet : Cet article a pour objet de prévoir le régime des peines applicables pour les infractions au régime juridique des produits de thérapie génique et produits cellulaires d'origine animale à finalité thérapeutique.
I - Le dispositif proposé
Le I de cet article propose de créer un titre VII au livre IV de la cinquième partie du code de la santé publique qui prévoit dans l'article unique de son chapitre unique que la cession ou la distribution (I), l'importation ou l'exportation (II) de préparations de thérapie génétique ou de thérapie cellulaire xénogénique sans autorisation valide est punie de deux années d'emprisonnement et de 30.000 euros d'amende. La conservation, la distribution, la cession, l'importation et l'exportation de ces mêmes produits qui ne respecteraient pas les règles de bonnes pratiques afférentes sont punies d'une amende de 4.500 euros (III).
Le II de cet article assure la mise en conformité de l'article L. 5311-1 du code la santé publique relatif aux produits de santé relevant de la compétence de l'AFSSAPS, avec les nouvelles catégories juridiques applicables aux cellules créées par le projet de loi.
II - Les modifications adoptées par l'Assemblée nationale
Sur proposition de sa commission spéciale, l'Assemblée nationale a adopté trois amendements :
- le premier vise à préciser, dans le I de cet article, que pour le non-respect de l'encadrement des activités utilisant des cellules d'origine animale, la tentative d'infraction est punie de la même peine que l'infraction elle-même ;
- le second, d'ordre rédactionnel, vise à inverser l'ordre des mots « céder ou distribuer » au I du texte proposé pour l'article L. 5471-1 du code de la santé publique ;
- le troisième complète ce même article par un paragraphe (IV) qui prévoit l'engagement de la responsabilité pénale des personnes morales en matière d'infractions relatives à l'utilisation des produits alimentaires d'origine animale et les produits de thérapie génique.
III - La position de votre commission
Votre commission vous propose d'adopter cet article sans modification .
TITRE
IV
-
PROCRÉATION ET EMBRYOLOGIE
CHAPITRE
PREMIER
Interdiction de clonage reproductif
Article 15
Interdiction du clonage reproductif
Objet : Cet article interdit explicitement tout procédé susceptible de conduire à un clonage reproductif de l'être humain.
I - Le dispositif proposé
Le présent article prévoit l'inscription, au deuxième alinéa de l'article 16-4 du code civil, l'interdiction expresse du clonage reproductif.
Cette opération est décrite comme « le fait de faire naître, ou de développer un embryon, qui ne serait pas directement issu des gamètes d'un homme et d'une femme ».
L'Assemblée nationale a adopté cet article sans modification.
II - La position de votre commission
Votre rapporteur tentera de simplifier cette question difficile en répondant à cinq questions.
Qu'est ce que le clonage reproductif ?
MM. Claude Huriet et Alain Claeys, dans le rapport de l'OPESCT consacré au clonage, à la thérapie cellulaire et à l'utilisation thérapeutique des cellules embryonnaires, ont défini le clonage avec une grande rigueur scientifique. Le clonage 66 ( * ) « est la production asexuée, à partir d'une cellule ou d'un organisme, d'entités biologiques génétiquement identiques à cette cellule ou à cet organisme. Il s'agit donc ici d'une reproduction et non d'une procréation qui « se ramène, au niveau cellulaire, à l'alliance au sein de l'élément féminin de deux moitiés aléatoires de l'ADN, chacune spécifique d'un des membres du couple ».
Deux procédés sont utilisables pour parvenir à ce résultat. Le clonage par scission d'embryon et le clonage par transfert cellulaire. Si le second est le plus connu parce qu'il nourrit les fantasmes collectifs les plus courants, le premier est en réalité le plus facile à réaliser.
|
Le clonage par scission d'embryon est le plus facile à mettre en oeuvre et, sans doute, le plus efficace . Il consiste à déclencher artificiellement in vitro ce qui se produit à l'état naturel chez les mammifères en cas de gémellité vraie (jumeaux monozygotes). Lorsque l'embryon fécondé se divise en deux cellules, on sépare celles-ci de façon que chacune d'elles produise à son tour un embryon. La scission de l'embryon de mouton ou de vache permet des taux de gestations gémellaires élevés (plus de 60 %). « Mais l'opération ne peut être renouvelée sur les demis (ou quarts) d'embryons obtenus, car les cellules qui ont été séparées se trouvent déjà engagées dans le programme de développement ». La faisabilité de cette méthode a été récemment démontrée chez le primate. L'objectif était de créer une fratrie composée d'animaux parfaitement identiques pouvant servir de modèles de maladies ou de cobayes pour l'expérimentation thérapeutique. Le clonage par transfert nucléaire consiste à introduire, dans le cytoplasme d'un ovule non fécondé dont on a retiré le matériel nucléaire, le noyau d'une cellule provenant d'un embryon, d'un foetus ou d'un organisme adulte. On cherche à leurrer le cytoplasme de l'ovocyte qui tente alors d'organiser le nouveau noyau pour lui redonner ses caractéristiques embryonnaires. Cela étant, on peut utiliser des cellules embryonnaires à un stade où elles sont encore peu différenciées (embryon de 32 à 64 cellules). Il est alors théoriquement possible de reproduire un embryon en autant d'exemplaires qu'il compte de cellules pourvoyeuses de noyaux. L'utilisation de cellules déjà différenciées prélevées sur un individu adulte permet de disposer d'une source illimitée de noyaux. Une simple biopsie de quelques millimètres carrés suffit pour fournir plusieurs milliers de cellules. Mais l'opération est alors plus aléatoire car l'activité de ces noyaux doit nécessairement être reprogrammée pour leur faire acquérir les caractéristiques de noyaux d'embryon. Source : rapport de l'OPECST précité p. 14. |
Le clonage reproductif viserait à utiliser l'une ou l'autre de cette technique pour laisser se développer un embryon et donner naissance à un être qui serait reproduit de manière non sexuée.
Le clonage reproductif est-il une pratique condamnable ?
La création d'un être humain de manière asexuée remet fondamentalement en cause le principe même d'humanité, puisque l'identité et l'unicité de l'être sont mises en cause. Aussi se trouve-t-il un consensus pour que cette pratique soit condamnée.
Le Comité national consultatif d'éthique dans son avis n° 54 du 22 avril 1997 avait en effet rappelé que « si le fait d'avoir même génome n'entraîne nullement que deux individus aient aussi même psychisme, le clonage reproductif n'en inaugurerait pas moins un bouleversement fondamental de la relation entre identité génétique et identité personnelle dans ses dimensions biologiques et culturelles. Le caractère unique de chaque être humain, dans quoi l'autonomie et la dignité de la personne trouvent support, est exprimé de façon immédiate par l'unicité d'apparence d'un corps et d'un visage, laquelle résulte de l'unicité du génome de chacun. On peut se représenter au contraire vers quelle réalité sociale nous orienterait une production de clones qui ne serait plus de hasard ni d'exception, et n'exclurait d'ailleurs plus les décalages dans le temps. Etres humains psychiquement individualisés comme des personnes singulières malgré leur similitude génétique, ils seraient cependant vus -au sens propre et figuré- comme des répliques à l'identique les uns des autres et de l'individu cloné dont ils seraient effectivement la copie. Ainsi serait minée la valeur symbolique du corps et du visage humains comme supports de la personne dans son unicité. A la différence de Dolly, des clones humains sauraient qu'ils sont des clones ; ils se sauraient aussi reconnus tels par autrui. Comment ne pas voir l'intolérable chosification de la personne que recèlerait une telle situation ? »
Au niveau international, plusieurs pays européens ont déjà adopté dans leur législation interne une disposition interdisant formellement le clonage reproductif.
Plusieurs organisations internationales ont, dans leur déclaration, banni le clonage reproductif : l'Organisation mondiale de la santé (OMS), dans sa déclaration du 11 mars 1997, le Conseil de l'Europe en janvier 1998 par la signature du protocole additionnel à la Convention d'Oviedo consacré à cette question. On peut également déduire du contenu de sa déclaration des droits fondamentaux que l'Union européenne prohibe une telle pratique.
L'interdiction mondiale du clonage, par l'ONU, est en cours d'examen.
Le clonage est-il déjà interdit par le droit français ?
Aujourd'hui, aucune disposition du droit français ne prohibe explicitement une telle pratique. Toutefois, il est couramment admis que les dispositions protégeant, au sein du code civil, l'intégrité de l'être humain ne permettent pas le recours à une telle dérive.
Le Conseil d'Etat rappelle, dans son rapport, la portée de l'article 16-4 du code civil ( cf. exposé général du présent rapport )
Quelle rédaction pour l'interdiction du clonage ?
S'il y a accord, sur la nécessité de prévoir explicitement cette interdiction dans le droit français, demeure l'interrogation de trouver sa meilleure rédaction.
Sur cet aspect, deux versions s'affrontent.
Les premiers s'accordent à insister sur la nécessité de définir cette interdiction comme une « intervention ayant pour but de faire naître un enfant ou de faire se développer un embryon humain dont le génome serait identique à celui d'un autre être humain vivant ou décédé » . C'est la rédaction proposée par le Conseil d'Etat. Cette rédaction est aussi celle du protocole additionnel à la Convention d'Oviedo, signé à Paris le 12 janvier 2001.
|
Est interdite toute intervention ayant pour but de créer un être humain génétiquement identique à un autre être humain vivant ou mort.
Au sens du présent article, l'expression être
humain « génétiquement identique » à
un autre être humain signifie un être humain ayant en commun avec
un autre l'ensemble des gènes nucléaires.
|
Cette définition est sans doute la plus significative en ce qu'elle définit le crime moral que décrivait le Comité d'éthique. Elle a en outre le mérite d'être une rédaction qui fait référence au niveau international.
C'est toutefois la plus fragile sur le plan scientifique et ce faisant sur le plan juridique. En effet, ainsi qu'insiste le rapporteur de l'Assemblée nationale, « cette définition paraît insuffisante dans la mesure où de récents travaux scientifiques démontrent le rôle du milieu de culture dans lequel se développe l'embryon, et surtout l'importance du cytoplasme dans le développement de ce dernier, ainsi que l'indiquait, devant la mission d'information, M. Jean-Paul Renard, lors de son audition du 12 juillet 2000 ».
« De fait, il est désormais scientifiquement prouvé que le cytoplasme ovocytaire intervient dans la formation de l'embryon, d'une part, en activant la division cellulaire de celui-ci et la reprogrammation du génome nucléaire par le biais des systèmes biochimiques contenus dans le cytoplasme et, d'autre part, en produisant l'énergie nécessaire à la cellule grâce à ses mitochondries qui sont dotées de leur propre génome. En conséquence, il ne peut y avoir d'individus ni de cellules issus d'un transfert de noyau dans un ovule énucléé, qui soient la copie génétique parfaite de la cellule transférée. M. Jean-Paul Renard indiquait ainsi, devant la mission d'information qu'« en biologie, la « photocopie » n'existe pas. Même les jumeaux monozygotes dits « jumeaux vrais » sont différents. Ainsi, l'être humain qui serait créé au moyen de la technique du clonage reproductif ne serait pas totalement identique génétiquement à l'être dont il serait le clone. La définition proposée par le Conseil d'Etat ne serait donc pas opérante ». 67 ( * )
La rédaction proposée par le présent article est sans doute plus proche de la réalité scientifique du clonage reproductif, définissant celui-ci comme un mode de reproduction asexué.
Aussi, en l'état actuel du débat, votre commission ne saurait trancher d'autorité entre la rédaction du protocole de Paris et la rédaction proposée par le projet initial.
Comment punir le clonage ?
Reste la question d'une sanction adaptée au crime que constitue la transgression de cette interdiction. Le présent projet de loi, à l'article 21 (cf. commentaire ci-après) , la réprime d'une peine de réclusion de vingt ans et l'extraterritorialité. Cette peine est-elle suffisante ?
Votre commission ne dispose pas d'une capacité d'appréciation du droit pénal identique à votre commission des Lois. Aussi a-t-elle choisi pour l'instant de ne pas modifier le dispositif en vigueur.
Pour autant, lors de son audition par votre commission, M. Jean-François Mattei avait préconisé la création d'un crime d'une catégorie nouvelle, celle de crime contre la dignité de l'homme (cf. commentaire de l'article 21 ci-après) .
Votre commission partage pleinement la préoccupation ainsi exprimée et votre rapporteur lui proposera, le moment venu, d'approuver l'initiative solennelle annoncée par le Gouvernement.
Sous le bénéfice de ces observations et dans cette attente, votre commission vous propose d'adopter cet article sans modification.
Article additionnel après l'article 15
Rapport sur les
initiatives françaises en faveur d'une législation internationale
réprimant le clonage reproductif
Objet : Cet article additionnel reprend, dans le chapitre consacré au clonage reproductif, les dispositions introduites par l'Assemblée nationale à l'article 21 bis (nouveau).
I - Le dispositif proposé
Le présent article additionnel qu'il est proposé d'insérer après l'article 15 reprend les dispositions prévues par l'article 21 bis nouveau, ce dernier étant, par cohérence, supprimé.
Il prévoit que, dans un délai d'un an, le Gouvernement remettra au Parlement un rapport sur les initiatives prises au niveau international pour faire adopter une législation réprimant le clonage reproductif.
II - La position de votre commission
Ainsi qu'il l'a développé à l'article précédent, votre rapporteur soutient les efforts entrepris par le Gouvernement pour faire adopter au niveau mondial un corpus contraignant en matière de clonage reproductif.
La France et l'Allemagne ont déjà formulé à l'ONU des propositions en ce sens 68 ( * ) .
Il semble qu'une question fasse l'objet d'un débat interne au sein de l'Organisation mondiale : peut-on interdire le clonage reproductif sans interdire le clonage thérapeutique ?
Le rapport du comité spécial, chargé des travaux préliminaires en vue de l'élaboration d'une convention internationale contre le clonage d'êtres humains à des fins de reproduction 69 ( * ) , précise, pour sa part, dans le compte rendu de ses travaux, qu'une telle distinction est difficile à établir.
« Pour ce qui est de l'étendue de la convention proposée, on a émis l'avis que le mandat du comité spécial n'était pas limité à une interdiction du clonage d'êtres humains à des fins de reproduction. Au contraire, le comité avait pour tâche d'examiner l'élaboration du mandat de la convention proposée. Ainsi, la résolution 56/93 de l'assemblée générale ne pouvait être considérée comme déterminant à l'avance la portée de la convention.
« En outre, on a exprimé l'idée qu'on ne pouvait véritablement contrecarrer la possibilité d'un clonage d'êtres humains à des fins de reproduction sans aborder la question du clonage thérapeutique, et que la portée de la convention proposée devait en tenir compte. On a donc proposé que toute interdiction porte sur le processus du clonage lui-même et non pas seulement sur le résultat final de celui-ci. On a également fait observer qu'en excluant le clonage thérapeutique, la communauté internationale risquait de laisser entendre qu'un tel clonage était susceptible d'être permis. On a en outre déclaré qu'une interdiction partielle, ne couvrant que le clonage à des fins de reproduction, serait une fausse interdiction et, en pratique, serait inefficace. »
A ce stade, votre rapporteur doit préciser trois points fondamentaux :
1°) La distinction en soi des deux clonages est inappropriée pour des raisons qu'il précise tant dans l'exposé général que dans son commentaire de l'article 19.
2°) Pour autant, la sanction ne saurait être la même dans les deux cas. A l'évidence, ce n'est que dans le premier cas que l'atteinte à la dignité de l'homme est constituée.
3°) Il doit être entendu que la nécessité d'introduire cette interdiction au niveau mondial est une urgence expresse que les événements récents ont soulignée. La recherche d'une interdiction globale du clonage, qui ne rassemble pas aujourd'hui de consensus, s'apparente en réalité à une manoeuvre dilatoire pour « gagner du temps », ainsi que l'ont, à juste titre, rappelé la France et l'Allemagne.
En l'état, votre rapporteur qui propose l'interdiction du clonage thérapeutique, en droit interne, préconise également que le Gouvernement, pour que les efforts ne soient ni vains, ni dispersés, mette tout en oeuvre pour que soit obtenue l'interdiction au niveau mondial de la pratique du clonage reproductif.
Sous le bénéfice de ces observations, votre commission vous propose d'adopter un amendement insérant cet article additionnel.
CHAPITRE II
AGENCE DE LA PROCRÉATION, DE L'EMBRYOLOGIE ET DE LA
GÉNÉTIQUE HUMAINES
Article 16
Agence de la procréation, de l'embryologie
et de la
génétique humaines
Objet : Cet article crée une Agence de la procréation, de l'embryologie et de la génétique humaine et précise son statut et ses missions.
I - Le dispositif proposé
Le I du présent article propose de créer un nouveau chapitre VII au sein du titre premier du livre IV de la première partie du code de la santé publique.
Ce chapitre nouveau est composé de huit articles nouveaux, numérotés de L. 1417-1 à L. 1417-8, qui prévoient la création d'une nouvelle Agence de la procréation, de l'embryologie et de la génétique humaine (APEGH).
Article L. 1417-1 du code de la santé publique
Cet article prévoit les missions de la nouvelle Agence, établissement public placé sous la tutelle des ministres en charge de la santé et de la recherche. Elles sont au nombre de trois :
- participer à l'élaboration des règles et au suivi du domaine de l'AMP, du diagnostic prénatal ou du diagnostic biologique. Elle participe également à l'élaboration des règles, au suivi et à l'évaluation des activités médicales et scientifiques en ce qui concerne la génétique humaine (1° de cet article) ;
- évaluer les protocoles de recherche sur l'embryon in vitro , les cellules embryonnaires ou foetales (2° de cet article) ;
- assurer une veille sur le développement des connaissances et des techniques et formuler au Gouvernement des propositions sur les sujets de sa compétence (3° de cet article) .
Article L. 1417-2 du code de la santé publique
Cet article prévoit que l'Agence est dotée d'un Haut Conseil.
Ce Haut Conseil rassemble des membres du Parlement, du Conseil d'Etat, de la Cour de cassation et du Comité national consultatif d'éthique (CNCE), des représentants d'usagers du système de santé et des associations de malades. Il comprend, en outre, des personnalités qualifiées désignées par les ministres chargés de la santé et de la recherche, d'une part, et par le Président de la République et les présidents des assemblées, d'autre part.
Article L. 1417-3 du code de la santé publique
Cet article précise les missions du Haut Conseil.
Il est chargé, en premier lieu, d'évaluer les protocoles et d'assurer la veille prévus aux 2° et 3° de l'article L. 1417-1 susmentionné.
Il est, en outre, chargé de rédiger un rapport scientifique remis au Parlement, au Gouvernement et au CNCE, qui est, de même que ses avis, rendu public.
Article L. 1417-4 du code de la santé publique
Cet article prévoit, pour le Haut Conseil, la faculté de saisir le Comité consultatif national d'éthique et d'être consulté, à son tour, sur le sujet de sa compétence par ce Comité.
Article L. 1417-5 du code de la santé publique
Cet article prévoit le régime administratif de l'Agence. Ce régime est de droit public, comparable à ceux des autres agences du secteur sanitaire. Les personnels de l'Agence sont les fonctionnaires d'Etat, des collectivités locales ou des praticiens hospitaliers en activité, mis à disposition ou détachés. L'Agence peut, en outre, faire appel à des personnels contractuels de droit public (troisième alinéa) et, pour des fonctions scientifiques ou techniques, à des agents de droit privé. Les dispositions de non-cumul de fonctions et de rémunérations ne seront pas opposables à ces derniers, ce qui permettra à l'Agence de recruter des personnels spécialisés et hautement qualifiés (quatrième alinéa).
Article L. 1417-6 du code de la santé publique
Cet article propose que les ressources de l'APEGH soient constituées de subventions de l'Etat ainsi que de produits divers, dons et legs.
Article L. 1417-7 du code de la santé publique
Le premier alinéa de cet article prévoit le régime des règles déontologiques applicables au personnel de l'Agence ainsi qu'aux membres du Haut Conseil.
Il leur est ainsi interdit d'entretenir des intérêts, directs ou indirects, avec des établissements ou entreprises en relation avec l'Agence, de nature à compromettre leur indépendance.
En outre, cet article prévoit que les collaborateurs occasionnels sont :
- tenus aux règles de discrétion et de secret professionnel ;
- soumis aux dispositions de la loi n° 93-122 du 29 janvier 1993, en vertu de laquelle ils devront consulter une commission de déontologie chargée d'apprécier la compatibilité entre leur fonctions à l'APEGH et celles qu'ils souhaiteraient exercer dans le secteur privé ;
- interdits de recevoir des avantages en espèces ou en nature dans le cadre de leurs fonctions au sein de l'Agence.
Le sixième alinéa proposé pour cet article prévoit une impossibilité de siéger au sein du Haut Conseil ou des commissions de l'Agence en cas de risque de conflit d'intérêts.
Le dernier alinéa prévoit qu'en cas de manquement aux règles ainsi édictées, l' « autorité compétente » peut mettre fin aux fonctions des « personnes contrevenantes » .
Article L. 1417-8 du code de la santé publique
L'article L. 1417-8 prévoit que les modalités d'application seront déterminées par décret en Conseil d'Etat.
Le II de cet article est de conséquence ; la création de l'APEGH rendant superfétatoire son existence, la Commission nationale de la médecine et de la biologie de la reproduction et du diagnostic prénatal (CNMBRDP) est supprimée et le chapitre III du titre premier de la deuxième partie du code de la santé publique, où ses missions et composition sont précisées, est abrogé.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a modifié substantiellement cet article au moyen de 19 amendements adoptés, pour 18 d'entre eux, sur l'initiative de sa commission spéciale et, pour l'un d'entre eux, sur proposition de M. Jean-Michel Dubernard.
La refonte des missions de l'Agence
A l'initiative de sa commission spéciale, l'Assemblée nationale a modifié les missions de l'Agence.
Dans cette nouvelle version, l'APEGH aura pour mission :
- d'évaluer et de suivre les activités médicales et biologiques qui relèvent de sa compétence ;
- de se prononcer pour avis sur les demandes d'autorisation et les décisions de retrait d'autorisation des laboratoires concernés par les activités ;
- de contribuer à l'élaboration des règles de bonnes pratiques ;
- d'autoriser les protocoles de recherche sur l'embryon, les cellules foetales ou les nouvelles techniques d'AMP ;
- d'assurer une information permanente du Parlement.
De toutes les missions assignées par l'Assemblée nationale à l'APEGH, l'une d'entre elles change véritablement la philosophie du dispositif initial. En effet, sous la réserve d'un pouvoir de veto ministériel (prévu à l'article 19) , le pouvoir décisionnel d'autoriser les protocoles de recherche sur l'embryon appartiendra à l'Agence et non plus au pouvoir politique.
La création d'un conseil d'administration
Par la création d'un article L. 1417-1-1, l'Assemblée nationale a doté l'APEGH d'un conseil d'administration composé pour moitié de représentants de l'Etat et pour l'autre moitié de personnalités qualifiées et de représentants du personnel.
Il est proposé que son président et son directeur général soient nommés par décret.
Le dernier alinéa prévoit, en outre, que le directeur général prend au nom de l'Etat les décisions relevant de l'Agence. Cette disposition, combinée avec la redéfinition des missions de l'Agence et de celles de son Haut Conseil, aboutit à une position forte : le directeur général de l'APEGH, fonctionnaire nommé par décret aura compétence pour autoriser ou ne pas autoriser les protocoles de recherches susmentionnés.
La dilution du Haut Conseil
En modifiant les articles L. 1417-2 et L. 1417-3 proposés par cet article, l'Assemblée nationale a :
- d'une part, accentué le caractère pléthorique du Haut Conseil qui ne comprendrait pas moins de vingt membres. Le nombre des personnalités déjà prévu a été précisé. Il a été prévu deux nouveaux membres, l'un issu de la Commission nationale consultative des droits de l'homme et l'autre du Conseil économique et social, tandis que la composition du Haut Conseil s'est vu assigner un objectif de « représentation équilibrée d'hommes et de femmes » ;
- d'autre part, dilué ses prérogatives en prévoyant que « l'Agence » et non plus le « Haut Conseil » établit le rapport d'activité de l'APEGH qui fait mention des avis délivrés par ce dernier. Or, la modification introduite a supprimé la référence initiale à l'évaluation initiale par le Haut Conseil des protocoles de recherche.
En outre, sur proposition de M. Jean-Michel Dubernard, l'Assemblée nationale a précisé les liens entre l'Agence et le Parlement, le dernier alinéa proposé par cet article pour l'article L. 1417-3 du code de la santé publique prévoyant en effet une faculté de saisine de l'APEGH ou de son Haut Conseil par le président de chaque Assemblée ainsi que l'examen par les commissions compétentes de ces dernières du rapport annuel de l'Agence.
Enfin, l'Assemblée nationale a supprimé la référence au devoir de « discrétion professionnelle » ; s'impose seule, au personnel de l'Agence, la notion de « secret professionnel ».
III - La position de votre commission
La genèse de l'Agence
L'évaluation et le contrôle du domaine de l'Assistance médicale à la procréation, qui reposent en partie sur la CNMBRDP, ont fait l'objet de critiques croissantes. Cette commission, dans son rapport de 1996, mettait d'elle-même en évidence les faiblesses de l'appareil d'Etat en matière de santé, faiblesses qui entravent sa mission : mauvaise qualité des dossiers, insuffisance, d'une part, des vérifications préalables des DDASS et, d'autre part, des informations complémentaires fournies par les médecins inspecteurs de santé publique.
Réalisées à l'occasion de l'évaluation de la loi n° 94-654 du 29 juillet 1994, les auditions de l'OPESCT 70 ( * ) ne révèlent pas autre chose. Les auteurs du rapport soulignent « les observations de la CNMBRDP concordent avec les constats très critiques recueillis au cours de nos auditions : les médecins-inspecteurs sont en nombre insuffisant et accaparés par une multitude de tâches techniques. La DDASS de Paris , par exemple, ne compte qu'un emploi de médecin à temps plein pour 45 sites à contrôler ; ils ne disposent pas d'une formation spécifique leur permettant d'effectuer une analyse critique des bilans d'activité des centres. En l'absence d'indicateurs fiables permettant d'éliminer les incidences de la « course aux résultats », l'exactitude des résultats affichés ne peut donc être vérifiée alors que le public ne dispose en ce domaine, comme l'a souligné Jacques Testart, d'aucune information sérieuse. La complexité du contrôle nécessiterait l'établissement d'un guide d'inspection. Un projet élaboré par la DDASS de Paris n'a pas été validé par la Direction générale de la santé. Le ministère de la Santé préconise une spécialisation et une mutualisation des moyens à l'échelon régional mais les ressources budgétaires font actuellement défaut pour y parvenir » .
D'elle-même donc, la Commission nationale soulignait l'insuffisance des moyens dont elle disposait pour assurer ce suivi, les rapports d'activité devant être évalués par des contrôles sur pièces et sur place. Le rapport de l'OPESCT rappelle les propos du président de cette Commission pour qui les missions dévolues à l'Agence contrastent avec les moyens dont elle dispose.
Pour le Conseil d'Etat, la Commission n'a certes pu remplir la mission que la loi lui confiait mais, « en l'état actuel de son champ d'intervention et de ses responsabilités, ces critiques apparaissent excessives. En effet, c'est le ministre qui accorde les autorisations et les agréments, et c'est l'administration qui est responsable du suivi des activités d'AMP» .
Toutefois, le Conseil ajoutait 71 ( * ) que « si l'on estime, d'une part, que l'amélioration du contrôle des activités d'AMP constitue aujourd'hui une priorité, et si, d'autre part, on autorise sous des conditions strictes la recherche sur l'embryon, il apparaît nécessaire de revoir les missions de la CNMBRDP ».
L'évolution de l'AMP et l'éventualité d'une ouverture des recherches sur l'embryon humain rendaient plausible la création d'une Agence plus à même d'exercer l'important pouvoir d'évaluation et de contrôle que la loi lui confierait.
|
Conçue comme un office spécifique ou un sous-ensemble de l'Etablissement français des greffes, cette structure devrait disposer de l'autonomie et des moyens qui font défaut à la CNMBRDP : - elle exercerait les missions actuellement dévolues à cette dernière pour l'agrément des établissements et des praticiens avec des moyens renforcés d'inspection et d'expertise ; - elle évaluerait l'activité d'AMP, non pas seulement d'un point de vue quantitatif, mais sous l'angle des conséquences des actes accomplis, de la qualité des pratiques et de leurs répercussions sociales ; - elle favoriserait et démocratiserait la réflexion dans le domaine de l'AMP, prenant modèle ici encore sur les consultations nationales organisées en Grande-Bretagne par la HFEA ; - elle mènerait, en direction des personnes touchées par le problème de la stérilité mais aussi du grand public, des actions d'information sur l'évolution des connaissances et des pratiques, les causes et les effets de la stérilité, les conséquences des traitements ; - elle élaborerait les règles de bonne pratique, développerait l'assurance qualité et organiserait la formation des praticiens. Source, rapport OPESCT, p. 149 |
De fait, le présent article propose la création d'une Agence de la procréation, de la génétique et de l'embryologie (APEGH). L'Assemblée nationale a fortement rapproché le dispositif initial de celui que M. Jouannet appelait de ses voeux (cf. ci-dessus).
Les évolutions possibles : vers une Agence de la biomédecine ?
Lors de son audition par votre commission 72 ( * ) , M. Jean-François Mattei s'est déclaré sceptique à l'idée de la création d'une nouvelle Agence, du fait du nombre déjà élevé des agences exerçant des compétences dans le domaine sanitaire.
« Cette Agence me paraissait mal composée et un peu anormale quant aux compétences qu'on voulait lui attribuer. J'ai dans l'idée de vous proposer une architecture et des compétences différentes ».
Il a formulé la proposition d'une refonte du paysage des agences sanitaires en deux temps.
« Pour tout dire, mon idéal -mais je ne pense pas que nous pourrons l'atteindre tout de suite- aurait été de regrouper l'AFSSAPS, l'Etablissement français des greffes et l'APEGH dans une grande Agence de biomédecine et de produits de santé.
« On aurait une grande cohérence avec cinq départements ayant une autonomie et une spécificité particulières : les trois départements de l'AFSSAPS -le médicament, les dispositifs et le sang- le département de transplantation des greffes et le département correspondant à l'embryon, à la reproduction et aux cellules, dont nous sommes en train de parler ».
Cela étant, les difficultés techniques et juridiques qui sous-tendent la mise en oeuvre d'un tel regroupement semblent difficilement réalisables d'emblée. Aussi le ministre a-t-il préféré proposer de « faire les choses en deux temps avec, dans un premier temps, une agence qui rassemblerait l'Etablissement français des greffes et l'APEGH en gardant l'AFSSAPS en l'état, la mission de cette nouvelle agence se justifiant parce qu'il y a un continuum absolu entre organe, tissu, cellule, gène. Vouloir faire passer la barrière de façon artificielle n'est pas cohérent » .
En effet, pour le ministre, « regrouper l'Etablissement français des greffes et l'APEGH (...) paraît donc être d'une logique imparable, étant entendu que l'idéal à deux ans serait de préparer le rapprochement de l'AFSSAPS et de cette nouvelle agence, que j'appellerais volontiers, après fusion, si vous en étiez d'accord, l'Agence de biomédecine car, en définitive, c'est bien de biomédecine qu'il s'agit.
« Quand nous faisons de la transplantation d'organes, nous transmettons des organes vivants : c'est de la biomédecine. Quand nous faisons de la thérapie cellulaire, que nous donnons la vie in vitro, c'est aussi de la biomédecine. On aurait donc là une grande agence de médecine, qui pourrait ensuite, se mariant à l'AFSSAPS, devenir agence de biomédecine et des produits de santé. »
Votre commission souscrit à la proposition faite par le ministre d'une telle fusion et votre rapporteur proposera d'approuver les amendements du Gouvernement ainsi annoncés.
Les propositions que votre commission formule dans le cadre actuel de l'APEGH restent pertinentes dans l'hypothèse de la création d'une Agence de la biomédecine , sous réserve d'adaptations formelles.
Les propositions de votre commission
Votre rapporteur estime que l'équilibre recherché par l'Assemblée nationale n'est pas entièrement satisfaisant. En effet, à l'initiative de sa commission spéciale, les compétences de l'agence ont été considérablement renforcées. Elles incluent un pouvoir décisionnel de plein exercice sur l'évaluation des protocoles de recherche consacrés aux embryons ou aux cellules foetales. Ce pouvoir est exercé par le directeur général et lui seul, avec comme seule sauvegarde le veto conjoint des ministres de la santé et de la recherche.
Dans le même temps, le Haut Conseil a été vidé de sa substance, par l'élargissement de sa composition et la réduction de ses prérogatives, qui sont devenues, en vérité, très floues.
Votre commission n'est pas défavorable à l'orientation donnée d'un renforcement des pouvoirs de l'Agence, et notamment ses compétences décisionnelles mais estime, à l'instar de M. Jean François Mattei, qu'il faut que ce pouvoir d'autorisation, de contrôle, d'inspection, soit contrebalancé par une composition de ses organes qui n'aboutisse pas en droit ou en fait à ce que les scientifiques disposent seuls du pouvoir.
Aussi votre commission vous propose-t-elle une série d' amendements qui tendent en premier lieu à substituer au Haut Conseil un Conseil d'orientation médical et scientifique dont les attributions sont précisées et la composition revue en conséquence.
Ce conseil ne comprendra plus, en effet, que dix-sept membres dont dix personnalités scientifiques et sept membres exprimant des préoccupations relevant davantage de la « société civile ». La présence d'un membre du Comité national consultatif d'éthique et de la Commission nationale consultative des droits de l'Homme garantit ainsi la dimension éthique de la réflexion du conseil d'orientation. La présence d'un membre du Conseil d'Etat et d'un conseiller à la Cour de cassation favorise, quant à elle, la pertinence de ses raisonnements juridiques. Enfin, celle de deux parlementaires assure que l'analyse des protocoles se fait véritablement en conformité avec la volonté du législateur.
La composition du conseil d'administration est également revue. Aux « représentants de l'Etat » qui constituent la moitié des membres dans la rédaction adoptée par l'Assemblée nationale, votre commission substitue une représentation plus fine et plus diversifiée : représentants des ministères, chargés de la santé, de la justice et de la recherche ainsi que de la CNAMTS, des établissements publics administratifs à caractère sanitaire et des établissements publics de recherche.
Le contenu du rapport de l'Agence est précisé afin qu'une information claire et précise du Parlement, en matière de recherche sur l'embryon, soit assurée. Ce rapport, qui sera rendu public, comportera les avis formulés par le Conseil d'orientation médical et scientifique.
Compte tenu du nouveau dispositif, votre commission vous propose en outre de prévoir que les associations représentant les malades et les usagers du système de santé puissent saisir l'Agence.
Votre commission vous propose d'adopter cet article ainsi amendé .
CHAPITRE III
Diagnostic prénatal et assistance médicale
à la procréation
Article 17
(art. L. 2131-1, L. 2131-3 à L. 2131-5 du
code de la santé publique)
Diagnostics prénatal et
préimplantatoire
Objet : Cet article actualise le régime applicable aux diagnostic prénatal et préimplantatoire pour tenir compte, notamment, de la création de la nouvelle Agence de la procréation, de l'embryologie et de la génétique humaine.
I - Le dispositif proposé
Le dispositif proposé par le présent article vise à préciser le régime juridique du diagnostic prénatal (DPN) (1°, 2° et 4°) et du diagnostic préimplantatoire (DPI°) (3°).
Le 1° modifie l'article L. 2131-1 du code de la santé publique relatif au diagnostic prénatal.
La « consultation médicale de conseil génétique » prévue à cet article est remplacée par la notion plus large de « consultation médicale adaptée à l'affection recherchée » [ a) du 1°]. En outre, les établissements pratiquant les analyses de cytogénétique ou de biologie en vue de DPN devront désormais faire figurer, sur l'autorisation d'exercice qui leur est délivrée pour cinq ans, le nom des praticiens habilités à mettre en oeuvre ces analyses [ b) du 1°].
Ainsi, cet article prévoit un système de double autorisation pour l'établissement et le praticien. S'il arrive qu'un praticien quitte un établissement pour un autre, il ne pourra y pratiquer ces analyses sauf si l'établissement obtient une nouvelle autorisation mentionnant son nom. De même, si l'établissement ne dispose pas de la collaboration de praticiens « mentionnés » par son autorisation, il ne pourra plus réaliser ce type d'analyse.
Cette avancée ne devrait toutefois pas poser de difficultés d'organisation auxdits établissements et praticiens puisque cette règle de « double autorisation » est déjà prévue par les dispositions du décret du 6 mai 1995, auxquelles le présent article donne force de loi.
Le c) du 1° supprime l'avis de la Commission nationale de médecine et de biologie de la reproduction et du diagnostic prénatal (CNMBRDP) ainsi que celui du Comité national d'organisation sanitaire et sociale (CNOSS) accompagnant la délivrance des autorisations susmentionnées.
Le 2° ajoute une nouvelle condition de retrait des autorisations délivrées. Le texte en vigueur prévoyant déjà pour motif la violation des réglementations, sont introduites les notions de volume d'activité et de résultats. Ce principe, déjà appliqué pour certains services de maternité 73 ( * ) , est appliqué en fonction des résultats analysés au travers du bilan annuel d'activité.
Le 3° prévoit, par coordination avec la création de l'APEGH, le remplacement de la référence à la CNMBRDP, pour les autorisations relatives au diagnostic préimplantatoire. Ainsi que le relève le rapporteur de l'Assemblée nationale 74 ( * ) , « En premier lieu, on ne peut que relever le manque de cohérence interne du présent article qui prévoit, dans son 3°, de modifier l'article L. 2131-4 du code de la santé publique afin de substituer à l'avis de la CNMBRDP sur les demandes d'autorisation concernant la DPI, l'avis de la future APEGH sans retenir cette solution pour le DPN. On comprend difficilement pourquoi cette différence de traitement serait introduite entre les demandes d'autorisation relatives aux activités de DPN et celles relatives au DPI. Pourquoi considérer, en effet, que la future agence doit intervenir pour donner son avis sur les demandes d'agrément de DPI mais non pour celles relatives au DPN alors même que le présent projet de loi lui donne pour mission de « contribuer à l'élaboration des règles, au suivi et à l'évaluation des activités de diagnostic, de soin et de recherche » dans les domaines de l'AMP, du DPN et du DPI ? »
Le 4° renvoie à un décret en Conseil d'Etat en modifiant le 2° de l'article L. 2131-5 du code de la santé publique, le soin de définir la nature des analyses de cytogénétique et de biologie prénatale soumise à autorisation.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a modifié cet article à quatre reprises.
Sur proposition de sa commission spéciale, elle a adopté un amendement, sous-amendé par le Gouvernement, qui prévoit que l'APEGH sera compétent pour se prononcer sur les décisions de retrait d'autorisation d'exercice des activités de DPN, ainsi qu'un amendement confiant à l'APEGH le rôle de formuler l'avis préalable à l'autorisation délivrée aux centres de DPN.
Sur proposition de M. Jean-François Mattei, elle a adopté un amendement prévoyant une extension de l'indication de DPI aux couples dont l'un des ascendants est victime de la maladie de Huntington.
Sur proposition de sa commission spéciale, elle a en outre adopté un amendement rédactionnel.
III - La position de votre commission
Votre rapporteur procèdera ici à un bref rappel des deux notions de DPI et DPN avant d'aborder deux enjeux de ces diagnostics évoqués par des personnalités lors de leur audition par votre commission.
Le DPN s'entend des examens médicaux mis en oeuvre pour détecter intra utero chez l'embryon ou le foetus une affection d'une particulière gravité.
Ainsi que le souligne le Conseil d'Etat 75 ( * ) , « la pratique actuelle du DPN fait l'objet d'un débat dans la mesure où les connaissances en matière de diagnostic ont rapidement progressé alors que les traitements des maladies que le DPN permet de diagnostiquer sont limités ou n'existent pas encore. Ce décalage place les couples face à un arbitrage cruel entre une interruption thérapeutique de grossesse et la naissance d'un enfant dont ils savent, par avance, qu'il sera atteint d'une maladie ou d'un handicap d'une particulière gravité. De manière très importante, ils font le choix d'une interruption thérapeutique de grossesse » .
Le DPI vise pour sa part à identifier avec précision des caractéristiques génétiques d'un embryon, afin que les couples porteurs de maladies génétiques graves puissent procéder au choix d'un embryon qui en soit indemne.
DPN, DPI et eugénisme
Ces deux pratiques soulèvent nécessairement des interrogations quant au risque potentiel d'une dérive eugéniste de notre société.
En effet, le DPN devenant de plus en plus précis, les parents pourraient connaître ex ante , avant même le délai limite posé pour une interruption volontaire de grossesse, une affection mineure de l'embryon et décider de recourir à une IVG pour ne pas conserver un foetus qui ne serait pas « parfait ».
Pour le Conseil d'Etat 76 ( * ) , il appartient aux pouvoirs publics de « veiller à ce que la loi qui limite le DPN à la recherche d'une affection d'une particulière gravité soit pleinement respectée et notamment que sa pratique ne puisse pas évoluer vers la recherche de pathologies ou de handicaps limités, voire de simples caractéristiques de l'enfant à naître. À ce titre, la responsabilité des équipes soignantes sera de plus en plus importante, car c'est elles qui sont en première ligne face à la demande de certains couples d'utiliser le DPN comme outil de convenance ».
De son côté, le DPI offre la possibilité d'effectuer un véritable « tri génétique » entre les embryons. Le risque est souvent évoqué d'une ouverture totale de cette pratique qui pourrait s'imposer, dans les fantasmes les plus fous comme un moyen de sélection de l'espèce.
|
« En ce qui concerne l'eugénisme, un des sénateurs de la commission faisait remarquer que le diagnostic prénatal ne constitue pas de l'eugénisme puisqu'il est librement consenti par tout le monde. Il y a là un réel problème de définition du mot eugénisme. En effet, l'eugénisme est, pour une partie du concept, la sélection des enfants à naître. L'autre partie du concept traite des moyens divers d'améliorer l'espèce humaine. Lorsqu'une femme par exemple choisit comme compagnon un bel homme dans le but de faire avec lui de beaux enfants, son choix entre parfaitement dans la définition de l'eugénisme. « On peut donc se poser la question de savoir s'il y aurait un bon et un mauvais eugénisme ou plutôt un eugénisme acceptable et un eugénisme non acceptable et quelle serait dans cette hypothèse la ligne de démarcation ? C'est un philosophe américain, Philip Kitcher, qui, par l'analyse du concept, peut nous aider dans la compréhension de ce mot complexe. Selon lui, un programme eugénique peut être envisagé et analysé selon quatre angles différents et dans chacune de ces catégories le programme peut être plus ou moins acceptable. Ces catégories sont : « - l'aspect coercitif ou non du programme ; « - l'aspect discriminatoire ou non du programme ; « - la qualité des fondements génétiques du programme ;
« - le but et l'enjeu du programme.
« En effet, lorsque l'on parle d'eugénisme, le grand public effectue souvent un rapprochement avec la médecine qu'exerçaient les médecins nazis (qui ont fait l'objet du procès de Nuremberg bis, un des fondements modernes de la bioéthique). On ne peut bien sûr pas comparer cette médecine là au diagnostic prénatal en les rangeant toutes deux sous la même bannière de l'eugénisme. Si l'on compare ces deux programmes (la médecine nazie et le diagnostic prénatal) sous chacun des angles d'analyse de Philip Kitcher, on peut dire que la médecine nazie était coercitive alors que le diagnostic prénatal ne l'est pas, qu'elle était discriminatoire, ce qui n'est pas le cas pour le diagnostic prénatal, qu'elle reposait sur un fondement génétique erroné alors que le diagnostic prénatal a des fondements génétiques scientifiquement élaborés et corrects et, enfin, que le but de la médecine nazie était d'obtenir une amélioration de la race aryenne alors que le propos du diagnostic prénatal est d'avoir des enfants en bonne santé. Les deux programmes sont eugéniques mais l'un est inacceptable, alors que l'autre (qui répond bel et bien à la définition philosophique de l'eugénisme) est parfaitement accepté par une large majorité de la société française. « On peut donc dire à mon sens qu'il y a un eugénisme acceptable et un eugénisme non acceptable et la difficulté est précisément de définir les limites que notre société accepte et de poser les valeurs qu'elle ne souhaite pas franchir ou profaner. » Audition par la commission des Affaires sociales le 4 décembre 2002 |
En réalité, les dilemmes qu'affronte le scientifique, mais également le législateur, notamment pour les indications du diagnostic préimplantatoire, relèvent de situations la plupart du temps très douloureuses.
La question du « bébé médicament »
Une application du diagnostic préimplantatoire pourrait permettre aux parents d'un enfant très malade d'isoler un embryon qui serait potentiellement compatible et du même coup sauver leur enfant.
Le professeur Arnold Munnich a fait part à votre commission des difficultés du praticien confronté à ces demandes concrètes et à une réglementation qui les légitime dans certains cas et non dans d'autres 77 ( * ) .
« Je vais vous livrer ma perception sur les demandes relatives à ce que l'on appelle, en de très mauvais termes, « l' enfant médicament », ce qui me heurte énormément. Beaucoup d'émotion a été soulevée autour du DPI et je voudrais témoigner après deux années d'activité de ces pratiques.
« Dans un certain nombre de cas, nous avons été confrontés à des demandes concernant effectivement le DPI d'une maladie génétique, l'anémie de Fanconie, assortie d'une demande d'HLA compatibilité dans la perspective d'un don de moelle ou de cordon dans l'éventualité où le premier enfant malade développerait une rechute de sa leucémie. En face de moi, les parents ont fait preuve d'une très grande maturité, d'un très grand sens des responsabilités et ne m'ont à aucun moment donné l'impression d'être des fous furieux.
« Je souhaite que les dispositions réglementaires nous autorisent à faire, non seulement le diagnostic génétique préimplantatoire de l'anémie de Fanconie, mais également à identifier parmi les embryons ceux susceptibles de devenir des enfants potentiellement donneurs de sang, de cordon ou de moelle pour aider un aîné leucémique. Cette disposition va dans le bon sens. Que l'on ne me dise pas que l'enfant va être asservi à un quelconque projet d'instrumentalisation. Pensez une seconde à ce qui attend l'enfant à naître s'il n'est pas un donneur compatible et s'il survit à son germain décédé alors qu'il aurait pu être son sauveur ! Nous sommes plus ou moins les thérapeutes de nos frères et soeurs, comme disent les psychanalystes. Au fond, je suis persuadé que l'on ne peut pas être mieux accueilli dans une famille que lorsque l'on a sauvé, en arrivant à la vie, son frère ou sa soeur. Je crois que cet enfant, loin d'être mal reçu, ne sera pas instrumentalisé. Il serait réductionniste de le considérer comme un enfant médicament, c'est plutôt un enfant sauveur, un petit « Messie ». Nous devons surtout garder les pieds sur terre puisque ces demandes sont rares. Ne nous agitons pas pour des problèmes devant s'arbitrer dans l'intimité du dialogue singulier.
« Mon problème, et je finirai par là, est bien plus délicat et douloureux lorsque des couples, dont un premier enfant présente une hémopathie maligne avec une deuxième ou troisième rechute, viennent réclamer l'assistance de la PMA pour identifier l'embryon potentiellement sauveur de son frère ou de sa soeur.
« Dans ce contexte particulier, nous sommes hors la loi. Or, il n'y a pas de risques pour l'embryon à naître lorsqu'il s'agit d'utiliser la PMA ou la HLA compatibilité. Pourtant, c'est un premier accrochage à l'esprit de la loi. C'est très difficile de dire non, croyez moi. Nous ne pouvons pas dire oui, c'est très douloureux de dire non . Dans le dialogue singulier, je vous le confesse, j'ai eu la faiblesse, monsieur le sénateur, collègue et praticien, de donner des adresses à l'étranger aux couples me demandant de recourir à la PMA. Nous ne pouvons pas rester indifférents à la souffrance de couples en larmes. Alors, je ne me suis pas cru autorisé à me substituer au Créateur et à leur dire non. Je n'ai dit ni oui, ni non, j'ai donné une adresse ».
L'Assemblée nationale a introduit une extension des indications de DPI aux couples dont l'un des membres a des ascendants victimes de la maladie de Huntington. Cette maladie terrible se transmet à 50 % des enfants d'un sujet malade. Elle commence entre 40 et 50 ans et se termine dans une déchéance psychiatrique intolérable.
Le professeur Israël Nisand s'est exprimé devant votre commission sur l'initiative prise par l'Assemblée nationale 78 ( * ) .
« Le DPI permet de repérer chez les embryons les chromosomes issus des grands-parents porteurs de la maladie et permet d'éviter de réaliser l'analyse au niveau parental.
« Cette situation se retrouve dans beaucoup de maladies à révélation tardive. La loi votée par l'Assemblée nationale, dans son article L. 2131-4, comporte dans son troisième alinéa les mots « chez l'un des parents » à la suite desquels est insérée la mention « ou l'un de ses ascendants immédiats dans le cas de la maladie de Huntington ». Je vous propose de supprimer la restriction à la maladie de Huntington car d'autres maladies à révélation tardive nous placeront dans le besoin d'analyser les chromosomes des grands-parents pour savoir ceux dont l'embryon a hérité . La situation de la maladie de Huntington devrait se produire pour d'autres maladies à révélation tardive et ne pas alors nécessiter une modification du texte de loi.
« Je rappelle à ce propos que toutes les demandes de DPI sont analysées préalablement par les centres pluridisciplinaires de diagnostic prénatal qui doivent donner leur accord après analyse du dossier. Si la maladie de Huntington est pour l'instant la seule maladie à révélation tardive, elle ne restera pas la seule et il n'y a pas de risque à laisser simplement la mention de « l'un des ascendants immédiats » sans préciser le type de maladie que l'on recherche. »
Dans cet esprit, votre rapporteur estime qu'il n'est pas opportun de viser une pathologie précise dans la loi. Aussi votre commission vous propose de substituer à celle-ci la notion de « maladie gravement invalidante, à révélation tardive et mettant prématurément en jeu le pronostic vital » .
Votre commission vous propose d'adopter cet article ainsi amendé.
Article 18
Assistance médicale à la procréation
Objet : Cet article propose de modifier le régime juridique de l'assistance médicale à la procréation .
I - Le dispositif proposé
Le I de cet article modifie le chapitre premier dans le titre IV du livre premier de la deuxième partie du code de la santé publique relatif aux dispositions générales.
Le 1° modifie les articles L. 2121-1 et L. 2141-2.
Article L. 2141-1du code de la santé publique
L'alinéa unique de l'actuel article L. 2141-1 relatif à la définition d'une AMP n'est pas modifié. Cette dernière demeure une pratique clinique ou biologique (...) permettant le procréation en dehors du cadre naturel.
A cet alinéa sont ajoutés deux alinéas supplémentaires qui prévoient le régime de la stimulation de l'ovulation :
- pour faire entrer cette pratique dans le champ d'une AMP lorsqu'elle est conduite dans le cadre de cette dernière ;
- pour préciser que les règles de prescription et de suivi des traitements d'induction sont fixées par voie réglementaire.
Article L. 2141-2 du code de la santé publique
Cet article prévoit la finalité de l'AMP. Celle-ci est de répondre à la « demande parentale d'un couple » . La nouvelle rédaction proposée élargit les conditions d'accès à cette assistance au risque de transmission d'une maladie particulière grave au sein du couple. Désormais, l'AMP est ouverte à la fois aux couples infertiles et aux couples risquant de se transmettre entre eux ou à l'enfant, une maladie d'une particulière gravité. Ainsi qu'il a été précisé dans l'exposé général, cette extension ne fait que légaliser une pratique ayant déjà une base réglementaire 79 ( * ) .
Il est en outre rappelé les conditions que doit remplir le couple pour bénéficier d'une AMP : être un homme et une femme, ce qui n'autorise pas l'AMP pour des couples homosexuels, être non pas majeur mais en âge de procréer, être marié ou en mesure de prouver au moins deux années de vie commune. Il faut en outre, évidemment, consentir préalablement aux techniques de l'AMP, soit le transfert d'embryons, soit l'insémination. Le texte proposé pour cet article par le présent projet de loi prévoit enfin que la « dissolution » du couple fait obstacle à la réalisation de l'AMP.
Le 2° proposé par cet article prévoit des renumérotations au sein de ce chapitre du code de la santé publique.
Le 3° propose une nouvelle rédaction des articles L. 2141-3 et L. 2141-4 du code de la santé publique.
Article L. 2141-3 du code de la santé publique
Le premier alinéa édicte les conditions dans lesquelles peut être créé un embryon dans le cadre d'une AMP. Cette création doit se faire obligatoirement avec les gamètes d'au moins un des deux membres du couple.
Le deuxième alinéa prévoit la congélation d'embryons en vue de la réalisation différée du projet parental. Cet alinéa prévoit en outre l'obligation d'une « information détaillée » des deux membres du couple sur le devenir possible des embryons dans le cas où ces embryons ne trouveraient pas d'utilisation dans le cadre du projet parental.
L'article est complété par un dernier alinéa qui limite la création d'embryons, en n'en permettant pas la création de nouveaux si le couple dispose encore d'embryons congelés.
Article L. 2141-4 du code de la santé publique
Cet article précise le sort de l'embryon créé in vitro . Ce dernier est intimement lié au projet parental.
Le premier alinéa reprend la teneur de l'actuel dernier alinéa de l'article L. 2141-3 ; il prévoit que les membres du couple, chaque année, sont consultés « sur le point de savoir s'ils maintiennent leur projet parental » .
Le deuxième alinéa dispose qu'en cas de réponse négative, trois alternatives s'offrent à eux pour les embryons qui ne seront, in fine , pas transférés : l'embryon est accueilli par un autre couple, il fait l'objet d'une recherche ou il est mis fin à sa conservation.
Dans le seul cas, ce qui est contestable, où le couple choisit la destruction, la demande est écrite et confirmée par écrit après un délai de réflexion de trois mois.
Le troisième alinéa prévoit que, si les membres du couple ne répondent pas, ou s'ils sont en désaccord sur le maintien du projet parental ou sur le devenir des embryons, il est mis fin à la conservation de ces derniers « si la durée de celle-ci est au moins égale à cinq ans ».
Il doit bien être compris que ce n'est qu'au bout d'un délai de cinq ans, qu'en cas de désaccord dans le couple, même survenu précocement, qu'il est mis fin à la conservation des embryons.
Le quatrième alinéa prévoit également la fin de la conservation de l'embryon lorsque ce dernier avait été l'objet d'un don en vue d'un accueil et que cet accueil n'a pas eu lieu dans un délai de cinq ans.
Le 4° prévoit une renumérotation des articles du code.
Le 5° modifie les règles entourant l'accueil de l'embryon : le a) prévoit que l'autorisation par l'autorité judiciaire, à laquelle est subordonné l'accueil de l'embryon, est de trois ans ; le b) prévoit, pour sa part, que seuls les établissements à but non lucratif pourront se livrer à des activités d'accueil.
Le 6° propose une rédaction nouvelle pour les articles L. 2141-7 et L. 2141-9 du code de la santé publique.
L'article L. 2141-7 prévoit les possibilités de recours à l'AMP avec tiers donneur.
La structure de la phrase pourrait tout d'abord laisser entendre que « L'AMP avec tiers donneur peut être mise en oeuvre (...) lorsque le couple dûment informé y renonce ». Il faut bien évidemment comprendre que l'AMP avec tiers donneur peut être mise en oeuvre lorsque le couple renonce à l'AMP au sein du couple . Ce point étant précisé, il reste que les conditions d'ouverture de l'AMP avec tiers donneur peuvent paraître paradoxales : si en effet les deux premières conditions semblent restrictives (risque de transmission d'une maladie grave ou échec de toute autre technique d'AMP) , la troisième condition, (le renoncement du couple à une AMP au sein du couple), qui n'en est pas véritablement une, affaiblit singulièrement la portée des deux premières. Il reste que la rédaction retenue, qui veut que le couple renonce après avoir été « dûment informé », renvoie implicitement, sinon juridiquement, aux risques et impossibilités qui peuvent le conduire à renoncer.
L'article L. 2141-9 prévoit le régime juridique de l'entrée et de la sortie du territoire des embryons.
Le 7° de cet article modifie les caractéristiques de l'équipe d'accueil au sein des centres d'AMP ; en effet, cette dernière cesserait d'être pluridisciplinaire pour devenir « clinico-biologique ».
Le 8° prévoit une nouvelle rédaction pour l'article L. 2141-11 du code de la santé publique, l'ancienne rédaction étant transférée et modifiée à l'article L. 2141-12.
Article L. 2141-11 du code de la santé publique
Cet article prévoit que les personnes subissant un traitement potentiellement attentatoire à leur fertilité pourront bénéficier du recueil et de la conservation de leurs gamètes. L'autorisation d'accéder à cette technique est, pour les mineurs et les majeurs sous tutelle, donnée par les titulaires de l'autorité parentale ou le tuteur. Certes, le principe d'un consentement à cette conservation est nécessaire mais il heurte celui, juridique, du parallélisme des formes puisque, pour pouvoir bénéficier d'une AMP, il suffit d'être en âge de procréer.
Article L. 2141-12 du code de la santé publique
Cet article prévoit que les modalités d'application de ce chapitre seront mises en oeuvre par un décret en Conseil d'Etat.
Le II de cet article modifie le chapitre II relatif aux conditions d'autorisation et de fonctionnement des établissements.
Le 1° ajoute à l'article L. 2142-1 relatif aux activités cliniques d'AMP la stimulation ovarienne, par cohérence avec les modifications apportées à l'article L. 2141-11.
Le 2° prévoit la suppression de la référence à la CNMBRDP et au CNOSS pour l'instruction des demandes d'autorisation des centres d'AMP pour pratiquer ces activités. A l'instar des activités de DPI et DPN, le précédent gouvernement avait prévu de régionaliser ces activités. Cette compétence sera désormais confiée aux ARH sous la direction de l'APEGH.
Le 3° prévoit, pour les centres d'AMP, la même procédure que pour les centres de DPN ( cf. article 17 ), à savoir que l'autorisation du centre devra mentionner le nom des praticiens habilités à y exercer les actes fixés par l'autorisation.
Il subordonne, en outre, la mise en oeuvre d'une fécondation in vitro (FIV) auxdites autorisations biologiques et technologiques. En effet, cette activité exige l'accomplissement d'actes des deux natures, cliniques et biologiques.
Cette obligation permettra le regroupement de tous les actes au sein d'un même centre et d'éviter la dispersion des responsabilités entre plusieurs établissements ou laboratoires successifs.
Le Conseil d'Etat avait formulé une telle proposition (cf. ci-dessous).
Le 4° prévoit le retrait ou la suppression des autorisations pour les mêmes raisons que le retrait d'autorisation des DPN et DPI : violation des dispositions légales, d'une part, volume d'activités et résultats insuffisants, d'autre part.
Le 5° propose de compléter l'article L. 2142-4 en renvoyant à un décret en Conseil d'Etat les modalités d'application du présent chapitre et notamment les dispositions relatives :
- aux actes cliniques et biologiques d'AMP ;
- aux conditions de fonctionnement des établissements pratiquant l'AMP ;
- aux conditions de formation et d'expérience des praticiens ;
- aux conditions d'exercice et d'organisation d'AMP ;
- aux conditions dans lesquelles sont tenus les registres de gamètes et d'embryons dans les centres d'AMP.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a modifié substantiellement cet article.
a) L'élargissement du recours à l'AMP
L'Assemblée nationale a élargi les conditions de recours à l'AMP, en adoptant deux amendements.
Le premier, à l'initiative de la commission spéciale et de Mme Yvette Roudy, supprime la condition de deux ans de vie commune pour les personnes non mariées et la remplace par la notion de « concubins ».
Les auteurs de l'amendement ont justifié de modifier ainsi les conditions prévues par le législateur de 1994 pour deux raisons : la discrimination résultant du dispositif en vigueur entre couples mariés et non mariés et l'âge tardif auquel, parfois, beaucoup de femmes font des demandes d'AMP.
Le second, adopté à l'initiative de la commission spéciale, prévoit d'autoriser le recours au transfert post mortem d'embryons.
Ainsi, dans un délai compris entre six mois et dix-huit mois après le décès du père, la femme peut demander à ce que soit réalisé le transfert de l'embryon. Elle doit, en outre, bénéficier d'un accompagnement personnalisé. Le mariage ou remariage fait obstacle à ce transfert.
b) Le principe de l'évaluation systématique de toute nouvelle technique d'AMP
Sur proposition de sa commission spéciale, l'Assemblée nationale a prévu, en introduisant un article L. 2141-1 nouveau, que toute nouvelle technique d'AMP fasse l'objet d'une évaluation préalable.
Cette évaluation est l'objet d'un protocole autorisé par l'APEGH qui juge de sa pertinence scientifique, de l'importance de ses objectifs ainsi que de l'acceptabilité éthique du projet.
Dans les mêmes conditions que pour la recherche sur l'embryon ( cf. article 19 ), les protocoles sont transmis aux ministres en charge de la santé et de la recherche qui peuvent les suspendre ou les interdire.
Le protocole doit prévoir l'accord du couple, qui est exprimé après un délai de réflexion. A l'issue de l'évaluation, les embryons éventuellement conçus à cette fin d'évaluation sont détruits.
Une liste des établissements aptes à réaliser ces évaluations est établie par l'APEGH.
Ce dispositif est complété par un article L. 2141-1-2 nouveau qui soumet à l'autorisation expresse du ministre chargé de la santé le passage à l'application clinique d'une nouvelle technique d'AMP. Car, s'agissant d'une application sur le vivant, la mère sur laquelle sera transféré un embryon conçu au moyen de cette nouvelle technique bénéficiera des dispositions de la loi Huriet de 1988 sur les recherches biomédicales, ce qui ne sera pas le cas de l'embryon qui n'est lui-même qu'une personne potentielle. Aussi l'application clinique de cette technique nouvelle est-elle soumise à l'autorisation du ministre.
c) Les garanties entourant la stimulation ovarienne
L'Assemblée nationale a adopté plusieurs autres amendements de précision ou de nature rédactionnelle :
- à l'initiative de Mme Marie-Thérèse Boisseau et de la commission spéciale, elle a adopté un amendement rédactionnel supprimant le pléonasme, réitéré par le texte initial, des « deux » membres du couple ;
- à l'initiative de sa commission spéciale et de M. Yves Bur, est introduite à l'article L. 2141-3 une exception à l'interdiction par le couple de recourir à une nouvelle FIV lorsqu'il dispose encore d'embryons congelés. Conformément à une observation du Comité national consultatif d'éthique, il sera autorisé à recourir à une nouvelle FIV si la qualité des embryons se trouvait affectée par le processus de congélation ;
- à l'initiative de M. Jean-François Mattei, est précisé à l'article L. 2141-4 que les couples sont consultés annuellement par écrit sur le maintien de leur projet parental ; est en outre ajouté, sur proposition de la commission spéciale, qu'ils peuvent manifester leur intention à tout moment ;
- à l'initiative de la commission spéciale, de M. Jean-François Mattei et de plusieurs de ses collègues, l'Assemblée nationale a adopté un amendement rédactionnel qui prévoit que les couples ne « demandent » pas mais « consentent auprès du médecin qui les interroge » à ce que leurs embryons surnuméraires fassent l'objet d'un accueil, les membres du couple pouvant rarement demander d'eux-mêmes que cet accueil soit possible, sans qu'on leur en ait préalablement exposé la possibilité.
La procédure retenue par l'article L. 2141-4 pour la destruction anticipée des embryons, -une demande écrite, confirmée par écrit après un délai de trois mois- est, en outre, étendue à l'utilisation de ces embryons à des fins de recherche.
Est enfin précisé, sur proposition de la commission spéciale, qu'il est mis fin à la conservation des embryons, non seulement si le couple mais encore l'un seulement de ses membres ne confirme pas le maintien de leur projet parental. Ainsi, devant le silence de l'un des membres du couple, sollicité à plusieurs reprises et qui ne répond pas, il est possible de présumer du silence de l'autre et de mettre fin après cinq ans à la conservation des embryons.
Sur proposition de la commission spéciale, il est précisé que les embryons introduits sur le territoire national respectent les principes prévus par les articles 16 à 18 du code civil, c'est-à-dire concrètement qu'ils n'ont pas été réalisés par un procédé de clonage :
- à l'initiative de Mmes Yvette Roudy et Martine Lignières-Cassou, l'Assemblée nationale a adopté un amendement à l'article L. 2141-10 sur les effets secondaires, les risques et la pénibilité des techniques d'AMP ;
- à l'initiative de la commission spéciale, elle a adopté un amendement précisant que le consentement d'un des deux titulaires de l'autorité parentale suffit à procéder à la conservation des gamètes de mineurs, notamment un traitement potentiellement attentatoire à leur fertilité ;
- à l'initiative de la commission spéciale, l'Assemblée nationale a ajouté un 3° à l'article L. 2141-12 pour prévoir, dans le champ du décret en Conseil d'Etat pour l'application de ce chapitre, les modalités de recueil et de traitement des informations relatives au consentement des hommes ayant accepté l'éventualité d'un transfert post mortem d'embryons ;
- elle a ensuite, sur proposition de la commission spéciale, adopté deux amendements au 2° et après le huitième alinéa de cet article, prévoyant la compétence de l'APEGH pour se prononcer à titre consultatif sur les demandes d'autorisation des centres d'AMP et sur le retrait de ces autorisations ;
- elle a, enfin, à l'initiative de sa commission spéciale, adopté un amendement précisant que les modalités de mise en oeuvre des déplacements d'embryons seront fixées par décret.
III - La position de votre commission
Le renforcement de l'encadrement du secteur de l'AMP
Les dispositions du présent article prévoient deux séries de mesures susceptibles de contribuer à un meilleur encadrement des activités d'AMP.
A l'instar de ce qui est pratiqué pour les examens de DPN et DPI, il est prévu (3° du II) que les activités d'AMP seront pratiquées dans des centres dont l'autorisation devra mentionner le nom des praticiens habilités à y exercer.
Il a été à plusieurs reprises souligné que les difficultés d'application de la loi étaient d'abord issues des notions d'agrément et des responsabilités des praticiens, le droit en vigueur permettant à un praticien non agréé d'exercer dans une clinique « sous la responsabilité d'un praticien nommément agréé ».
Le Conseil d'Etat rappelle dans son étude 80 ( * ) que « certaines caisses d'assurance maladie se sont opposées à la prise en charge des actes d'AMP effectués dans un centre autorisé quand ils n'étaient pas réalisés par un praticien agréé, estimant qu'il y avait une contradiction entre les dispositions de la loi 1994 et le code de déontologie médicale qui précise que chaque médecin est responsable de ses décisions et de ses actes. En réalité, la responsabilité du praticien dans l'esprit de la loi n'a pas cette portée et semble plutôt désigner une responsabilité administrative de gestion et d'organisation des activités. Cette responsabilité paraît avoir été fixée par référence au service public et non au mode d'organisation du secteur privé. Pourtant, la CNMBRDP a en conséquence été amenée à accorder un agrément à plusieurs praticiens par centre d'AMP, sans qu'un rapport ait été bien établi entre le volume d'activité en AMP et le nombre d'agréments accordés par centre ».
En outre, le Conseil d'Etat s'était inquiété des situations peu logiques engendrées par le système d'autorisations séparées dont font l'objet les activités cliniques et les activités biologiques d'AMP.
« Les activités cliniques et les activités biologiques d'AMP font ensuite l'objet d'autorisations séparées, ce qui conduit parfois à des situations peu logiques : un laboratoire de médecine libérale qui a déposé un dossier en même temps qu'une clinique privée pour travailler avec elle peut se voir accorder une autorisation tandis qu'elle sera refusée à la clinique. Le laboratoire n'est alors pas en mesure de mettre en oeuvre son autorisation. Insatisfaisante du point de vue de ces « établissements orphelins » , cette situation l'est aussi du point de vue de la planification sanitaire, puisqu'un certain nombre d'autorisations sont bloquées et indisponibles pour d'autres équipes.
« Il est ainsi souhaitable de lier l'autorisation accordée aux établissements de biologie et aux établissements cliniques 81 ( * ) . Pour prévoir le couplage des autorisations accordées aux établissements de biologie et aux établissements cliniques, il est nécessaire de modifier l'article L. 184-1 du code de la santé publique qui leur est relatif, ainsi que l'article L. 152-10 pour y inscrire que les équipes pluridisciplinaires des centres d'AMP ont un caractère clinico-biologique. »
Or, votre commission constate que la substitution de la qualification « clinico-biologique » à celle de « pluridisciplinaire » n'est pas conforme à ce que souhaitait le Conseil d'Etat, ni même l'exposé des motifs du présent projet de loi, au demeurant fort obscur, qui justifie le 7° du I de cet article en ces termes « au 7° l'article L. 2141-10 relatif à la procédure de mise en oeuvre de l'AMP est modifié. La notion d'équipe pluridisciplinaire, clinico-biologique est introduite pour insister sur l'importance que la prise en charge du couple soit collective (sic) ».
Elle vous propose en conséquence de modifier le 7° du I du présent article pour y inscrire la notion d'équipe pluridisciplinaire clinico-biologique .
Le présent article prévoit en outre la possibilité de retirer ou suspendre l'autorisation de certains centres en raison de leurs résultats trop faibles. Cette proposition avait également été formulée par le Conseil d'Etat 82 ( * ) pour qui « la faculté de révoquer l'autorisation accordée à un centre ou à une équipe avant le terme des cinq ans prévu par la loi donnerait à ces contrôles un poids accru. Plus ouvert, le régime d'autorisation des centres d'AMP y gagnerait aussi une forme de respiration. Le système, en effet, est aujourd'hui bloqué car presque toutes les autorisations qui pouvaient être accordées conformément aux impératifs de la carte sanitaire l'ont été. Il est donc très difficile pour de nouvelles équipes d'obtenir l'autorisation de pratiquer ces activités, alors même que certains centres ou laboratoires autorisés ont soit une activité trop peu importante pour pouvoir entretenir leur savoir-faire, soit des résultats insuffisants ».
Il faudrait donc compléter l'article L. 184-2 du code de la santé publique, qui dispose que « tout établissement ou laboratoire autorisé à pratiquer des activités d'AMP ou de DPN, tout centre pluridisciplinaire de DPN est tenu de présenter au ministre chargé de la santé un rapport annuel d'activité » , en prévoyant que l'autorisation accordée peut être révoquée avant cinq ans, en cas d'activité ou de résultats insuffisants.
Le sort de l'embryon conçu in vitro
Le présent article comble une lacune de la loi du 29 juillet 1994 qui n'avait pas, alors, tranché le sort des embryons créés in vitro et qui ne trouvaient plus, dans le cadre de la « demande parentale » la perspective d'être transférés.
Certes, le principe de l'accueil avait été prévu mais il n'avait pas permis, à lui seul, de régler la difficulté ouverte pour les embryons surnuméraires.
Le texte proposé prévoit tous les cas pour l'embryon in vitro .
Les parcours possibles de l'embryon conçu in vitro
|
Embryon conçu in vitro dans le cadre d'un projet parental |
|||||||||||||||
|
|
|
||||||||||||||
|
Il n'y a plus de projet parental :
|
Il maintient son projet parental |
Si aucun des membres du couple n'a répondu sur le maintien |
Si désaccord du couple sur le maintien du projet parental |
Si maintien du projet parental |
|||||||||||
|
A la recherche |
|
Il est mis fin à sa conservation |
Conservation des embryons |
Fin de conservation |
Fin de conservation |
Conservation |
|||||||||
|
Si pas accueilli dans les cinq ans : fin de conservation |
|||||||||||||||
Seules quelques difficultés rédactionnelles attirent l'attention de votre rapporteur. Ainsi la notion de « dissolution » du couple n'apparaît pas suffisamment précise pour permettre au praticien de s'opposer à une demande de transfert devenue, selon les termes de la loi, illégale. La notion de dissolution vise-t-elle le divorce pour les couples mariés ? A la date du dépôt de la demande, de l'audience de conciliation ou du jugement définitif ? S'agit-il pour les couples non mariés d'une séparation de corps, d'un arrêt de la vie commune ? Comment devra-t-il contrôler que cette condition de dissolution ne fait pas obstacle au transfert ?
Aussi, votre commission vous propose-t-elle sur ce point un amendement de précision qui, par un renvoi au troisième alinéa du code civil, définit strictement les conditions dans lesquelles cette dissolution doit être entendue comme le « cas de décès, de dépôt d'une requête en divorce ou en séparation de corps ou de cessation de la communauté de vie, survenant avant la réalisation de la procréation médicalement assistée ». Cet alinéa prévoit en outre que le consentement « est également privé d'effet lorsque l'homme ou la femme le révoque, par écrit et avant la réalisation de la procréation médicalement assistée, auprès du médecin chargé de mettre en oeuvre cette assistance ».
La grande prudence de votre commission sur les propositions d'ouverture de l'Assemblée nationale
L'Assemblée nationale a ouvert plusieurs possibilités que votre commission vous proposera de modifier ou de supprimer.
L'Assemblée nationale a souhaité mieux encadrer la pratique entourant la stimulation ovarienne.
Votre rapporteur a déjà détaillé, dans son exposé général, les raisons pour lesquelles il était conduit à proposer le renvoi à des recommandations de bonnes pratiques et non à un décret comme il est à présent prévu.
Votre commission ne saurait non plus agréer l'élargissement proposé par l'Assemblée nationale d'ouvrir l'AMP à des couples non mariés qui ne font pas la preuve d'au moins deux ans de vie commune. L'une des instigatrices de cet élargissement, Mme Yvette Roudy, au nom de la délégation aux droits des femmes, a également proposé avec Mme Martine Lignères-Cassou un amendement prévoyant une information du couple sur le caractère pénible et les effets secondaires induits par l'AMP. C'est en effet reconnaître le caractère lourd de cette assistance. En conséquence, l'exigence d'une durée de vie commune n'est sans doute pas superfétatoire afin de s'assurer de la solidité du couple et que les embryons conçus in vitro le sont dans le cadre d'un projet parental solide. Aussi, votre commission vous propose-t-elle, par amendement, de revenir à cette exigence initiale du projet de loi qui était déjà celle posée par le législateur de 1994.
Votre commission vous proposera en outre de supprimer par amendement deux transgressions qui, en l'état, ne lui semblent pas devoir être confirmées.
La première est relative au transfert post mortem d'embryons. Votre rapporteur a, dans son exposé général, détaillé les raisons pour lesquelles il s'opposait à un tel transfert.
La seconde est relative à l'évaluation des nouvelles techniques d'AMP. Présentant ce dispositif, le rapporteur de l'Assemblée nationale avait reconnu que cette évaluation supposait la création d'embryons à des fins de recherche.
Le principe de la création d'embryons à des fins de recherche correspond à deux réalités. La première est la création d'un matériau pour la recherche, ce qui n'est, pour personne, tolérable. La seconde est l'éventualité qu'au cours des essais de recherche sur une technique nouvelle d'AMP, un embryon se trouve conçu et viable.
Même entourée de toutes les précautions, une telle perspective est par principe inacceptable. Selon les mots exprimés par M. Jean-François Mattei devant votre commission, il ne saurait y avoir « des essais d'homme ».
Sans doute le législateur devra-t-il s'interroger sur les moyens de mieux accompagner la mise en oeuvre de nouvelles techniques d'AMP. Les partisans des évaluations soulèvent à juste titre que les erreurs qui ne sont pas constatées in vitro risquent de l'être in vivo . Néanmoins constatant le risque de dérive et de contournement de l'interdit absolu qu'elle entend réaffirmer, votre commission vous propose de supprimer cette disposition.
Enfin, votre commission vous propose d'adopter un amendement de conséquence avec l'amendement proposant l'interdiction du clonage thérapeutique, à l'article 19.
Votre commission vous propose d'adopter cet article ainsi amendé.
Article 18 bis
Dispositions permettant d'assurer la filiation et les
droits successoraux
de l'enfant né d'un transfert d'embryon
réalisé après le décès du père
Objet : Cet article, introduit par l'Assemblée nationale, organise les conséquences sur le plan civil et successoral de la possibilité qu'elle a ouverte d'un transfert d'embryon post mortem.
I - Le dispositif proposé
Le présent article a été introduit par l'Assemblée nationale, afin de prévoir, par coordination, les conséquences sur le plan civil et successoral de la possibilité ouverte par l'article 18 ( cf. commentaire ci-dessus) de transfert d'embryon post mortem .
Votre rapporteur salue l'ingénierie juridique mise en place par la commission spéciale de l'Assemblée nationale et par, semble-t-il, les services de la Chancellerie.
La présentation de cet article nouveau, tel qu'il figure dans le rapport de la commission spéciale de l'Assemblée nationale, en témoigne :
« Le I tend à modifier le titre VII du livre Ier du code civil relatif à la filiation.
« Le 1° du I a pour objet d'assurer la filiation de l'enfant ou des enfants nés d'un transfert d'embryon post mortem dans la section IV, relative à la procréation médicalement assistée, du chapitre Ier, regroupant les dispositions communes à la filiation légitime et à la filiation naturelle, du titre VII.
« S'agissant de la filiation légitime, le a) du 1° du I prévoit une dérogation à la règle de la nullité du consentement donné à une procréation médicalement assistée, recueilli par le juge, qui interdit toute action ou contestation de filiation pour les enfants issus de cette procréation, en cas de décès de l'époux ou du concubin. Il convient de rappeler qu'en matière de filiation, la notion de conception correspond au commencement de la grossesse. L'enfant est ainsi présumé conçu pendant la période qui s'étend du 300 ème au 180 ème jour précédant sa naissance. Dans le cas d'une fécondation in vitro, la conception ne débute qu'à compter du transfert de l'embryon.
« Il est ainsi prévu que, dans le cas d'un transfert post mortem réalisé dans les conditions posées par l'article L. 2141-2 du code de la santé publique, le consentement donné par l'homme, lorsqu'il entre dans un processus d'AMP, qui vaut présomption de paternité, est toujours valable dans les dix-huit mois qui suivent son décès, à la condition qu'il ait expressément consenti, auprès du centre d'AMP dont il relève, à la poursuite par sa femme ou sa concubine, de leur projet parental après son décès.
« S'agissant de la filiation naturelle, le b) du 1° du I a pour objet de créer un nouvel article 311-21, prévoyant la filiation automatique de l'enfant né d'un transfert post mortem réalisé dans les conditions prévues à l'article L. 2141-2 précité, dès lors que le père a donné son consentement par écrit à la poursuite, par sa concubine, de leur projet parental après sa mort. Le deuxième alinéa de ce nouvel article prévoit l'interdiction de toute contestation de filiation, à moins qu'il ne soit prouvé que l'enfant n'est pas issu de l'AMP ou que le consentement a été révoqué par le père de son vivant. Il faut, en effet, rappeler que l'article L. 2141-2 donne à l'homme la faculté de retirer à tout moment le consentement qu'il a pu exprimer au centre d'AMP dont il relève.
« Le c) du 1° du I tend à modifier l'article 313-1 du code civil, qui écarte la présomption de paternité lorsqu'un enfant n'est pas déclaré par le mari de la femme qui l'a mis au monde, afin de créer une exception à cette règle lorsque l'enfant est issu d'un transfert post mortem dans les conditions prévues par le second alinéa de l'article 315 du même code, créé à l'alinéa suivant (2°), ce qui signifie que cette filiation sera reconnue en faveur de l'enfant dès lors que le père a donné son consentement de son vivant au transfert d'embryon après sa mort dans les conditions prévues à l'article L. 2141-2 précité.
« Le 2° du I tend à compléter l'article 315 du code précité afin de ne pas écarter la présomption de paternité, lorsqu'il est établi que le mari a donné son consentement à ce que le transfert d'embryon soit réalisé après son décès et lorsque ce transfert a été réalisé dans les conditions prévues par l'article L. 2141-2 précité, c'est-à-dire lorsque ce transfert a été réalisé entre le sixième et le dix-huitième mois suivant le décès.
« Le II a pour objet de modifier le titre I er consacré aux successions du livre III du code civil relatif aux « différentes manières dont on acquiert la propriété ».
« Le 1° du II tend à créer quatre articles nouveaux, 724-2 à 724-5, dans le titre précité.
« L'article 724-2 nouveau permet de déroger à l'article 715 du même code, d'après lequel les enfants qui ne sont pas encore conçus au décès de leur père sont écartés de sa succession, afin que l'enfant né d'un transfert d'embryon post mortem, dans les conditions posées par l'article L. 2141-2 précité, soit appelé à la succession du défunt au même titre que ses éventuels frères et soeurs vivants. Il convient de noter que l'usage du singulier pour l'enfant concerné n'a pas pour conséquence d'empêcher d'assurer la succession de plusieurs enfants qui seraient issus d'un tel transfert en cas de naissance multiple.
« L'article 724-3 nouveau donne au président du tribunal de grande instance (TGI), la faculté de désigner un administrateur pour assurer la gestion de la succession du défunt, dès lors que ce dernier a consenti au transfert d'embryon après sa mort et dès lors que subsistent des embryons conçus de son vivant. Il est cependant nécessaire que le président du TGI soit expressément saisi d'une requête en ce sens par « tout intéressé ». On peut donc penser qu'il s'agira, en premier lieu, de la femme qui souhaiterait poursuivre le projet parental, après le décès de son mari ou de son concubin. Il convient de noter que ce gel de la succession, par nomination d'un administrateur, est une possibilité reconnue au juge qui doit apprécier si la consistance du patrimoine et la nature des actes à accomplir pour en assurer la gestion, l'exigent.
« Le deuxième alinéa de l'article 724-3 précise la durée durant laquelle la mission de l'administrateur judiciaire s'exercera. Au maximum, cette mission pourra durer pendant les dix-huit mois suivant le décès de l'homme, c'est-à-dire pendant la durée au cours de laquelle le transfert post mortem pourra être réalisé. En effet, si la femme développe la grossesse à la fin du délai imparti pour le transfert, la règle d'après laquelle la mère est considérée comme assurant la sauvegarde des intérêts de l'enfant à naître, s'applique, ce qui permet de « débloquer » la succession.
« Trois cas sont prévus pour mettre fin à la mission de l'administrateur judiciaire avant le terme des dix-huit mois précités :
« - le premier, dans l'hypothèse où la femme renonce, à son initiative, à la réalisation du transfert, comme le prévoit d'ailleurs l'article L. 2141-2 du code de la santé publique ;
« - le deuxième, lorsqu'une naissance est constatée à la suite d'un transfert réussi d'embryon ou qu'une grossesse, correspondant à la dernière tentative possible de transfert, est constatée. Cette précision a plusieurs conséquences. En premier lieu, elle limite les transferts d'embryons qui peuvent être réalisés dans les dix-huit mois suivant le décès du père à une seule naissance. Ainsi, dans le cas où subsisteraient des embryons congelés après qu'une tentative de transfert ait réussi et abouti à la naissance d'un ou de plusieurs enfants, il serait mis fin au gel de la succession ;
« - le troisième, dès lors qu'est constaté l'échec de la dernière tentative possible de transfert d'embryon, c'est-à-dire lorsque tous les embryons ont été utilisés.
« L'article 724-4 nouveau donne compétence à l'administrateur désigné par le président du TGI pour faire l'inventaire de la succession.
« L'article 724-5 nouveau décrit les missions et les pouvoirs de l'administrateur. Il peut accomplir tout acte de conservation et d'administration nécessaire à la gestion de la succession et exercer également les pouvoirs de représentation prévus en cas d'indivision, tels que prévus par l'article 1873-6 du code civil. Il ne pourra cependant prendre aucun acte de disposition, sauf si celui-ci est nécessaire à l'exploitation normale des biens ou à leur conservation, sous réserve de l'autorisation du juge des tutelles.
« Le deuxième alinéa de cet article 724-5 nouveau prévoit la possibilité pour l'administrateur d'exercer ses pouvoirs en dépit de l'existence, parmi les autres héritiers, d'un mineur ou d'un majeur faisant l'objet d'une mesure de protection légale.
« Le 2° du II a pour objet de modifier en deux points l'article 815 du code civil relatif à l'indivision.
« Le a) du 2° du II complète le premier alinéa de l'article précité, afin que la règle d'après laquelle nul ne peut rester en indivision ne soit pas appliquée, non seulement lorsqu'un jugement le décide ou qu'une convention le prévoit, mais aussi si l'« effet de la loi » y conduit. Cette mention permet donc de laisser en indivision la succession d'un homme qui aurait consenti au transfert d'embryons après sa mort, afin que sa succession soit gelée dans les délais évoqués précédemment.
« Le b) du II précise les circonstances de l'indivision dans le cas d'un transfert post mortem, en indiquant que celle-ci est maintenue de plein droit dès lors que le défunt a consenti à la poursuite du processus d'AMP après sa mort et dès lors qu'existent des embryons. Il est spécifié que l'indivision prendra fin dans les mêmes conditions que celles prévues à l'article 724-3, c'est-à-dire si la femme renonce au transfert, si une naissance a été constatée ou lorsque la dernière tentative possible d'embryon a échoué. »
II - La position de votre commission
Les difficultés posées au droit civil et successoral avaient été soulignées par le Conseil d'Etat qui avait préconisé d'autoriser ce type de transfert.
La Haute juridiction avait, en conséquence, tenté d'établir les contours d'un régime civil dérogatoire afin de prévoir la filiation de l'embryon, s'il venait un jour au monde, et de lui permettre d'hériter, le cas échéant.
Sur le plan de la filiation, le Conseil d'Etat avait souligné « la nécessité de modifier le code civil afin de régler le sort de l'enfant quant à sa filiation paternelle, qu'elle soit légitime ou naturelle » et notamment dans le cas du couple marié car dans ce dernier cas « la présomption de paternité inscrite à l'article 312 alinéa 1 er du code civil ne s'applique plus. Certes, ce texte dispose que « l'enfant conçu pendant le mariage a pour père le mari » , mais la possibilité de faire jouer cet énoncé en cas de naissance issue d'un transfert d'embryon post mortem semble se heurter aux termes de l'article 315 du code civil, suivant lequel : « La présomption de paternité n'est pas applicable à l'enfant né plus de trois cents jours après la dissolution du mariage, ni, en cas d'absence déclarée du mari, à celui qui est né plus de trois cents jours après la disparition » . »
La construction d'un régime successoral s'avérait encore plus délicate.
|
Enfin, il est nécessaire de prévoir les dispositions répondant à l'autorisation du transfert d'embryon post mortem en termes de droit de la succession. Un enfant issu d'un transfert d'embryon post mortem pourrait bénéficier de la maxime « Infans conceptus... « , à laquelle renvoie l'article 725 du Code civil, dès lors qu'il naît vivant et viable et qu'il est établi qu'il est issu d'une AMP ayant permis la congélation d'embryons antérieurement au décès de l'homme. En revanche, l'incertitude concernant la dévolution successorale, quant à son calendrier comme quant aux qualités respectives dont peuvent se prévaloir les héritiers, paraît devoir être la source de difficultés pratiques. L'usage en cas de grossesse naturelle -la suspension des opérations successorales jusqu'à la naissance d'un enfant vivant et viable- peut-il être transposé au cas du transfert d'embryon post mortem ? Dans cette hypothèse, en effet, la durée de la suspension serait indéterminée, puisqu'elle résulterait du cumul du délai de réflexion laissé à l'intéressée, du temps nécessaire à l'implantation et de la durée de la grossesse. On peut s'interroger sur le coût d'une telle suspension pour les héritiers ainsi que la difficulté probable pour obtenir du ministère de l'économie et des finances une suspension de la perception des droits de mutation à titre gratuit jusqu'à la naissance éventuelle d'un enfant, quand bien même leur taux pour chaque héritier, leur répartition et les éventuels abattements resteraient des hypothèses incertaines. Compte tenu de ces difficultés, on pourrait envisager une option consistant à procéder au partage et à le remettre en cause si l'éventualité de la naissance d'un enfant se concrétise, mais les risques de conflit et les difficultés de toute nature imposés aux copartageants par une telle remise en cause invitent à écarter cette solution. Une dernière option consisterait à réserver la part de l'enfant dans le partage successoral, faire administrer celle-ci par un mandataire ou un administrateur ad hoc et réaliser le partage pour le surplus. Cette solution n'est cependant pas non plus exempte de difficultés : si l'enfant ne naît pas ou naît sans être viable, il ne s'agira pas seulement d'attribuer aux copartageants la part laissée vacante pour cet enfant, mais aussi de prendre en compte la qualité héréditaire réelle de chaque héritier compte tenu des modifications entraînées par rapport à la qualité virtuelle conférée à chacun d'eux à la première étape du partage. Si c'est une grossesse multiple qui est menée à terme, ces difficultés prennent plus d'ampleur encore : le partage serait à recommencer ab initio, comme si l'on se trouvait dans une situation d'intervention après coup d'un nouvel héritier. Enfin, cette troisième option ne résout pas les difficultés liées aux droits de mutation. Au total, c'est un choix entre la première et la troisième option qui paraît s'imposer. Compte tenu des limitations dans le temps prévues pour la réalisation de la tentative d'implantation, la première solution paraît la plus satisfaisante ». Conseil d'Etat, étude précitée page 37 |
Les interrogations que suscite cette construction juridique illustrent les difficultés de la dérogation qui la justifient. Votre rapporteur s'interroge à nouveau, comme il l'a fait à l'article précédent, sur les conditions dans lesquelles cet enfant viendrait au monde.
En effet, aux termes du présent article, l'embryon orphelin de père, encore incertain sur l'accueil d'un ventre maternel, bénéficie déjà, en revanche, des conseils avisés d'un notaire et d'un administrateur judiciaire !
Par coordination avec la suppression de la possibilité du transfert post mortem qu'elle vous a précédemment proposée, votre commission vous propose d'adopter un amendement de suppression de cet article.
CHAPITRE IV
-
RECHERCHE SUR L'EMBRYON ET LES CELLULES EMBRYONNAIRES ET
FoeTALES
Sur proposition de M. Nicolas About, président, votre commission a adopté un amendement proposant qu'à l'actuel intitulé proposé pour le chapitre IV soit substitué un intitulé plus large :
« Recherche sur l'embryon et les cellules souches humaines ».
Article 19
Recherche sur l'embryon et les cellules embryonnaires
Objet : Cet article détermine les conditions dans lesquelles pourraient être menées des recherches sur l'embryon humain.
I - Le dispositif proposé
Le I du présent article procède, selon le syndrome dit « du pont de la rivière Kwaï » , diagnostiqué par votre rapporteur 84 ( * ) , à un déplacement du titre V (dispositions pénales) du livre premier de la deuxième partie du code de la sécurité sociale, qui devient un titre VI (cf. article 21 du présent projet de loi) avant que le II (cf. ci-après) ne le rétablisse avec un contenu différent.
Le II consacre ce nouveau titre V à la recherche sur l'embryon et les cellules embryonnaires .
Le chapitre unique proposé pour ce titre prévoit quatre articles :
L'article L. 2151-1 reproduit le troisième alinéa de l'article L. 16-4 du code civil résultant de l'article 15 du présent projet de loi portant interdiction du clonage reproductif ;
L'article L. 2151-2 prévoit l'interdiction de créer des embryons à des fins de recherche ;
L'article L. 2151-3 définit les conditions dans lesquelles peuvent être menées des recherches sur l'embryon.
Le premier alinéa de l'article L. 2151-3 prévoit que ces recherches doivent avoir une finalité médicale et ne pouvoir être menées par une « méthode alternative d'efficacité comparable en l'état des connaissances scientifiques » .
Le deuxième alinéa prévoit que cette recherche ne peut avoir lieu que sur des embryons « surnuméraires », c'est-à-dire ne faisant plus l'objet d'un projet parental, après que les membres du couple, informés des alternatives pour cet embryon -accueil ou arrêt de leur conservation-, aient consenti à cette recherche. Ce consentement préalable est exprimé par écrit, après un délai de réflexion. L'embryon sur lequel une recherche a été conduite ne peut plus faire l'objet d'un transfert.
Le troisième alinéa impose la nécessité d'un protocole agréé par l'APEGH pour toute recherche sur l'embryon. L'Agence se prononce au regard de la pertinence scientifique, médicale et éthique du projet de recherche.
Le quatrième alinéa prévoit la suspension ou le retrait de l'agrément par les ministres compétents (santé et recherche) en cas de non-respect des dispositions législatives en vigueur.
L'article L. 2151-4 prévoit que les modalités d'application du présent article seront prises par décret en Conseil d'Etat, après avis de l'APEGH.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a modifié cet article à sept reprises.
A l'initiative de sa commission spéciale, elle a adopté :
- un amendement de coordination de l'amendement adopté à l'article 18 pour l'article L. 2141-1-1du code de la santé publique qui prévoit une évaluation des nouvelles techniques d'AMP. Cette dernière proposition suppose la création d'embryons à des fins de recherche. Il fallait donc prévoir une exception à l'interdiction de principe posée par l'article L. 2151-2 ;
- un amendement fixant à « trois mois » le délai de réflexion à l'issue duquel le couple peut consentir à la recherche sur l'embryon ;
- un amendement prévoyant une double précision : la première indique que le « transfert » « à des fins de gestation » de l'embryon est rendu impossible par la recherche dont il a été l'objet, (la précision tient à l'ajout des termes « à des fins de gestation ») ; la seconde prévoit que le consentement à ces recherches par le couple est révocable sans forme et à tout moment ;
- un amendement rédactionnel et un amendement de conséquence.
L'Assemblée nationale a, en outre, adopté, sur proposition de Mme Marie-Thérèse Boisseau et de sa commission spéciale, deux amendements visant à :
- supprimer dans la deuxième phrase du deuxième alinéa du texte proposé pour l'article L. 2151-3 les mots « des deux membres », les membres d'un couple étant en effet rarement trois ;
- insérer dans la deuxième phrase du deuxième alinéa de l'article L. 2151-3 les mots « par ailleurs dûment » afin de préciser la portée de l'information reçue par le couple avant qu'il puisse consentir à une recherche sur l'embryon.
III - La position de votre commission
Le droit en vigueur
Votre rapporteur ne commentera pas longuement les motifs du législateur de 1994 qui a choisi de ne pas autoriser la recherche sur l'embryon. L'étude réalisée par le Conseil d'Etat en 1999, présentée dans l'exposé général, commente les tenants et les aboutissants dudit choix.
Aujourd'hui, la recherche en France sur l'embryon ou les cellules qui en sont issues est interdite. Le pouvoir réglementaire a fait une stricte interprétation de ces dispositions. Ainsi la tentative en 2002 de M. Roger-Gérard Schwarzenberg, alors ministre de la recherche, d'importer des cellules souches embryonnaires à des fins de recherche, n'a pu aboutir.
|
1° Les faits Fin mars 2002, le ministre de la recherche, M. Roger-Gérard Schwarzenberg annonce son intention d'autoriser l'importation de cellules souches pluripotentes d'origine embryonnaire en provenance d'Australie à des fins de recherche, en s'appuyant sur les dispositions du décret du 23 février 2000 relatif à l'importation ou l'exportation de produits et éléments du corps humain. Le 30 avril 2002, à la veille de quitter ses fonctions, il autorisait le CNRS à importer lesdites cellules pour effectuer des recherches scientifiques. Fin juin, une association a saisi le Conseil d'Etat pour obtenir la suspension de l'exécution de la décision ministérielle autorisant le CNRS à pratiquer des recherches sur des cellules souches embryonnaires importées. 2° L'arrêt du Conseil d'Etat Le Conseil d'Etat a formulé un « doute sérieux sur la légalité de la décision attaquée » , le ministre ne pouvant prendre à l'époque une décision sans méconnaître les dispositions de l'article L. 2141-8 du code de la santé publique qui interdisent la conception in vitro d'embryon à des fins de recherche, ainsi que l'expérimentation sur ce dernier. Le 13 novembre 2002, le Conseil d'Etat a ordonné la suspension de l'exécution ministérielle attaquée jusqu'à l'expiration d'un délai de quatre mois (13 mars 2003), délai devant permettre au tribunal administratif de Paris d'instruire la décision contestée. |
Votre rapporteur formulera à ce stade deux remarques :
- il n'était sans aucun doute impossible d'arguer que le présent projet de loi, adopté en première lecture par l'Assemblée nationale, permettait, en effet, que soit remise en cause la volonté du législateur de 1994. Jusqu'à la promulgation du présent projet, la loi du 29 juillet 1994 demeure le droit en vigueur ;
- la question de l'importation de cellules souches pour effectuer des recherches scientifiques ou thérapeutiques pose en soit une difficulté d'ordre éthique : peut-on s'autoriser à « prélever à l'étranger », ce en quoi consistait l'importation, au motif que, pour des raisons éthiques, le prélèvement sur des embryons en France est interdit ? Votre rapporteur ne le pense pas.
Les perspectives de la recherche
Des expériences menées sur des rongeurs ont mis en évidence, voilà une dizaine d'années, la possibilité de cultiver des cellules souches embryonnaires , dites « cellules E.S » qui, au contact d'un certain milieu, ont le pouvoir de se transdifférencier en cellules potentiellement donneuses de tissus nerveux, sanguin, osseux, musculaire, etc. Une expérience plus récente, conduite sur le rat, a montré que l'injection directe de cellules cultivées pouvait provoquer une réparation de lésions dans la zone où elles étaient inoculées.
La question de la transposition de ces cellules à l'homme s'est donc naturellement posée, en ce qu'elle pourrait représenter un prémisse de piste thérapeutique contre des pathologies diverses telles que la maladie de Parkinson ou le diabète.
En outre, certaines des caractéristiques des cellules pluripotentes s'apparentent aux caractéristiques des cellules précancéreuses. Leur état instable offre un modèle d'étude pour, éventuellement un jour, mieux comprendre les mécanismes qui transforment une cellule vers un état cancéreux.
Mais les perspectives suscitées par les recherches sur les cellules embryonnaires ne sont pas uniques. Certaines cellules souches chez l'adulte sont capables de se multiplier, de générer des copies de ces cellules ainsi que de se « transdifférencier », telles les cellules souches hématopoïétiques (moelle osseuse) qui pourraient donner des cellules spécialisées (chondrocytes cartilagineux, globules rouges, blancs, plaquettes, etc.).
A Milan (Italie), les travaux de l'équipe du professeur Vescovi ont démontré, sur des souris, l'étonnante capacité de certaines cellules souches nerveuses adultes à se transformer in vivo en précurseurs médullaires hématopoïétiques et d'engendrer les lignées des cellules sanguines. Cette découverte montre la vitesse à laquelle les perspectives offertes par l'une ou l'autre voie évoluent et interdisent véritablement de trancher.
Or, l'utilisation de telles cellules ne pose pas, à la différence des cellules embryonnaires, de difficultés éthiques.
Doit-on et peut-on en limiter le champ de la recherche sur les seules cellules souches adultes ?
Pour sa part, le Conseil d'Etat 85 ( * ) , estime que « les expérimentations viennent poser sous un jour nouveau la question de la recherche sur l'embryon. En effet, bien que des expériences récentes montrent que les cellules souches présentes dans tous les tissus dont elles assurent le renouvellement sont capables de se comporter plus ou moins efficacement comme des cellules souches d'autres tissus, les cellules embryonnaires issues du blastocyste ou les cellules germinales primordiales par leur pluripotence sont les meilleurs modèles pour comprendre le processus de différenciation cellulaire et servir de base à l'élaboration de lignées cellulaires différenciées. Cela ne veut pas dire que les thérapies cellulaires auront nécessairement comme base dans l'avenir, des cellules souches embryonnaires mais que, sans l'étude de ces cellules, il est probablement illusoire d'espérer que ces thérapies cellulaires puissent voir le jour à partir d'autres cellules souches existant dans les organismes adultes » .
De même, la Commission nationale de bioéthique américaine, en remettant son rapport au président Clinton, avait en 1999 déclaré qu' « en raison des importantes différences biologiques qui séparent les cellules souches adultes et embryonnaires, cette source de cellules souches ne devrait pas être considérée comme une alternative à la recherche sur les cellules ES et EG » .
MM. Alain Claeys et Claude Huriet 86 ( * ) , qui commentent ces propos, déclarent ne pas souscrire « à ce point de vue et (pensent) que ces deux voies doivent être explorées avec la même détermination. L'un des éminents scientifiques que nous avons entendus, américain de surcroît, ne professe pas une opinion opposée : « il n'existe pas tant une compétition entre cellules qu'une compétition entre chercheurs qui utilisent différentes sources de cellules. Elle permettra de déterminer les cellules qui se prêtent le mieux aux applications cliniques. Exclure l'une ou l'autre approche ne serait pas bénéfique à long terme ».
Au stade actuel de la science, chacune des deux techniques doit être développée. Mais cette question, votre rapporteur l'a déjà dit, doit être traitée avec une grande prudence, notamment vis-à-vis des malades et de leurs familles, car ces techniques n'en sont qu'à des balbutiements et ne laissent pas entrevoir de perspectives thérapeutiques concrètes à court terme.
|
Les avancées récentes de la recherche fondées sur l'expérimentation animale laissent entrevoir la possibilité de progrès médicaux décisifs à partir de ces cellules souches adultes. Si les propriétés des cellules souches adultes mises récemment en évidence chez l'animal et, principalement, leur pouvoir élevé de transdifférenciation, sont transposables à l'homme, on perçoit aisément les importantes ressources qu'elles peuvent offrir à la thérapie cellulaire. Deux avantages doivent être soulignés : - prélevées sur l'organisme adulte, elles ne soulèvent, au plan éthique, aucune objection dès lors que seront respectées par ailleurs les règles générales touchant le recueil du consentement et l'évaluation du bénéfice-risque ; - si l'on parvient à isoler les cellules d'un patient puis à conduire in vitro leur division et leur spécialisation, on pourra pratiquer des greffes autologues permettant de résoudre les problèmes d'immunocompatibilité sans passer par le clonage thérapeutique, méthode dont nous avons pu souligner le caractère coûteux, complexe et controversé. Pour autant, on ne doit pas sous-estimer les limites importantes auxquelles se heurte pour l'instant l'utilisation des cellules souches adultes : - s'il est bien établi que ces cellules peuvent se multiplier en culture en conservant leur caractère propre, leur division n'est pas infinie, contrairement à celle des cellules souches embryonnaires, de sorte que leur développement en culture tissulaire est, lui-même, nécessairement limité ; - elles n'ont pas été isolées dans tous les tissus du corps humain : ainsi n'a-t-on pas pu localiser des cellules souches cardiaques ou pancréatiques ; - l'utilisation de ces cellules en greffe autologue requiert au préalable qu'elles soient isolées et mises en culture en nombre suffisant pour obtenir les quantités nécessaires au traitement. En cas de trouble aigu nécessitant une intervention rapide, le délai risque d'être trop court pour parvenir à ce résultat ; - d'après les études menées sur les animaux, les cellules souches dérivées du système nerveux central n'ont pas le profil génétique des cellules souches « normales » observées au cours de l'embryogenèse. John Gearhart se déclare « préoccupé » par leur évolution après la greffe, certains résultats tendant à prouver qu'elles pourraient ne pas se différencier ; - le recours à la greffe autologue pour le traitement des maladies génétiques peut poser problème si l'anomalie affecte les cellules souches destinées à la transplantation.
Rapport de l'OPESCT sur le clonage, la thérapie
cellulaire
|
La proposition de votre commission
Votre commission n'ignore rien des perspectives ouvertes par la science de même que les difficultés éthiques qu'engendre l'utilisation des embryons humains ou des cellules qui en sont issus à des fins de recherche médicales ou thérapeutiques.
Il a souvent été affirmé que de telles recherches devaient être autorisées pour des raisons de compétition internationale. Cet argument est sans doute le moins pertinent. De nombreux pays n'autorisent pas ces recherches. Cela ne présume en rien de la qualité de leur recherche médicale.
Le Conseil d'Etat avait, pour sa part, formulé trois pistes d'ouverture pour la recherche sur l'embryon :
- la possibilité de mener des recherches larges, sur l'embryon et les cellules souches embryonnaires ;
- la possibilité de mener des recherches sur les seules cellules embryonnaires ;
- l'opportunité de prévoir un caractère transitoire pour cette recherche.
Votre commission ne souhaite pas remettre en cause les principes affirmés par le législateur de 1994.
Aussi, propose-t-elle un amendement pour le premier alinéa de l'article L. 2151-3 du code de la santé publique afin d'affirmer que la recherche sur l'embryon humain est interdite .
Le législateur de 1994 avait ouvert la faculté de procéder à des études qui ne remettent pas en cause l'intégrité de l'embryon. Cette faculté a donné lieu à une dizaine de demandes de protocoles et cinq recherches seraient conduites. Cette faculté, qui a été implicitement supprimée par le 3° de l'article 18, ne doit pas être abrogée. Il doit perdurer une distinction entre la recherche sur l'embryon, qui, in fine , porte atteinte à son intégrité et l'étude qui ne l'affecte pas. Votre commission vous propose donc un amendement insérant un nouvel alinéa qui prévoit le maintien de cette faculté de conduire des études qui ne portent pas atteinte à l'embryon.
Votre commission ne souhaite pas fermer une porte à la recherche de manière définitive mais constate qu'une telle recherche est une transgression du principe de protection de la vie dès son commencement. Elle souhaite aussi que l'autorisation soit strictement encadrée. Aussi, propose-t-elle un amendement introduisant un nouvel alinéa afin que la recherche sur l'embryon et les cellules embryonnaires soit assortie de toutes les garanties possibles :
- cette transgression doit être transitoire. Un délai de cinq ans permettra peut-être de vérifier que l'utilisation des cellules souches adultes rend inutile le recours à l'embryon. Aussi, cette dérogation est prévue pour une durée de cinq ans ;
- cette transgression ne saurait concerner que des embryons surnuméraires, c'est-à-dire créés dans le cadre d'une AMP mais ne faisant plus l'objet d'un projet parental, la création d'embryons pour la recherche devant demeurer un tabou absolu ;
- le recours à une recherche sur l'embryon doit constituer un dernier ressort, dans le cas où aucune autre technique n'a pu s'y substituer. Il faudra donc apporter la preuve que des essais réalisés notamment sur les primates ont justifié de l'intérêt d'une telle recherche sur l'embryon. Il serait insupportable que, pour des raisons de coûts, l'utilisation de l'embryon humain soit préférée à toute autre technique d'expérimentation sur les animaux ;
- la pertinence des recherches devra en outre être démontrée en regard de ses perspectives thérapeutiques. Il ne saurait être question de poursuivre des recherches à des fins industrielles ou commerciales. L'APEGH ou la nouvelle agence de biomédecine sera ici sollicitée pour viser le contenu des protocoles et s'assurer, notamment via son conseil d'orientation médical et scientifique, de la conformité éthique et scientifique de ces derniers à la volonté exprimée par le législateur ;
- votre rapporteur préconise enfin de faire figurer les termes embryons et cellules souches embryonnaires mais pour des finalités différentes. Il doit être entendu que des recherches sur l'embryon doivent pouvoir être menées sur ce dernier afin de faire progresser la médecine embryonnaire. La recherche thérapeutique doit porter, pour sa part, sur les seules cellules souches embryonnaires. M. Jean-François Mattei l'a rappelé devant votre commission 87 ( * ) :
« La recherche sur l'embryon qui profite à l'embryon lui-même ou d'ailleurs à d'autres embryons, me paraît une ouverture indispensable, sauf à rester dans une espèce de statut assez invraisemblable où l'on dirait : «On le respecte tellement qu'on ne veut pas lui venir en aide le cas échéant !». La recherche sur l'embryon, malgré la difficulté et malgré le fait que, dans un certain nombre de situations, cet embryon ne survivra probablement pas -mais d'autres pourront bénéficier de ces recherches- me paraît donc devoir être désormais ouverte, dans des conditions très strictes, très fermement encadrées, car la médecine en est arrivée à l'embryon, qu'elle considère comme accessible à son diagnostic et à son éventuelle thérapeutique. La recherche sur l'embryon dans des conditions précises doit donc être à mon sens désormais autorisée. On passe insensiblement de l'étude à la recherche, et je ne vois pas comment nous pourrions l'éviter ».
Il appartiendra à l'APEGH de veiller au respect de la distinction entre la recherche sur les cellules souches embryonnaires, à des fins thérapeutiques et la recherche sur l'embryon dans un but d'amélioration de la médecine de l'embryon.
Par amendement au troisième alinéa de l'article L. 2151-3, votre commission prévoit, en outre, que chacun des ministres chargés de la santé et de la recherche dispose d'un droit de veto à l'encontre des décisions d'autorisation des protocoles de recherche par l'APEGH. En clair, cela veut dire que le ministre de la santé pourra s'opposer à une recherche quand bien même son collègue chargé de la recherche serait favorable à l'autorisation accordée par l'Agence.
En outre, votre commission précise que les avis du Conseil d'orientation médical et scientifique sont communiqués « en temps réel » aux ministres afin d'éclairer l'exercice de leur droit de veto sur les décisions de l'Agence.
La question du clonage thérapeutique
Votre commission tient à affirmer deux interdits : la création d'embryon à des fins de recherche et le clonage thérapeutique.
Il a été précisé, dans l'exposé général ainsi qu'au cours du commentaire de l'article précédent, les raisons pour lesquelles ces recherches ne sauraient, sous aucun motif, être autorisées.
Votre rapporteur détaillera en revanche les raisons qui l'amènent à refuser le principe du clonage thérapeutique.
Le principe du clonage thérapeutique est le transfert au sein d'un ovocyte énucléé d'une cellule souche adulte qui, du fait de son milieu, développe la potentialité d'un embryon. Devant votre commission, M. Axel Kahn, en mettant des « guillemets », a défini « le clonage thérapeutique, comme la fabrication d'embryons humains par transfert de noyau à partir d'une cellule somatique » . Ces dernières cellules, que l'on tenterait de transdifférencier pour produire les cellules recherchées (sanguines, musculaires, organiques, etc.) auraient l'avantage d'être immunocompatibles avec le receveur puisqu'elles en dériveraient.
En l'état actuel des choses, trois risques décisifs incitent votre commission à repousser cette pratique.
Le premier de ces risques est d'ordre éthique . Les risques pris sous cet aspect sont importants. Il s'agit de permettre le développement d'une technique en tout point identique avec le clonage reproductif. Votre rapporteur l'a dit dans son avant-propos. M. Axel Kahn l'a rappelé devant votre commission 88 ( * ) :
« Le premier scientifique qui, soi-disant pour les besoins d'un clonage thérapeutique dont l'utilité thérapeutique n'est pas claire, publiera dans une grande revue scientifique la technique « clés en main » pour fabriquer des embryons humains, donnera rapidement et très simplement à M. Antinori et aux raëliens la technique qui leur manque peut-être aujourd'hui pour passer à l'acte. Finalement, l'utilité thérapeutique paraît incertaine et celle pour la recherche possible. Les éléments négatifs me semblent donc, aujourd'hui, l'emporter de loin sur les éléments positifs » .
Le second de ces risques est d'ordre technique . Pour réaliser ce clonage thérapeutique -certains disent cellulaire- il faut disposer d'un grand nombre d'ovocytes. Le don d'ovules féminins ne va pas de soi. Il en résulterait les risques des pires trafics conduisant à une marchandisation du corps humain dont seraient victimes, comme souvent, les plus faibles. Des scientifiques préconisent le recours à des ovocytes d'origine animale. Une expérience a même pu être menée à partir d'ovocytes bovins. MM. Claude Huriet et Alain Claeys rappellent dans leur rapport 89 ( * ) :
« De nombreux scientifiques expriment leur scepticisme face à cette annonce spectaculaire . Pour le professeur Thibault, l'expérience visant à fusionner un noyau humain et un ovocyte de bovin est « hérétique du point de vue du fonctionnement cellulaire : la température de l'ovocyte bovin est de 39°5, celle de l'ovocyte humain de 37°, et tout donne à penser que cette différence perturbe les mécanismes moléculaires, biochimiques et enzymologiques ». John Gearhart rappelle que, chez les espèces animales, les gènes situés dans le noyau et les gènes situés dans le cytoplasme ont connu une évolution qui n'est pas seulement génétique mais cytoplasmique. « On sait, grâce à des études de laboratoire, que le noyau et le cytoplasme ne peuvent pas être échangés entre espèces. Lorsqu'ils le sont, le métabolisme ne peut pas se mettre en place. Il est donc difficile de concevoir qu'une expérience consistant à implanter des noyaux humains dans des ovocytes bovins puisse aboutir ».
Le dernier risque est d'ordre médical . Les tentatives menées sur les animaux font apparaître des risques d'effets pathologiques durables, qui justifient que des expérimentations sur les animaux soient menées sérieusement avant d'envisager tout recours à l'homme. Ainsi le rapport de l'OPECST précité 90 ( * ) évoque les commentaires du professeur Samarut :
« Certains chercheurs, tel Jacques Samarut, se déclarent défavorables au clonage thérapeutique qui présente, à leur point de vue, d'énormes risques : à partir du moment où l'on prélève un noyau sur une cellule déjà engagée dans une voie de différenciation, on ne peut être certain de l'intégrité de son patrimoine génétique. On sait que dans un tissu somatique, la proportion de cellules qui renferment des anomalies génétiques est très importante. On pourra détecter un réarrangement chromosomique mais non des anomalies ponctuelles et ce risque paraît trop élevé pour une utilisation thérapeutique » .
Ainsi votre commission préconise-t-elle, pour ces trois raisons, de prévoir l'interdiction de création d'embryons par FIV comme par clonage à des fins de recherches.
Sous le bénéfice de ces observations, elle vous propose d'adopter cet article ainsi amendé.
Article 20
Cellules embryonnaires ou foetales issues
d'interruptions de
grossesse
Objet : Cet article précise le régime des cellules embryonnaires ou foetales issues d'interruptions de grossesse, s'agissant de leur prélèvement, de leur conservation et de leur utilisation.
I - Le dispositif proposé
Le présent article propose d'insérer un nouvel article L. 1241-5 dans le code de la santé publique au sein du chapitre relatif au prélèvement et à la collecte des tissus, cellules et produits issus du corps humain.
Le texte proposé pour l'article L. 1241-5 précise le statut juridique des tissus et cellules embryonnaires ou foetaux prélevés à la suite d'une interruption de grossesse. Il est composé de cinq alinéas :
- le premier prévoit que ces tissus ou cellules ne peuvent être prélevés qu'à des fins scientifiques ou thérapeutiques, et que la personne ayant subi l'interruption de grossesse, après avoir reçu une information appropriée sur les finalités du prélèvement, dispose de la faculté de s'y opposer ;
- le deuxième alinéa prohibe tout prélèvement sur mineure ou majeure protégée sauf afin de rechercher les causes de l'interruption de grossesse ;
- le troisième alinéa dispose que lorsque ces produits sont conservés, ils sont soumis aux principes généraux du code de la santé publique relatifs aux don et utilisation des produits du corps humain, tels que modifiés par le présent projet de loi à son article 5 ;
- le quatrième alinéa prévoit l'obligation d'établir un protocole pour les prélèvements à des fins scientifiques, protocole soumis à l'APEGH qui en communique la liste à l'EFG et au ministre en charge de la recherche ;
- le cinquième alinéa prévoit, enfin, que ce ministre peut suspendre ou interdire ces protocoles lorsque leur nécessité ou leur pertinence scientifique n'est pas établie.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a modifié à quatre reprises la rédaction proposée pour l'article L. 1241-5 du code de la santé publique :
- à l'initiative de sa commission spéciale, elle a adopté un amendement ajoutant à la liste des finalités possibles de ces prélèvements, scientifiques ou thérapeutiques, la finalité diagnostique afin de permettre de déterminer les causes d'une interruption non volontaire de grossesse ;
- à l'initiative de sa commission spéciale et de M. Jean-François Mattei et plusieurs de ses collègues, elle a adopté un amendement disposant que l'information relative à la finalité du prélèvement doit être postérieure à la décision prise par la femme d'interrompre sa grossesse ;
- à l'initiative de sa commission spéciale, elle a adopté un amendement rédactionnel précisant que la pertinence des protocoles est appréciée d'un point de vue « scientifique ».
III - La position de votre commission
Une carence législative ancienne
Les interrogations relatives à l'utilisation des tissus et cellules foetaux issus d'une interruption de grossesse sont anciennes. Elles ont fait l'objet du premier avis rendu par le Comité consultatif national d'éthique, le 22 mai 1984. A cette occasion, ce Comité a formulé quatre principes :
- « l'embryon ou le foetus doit être reconnu comme une personne humaine potentielle qui est ou a été vivante et dont le respect s'impose à tous » . De ce principe, il déduit deux interdits : la recherche in utero ou le maintien artificiel de la vie du foetus à des fins de recherche, et l'utilisation commerciale ou industrielle de ces derniers ;
- « les principales objections d'ordre éthique élevées contre la légitimité des prélèvements de tissus d'embryons ou de foetus morts ont pour cause la provenance de ceux-ci lorsque leur mort est due à une interruption volontaire de grossesse » . Le comité prévoit à ce titre la nécessité d'une clause de conscience pour les praticiens ne souhaitant pas se livrer à de tels prélèvements et pour les autres, deux catégories de directives à suivre.
Les premières sont d'ordre éthique et visent à limiter les finalités de ces recherches. Ainsi le prélèvement à des fins thérapeutiques « doit avoir un caractère exceptionnel justifié, en l'état actuel des connaissances, à la fois par la rareté des maladies traitées, l'absence de toute autre thérapeutique également efficace, et l'avantage manifeste, tel que la survie, que retirera le bénéficiaire du traitement ». Les prélèvements à des fins de recherche, quant à eux, doivent « poursuivre un but spécialement important et spécialement utile au progrès des thérapeutiques ». Dans tous les cas, le comité prévoit le recours à un comité d'éthique qui apprécie la conformité des prélèvements aux principes susmentionnés.
Les directives déontologiques et médicales visent d'une part à préserver les intérêts de la femme, et pour cela, que « la décision et les conditions de l'interruption de grossesse ne doivent en aucun cas être influencées par l'utilisation ultérieure possible ou souhaitée de l'embryon ou du foetus ». Le Comité a en outre insisté pour qu'« une totale indépendance soit établie et garantie, sous le contrôle du Comité d'éthique, entre l'équipe médicale qui procède à l'IVG et l'équipe susceptible d'utiliser les embryons ou les foetus » ;
- il a précisé que « seuls peuvent être utilisés les embryons ou foetus n'ayant pas atteint le seuil de la viabilité et dont la mort a été préalablement constatée » ;
- enfin, « les prélèvements de tissus embryonnaires ou foetaux à des fins thérapeutiques ou scientifiques peuvent être interdits par la mère ou le père qui disposent de la faculté de s'y opposer. »
Pour autant, ces directives nombreuses et précises n'ont pas fait l'objet d'une traduction législative, la loi n° 94-654 du 29 juillet 1994 restant silencieuse sur la question du prélèvement de tissus et cellules foetaux et embryonnaires.
Dans leur rapport relatif à l'application de cette loi, MM. Claude Huriet et Alain Claeys 91 ( * ) ont rappelé les enjeux de cette question :
« Cette question, déjà posée sous l'empire de la loi Caillavet, n'a pas été davantage tranchée par le législateur de 1994 qui ne l'a même pas évoquée dans les travaux préparatoires.
« La finalité de ces prélèvements, en dehors des visées diagnostiques qui ne posent pas de problème, peut être thérapeutique ou scientifique.
« Sur le plan thérapeutique, la transplantation de cellules souches hépatiques embryonnaires a été réalisée pour traiter les déficits immunitaires héréditaires. Plus récemment, se sont développées des recherches sur l'intérêt des transplantations de cellules nerveuses embryonnaires pour le traitement de certaines maladies neurovégétatives : maladie de Parkinson, chorée de Huntington.
« Dans le silence de la loi, certains juristes ont cru pouvoir considérer que le régime des résidus opératoires s'appliquait de plano aux prélèvements et à l'utilisation des tissus, cellules ou produits d'embryons ou de foetus humains morts des suites d'une intervention médicale et, notamment, d'une interruption volontaire de grossesse. Rien, dans les travaux préparatoires, ne permet de l'affirmer et ceux-ci autorisent même une argumentation inverse : en effet, si la notion de déchet opératoire a pu être jugée insuffisante pour inclure le placenta (celui-ci ayant été rajouté au cours de la navette), il est difficilement admissible qu'elle s'applique, sans disposition expresse, aux prélèvements sur foetus et embryons morts . »
Certes les auteurs de l'évaluation soulignent que « face à la carence de la loi, les professionnels se réfèrent, pour guider leur pratique, aux avis du Comité consultatif national d'éthique » .
Mais, c'est à juste titre qu'ils concluent que « la multiplication vraisemblable de ces types de greffes à partir de prélèvements embryonnaires et foetaux nécessitera sans doute une intervention du législateur , les lacunes des textes ne pouvant être comblées par les seuls avis d'une instance consultative, si éminente qu'elle soit ». C'est en partie chose faite par les dispositions du présent article 20.
Des difficultés en suspens ?
Le présent article résout sans nul doute la plupart des difficultés qu'entraînait l'absence de régime juridique pour les tissus et cellules prélevés au cours d'une interruption de grossesse. Il est aujourd'hui bien établi qu'en aucun cas ces tissus peuvent être assimilés à des résidus ou déchets opératoires.
Cela étant, un certain nombre de questions restent posées.
Il s'agit en premier lieu de la nature du consentement de la femme subissant l'interruption de grossesse. La règle du consentement présumé est-elle en elle-même satisfaisante ? A cet égard, M. Jean-François Mattei, député, a proposé à la commission spéciale de l'Assemblée nationale « que la personne consente expressément au prélèvement. [Estimant que] le choix visant à lui reconnaître qu'un droit de s'y opposer relève d'une conception contestable des modes d'expression du consentement » 92 ( * ) .
La séparation des activités de prélèvement des activités médicales d'interruption n'est pas consacrée alors même que le comité consultatif d'éthique la faisait figurer parmi les principes déontologiques essentiels.
La place du père est, là encore, une des difficultés suscitées par le présent texte. Doit-on, ainsi que l'envisage le comité d'éthique, prévoir la faculté d'opposition de ce dernier ? Votre rapporteur, qui n'ignore pas que la présence du père est hasardeuse dans le processus d'une interruption de grossesse dont la décision in fine appartient à la mère, ne voit pas en l'état comment assurer la conciliation de ces principes.
Votre commission vous propose néanmoins d'adopter un amendement précisant que le droit de veto du ministre de la recherche sur les protocoles prévus par cet article s'exerce également au regard du respect des « principes éthiques» , c'est-à-dire, selon une formule similaire à celle prévue par l'article L. 2151-3 du code de la santé publique (article 19 du présent projet de loi) pour autoriser la recherche sur l'embryon. Il sera bien évidemment compris que cette référence est constituée des principes éthiques susmentionnés, formulés par le Comité consultatif national d'éthique.
Votre commission vous propose d'adopter cet article ainsi amendé.
CHAPITRE V
-
DISPOSITIONS PÉNALES
Article 21
Dispositions pénales
Objet : Cet article fixe les conséquences, en matière pénale, des modifications apportées notamment aux dispositions relatives à l'embryon.
I -Le dispositif proposé
Le présent article précise le régime des peines applicables aux infractions en matière d'assistance médicale à la procréation, de manipulations sur l'embryon ou de cellules et tissus foetaux.
Le 1° propose une modification de l'article 511-1 du code pénal, article qui rend aujourd'hui la pratique de l'eugénisme passible d'une peine de réclusion de vingt années.
La rédaction proposée par le présent article propose de maintenir cette peine pour réprimer les pratiques eugéniques (1°) et de l'étendre au clonage reproductif (2°) défini juridiquement comme « le fait de procéder à une intervention en vue de faire naître un enfant qui ne serait pas directement issu des gamètes de l'homme et de la femme ».
Le 2° tire les conséquences, au sein de l'article 511-1 du code pénal, de la renumérotation des articles L. 2141-4 et 2141-5 du code de la santé publique décidée à l'article 18 du projet de loi selon une pratique contre laquelle votre commission s'élève vainement depuis trois ans.
Le 3° propose une modification de l'article 511-19 du code pénal sanctionnant le non-respect des dispositions régissant les études ou les expérimentations sur l'embryon.
La peine aujourd'hui prévue est de sept ans de prison et 106.715 euros (700.000 francs) d'amende.
La modification vise à prendre en compte l'introduction par l'article 19 du projet de loi, de l'autorisation de mener des recherches sur l'embryon. Ces dernières étant très strictement encadrées, la violation des dispositions prévues pour cet encadrement doit nécessairement être lourdement sanctionnée. L'article prévoit en conséquence la même peine -sept ans de prison et 100.000 euros d'amende- pour le fait de se livrer à des recherches sur l'embryon hors d'un protocole validé par l'APEGH (1° de la rédaction proposée pour l'article 511-19) ou si ces recherches ne respectent pas les dispositions dudit protocole (2° de la rédaction proposée pour l'article 511-19).
Le 4° propose la création d'un nouvel article 511-19-1 du code pénal qui fixe le régime de peine applicable au non-respect du régime juridique des prélèvements, conservation et utilisation des tissus ou cellules embryonnaires ou foetales, régime juridique prévu par l'article 20 du présent projet de loi. Ce non-respect est puni de deux ans de prison et 30.000 euros d'amende.
Le 5° modifie l'article 511-22 du code pénal qui réprime la poursuite d'activité d'AMP sans être titulaire de l'autorisation prévue à l'article L. 2142-1 du code de la santé publique. La rédaction proposée par le 5° de cet article vise à punir les mêmes faits ou celui qui consisterait à ne pas se conformer aux dispositions dudit article (obligations applicables aux activités cliniques d'assistance médicale à la procréation). L'ancienne peine est maintenue, soit deux ans d'emprisonnement et 300.000 euros d'amende.
Le 6 ° propose un nouveau contenu pour l'article 511-23 du code pénal. Celui-ci prévoyait précédemment une peine de deux ans d'emprisonnement et 200.000 francs d'amende pour la divulgation d'informations nominatives visant à identifier les couples ayant consenti à l'accueil d'un embryon et le couple l'ayant accueilli.
La nouvelle rédaction prévoit de punir de trois ans d'emprisonnement et 45.000 euros d'amende le fait d'introduire ou de faire sortir du territoire des embryons sans l'accord préalable du ministre de la santé.
L'ancienne rédaction est reproduite au II de l'article 511-25 du même code (cf. 7° ci-dessous).
Le 7° modifie les articles 511-25 et 511-26 du code pénal.
Dans sa rédaction actuelle, l'article 511-25 punit le fait de réaliser un transfert d'embryons sans avoir respecté une règle de sécurité sanitaire essentielle -avoir pris connaissance des résultats des tests de dépistage de maladies infectieuses- d'une peine de deux ans de prison et 200.000 francs d'amende.
Le I de la nouvelle rédaction proposée pour cet article prévoit cette même peine pour les infractions suivantes :
- le transfert d'embryon hors de l'autorisation donnée par un juge (2°) à un couple d'accueillir cet embryon ;
- le fait de n'avoir pas pris connaissance des tests cités ci-dessus (3°). Il s'agit de l'ancien article 511-25 ;
- le fait de n'avoir pas eu recours à un établissement dûment habilité.
Le II de cet article reproduit l'ancienne rédaction du code pénal pour l'article 511-23 (cf. ci-dessus) .
L'article 511-26 punit des mêmes peines la tentative des faits incriminés ci-dessus.
II - Les modifications adoptées par l'Assemblée nationale
L'Assemblée nationale a modifié cet article à sept reprises.
Sur proposition de sa commission spéciale, elle a adopté un amendement modifiant le 2° du texte proposé pour l'article 511-1 du code pénal pour y préciser l'incrimination relative au clonage (cf. ci-dessous) .
Sur proposition de sa commission spéciale, elle a adopté un amendement durcissant la répression du clonage reproductif en prévoyant l'incrimination du donneur de gamètes à cette fin (article 511-1-1) et l'extraterritorialité de la répression de ce dernier (article 511-1-2) .
Les couples de nationalité française ou résidant habituellement en France, qui tenteraient de faire naître un enfant par clonage, risqueraient ainsi une peine de cinq ans de prison.
Sur proposition de sa commission spéciale, elle a adopté un amendement étendant l'incrimination prévue par l'article 511-19 du code pénal au cas où une recherche sur l'embryon serait réalisée sans respecter les prescriptions législatives et réglementaires posées pour autoriser cette recherche.
Sur proposition de sa commission spéciale, elle a étendu la peine prévue par l'article 511-19-1 du code pénal aux cas où le protocole prévu par l'article 20 du présent projet a été interdit ou suspendu.
Sur proposition de sa commission spéciale et de M. Jean-François Mattei et plusieurs de ses collègues, elle a adopté un amendement visant à doubler la peine prévue à l'article 511-19-1.
Elle a enfin, à l'initiative de sa commission spéciale, adopté un amendement corrigeant une erreur matérielle.
III - La position de votre commission
Le durcissement du régime pénal des infractions à la législation sur l'AMP et l'embryon
Les dispositions proposées par le présent article relatif au régime pénal des infractions à la législation sur l'AMP et l'embryon établissent les barrières qu'une société doit nécessairement poser à ce type d'activité.
Les lois bioéthiques de 1994 prévoyaient déjà, pour leur part, des dispositions essentielles tendant à éviter certaines des plus effroyables dérives. Votre rapporteur pense ici notamment à l'eugénisme.
La science et les techniques ont, en cinq ans, formidablement évolué. Ces évolutions justifient aujourd'hui un meilleur encadrement qui doit, pour être respecté, être assorti de sanctions pénales plus en rapport avec les transgressions que ces sujets peuvent susciter.
Dans bien des cas, il est donc prévu par cet article de préciser des régimes pénaux afin de les rendre plus adéquats.
Ce présent projet de loi propose trois innovations nécessaires.
Les deux premières visent à assurer le respect de dispositions nouvelles qui entourent le transfert hors frontières d'embryons et l'utilisation des tissus et cellules issus d'une interruption de grossesse. Ces dispositions étaient nécessaires. La sanction accompagnant leur non-respect l'est également.
La troisième vise à pénaliser lourdement la notion de clonage reproductif. Sans revenir sur les difficultés soulevées par la rédaction proposée, qui sont exposées à l'article 15, votre commission s'interroge sur la peine qu'il est nécessaire d'infliger à ce type de pratiques. Le droit en vigueur ne prévoyait pas de peine. C'est en effet par déduction qu'il était convenu que ces dispositions contrevenaient à l'article 16-10 du code civil.
Quelle peine pour le clonage reproductif ?
La question qui a été in fine posée devant l'Assemblée nationale était de savoir si cette pratique relevait d'une variante de la notion de crime contre l'humanité ou non.
Pour sa part, M. Jean-François Mattei a précisé devant votre commission son souhait de voir créer la notion de « crime contre la dignité de l'homme ».
« Pour moi, le clonage reproductif est, au niveau de la personne, l'équivalent de ce qu'est le crime contre l'humanité au niveau collectif.
« Le crime contre l'humanité est un crime contre l'espèce humaine en ce sens que, d'une façon massive et organisée, on vient porter atteinte à la dignité de la personne.
« Concevoir quelqu'un en l'enfermant dans un destin génétiquement programmé, choisi et délibéré, c'est le priver de sa liberté et, le privant de sa liberté, c'est porter atteinte à sa dignité !
« Je pense donc -et j'ai l'accord du Garde des Sceaux- vous proposer une nouvelle incrimination, basée par comparaison sur les peines les plus lourdes dans des champs voisins, en ayant d'une part, à partir de la majorité éventuelle de l'enfant cloné, une prescription trentenaire, ce qui équivaut quasiment à une imprescriptibilité, et en instituant, d'autre part, une extraterritorialité, car on peut être Français et aller se faire cloner dans des zones internationales, puis revenir en France.
« Comme pour le tourisme sexuel -pardonnez-moi la comparaison, mais c'est comme cela et je peux justifier que ceci existe déjà- le clonage sera condamné en France pour des citoyens français vivants en France, quand bien même il aurait eu lieu à l'étranger !
« C'est à mon avis la seule force que nous ayons pour continuer à mener notre croisade internationale et déboucher sur une interdiction formelle par les Nations-Unies. »
Votre Commission partage pleinement la préoccupation exprimée par le ministre et soutiendra l'initiative qu'il annonce. Dans l'immédiat, elle propose deux amendements au présent article. En effet, ce dernier :
- ne prévoit plus d'incrimination pour le non-respect des dispositions entourant la conduite d'études sur l'embryon expressément mentionnées à l'amendement que votre commission vous propose pour l'article L. 2151-3 du code de la santé publique (article 19) . Par coordination, votre commission vous propose de maintenir cette incrimination ;
- comporte une erreur de référence, les dispositions visées à l'article 123-6 du code pénal figurant en réalité à l'article 113-6 du code pénal.
Elle vous propose d'adopter cet article ainsi amendé.
Article 21 bis
Rapport sur les initiatives françaises en faveur
d'une législation internationale réprimant le clonage
reproductif
Objet : Cet article a pour objet de prévoir un rapport sur les initiatives prises au niveau international pour lutter contre le clonage.
A l'initiative de M. Jean-Pierre Foucher et de sa commission spéciale, l'Assemble nationale a adopté un rapport prévoyant que le Gouvernement devra, dans un délai d'un an après la publication de la présente loi, remettre un rapport sur les initiatives prises par la France au niveau international contre le clonage reproductif.
Votre commission, qui a transféré par amendement cet article après l'article 15, vous propose, par coordination, d'adopter un amendement de suppression de cet article.
Article 22
Coordination
Objet : Cet article a pour objet de prévoir, en miroir, dans le code de la santé publique, le régime pénal prévu en cas d'infraction à la législation sur l'AMP et l'embryon.
Selon la technique dite du « code suiveur », le présent article insère, en miroir, au sein du code de la santé publique les dispositions pénales prévues par l'article 21 du présent projet de loi.
Le premier titre disposait déjà, en miroir, d'un chapitre rappelant solennellement les dispositions pénales réprimant les atteintes à l'embryon. Ce chapitre était le cinquième de ce titre. L'article 19 du présent projet prévoit la création d'un nouveau chapitre consacré à la recherche sur l'embryon, qui devient le cinquième. Les dispositions pénales deviennent donc, en conséquence, le sixième chapitre.
I - Le dispositif proposé
Le I , par coordination, vise à renuméroter le chapitre III de l'actuel titre V, consacré aux « dispositions communes » en chapitre V.
Le II du présent article modifie le chapitre II de l'ancien titre V devenu titre VI qui concerne les sanctions pénales relatives à l'AMP.
Le 1° renumérote les articles L. 2162-6 à L. 2162-11 en articles L. 2162-4 à L. 2162-9.
Le 2° réécrit l'article L. 2162-8 -actuellement L. 2152-10- pour étendre la possibilité de condamner les tentatives au même titre que les faits incriminés par les articles L. 2162-2 et L. 2164-1.
Le 3° abroge l'article L. 2162-9 du code de la santé publique devenu inutile.
Le III crée un nouveau chapitre III dans le titre susmentionné pour y faire figurer les dispositions prévues à l'article 511-1 du code pénal, condamnant le clonage reproductif et 511-19 du même code sanctionnant le non-respect des conditions légales pour mener la recherche sur l'embryon.
Le IV complète le chapitre II du titre VII du livre II de la première partie du code de la santé publique afin d'y faire figurer les dispositions de l'article 511-19 (nouveau) du code pénal relatif au non-respect des conditions légales posées pour le prélèvement et l'utilisation de cellules embryonnaires ou foetales.
II - Les modifications adoptées par l'Assemblée nationale
Sur proposition de sa commission spéciale, l'Assemblée nationale a adopté un amendement rédactionnel faisant précéder le I proposé par cet article d'un « A » et le IV d'un « B », un amendement rectifiant une erreur matérielle, un amendement de cohérence avec la rédaction modifiée de l'article 21 pour prévoir le rappel, au sein du code de la santé publique, des articles L. 511-1-1 et L. 511-1-2 nouveau, enfin un amendement rédactionnel.
III - La position de votre commission
Par coordination, votre commission proposera les mêmes amendements qu'à l'article 21 visant les articles 511-12, 511-19 et 511-19-1 du code pénal.
Elle réitère en outre (cf. commentaire ci-dessus de l'article 6) ses plus extrêmes réserves quant à la démarche choisie de déplacement du contenu des articles du code de la santé publique, assorti de dénumérotation et de renumérotation des articles, qui fait peu de cas de la lisibilité de la loi.
Sous le bénéfice de ces informations, votre commission vous propose d'adopter cet article ainsi amendé.
TITRE
V
-
DISPOSITIONS DIVERSES ET TRANSITOIRES
Article 23
Prorogation des mandats des membres
des comités
d'experts
Objet : Cet article a pour objet de proroger les mandats des comités d'experts autorisant le prélèvement de moelle osseuse sur mineur.
Le dispositif proposé par le présent article vise à prolonger les mandats des comités chargés d'autoriser les prélèvements de moelle osseuse sur mineurs. Afin de prévenir toute discontinuité, et avant l'installation des comités chargés d'autoriser les prélèvements de moelle hématopoïétique sur mineurs, le mandat de ces comités doit être prolongé par une disposition législative, puisque la durée de leur mandat était fixée par la loi pour une durée de trois ans.
L'Assemblée nationale a adopté cet article sans modification.
Sans aucun doute, le dispositif proposé est en soi nécessaire mais son utilité est lourdement remise en cause par la lenteur de la navette. En effet, si l'exposé des motifs est exact, le mandat de ces derniers est déjà venu à échéance. L'exposé des motifs du présent projet de loi indique en effet que cette échéance était le 4 juin 2002.
Sous le bénéfice de cette information, votre commission vous propose d'adopter cet article sans modification .
Article 24
Prorogation d'autorisations de prélèvements de
moelle osseuse
et de cellules de la moelle
hématopoïétique
Objet : Cet article organise un régime transitoire en matière d'autorisation de prélèvement de moelle osseuse qui cesse de relever du régime des organes pour être rattachée à celui des cellules.
Le I de cet article vise à proroger, pour un an, l'autorisation délivrée aux établissements de santé de prélever de la moelle osseuse.
Cette dernière change en effet de statut, du fait des dispositions du présent projet de loi. Désormais le régime juridique du prélèvement de tissus et cellules leur sera applicable et non plus celui relatif aux organes.
Ainsi que l'indique l'exposé des motifs, cette prorogation était dicté par une double préoccupation :
- la prorogation des autorisations actuelles : ce changement de catégorie juridique a des conséquences au regard de la validité des autorisations actuelles de prélèvement, qui sont délivrées pour la moelle osseuse selon les règles applicables aux organes, et non pour les cellules de la moelle hématopoïétique, selon un décret à prendre pour les prélèvements de cellules. Ces autorisations devraient arriver à échéance courant 2002. Si, à cette date, le projet de loi n'a pas encore abouti, ces autorisations seront renouvelées selon le régime actuel et il n'y aura pas de rupture de l'activité de prélèvement ;
- en revanche, si la loi intervient avant l'échéance des autorisations actuelles, il convient de prolonger leur validité pour permettre la continuité de ces activités pendant la période nécessaire à l'intervention du décret encadrant les prélèvements de cellules prévu à l'article L. 1242-1 du code de la santé publique issu du projet de loi, et le dépôt des demandes d'autorisation.
C'est in fine la première hypothèse qui s'est réalisée, du fait du retard pris dans l'adoption de ce projet de loi.
Non seulement les autorisations des établissements sont venues à échéance, et le pouvoir réglementaire les aura renouvelées, mais à la date d'entrée en vigueur de la loi, leur validité devra, contrairement à ce que laisse entendre l'exposé des motifs, être maintenue dans l'attente de l'édiction du décret encadrant les prélèvements de cellules sans lequel le dépôt des demandes d'autorisation ne pourrait avoir lieu.
Le II prévoit d'ouvrir, pour les mêmes raisons, la faculté au directeur des Agences régionales d'hospitalisation d'autoriser les établissements de santé remplissant les conditions techniques et sanitaires prévues actuellement à effectuer des prélèvements de moelle osseuse.
Cette autorisation exceptionnelle s'exerce sous deux conditions :
- elle est limitée dans le temps,
- elle n'est possible qu'en cas d'insuffisance d'établissements déjà autorisés sur la région.
L'Assemblée nationale a adopté cet article sans modification.
Votre commission vous propose d'adopter cet article sans modification.
Article 25
Dispositions transitoires relatives aux préparations de
thérapie génique
et cellulaire xénogénique
Objet : Cet article met en place, pour les préparations de thérapie génique et les préparations de thérapie cellulaire xénogénique, des équivalences entre les autorisations accordées sous l'empire des dispositions actuellement en vigueur et celles que prévoit le présent projet de loi.
Les préparations de thérapie génique et les préparations de thérapie cellulaire xénogénique sont effectuées dans des conditions qui n'impliquent pas un régime différent de celui fixé par les dispositions prévues par le présent projet de loi.
Ainsi le présent article prévoit-il un régime d'équivalence pour les autorisations délivrées aux établissements se livrant à des activités de transformation, conservation, distribution, cession importation, exportation, greffe ou administration des produits cellulaires, lorsque cette autorisation a été délivrée dans des conditions respectueuses de la législation alors en vigueur et modifiée par le présent projet de loi.
Le I de cet article pose le principe d'équivalence pour les autorisations visées aux articles L. 1243-2, L. 1243-6 et L. 5152-3 du présent code (cf. articles 8 et 13).
Le II propose un dispositif identique pour les autorisations délivrées pour les produits visés aux articles L. 1243-5 et L. 5152-1 du présent code (cf. articles 8 et 13).
L'Assemblée nationale a adopté un amendement substituant, dans le I de cet article, les références L. 1245-5 et L. 5152-2 à la référence L. 5124-3.
Votre commission vous propose d'adopter cet article sans modification.
Article 26
Dispositions transitoires relatives aux activités de
conservation
et cession d'éléments du corps humain
Objet : Cet article aménage un délai pour la mise en conformité des organismes se livrant à des activités de conservation et de cession d'éléments du corps humain à des fins de recherche.
Le présent article, adopté sans modification par l'Assemblée nationale, prévoit un régime transitoire pour les activités et établissements exerçant des activités de conservation et de cession d'éléments du corps humain à des fins de recherche.
Le I prévoit que les activités prévues à l'article L. 1243-3 (cf. article 8), c'est-à-dire la conservation, la transformation à des fins scientifiques des éléments et produits du corps humain et la constitution et l'utilisation de collections d'échantillons biologiques humains, fassent l'objet d'une déclaration au ministre en charge de la recherche.
Le II prévoit que les organismes se livrant à des opérations de préparation ou conservation en vue de cession d'éléments et produits du corps humain pour un usage scientifique prévu par l'article L. 1243-4 (article 8), disposeront d'un régime transitoire quelque peu différent. Ils devront, en effet, dans un délai de deux ans, déposer leur demande d'autorisation. Leur activité pourra être poursuivie jusqu'à la décision du ministre en charge de la recherche de leur délivrer ou de leur refuser cette autorisation.
Votre commission vous propose d'adopter cet article sans modification.
Article 27
Entrée en vigueur des dispositions relatives
à
la recherche sur l'embryon
Objet : Cet article conditionne l'entrée en vigueur des dispositions relatives à la recherche sur l'embryon à la mise en place de la nouvelle Agence de la procréation, de l'embryologie et de la génétique humaine.
Le présent article conditionne l'entrée en vigueur des dispositions prévues aux articles L. 1241-5 et L. 2151-3 du code de la santé publique, tels que prévus par le présent projet de loi, à l'installation de l'APEGH.
Le premier de ces articles prévoit le régime juridique des recherches scientifiques menées sur des cellules ou tissus issus de foetus ou d'embryons prélevés à l'occasion d'interruption de grossesse (cf. article 20).
Le second prévoit le régime juridique des recherches sur l'embryon.
Ces deux types de recherches supposent l'existence préalable de protocoles scientifiques autorisés par l'APEGH.
Par coordination, votre commission vous propose un amendement substituant aux mots « Haut Conseil » les mots « conseil d'orientation médical et scientifique ».
Votre commission vous propose d'adopter cet article ainsi amendé.
Article 28
Dispositions applicables à Mayotte, au territoire des
îles Wallis-et-Futuna, des terres australes et antarctiques
françaises, en Polynésie française
et en
Nouvelle-Calédonie
Objet : Cet article autorise le Gouvernement à étendre par ordonnance les dispositions du présent projet de loi à Mayotte, aux îles Wallis-et-Futuna, aux terres australes et antarctiques françaises, à la Polynésie française et à la Nouvelle-Calédonie.
Les projets d'ordonnance, pris en application de l'habilitation prévue au présent article, devront, le cas échéant, être soumis pour avis aux autorités de ces territoires, dans la mesure des compétences qui leur sont dévolues.
Il appartiendra au Parlement de veiller, lors de la ratification des dispositions adoptées par voie d'ordonnance, au respect des prérogatives de chaque territoire.
Sous le bénéfice de cette observation, votre commission vous propose d'adopter cet article sans modification .
Article 29 (nouveau)
Révision de la loi et évaluation de son
application
Objet : Cet article, introduit par l'Assemblée nationale, prévoit une révision de la loi dans un délai de quatre ans et son évaluation par l'Office parlementaire des choix scientifiques et technologiques.
L'Assemblée nationale, sur proposition de sa commission spéciale, a adopté le présent article additionnel prévoyant la révision de la loi et l'évaluation de son application dans un délai de quatre ans.
Votre commission a bien entendu les arguments avancés lors de son audition par M. Jean-François Mattei sur le principe d'une révision périodique de la loi, prévue selon un échéancier fixe.
« Je ne suis pas favorable à ce que, dans cette révision, on fixe à nouveau une clause de révision à cinq ans ! C'était nécessaire la première fois parce qu'on était dans le doute, mais je ne suis pas sûr qu'il faille à nouveau nous avancer vers une révision systématique, si ce n'est sur certains points précis, sauf à laisser croire que la biomédecine forgerait, au fil des années, sa propre éthique.
« Vous avez, au Sénat ou à l'Assemblée nationale, abordé le sujet de l'interruption volontaire de grossesse ainsi que celui de la prolongation du délai et, chemin faisant, le problème de la stérilisation des femmes adultes handicapées. Personne ne peut nier qu'il y avait une dimension éthique dans ces textes-là ! Dans le texte sur le droit des malades, l'éthique était sous-jacente.
« Le seul fait de dire que l'on va légiférer sur la bioéthique pourrait laisser penser qu'il n'y a pas d'éthique ailleurs. C'est un grave danger !
« Second danger : pendant les cinq années qui se sont écoulées, on a bien vu qu'il était nécessaire de prendre des décisions, parfois sans trop attendre. On nous disait pourtant de ne pas nous inquiéter, qu'on allait le traiter avec les lois de bioéthique.
« On a donc pris du retard dans certaines dispositions qui auraient dû s'imposer plus tôt. Inversement, on nous demande de saisir l'occasion de prendre en compte des techniques dont on voit bien qu'elles ne sont pas encore suffisamment matures pour que l'on puisse d'ores et déjà en définir clairement les usages et les indications.
« Je dois vous dire que je ne souhaite pas cette clause. Désormais, la bioéthique s'est installée dans notre paysage et, plutôt que d'être fragilisé sur cette durée provisoire, je souhaite que l'on consolide nos positions. Je vous le redis donc : l'inscription dans la loi du principe de sa révision m'apparaît comme un procédé ambigu et néfaste.
« Il est ambigu désormais car, finalement, il est dépourvu de toute valeur normative. Il ne contraint en rien le législateur et ne modifie pas la faculté dont dispose celui-ci, à tout moment, de remettre la loi en chantier, si cela s'avère nécessaire.
« On a fini par dire : « On verra dans cinq ans ». Non ! On verra quand le besoin s'en fera sentir et, parfois, sans attendre.
« Probablement est-ce même néfaste, parce que le législateur n'a pas, en particulier lorsqu'il édicte des principes, vocation à faire une oeuvre dont la date de péremption est par avance annoncée. Comment ne pas voir que c'est la loi dont la solennité et la légitimité se trouveraient malmenées ?
« Si l'on veut que les normes édictées aient toute leur valeur, il ne faut pas, dans une perspective instrumentale, qu'elles soient constamment remodelées.
« Il est donc à mon avis essentiel qu'elles ne soient pas conçues d'emblée comme caduques. Autrement dit, nous avons pris le temps nécessaire pour fixer notre ensemble en deux étapes -l'adoption première et la révision ».
Si votre commission n'est, à l'instar du ministre, pas favorable au principe d'une révision en quelque sorte « à terme échu », puisque ce terme ne s'impose pas clairement, elle souhaite néanmoins formuler une remarque et une proposition :
- le maintien de la révision dans un délai de cinq ans est d'autant plus superfétatoire que la loi fixe elle-même des points particuliers sur lesquels le législateur devra se pencher. Ainsi en est-il de l'ouverture dérogatoire des recherches sur l'embryon qui n'est que transitoire. Un rendez-vous est pris dès aujourd'hui pour dans cinq ans ;
- l'excellent travail réalisé par MM. Claude Huriet et Alain Claeys a montré l'utilité d'une évaluation de l'application de la loi par l'OPESCT. Sans doute cet Office pourrait procéder à cette évaluation hors de toute habilitation législative expresse. Néanmoins, cette dernière lui confère une autorité particulière que votre commission n'a pas jugé bon de supprimer.
Elle vous propose en conséquence d'adopter cet article ainsi amendé .
TRAVAUX DE LA COMMISSION
Réunie le mercredi 15 janvier 2003 , sous la présidence de M. Nicolas About, président , la commission a procédé à l'examen du rapport de M. Francis Giraud, sur le projet de loi n° 189 (2001-2002) relatif à la bioéthique.
|
M. Nicolas About, président, a rappelé que M. Francis Giraud, rapporteur, avait conduit depuis février 2002 un large programme d'auditions auquel il avait souhaité convier les commissaires intéressés. Ces travaux ont été complétés par une journée d'auditions publiques de la commission, le 4 décembre 2002, dont le compte rendu intégral, déjà adressé aux membres de la commission, sera annexé au rapport sur le projet de loi. M. Nicolas About, président, a rappelé également que la commission avait accepté de saisir la délégation sénatoriale aux droits des femmes et à l'égalité des chances entre les hommes et les femmes. Il a demandé en conséquence à Mme Sylvie Desmarescaux, rapporteur pour la délégation, de présenter les recommandations formulées par cette dernière sur le projet de loi. Mme Sylvie Desmarescaux, rapporteur de la délégation , a précisé que la délégation s'était intéressée plus particulièrement aux dispositions du projet de loi relatives à l'assistance médicale à la procréation (AMP). Rappelant l'esprit dans lequel elle avait souhaité aborder ces dispositions, Mme Sylvie Desmarescaux, rapporteur de la délégation , a souligné que l'AMP n'était pas seulement une « médecine du désir » : elle soumettait les femmes à des traitements contraignants, et les engageait dans un parcours long et souvent douloureux. Aussi, sans freiner le progrès scientifique, il apparaissait indispensable de protéger les femmes contre d'éventuels risques pour leur santé, ou pour celle de l'enfant à naître. A cet égard, la mise en oeuvre des nouvelles techniques d'AMP soulevait aujourd'hui des questions. Mme Sylvie Desmarescaux, rapporteur de la délégation, a tenu à souligner qu'au-delà des risques médicaux, les implications humaines et psychologiques des décisions et l'accompagnement personnalisé des couples devaient être pris en considération et que la réflexion sur l'AMP devait être guidée par le souci de l'intérêt de l'enfant à naître et la responsabilité des couples au regard de leur projet commun. Puis Mme Sylvie Desmarescaux, rapporteur de la délégation, a communiqué la teneur des sept recommandations adoptées par la délégation le 14 janvier 2003 [voir rapport d'information de la délégation aux droits des femmes et à l'égalité des chances entre les hommes et les femmes n° 125 (2002-2003)]. La commission a alors entendu l'exposé de M. Francis Giraud, rapporteur. M. Francis Giraud, rapporteur, a rappelé qu'en 1994, après plusieurs années de réflexions, encouragé par les avancées considérables réalisées dans les domaines de la génétique et de la médecine de la reproduction, le Parlement s'était résolu à doter la France d'un cadre législatif : loi du 1 er juillet 1994 relative au traitement des données nominatives ayant pour fin la recherche dans le domaine de la santé, et deux lois du 29 juillet 1994, l'une relative au respect du corps humain et l'autre relative au don et à l'utilisation des éléments et produits du corps humain, à l'assistance médicale à la procréation et au diagnostic prénatal. Confronté à des questions éminemment complexes, pour lesquelles aucune solution évidente ne s'imposait, le législateur avait alors fait preuve de sagesse et de modestie, fixant des principes acceptés par tous dans les domaines qui s'y prêtaient, laissant dans l'ombre les aspects encore rebelles à son intervention et, surtout, prévoyant de lui-même qu'il lui faudrait remettre l'ouvrage sur le métier dans le délai, somme toute bref, de cinq années. Aussi, M. Francis Giraud, rapporteur, a tenu à rendre hommage à M. Jean Chérioux qui était alors le rapporteur de la commission. Il a souligné la qualité des travaux qui ont été conduits dans la perspective de la révision des lois bioéthiques, ceux notamment réalisés par l'Office parlementaire d'évaluation des choix scientifiques et technologiques, par le Conseil d'Etat et par la mission d'information de l'Assemblée nationale. Il a observé que rarement un projet de loi aura été précédé d'une réflexion préalable aussi complète, ce qui ne justifie pas pour autant le retard pris par le précédent Gouvernement qui n'a déposé le projet de loi sur le bureau de l'Assemblée nationale que le 21 juin 2001. Il s'est félicité que le nouveau Gouvernement ait pris la sage décision de ne pas interrompre la procédure législative pour présenter son propre projet de loi. En effet, le présent projet comporte beaucoup de mesures consensuelles, ou d'autres qui traversent les clivages partisans. Ainsi, pour la deuxième fois, le projet de loi relatif à la bioéthique sera examiné à cheval sur deux législatures séparées par une alternance politique. M. Francis Giraud, rapporteur, a considéré que le présent projet de loi apportait sans aucun doute des réponses aux difficultés sur lesquelles les lois de 1994 étaient restées silencieuses, où qui se sont trouvées posées du fait de l'application de cette dernière. Ainsi, en est-il du régime juridique applicable aux tests génétiques ou celui relatif à l'utilisation des éléments du corps humain. M. Francis Giraud, rapporteur, a constaté, à cet égard, la situation de déficit en greffons que notre pays connaît et souligné que le prélèvement post mortem fonctionnait en France moins bien que dans d'autres pays qui partagent pourtant les mêmes règles de consentement tel l'Espagne. Il a estimé que le « recours à la générosité des vivants » ne pouvait constituer la réponse à cette situation car les conséquences du don entre vifs peuvent être, pour le donneur, gravissimes. Aussi, a-t-il considéré que l'extension, par l'Assemblée nationale, du cercle des donneurs vivants à toute personne « ayant des liens étroits et stables » avec le receveur n'était pas souhaitable et qu'il convenait de mieux encadrer un élargissement raisonnable du cercle des donneurs vivants. Abordant l'évolution des pratiques d'AMP, M. Francis Giraud, rapporteur, a tout d'abord remercié Mme Sylvie Desmarescaux, rapporteur de la délégation aux droits des femmes et à l'égalité des chances entre les hommes et les femmes, pour les recommandations dont elle a bien voulu faire part à la commission, au nom de la délégation. Il a ensuite considéré que le projet de loi proposait des ouvertures utiles, s'agissant notamment de l'élargissement de l'indication d'AMP aux couples pouvant potentiellement se transmettre une maladie grave ainsi que du recueil et de la conservation de gamètes pour des personnes bénéficiant d'un traitement médical potentiellement attentatoire à leur fertilité. Il a observé que le texte initial du précédent gouvernement avait écarté deux dispositions sur lesquelles s'était pourtant interrogé le Conseil d'Etat : le transfert post mortem d'embryon et l'évaluation des techniques d'AMP lorsque celles-ci supposent la création d'embryon à cette fin. Il a regretté que l'Assemblée nationale n'ait pas retenu une telle prudence. L'évaluation préalable de toute nouvelle technique d'assistance médicale à la procréation avant sa mise en oeuvre lui a semblé partir d'un bon principe : éviter que ne se reproduise ce qui s'est passé dans le cas de l'injection cytoplasmique de sperme (ICSI). Mais le rapporteur a constaté également qu'elle conduisait à l'autorisation de concevoir des embryons pour cette évaluation, ce qui constituait une exception forte au principe selon lequel la conception in vitro d'embryons humains à des fins de recherche est interdite, principe qu'il proposait à la commission de confirmer. Il a précisé que c'était contre l'avis du Gouvernement que l'Assemblée nationale avait introduit la possibilité d'un transfert post mortem d'embryon et a souligné la gravité des interrogations éthiques et psychologiques que suscitait la mise au monde consciente d'un orphelin et le très petit nombre de cas concrets qui seraient concernés par cette disposition. Abordant la création d'une nouvelle agence de la procréation, de l'embryologie et de la génétique humaine (APEGH), M. Francis Giraud, rapporteur, a rappelé les propos du ministre de la santé, de la famille et des personnes handicapées devant la commission lors de son audition et a déclaré approuver la proposition faite d'un regroupement éventuel de cette agence avec l'Etablissement français des greffes (EFG) au sein d'une agence de biomédecine. Mais il a formulé un certain nombre d'observations pouvant s'appliquer aussi bien à l'APEGH qu'à une agence de biomédecine. Il a ainsi évoqué la question de la place, au sein de l'Agence, de la société civile en général, et du politique en particulier. Il a observé que l'Assemblée nationale avait renforcé les pouvoirs de l'Agence en confiant à son directeur général le soin d'autoriser les protocoles de recherche, les ministres conservant toutefois un droit de veto. Mais la création d'un Haut Conseil dont les pouvoirs restent au demeurant incertains lui a semblé relever davantage d'une sorte de magistrature morale que d'une mission de véritable vigilance. Aussi, afin de garantir un examen attentif et faire en sorte que la société civile soit à même de veiller au contenu scientifique et éthique des protocoles de recherche, a-t-il proposé de substituer au Haut Conseil un Conseil d'orientation médical et scientifique composé de dix-sept membres, dix scientifiques d'une part, et deux membres de hautes juridictions (Conseil d'Etat et Cour de cassation), un membre du comité consultatif d'éthique, un membre de la Commission consultative des droits de l'homme et deux parlementaires, d'autre part. Il a estimé que les parlementaires devaient avoir notamment pour rôle de veiller à ce que l'application de la loi, à travers l'analyse des protocoles, soit conforme à l'esprit des délibérations des assemblées. Puis M. Francis Giraud, rapporteur, a abordé les trois points qui lui ont semblé les plus sensibles de ce projet de loi : le clonage, la recherche sur l'embryon humain et la brevetabilité du vivant. S'agissant en premier lieu des risques du clonage reproductif, il a constaté que l'actualité récente avait démontré qu'il incarnait à lui seul les dérives que peuvent engendrer les sciences du vivant. Il a rappelé que, lors de son audition par la commission, M. Jean-François Mattei, ministre de la santé, de la famille et des personnes handicapées avait fait part de sa volonté ferme que soit adopté, au niveau mondial, un corpus juridique contraignant ; il a estimé que les événements récents ne pouvaient qu'encourager une telle démarche. Il a précisé que, dans son avant-projet de loi, le précédent gouvernement avait envisagé d'autoriser la pratique du clonage à des fins thérapeutiques, arguant des perspectives médicales que celui-ci pourrait ouvrir : de nombreux avis négatifs, en particulier celui du Conseil d'Etat, l'avait incité à n'en rien faire. Il reste que le projet de loi, s'il n'autorise pas le clonage thérapeutique, ne le proscrit pas. L'interdiction du clonage reproductif pourrait même a contrario le légitimer. Pour deux raisons, M. Francis Giraud, rapporteur, a fait part de son opposition de principe au clonage thérapeutique. Fondé sur une technique identique à celle du clonage reproductif qu'elle banaliserait, le clonage thérapeutique conduirait tôt ou tard quelques scientifiques ayant appris à la maîtriser, à la tentation de devenir des « apprentis sorciers ». En second lieu, une telle technique supposerait, pour être mise en oeuvre, un approvisionnement suffisant en ovocytes. Or, le don d'ovule ne va pas de soi et il semble difficile d'assurer à la fois aux chercheurs une quantité d'ovocytes suffisants pour leurs recherches et la garantie que ceux-ci seront recueillis dans le strict respect d'un principe essentiel : la non-commercialisation d'une partie du corps humain. Aussi, M. Francis Giraud, rapporteur, a-t-il estimé que le clonage thérapeutique, s'il n'est peut-être pas en soi condamnable, devait être interdit parce qu'il risque de « coûter éthiquement très cher » par les dérives vers lesquelles il porte inéluctablement. Puis M. Francis Giraud, rapporteur, a estimé que la question de l'embryon était sans nul doute, comme elle l'avait été en 1994, le point le plus délicat abordé par le projet de loi. Il a rappelé que lors de l'examen des premières lois de bioéthique, le législateur avait renoncé à définir son statut juridique, se tenant ainsi prudemment à l'écart d'un débat philosophique et biologique que nul ne saurait prétendre trancher d'autorité. Il a considéré qu'en revanche, à défaut de définir le statut juridique de l'embryon, il était possible, et même nécessaire, de décider de son sort. En 1994, le législateur avait strictement interdit que des recherches soient menées sur l'embryon, mais avait admis qu'à titre dérogatoire, des études qui ne porteraient pas atteinte à son intégrité soient réalisées. M. Francis Giraud, rapporteur, a constaté que le sort des embryons, dont le nombre se chiffrait à plusieurs dizaines de milliers, créés dans le cadre d'un projet parental et qui, pour des raisons diverses, n'ont finalement pu être implantés, soulevait un grave dilemme. Pour les uns, aucune recherche ou prélèvement ne saurait être admis par respect pour cette « personne humaine potentielle », telle que définie par le comité national consultatif d'éthique. Pour d'autres, avec l'assentiment explicite du couple qui a accompli ou renoncé à son projet parental et qui n'a plus de projet pour les embryons restants, il pourrait être envisagé que ces derniers, ou des cellules prélevées sur ceux-ci, fassent l'objet de recherche. M. Francis Giraud, rapporteur, a souligné que le principe de l'interdiction de la recherche sur l'embryon devait être retenu et affirmé conformément au principe de protection de la vie tel qu'il figure dans le code civil. Toutefois, il s'est interrogé sur la possibilité et l'opportunité de fermer à jamais une porte à la recherche sans rien connaître de sa potentialité et de son innocuité. Il a estimé que le législateur devait, en 2003, conserver la même modestie qu'en 1994, et reconnaître lui-même la possibilité d'une dérogation transitoire et strictement encadrée aux principes fondamentaux qu'il a consacrés. Il a estimé que ces réflexions sur l'ouverture ou la fermeture de la recherche sur l'embryon devaient nécessairement s'accompagner d'une mise en garde solennelle quant à la présentation qui est faite des espoirs que font naître les thérapies cellulaires, qu'elles recourent aux cellules embryonnaires ou aux cellules souches adultes. Il a estimé à cet égard qu'il devait être clairement affirmé que des années de recherches seront nécessaires avant qu'apparaissent les premiers espoirs thérapeutiques concrets. Enfin, M. Francis Giraud, rapporteur, a abordé la question de la brevetabilité du vivant. Il a rappelé que les quelques années qui séparaient le présent projet de loi des lois de 1994 avaient été marquées par la formidable course au séquençage du génome humain et que l'Assemblée nationale avait adopté une position de principe forte qui avait le mérite de réaffirmer une opposition ferme à la brevetabilité du vivant mais qui prenait l'exact contre-pied des dispositions prévues par l'article 5 de la directive européenne relative à la protection des inventions biotechnologiques. Il s'est interrogé sur la vocation d'une telle disposition. Etait-elle d'affirmer un soutien ferme au Gouvernement dans l'optique d'une renégociation de la directive ou appelait-elle une rédaction de compromis entre le principe qu'elle défend et les dispositions du droit européen ? Sur cette question, M. Francis Giraud, rapporteur, a proposé à la commission d'attendre, dans sa traduction juridique, la proposition médiane évoquée par M. Jean-François Mattei devant la commission, car c'est au Gouvernement qu'il appartiendra in fine de défendre au niveau européen le contenu de cette rédaction nouvelle. Concluant son propos, M. Francis Giraud, rapporteur, a indiqué que la soixantaine d'amendements qu'il proposerait à la commission, constituait un dispositif que le Gouvernement compléterait par trois dispositions importantes sur le clonage reproductif, l'agence de biomédecine et la brevetabilité du vivant. Sur ces trois points, il a fait part de son plein accord avec le ministre et indiqué qu'il proposerait en conséquence, le moment venu, à la commission de les approuver. Aussi avait-il tenu à les évoquer tout en considérant qu'il appartenait au Gouvernement d'en prendre l'initiative conformément à l'annonce qu'il en a faite devant la commission. M. Louis Souvet a souligné les perspectives qu'ouvraient les nouvelles thérapies génique et cellulaire ; il s'est interrogé sur les raisons qui expliquaient la mise en place difficile du don d'organe post mortem. M. Gilbert Chabroux a salué l'intérêt des auditions auxquelles ont procédé tant le rapporteur que la commission mais il a constaté que les propositions du rapporteur se situaient en retrait par rapport au texte équilibré adopté à une très large majorité par l'Assemblée nationale en janvier 2002. Il a estimé que le droit des malades à bénéficier de nouvelles thérapies devait rester au coeur des préoccupations des pouvoirs publics et qu'il ne convenait pas en conséquence de fermer la porte à un certain nombre de recherches. Il a constaté que bon nombre de pays étrangers prenaient de l'avance sur notre pays et que dans le domaine de la bioéthique, l'édiction de règles internationales était particulièrement nécessaire. M. Jean Chérioux a souligné les éléments de continuité et de consensus existants dans les débats d'aujourd'hui et ceux de 1994. De même qu'une opposition unanime était alors apparue à l'encontre de l'eugénisme, de même aujourd'hui existe-elle à l'égard du clonage reproductif et de la mercantilisation du corps humain. Il a rappelé qu'en 1994, deux questions s'étaient posées : comment éviter d'une part la réification de l'embryon ? Quel sort d'autre part lui réserver en l'absence de transfert ? Seule la première question avait trouvé une réponse et il convenait aujourd'hui probablement d'accepter qu'il soit mis fin à la conservation des embryons dès lors que le projet parental aurait été réalisé ou aurait cessé. Il a estimé souhaitable que la loi fixe un terme à cette conservation de sorte que le sort de l'embryon ne dépende ni d'une décision des parents ni, a fortiori, d'une intervention de l'administration. M. Alain Vasselle a déclaré aborder le débat sur le présent projet de loi sans certitude arrêtée, s'agissant notamment des questions très délicates de la recherche sur les cellules embryonnaires et a fortiori sur le clonage thérapeutique. Il a estimé qu'une démarche prudente s'imposait au législateur car il était toujours possible de faire évoluer la loi par étape. M. André Lardeux a considéré que les questions de bioéthique ne devaient pas être le monopole des scientifiques et des experts et que la société civile avait bien évidemment son mot à dire. S'agissant du don d'organe post mortem, il a souhaité que soit développée l'information permettant de faciliter le consentement. Il a souligné les dérives possibles qu'entraînerait l'ouverture d'une possibilité de transfert d'embryon post mortem et la nécessité d'une position très ferme à l'égard du clonage tant reproductif que thérapeutique. Il a souhaité également que les perspectives de la médecine régénératrice soient appréciées avec plus de réalisme et rappelé à cet égard la formule de M. Axel Kahn selon laquelle cette médecine risquait, en l'état de la science, d'être pour longtemps réservée à des « milliardaires cacochymes ». Il a alors insisté sur la nécessité de mettre l'accent sur la recherche portant sur les cellules souches adultes. M. Gilbert Barbier a estimé que la question au coeur du projet de loi relatif à la bioéthique n'était pas les droits des malades mais bien l'évolution des sciences du vivant. Il s'est inquiété des amendements excessifs introduits par l'Assemblée nationale alors que le texte initial du précédent gouvernement faisait preuve de prudence. Il a partagé les orientations du rapporteur sur la nécessaire information sur le don d'organe post mortem ou sur le clonage thérapeutique et manifesté une préférence pour une autorisation, à titre transitoire, de la recherche sur les cellules issues de l'embryon. Souhaitant que la France ne cherche pas à s'aligner sur les pratiques étrangères, il s'est montré favorable en revanche à la mise en place d'une législation européenne. Tout en saluant les efforts de pédagogie réalisés par le rapporteur, M. Guy Fischer a témoigné de la difficulté que rencontraient les « non-spécialistes » à mesurer pleinement les enjeux du projet de loi. Il a estimé que l'actualité, marquée, en fin d'année, par la médiatisation spectaculaire d'une supercherie, risquait de discréditer la science. Il s'est toutefois inquiété du grand nombre d'amendements présentés par le rapporteur et il a craint qu'ils traduisent un recul ou la recherche d'un équilibre « plus frileux » que celui réalisé par l'Assemblée nationale. M. Jean-Louis Lorrain a souligné le caractère indispensable d'un vrai débat sur l'évolution des sciences du vivant, loin du débat médiatique qu'a suscité l'actualité de la fin d'année. Il a appelé à une grande vigilance à l'égard des tentatives de clonage, rappelant le débat sur l'eugénisme et le diagnostic préimplantatoire qui avait eu lieu en 1994. Il a considéré qu'une fuite en avant n'était pas inéluctable et qu'il appartenait précisément au législateur de prévenir les dérives de la recherche ; il a estimé en outre que notre pays devait veiller à ne pas se laisser imposer au plan européen des normes éthiques qui ne seraient pas les siennes. Enfin, il a souhaité la mise en place d'un observatoire pluridisciplinaire de suivi de la loi. M. Bernard Cazeau a souhaité aborder quatre questions. Il a regretté que le rapporteur souhaite revenir sur la possibilité d'un transfert d'embryon post mortem, estimant que cette position faisait peu de cas du droit des femmes et de l'évolution de notre société qui tolère un cadre monoparental. Il a regretté également que les questions du transfert d'embryon, non congelé, et des mères porteuses n'aient pas été abordées. S'agissant de la recherche sur l'embryon, il s'est inquiété du risque de retard que pourrait prendre la recherche dans notre pays, mais également d'une distinction pas assez claire entre l'embryon et la cellule embryonnaire. M. Bernard Seillier a fait part de ses réserves quant à l'autorisation de la recherche sur l'embryon. Il lui a semblé que le principe éthique de l'indisponibilité de l'être humain devait y faire obstacle et que le fait de cantonner cette recherche aux embryons surnuméraires ne constituait pas à cet égard une barrière assez solide. Après avoir entendu les réponses de M. Francis Giraud, rapporteur, la commission est passée à l'examen des articles et des amendements présentés par le rapporteur. A l'article 2 (examen génétique des caractéristiques d'une personne), la commission a adopté un amendement rectifiant une erreur matérielle et, après intervention de MM. Gilbert Barbier et André Vantomme , un amendement de précision prévoyant la révocabilité du consentement à un examen des caractéristiques génétiques. A l'article 3 (identification d'une personne par ses empreintes génétiques), elle a également adopté un amendement de rectification d'une erreur matérielle et un amendement de précision. A l'issue d'un débat au cours duquel sont notamment intervenus MM. Gilbert Barbier et Alain Vasselle , elle a adopté à cet article un amendement faisant obligation au médecin, en cas de diagnostic d'une anomalie génétique grave posée lors d'un examen des caractéristiques génétiques, d'informer la personne de la nécessité de prévenir les membres de sa famille si des mesures de prévention ou de soins peuvent leur être proposées. A l'article 5 (principes généraux du don et de l'utilisation des éléments et produits du corps humain), la commission a adopté un amendement demandant au médecin d'assurer une information de leurs patients âgés de seize à vingt-cinq ans sur les modalités de consentement au don d'organe, un amendement supprimant l'institution introduite par l'Assemblée nationale d'une « reconnaissance de la Nation » qui serait conférée aux personnes qui feraient don d'éléments ou de produits de leur corps ainsi qu'un amendement de coordination. A l'article 6 (collecte, préparation et conservation du sang, de ses composants et des produits sanguins labiles), elle a adopté un amendement rétablissant la seule compétence du ministre chargé de la recherche pour l'autorisation d'importation ou d'exploration de sang à des fins de recherches scientifiques. A l'article 7 (prélèvements d'organes), à l'issue d'un large débat au cours duquel sont intervenus MM. Bernard Cazeau, André Lardeux, Guy Fischer, Gilbert Barbier, Francis Giraud, rapporteur, et Nicolas About, président , la commission a adopté cinq amendements : le premier substitue à la notion de « lien étroit et stable » entre le donneur et le receveur introduit par l'Assemblée nationale une ouverture encadrée de la liste des donneurs potentiels d'organes visant le cercle de famille élargi (grands-parents, oncles et tantes, cousines et cousins germains, conjoint du père ou de la mère) ainsi que les personnes apportant la preuve d'une vie commune d'au moins deux ans avec le receveur ; les quatre autres amendements sont rédactionnels et de précision. A l'article 8 (principes généraux applicables aux prélèvements de tissus ou de cellules ou à la collecte de produits issus du corps humain), la commission a adopté treize amendements après l'intervention de MM. Jean-Louis Lorrain, Alain Vasselle, Gilbert Barbier, Mme Gisèle Printz, MM. Francis Giraud, rapporteur, et Nicolas About, président : - un amendement visant à simplifier le régime des prélèvements de tissus ou de cellules sur une personne vivante dans le cadre d'une recherche biomédicale ; - quatre amendements qui harmonisent les modalités du recueil du consentement à un prélèvement de moelle hématopoïétique sur un mineur ou un majeur protégé avec celles prévues pour les dons d'organe ; - deux amendements qui élargissent et harmonisent le cercle familial des bénéficiaires d'un prélèvement de moelle hématopoïétique sur les mineurs et majeurs protégés en l'absence d'autres solutions thérapeutiques ; - deux amendements qui prévoient que les prélèvements sur les mineurs et majeurs protégés ne peuvent être autorisés que si, au préalable, tous les moyens ont été mis en oeuvre pour trouver un donneur majeur compatible ; - un amendement précisant le régime des déclarations relatives aux collections d'échantillons biologiques ; - un amendement prévoyant, pour certaines recherches biomédicales, que l'autorisation de la recherche vaut également autorisation du lieu dans lequel s'effectuent le prélèvement, la conservation, la préparation et l'administration des cellules concernées par la recherche ; - un amendement rétablissant la seule compétence du ministre chargé de la recherche pour l'autorisation d'importation ou d'exportation de tissus et cellules à des fins de recherches scientifiques ; - un amendement enfin de précision. A l'article 13 (produits de thérapie génique et produits cellulaires d'origine animale à finalité thérapeutique), la commission a adopté un amendement d'harmonisation des rédactions des articles L. 5152-1 et L. 5152-2 du code de la santé publique. Après l'article 15 (interdiction du clonage reproductif), après un débat au cours duquel sont intervenus MM. Alain Vasselle, Guy Fischer, Gilbert Barbier, André Lardeux, Jean-Louis Lorrain, Francis Giraud, rapporteur, et Nicolas About, président , la commission a adopté un amendement portant article additionnel reprenant la teneur de l'article 21 bis (rapport sur les initiatives françaises en faveur d'une législation internationale réprimant le clonage reproductif) du projet de loi dont elle a adopté en conséquence la suppression. A l'article 16 (agence de la procréation, de l'embryologie et de la génétique humaines), la commission a adopté dix amendements : - un amendement de coordination avec la suppression qu'elle propose à l'article 18 des protocoles d'évaluation des nouvelles techniques d'AMP ; un amendement prévoyant que l'APEGH peut être saisie par les associations agréées de malades et d'usagers du système de santé ; - un amendement précisant la composition du conseil d'administration de l'APEGH ; - un amendement substituant au Haut Conseil introduit par l'Assemblée nationale, un conseil d'orientation médical et scientifique et fixant sa composition ; - un amendement précisant la teneur du rapport annuel de l'APEGH ; - un amendement précisant, dans le cas de conflit d'intérêts, les conditions dans lesquelles il peut être mis fin aux fonctions des différentes personnes siégeant au conseil d'orientation et dans les différentes commissions et groupes d'experts ; - quatre amendements rédactionnels ou de coordination. A l'article 17 (diagnostics prénatal et préimplantatoire), après intervention de MM. Jean-Louis Lorrain et Nicolas About, président , la commission a étendu les possibilités de diagnostic préimplantatoire aux ascendants immédiats dans le cas général de pathologie gravement invalidante, à révélation tardive et mettant prématurément en jeu le pronostic vital, là où l'Assemblée nationale avait spécifiquement visé la maladie dite « de la chorée d'Huntington ». A l'article 18 (assistance médicale à la procréation), la commission a adopté huit amendements à l'issue d'un large débat au cours duquel sont intervenus MM. Bernard Cazeau, Gilbert Barbier, Jean Chérioux, André Lardeux, Francis Giraud, rapporteur, et Nicolas About, président : - un amendement renvoyant l'encadrement des pratiques de stimulation ovarienne à des recommandations de bonnes pratiques homologuées par le ministre chargé de la santé ; - un amendement supprimant la possibilité introduite par l'Assemblée nationale d'une évaluation, préalable à leur mise en oeuvre, des nouvelles techniques d'AMP ; - un amendement rétablissant l'exigence d'une durée de vie commune d'au moins deux ans pour les couples souhaitant recourir à l'AMP ; - un amendement rédactionnel renvoyant au code civil les cas où le consentement à l'insémination ou au transfert des embryons est privé d'effet ; - un amendement supprimant la possibilité ouverte par l'Assemblée nationale de transfert d'embryon post mortem, M. Nicolas About, président, ayant souligné qu'il était préférable de faire prévaloir le droit des enfants d'avoir des parents, sur le droit des parents d'avoir des enfants ; - un amendement rétablissant le caractère pluridisciplinaire de l'équipe chargée de l'information du couple sur l'AMP ; - un amendement interdisant explicitement la constitution d'un embryon par la technique du clonage à des fins commerciales et industrielles ; - un amendement de coordination avec l'amendement de suppression du transfert d'embryon post mortem. A l'article 18 bis (dispositions permettant d'assurer la filiation et les droits successoraux de l'enfant né d'un transfert d'embryon réalisé après le décès du père), la commission a adopté un amendement de suppression, par coordination avec la suppression à l'article 18 de la possibilité d'un transfert d'embryon post mortem. Avant l'article 19 , la commission a adopté sur proposition de M. Nicolas About, président , un amendement modifiant l'intitulé du chapitre IV pour introduire la référence plus générale aux cellules souches humaines. A l'article 19 (recherche sur l'embryon et les cellules embryonnaires), à l'issue d'un large débat au cours duquel sont intervenus MM. Guy Fischer, Bernard Cazeau, Gilbert Barbier, Bernard Seillier, Mme Sylvie Desmarescaux, MM. Gilbert Chabroux et Jean Chérioux, Mme Michelle Demessine, MM. Jean-Louis Lorrain, Alain Vasselle, Mme Gisèle Printz, MM. André Lardeux, Francis Giraud, rapporteur, et Nicolas About, président , la commission a adopté trois amendements : - un amendement proscrivant la constitution par clonage d'embryon humain à des fins thérapeutiques ou de recherche, cet amendement complétant le dispositif d'interdiction du clonage, qu'il soit reproductif, à des fins thérapeutiques ou, a fortiori, à des fins commerciales et industrielles (cf. amendement à l'article 18 ci-dessus) ; - un amendement modifiant le premier alinéa de l'article L. 2151-3 du code de la santé publique, affirmant le principe d'une interdiction de la recherche sur l'embryon humain, permettant, dans un cadre strictement défini par les quatrième à sixième alinéas de cet article, les études qui ne portent pas atteinte à l'embryon, autorisant enfin, à titre dérogatoire, dans les mêmes conditions mais pour une période limitée à cinq ans, la recherche sur l'embryon et les cellules embryonnaires dès lors que ces recherches sont susceptibles de permettre des progrès thérapeutiques majeurs et à la condition de ne pouvoir être poursuivies par des méthodes alternatives d'efficacité comparable, M. Nicolas About, président, ayant estimé que le texte proposé par le rapporteur était à la fois prudent et équilibré ; - un amendement précisant que les décisions de l'APEGH autorisant des protocoles de recherche sur l'embryon sont communiquées aux ministres chargés de la santé et de la recherche, assorties de l'avis du conseil d'orientation médical et scientifique, et que le droit de veto qui peut être opposé aux décisions de l'Agence peut être exercé par chacun des ministres et non pas conjointement. A l'article 20 (cellules embryonnaires ou foetales issues d'interruptions de grossesse), la commission a adopté un amendement précisant que le ministre chargé de la recherche peut s'opposer à un protocole de recherche sur des cellules foetales lorsque le respect des principes éthiques, tels qu'ils ont été notamment exprimés par le Comité consultatif national d'éthique, n'est pas assuré. A l'article 21 (dispositions pénales), la commission a adopté quatre amendements de coordination et de correction d'erreurs matérielles. A l'article 22 (coordination), la commission a adopté deux amendements de coordination avec les amendements précédemment adoptés à l'article 21. A l'article 27 (entrée en vigueur des dispositions relatives à la recherche sur l'embryon), elle a adopté un amendement de coordination. Enfin, à l'article 29 (révision de la loi et évaluation de son application), elle n'a pas retenu le principe d'une révision, prévue par la loi elle-même, du présent texte dans un délai de cinq ans mais a maintenu une évaluation de son application par l'Office parlementaire d'évaluation des choix scientifiques et technologiques. La commission a adopté sans modification les autres articles du projet de loi et l'ensemble du projet de loi ainsi amendé . |
LISTE
DES PERSONNES AUDITIONNÉES
PAR LA COMMISSION
• Professeur Claude Huriet , président de l'Institut Curie
• Professeur Axel Kahn , directeur de l'Institut Cochin, directeur de recherche à l'Institut national de la santé et de la recherche médicale (INSERM)
• Professeur Arnold Munnich , chef du service de génétique médicale de l'hôpital Necker-Enfants malades, directeur de recherche à l'Institut national de la santé et de la recherche médicale (INSERM)
• Professeur Israël Nisand , chef de service de gynécologie-obstétrique au SIHCUS-CMCO de Strasbourg
• Professeur Laurent Degos , chef du service d'hématologie de l'hôpital St-Louis, directeur de l'Institut universitaire d'hématologie
• Professeur Didier Sicard , président du Comité consultatif national d'éthique pour les sciences de la vie et de la santé
• ain- M. Sadek Beloucif , professeur d'anesthésie-réanimation au CHU d'Amiens
• M. Michel Gugenheim , grand rabbin, directeur du séminaire israélite de France
• M. Patrick Verspieren , théologien, directeur du département d'Ethique biomédicale du Centre Sèvres
• M. Geoffroy de Turckheim , président de la Commission oecuménique de la Fédération protestante de France
• M. Stéphane Meyer , médecin, conseiller de l'Ordre du Grand Orient de France
• M. Alain Manville , conseiller fédéral de la Grande Loge de France
PAR LE RAPPORTEUR
• alvat, professeur de droit - Université Paris XIII, les entreprises du médicament (LEEM) médecin-chef de la maternité de Port-Royal, Maître , avocat Professeur Laurent Degos , chef du service d'hématologie de l'hôpital Saint-Louis, directeur de l'Institut universitaire d'hématologie
• Professeur Didier Houssin , directeur général de l'établissement français des greffes
• Professeur Claude Huriet , président de l'Institut Curie
• Professeur Pierre Jouannet , président de la fédération française des centres d'études et de conservation des oeufs et du sperme humains (CEDOS)
• Professeur Axel Kahn , directeur de l'Institut Cochin, directeur de recherche à l'Institut national de la santé et de la recherche médicale (INSERM)
• , senior conseil au cabinet d'avocat Herbert Smith Victor Dem-Pesce, Institut national de la santé et de la recherche médical (INSERM) M. Jean Michaud, membre du comité nationale consultatif d'éthique (CNCE)
• M. Jean-Paul
• de Professeur Didier Sicard , président du Comité consultatif national d'éthique pour les sciences de la vie et de la santé
I. AUDITION DE M. JEAN-FRANÇOIS MATTEI, MINISTRE DE LA SANTÉ, DE LA FAMILLE ET DES PERSONNES HANDICAPÉES SUR LE PROJET DE LOI RELATIF À LA BIOÉTHIQUE (JEUDI 12 DÉCEMBRE 2002)
M. Nicolas ABOUT, président - Mes chers collègues, nous avons le plaisir d'accueillir ce matin M. Jean-François Mattei, ministre de la santé, de la famille et des personnes handicapées, à propos du délicat dossier de la bioéthique.
Monsieur le ministre, pouvez-vous nous faire part de vos réflexions sur ce projet de loi ? Vous avez la parole.
M. Jean-François MATTEI, ministre de la santé, de la famille et des personnes handicapées - Monsieur le président, monsieur le rapporteur, mesdames et messieurs les sénateurs, je suis très heureux de la poursuite de l'oeuvre du législateur de 1994, tant il est vrai que nous n'en aurons probablement jamais fini de redéfinir le cadre juridique des sciences du vivant. Les sciences avançant au rythme que l'on sait, il est clair que nous sommes sans arrêt confrontés à de nouvelles questions.
Je voudrais diviser ma présentation en deux parties.
J'aimerais, dans un premier temps, vous faire part de quelques réflexions puis, dans un second temps, aborder les différents sujets qui constituent le corps du texte lui-même.
Je ferai dans un premier temps trois séries de réflexions.
Tout d'abord, les lois de 1994 ont été votées dans un contexte qu'il faut bien garder à l'esprit. Nous avons légiféré -certains s'en souviennent- habités par le doute, les mains tremblantes. A l'époque, la question qui était la suivante : « Légiférer est-il légitime ?» était sous-jacente à toutes les interrogations.
Le Comité d'éthique a été créé en 1983 ; le rapport de M. Braibant est venu en 1988 ; d'autres rapports ont suivi, qui montraient bien les hésitations, partagées d'ailleurs par les juristes, dont certains m'avaient dit à l'époque : « Laissez-nous faire ; la jurisprudence se dessinera peu à peu, avec le temps ».
« Est-il légitime », demandaient-ils, « de légiférer dans le domaine de la médecine de la reproduction ? Faire des enfants peut-il relever de la loi ? Faut-il légiférer à propos de la transplantation d'organe ? Ce n'est pas du commerce ! ».
Ils disaient encore : « Dans ce domaine de la génétique, qui représente le plus profond de l'intimité des êtres humains, que vient faire le législateur ? ».
Il y avait, à côté de ce doute des législateurs et des juristes, une sorte de méfiance des professionnels, à la fois des médecins et des scientifiques, les médecins se disant : « On va peut-être rencontrer des difficultés pour exercer et appliquer ce qui, pour nous, correspond à des progrès techniques », et les chercheurs craignant que l'on ne vienne délimiter par trop le champ de leurs recherches.
Un certain scepticisme général de la société conduisait par ailleurs les gens à craindre que l'on installe une morale commune qui, pour les uns, serait trop laxiste et, pour les autres, trop contraignante. Autrement dit, le doute et la perplexité prévalaient.
Or, aujourd'hui, il faut reconnaître que ces lois ont fait leurs preuves.
Les doutes, peu à peu, se sont taris. On a assisté à une pacification du débat. On n'a plus du tout les affrontements que l'on avait à l'époque, enflammés parfois.
On a assisté à une moralisation des pratiques. On a découvert le rôle capital que devait jouer le corps social en tant que partie prenante de l'évolution de la société.
Ce qui est assez significatif du succès de ces lois c'est que, la révision s'annonçant, les médecins comme les chercheurs sont demandeurs de précisions et réclament que l'on définisse mieux leur champ d'activités.
De fait, il faut bien reconnaître que ces lois de bioéthique ont en quelque sorte donné l'onction du droit à ces pratiques.
Elles ont par ailleurs accompagné l'acceptabilité sociale et, par ailleurs -ce qui n'est pas le moindre de leur succès- ont contribué à assumer une fonction éducative et à élever le niveau du débat en France.
Il y a quinze ans, quand on commençait à discuter de la bioéthique, les débats étaient véritablement dans les profondeurs de l'ignorance.
Or, aujourd'hui, grâce aux médias, grâce au débat, il est vrai que, d'une façon générale, la connaissance de ces progrès s'est élevée et que les gens y participent davantage, ce qui conduit d'ailleurs, parallèlement à la recherche elle-même, les gens remontant le fil de leurs interrogations, à en venir au coeur même du dispositif, à savoir l'embryon humain, le clonage, les frontières entre les fondements biologiques et sociaux du comportement humain.
Pourquoi le doute existait-il et pourquoi connaît-on aujourd'hui le succès?
Je vois deux raisons pour expliquer le succès de ces lois.
D'abord, elles ont fait selon moi émerger la conscience aiguë du fait que les sciences biomédicales nécessitent des limites.
On voit bien que toutes ces techniques nouvelles s'adressent à la personne et conduisent donc à mettre en cause la notion de personne, de corps, de respect, de don, de commerce, de contrat et, tout simplement, pose des questions de repères au-delà même de la biologie puisque, avec la possibilité éventuelle de transférer les embryons longtemps après la mort du père, c'est du temps dont on s'affranchit !
Autrement dit, il faut bien voir que le succès est dû au fait que la conscience est venue de ces problèmes. C'est d'ailleurs ce que j'appelle l'émergence de la conscience éthique dans notre société.
Le second facteur de ce succès réside dans la manière dont le législateur a conçu son rôle en matière de sciences du vivant.
Souvenez-vous : entre éthique de conviction et éthique de responsabilité, nous avons cherché les déséquilibres les moins mauvais.
En définitive, le législateur a choisi de ne prendre comme repère ni la morale, ni la philosophie, mais le droit, et cette juste conception de sa fonction est particulièrement manifeste dans la manière dont il parle de l'embryon humain.
Il a édicté un régime fondé sur le principe du respect dû à l'embryon et sur la définition des atteintes qui pouvaient lui être portées, mais il a renoncé à définir l'embryon.
Se faisant, le législateur s'est tenu à l'écart des querelles biologiques et philosophiques, car si l'on s'en tenait aux données biologiques, celles-ci nous montrent bien que l'embryon est humain dès le début, qu'il est un individu, c'est-à-dire un être organisé doué d'une unicité. Certains tâchent de trouver d'ailleurs un moment qui marquerait l'apparition de l'humain dans cet être-là.
Mais au plan philosophique, qui tend la biologie, on sait bien que la question ontologique du début de la personne fait l'objet de controverses, et il paraît donc impossible de résoudre par le seul droit la question de savoir si l'embryon est une personne !
Si nous ne pouvons pas trancher la question de la nature de l'embryon, en revanche, sur le plan pratique, nous pouvons et même devons définir quel doit être notre conduite à son égard.
Le législateur s'est donc situé sur le plan du devoir être à l'égard de l'embryon et non de son être.
Ce choix a été critiqué par certains au motif que c'est le statut qui doit imposer les limites et non le contraire. Je crois que ce choix, au contraire, est juste et efficace.
Il est juste parce que la loi n'a pas à qualifier les êtres humains, mais seulement à les constater et à les protéger.
A défaut, la qualité d'être humain, comme celle de personne, ne serait pas un droit, mais une concession !
Ce choix est efficace, parce qu'en ne déterminant pas ce qu'est l'embryon mais en disant comment on doit le traiter, l'éthique et le droit ont trouvé leur espace propre.
C'est à partir de ces acquis de fond et de forme, c'est-à-dire la nécessité de tracer des limites et de donner les repères d'une part, et la place du droit par rapport à la morale et à la biologie d'autre part, que j'entends continuer le travail entrepris.
Voilà ma première série de réflexions sur l'esprit et la méthode des lois de bioéthique.
Je voudrais aborder la seconde série de réflexions concernant le retard pris par le précédent Gouvernement.
Je vous rappelle que les lois de 1994 prévoyaient une révision à cinq ans.
Or, nous sommes à l'aube de 2003 et cette révision n'est pas achevée, la première lecture ayant eu lieu au mois de janvier 2002.
Certes, ce retard est dû à des difficultés dans la parution et la rédaction de certains décrets. Je ne fais pas partie de ceux qui se sont escrimés à démontrer la culpabilité du précédent Gouvernement dans le retard pris.
En revanche, quand on regarde les choses plus au fond, on se rend compte que ce retard a été en particulier dû à la difficulté qu'a éprouvé le Gouvernement de l'époque à assumer clairement certains de ses choix. L'exemple typique en est le clonage thérapeutique.
On voit bien qu'initialement l'option était prise d'aller vers le clonage thérapeutique. Après quelques hésitations, on y a renoncé. Quand on tente de comprendre les choses, on voit bien que toute la démarche a été d'avancer sans que cela soit dit vers un véritable bouleversement de l'équilibre entre le respect qui est dû à l'embryon, d'une part, et la confiance de la liberté du chercheur de l'autre.
Toute une série de dispositions, petit à petit, sont venues nous le montrer.
Je tire de cela deux enseignements. Tout d'abord, il faut poser clairement le débat, sans paravent sémantique, sans barrière langagière, et très clairement appeler les choses par leur nom. Par exemple, parlant de l'embryon pour la recherche, il ne faut pas confondre la recherche sur l'embryon et la recherche sur des cellules embryonnaires.
Il ne faut donc pas faire entrer de manière subreptice la conception de l'embryon pour la recherche au motif que l'on en a besoin pour évaluer de nouvelles techniques de procréation assistée. On est là typiquement dans la plus grande ambiguïté.
En second lieu -et je crois que je suis probablement l'un des mieux placés pour le dire- il nous faut clarifier la notion de bioéthique, sauf à entraîner son discrédit.
Je ne suis pas favorable à ce que, dans cette révision, on fixe à nouveau une clause de révision à cinq ans ! C'était nécessaire la première fois parce qu'on était dans le doute, mais je ne suis pas sûr qu'il faille à nouveau nous avancer vers une révision systématique, si ce n'est sur certains points précis, sauf à laisser croire que la biomédecine forgerait, au fil des années, sa propre éthique.
Vous avez, au Sénat, à l'Assemblée nationale, abordé le sujet de l'interruption volontaire de grossesse, ainsi que celui de la prolongation du délai et, chemin faisant, le problème de la stérilisation des femmes adultes handicapées. Personne ne peut nier qu'il y avait une dimension éthique dans ces textes-là ! Dans le texte sur le droit des malades, l'éthique était sous-jacente.
Le seul fait de dire que l'on va légiférer sur la bioéthique pourrait laisser penser qu'il n'y a pas d'éthique ailleurs. C'est un grave danger !
Second danger : pendant les cinq années qui se sont écoulées, on a bien vu qu'il était nécessaire de prendre des décisions, parfois sans trop attendre. On nous disait pourtant de ne pas nous inquiéter, qu'on allait le traiter avec les lois de bioéthique.
On a donc pris du retard dans certaines dispositions qui auraient dû s'imposer plus tôt. Inversement, on nous demande de saisir l'occasion de prendre en compte des techniques dont on voit bien qu'elles ne sont pas encore suffisamment mâtures pour que l'on puisse, d'ores et déjà, en définir clairement les usages et les indications.
Je dois vous dire que je ne souhaite pas cette clause. Désormais, la bioéthique s'est installée dans notre paysage et, plutôt que d'être fragilisé sur cette durée provisoire, je souhaite que l'on consolide nos positions. Je vous le redis donc : l'inscription dans la loi du principe de sa révision m'apparaît comme un procédé ambigu et néfaste.
Il est ambigu désormais car, finalement, il est dépourvu de toute valeur normative. Il ne contraint en rien le législateur et ne modifie pas la faculté dont dispose celui-ci, à tout moment, de remettre la loi en chantier, si cela s'avère nécessaire.
On a fini par dire : « On verra dans cinq ans ». Non ! On verra quand le besoin s'en fera sentir et, parfois, sans attendre.
Probablement est-ce même néfaste, parce que le législateur n'a pas, en particulier lorsqu'il édicte des principes, vocation à faire une oeuvre dont la date de péremption est, par avance, annoncée. Comment ne pas voir que la solennité et la légitimité de la loi se trouveraient malmenées ?
Si l'on veut que les normes édictées aient toute leur valeur, il ne faut pas, dans une perspective instrumentale, qu'elles soient constamment remodelées.
Il est donc, à mon avis, essentiel qu'elles ne soient pas conçues d'emblée comme caduques. Autrement dit, nous avons pris le temps nécessaire pour fixer notre ensemble en deux étapes -l'adoption première et la révision.
Désormais, l'éthique étant introduite dans notre processus législatif et dans nos esprits, il faudra sans attendre aborder ces problèmes quand ils se poseront ici où là, et notamment sans donner l'impression que l'on édicte des valeurs provisoires.
La troisième réflexion que je voudrais faire concerne l'importance croissante de la biomédecine au plan international.
Cela ne vous aura pas échappé : la bioéthique devient un sujet de discussion dans les grands sommets et sera un des sujets majeurs du prochain G 8.
Il nous faut, là-dessus, une concertation internationale. Le Conseil de l'Europe et les 43 pays de la grande Europe qui composent cette assemblée ont tout de même écrit et fait voter en 1997 la fameuse Convention d'Oviedo, convention de la biomédecine et des droits de l'homme qui pose le canevas des valeurs communes à la grande Europe.
Evidemment, cette convention reste sur de très grands principes. Pour avoir siégé, de 1997 à 2002, à l'Assemblée du Conseil de l'Europe, et plus particulièrement au Comité directeur de bioéthique, et ayant participé à toutes les négociations internationales sur le protocole additionnel contre le clonage, pour la transplantation d'organes, etc., je vois bien les difficultés qui existent au plan international.
La France et l'Allemagne viennent de prendre une initiative commune, il y a quelques mois, à l'ONU, pour interdire au plan mondial le clonage reproductif mais, immédiatement, d'autres pays, menés par les Etats-Unis, se sont élevés pour en faire encore davantage, en disant : «Il faut interdire simultanément le clonage reproductif et le clonage thérapeutique». L'affrontement de deux textes a, ainsi, conduit à un échec.
Il faut véritablement que nous soyons très forts pour tenter d'entraîner les autres. C'est la raison pour laquelle il faut que nous allions beaucoup plus loin que ce qui a été fait jusqu'à présent sur le clonage reproductif.
C'étaient là mes trois réflexions préliminaires : premièrement, le climat a changé et, si l'on en fait une analyse, on voit bien les contours vers lesquels il faut s'avancer ; deuxièmement, il faut clarifier les choses et ne pas s'abriter derrière de faux-semblants ; troisièmement, il y a des conséquences internationales.
J'aborde maintenant la deuxième partie, c'est-à-dire les sujets plus spécifiques sur lesquels nous allons avoir à légiférer.
Je voudrais commencer par le moins difficile qui, d'ailleurs, dans le texte, apparaît, je crois, en premier : les organes et la transplantation.
En définitive, c'est un des sujets les plus anciens, vous le savez mieux que moi. Le sénateur Caillavet a longtemps siégé ici. C'est lui qui avait pris l'initiative, en 1976, de la première loi instituant le consentement présumé.
En 1994, nous avons essayé d'arranger les choses, de mieux les préciser. Nous pensions les faciliter. Or, quels que soient les efforts -et je dois souligner les efforts faits par l'Etablissement français des greffes à l'initiative de Didier Roussin avec le plan 15-20, qui avait pour ambition de passer de quinze prélèvements à vingt par million d'habitants- les choses sont encore loin d'être suffisantes.
Nous avons une carence d'organes à greffer. Evidemment, la facilité consiste -et c'est ce qui a été fait- à se tourner vers les vivants, vers les proches. C'est toute la question de l'extension du don d'organes au cercle des vivants.
Cela est-il satisfaisant et cela doit-il être voté devant le Sénat, comme cela l'a été en janvier par l'Assemblée nationale ? Personnellement, je ne le crois pas.
Je crois naturellement qu'il nous faut faire un effort pour élargir le cercle des vivants, mais nous devrons avoir un débat très large pour savoir quelles sont les définitions dans lesquelles on va faire entrer le cercle des donneurs potentiels, sauf à laisser prise à toutes les dérives perverses.
On voit bien aussi les pressions morales qui pourraient s'exercer au sein même des familles. A mon sens, il faut que nous ayons une réflexion plus élaborée pour savoir jusqu'où on peut éventuellement étendre le cercle des donneurs vivants.
Je suis favorable à l'extension, mais je suis encore plus favorable à ce que l'on délimite clairement les choses.
Autre aspect qui me paraît important : imaginez un homme de 28 ans, sollicité pour donner la moitié de son foie parce que son cousin germain est en insuffisance hépatique gravissime, qui apparaît comme le seul donneur potentiel alors qu'il a la charge de deux enfants.
Qu'il ait spontanément la générosité de donner pour sauver, j'entends bien, mais s'il mourait -ce qui arrive dans ce type d'intervention- ou s'il en était définitivement amoindri, qui assumerait les responsabilités au regard des deux enfants à élever ?
Autrement dit, on ne peut déconnecter l'acte de donner de la générosité spontanée mais, quelquefois, il me semble que la société a le devoir de protéger les gens contre leur propre générosité dans la mesure où ils sont, par ailleurs, déjà en charge de responsabilités.
Il faudra donc que nous nous interrogions, notamment pour les couples constitués avec charge de famille, pour savoir si celui qui donne ne doit pas le faire avec le consentement de celui qui partage avec lui l'autorité parentale, afin que ce soit une décision partagée.
Nous avons véritablement là toute une série de questions qui se posent sur l'élargissement aux donneurs vivants.
Mais -et c'est presque le plus important dans mon esprit- on ne peut pas non plus ne pas s'interroger sur le fait de savoir si notre système de prélèvement cadavérique est suffisamment performant.
Je ne le crois pas, car la mort un tabou. Sur le terrain, à l'hôpital, mes collègues, qui sont moins sous les feux des commissions ou sous les feux des médias, mais qui n'en sont pas moins des transplanteurs réguliers, me disent que la difficulté réside dans le fait que les morts ne peuvent s'exprimer. Les familles, dans le doute, refusent tout prélèvement, alors qu'on peut s'adresser aux vivants et, éventuellement, les convaincre.
« En définitive », me disent-ils avec une certaine naïveté, « il est aujourd'hui plus facile d'obtenir un donneur vivant que de franchir la barrière de la mort au travers de l'aval d'une famille ». On sait bien que, dans la loi, ce n'est pas l'autorisation des familles mais simplement un témoignage que l'on va chercher. Toutefois, lorsque le médecin demande à la famille si elle sait si le défunt était opposé ou non au prélèvement, si celle-ci n'est pas informée, elle demande de ne rien faire.
Cela signifie que le médecin ne fera rien, même si, sur le plan juridique, il en a le droit.
Je pense qu'il faut que nous étudions des mesures plus précises pour rassurer, en quelque sorte, les familles en deuil sur la connaissance qu'avait la personne disparue de la réalité de la transplantation. Ayant la certitude que l'information a bien été donnée, que la personne ne s'est pas inscrite sur le registre des refus, il y a, dès lors, tout lieu de penser qu'elle était tacitement consentante, comme le prévoit la loi.
Il faut avoir un vrai débat sur les transplantations d'organes pour trouver un certain équilibre. Je ne suis pas opposé à ce qu'on l'élargisse aux donneurs vivants. Ce serait inhumain que de s'opposer à cette envie d'aider l'autre. Je pense toutefois qu'il faut resituer cela dans un contexte de responsabilités partagées, sans risquer de s'exposer à des dérives dangereuses, financières ou morales.
D'autre part, s'agissant des prélèvements cadavériques, je crois qu'il faut que l'on fasse mieux ; d'autres pays, comme l'Espagne, font beaucoup mieux et satisfont les besoins de la transplantation avec leurs seuls prélèvements cadavériques.
C'était le premier sujet.
Le second thème concerne l'assistance médicale à la procréation.
L'assistance médicale à la procréation, en définitive, avait été -je crois- assez bien encadrée et discutée, à tel point que la plupart des décisions prises en 1994 sont conservées dans cette révision, même après première lecture à l'Assemblée nationale.
J'y vois néanmoins deux éléments dont il faut que nous discutions et, en premier lieu, le fait qu'à l'initiative d'un parlementaire, le rapporteur à l'Assemblée nationale, et non à la demande du Gouvernement, a été réintroduite la possibilité de transfert d'embryon post mortem .
On traîne toujours cette jurisprudence «Pires», du nom de ce couple toulousain qui, après dix ans de stérilité, décide de concevoir un enfant in vitro . Deux embryons sont alors transférés, les autres sont congelés.
Mme Pires fait une fausse couche, est hospitalisée et son mari se tue en voiture en venant lui rendre visite. Elle demande, à quelque temps de là, à ce que l'on transfère les embryons restants dans le congélateur.
Il y a deux façons d'aborder le sujet et je me souviens, déjà en 1994, que c'était au coeur de « l'affaire Pires ». Le débat avait été houleux et difficile, car la compassion conduit, bien entendu, spontanément à dire : « Qui d'autre que cette femme a l'autorité pour décider du devenir de ses propres embryons ? ».
Néanmoins, on est là devant des situations pleines de contradictions, pleines de dangers.
Tout d'abord, nous n'avons pas défini totalement l'embryon -on parlera tout à l'heure de la recherche sur l'embryon et sur les cellules embryonnaires. Alors que nous n'avons pas encore arrêté une définition précise du concept, subitement, on extrapolerait en disant : « Ce sont ses enfants ! Pourquoi ne les lui rendrait-on pas ? », au motif que la vie, d'un coup, doit être respectée absolument !
C'est un premier argument qui conduit immédiatement à se demander ce qui adviendrait dans le cas contraire. Si c'est la mère qui mourrait et que le père demande à récupérer ses embryons, est-ce que cela voudrait dire qu'il faut légitimer le recours exceptionnel, dans des cas particuliers comme ceux-là, aux mères porteuses, cet homme disant : « Ma femme n'est plus là, mais ces embryons sont à moi ! » ? Certes, la physiologie crée une sorte de disparité de la nature, mais tout de même !
Cela pose aussi une série de limites, car cette femme qui est en deuil, ses embryons étant là, va s'interroger. On va lui donner un délai : six mois, un an, deux ans, peu importe. Pendant tout ce temps, son travail de deuil ne se fait pas. Sa réflexion est fixée sur le fait de savoir si elle va le faire ou non, avec cette notion de trahison éventuelle, en disant : « On avait décidé... Il faut que je le fasse ».
Qu'adviendrait-il si elle tombait malade et prenait des médicaments -pour dépression nerveuse, par exemple- qui interdisent le transfert pour des raisons médicales ? On repousserait le délai, mais jusqu'à quand ?
Si elle avait des difficultés sociales et économiques, que se passerait-il ? Si entre temps elle avait noué une nouvelle union -pas nécessairement, d'ailleurs, par contrat de mariage- et qu'elle demande le transfert des embryons conçus avec un premier conjoint ou compagnon, on ne voit plus très bien comment les choses conserveraient un semblant de cohérence !
J'ajoute que le droit vient nous dire que cette situation ouvrirait la possibilité d'héritiers réservataires dans un congélateur, venant bouleverser de manière profonde tout le droit de la succession et le droit patrimonial. Nous serions là, au-delà de ces problèmes, dans la transgression du temps !
Je ne suis pas sûr, au-delà des questions que cela peut poser, qu'il nous faille au fond bouleverser notre droit au regard des quelques cas d'exception qui ont pu se présenter au fil du temps.
Il me semblerait beaucoup plus raisonnable d'informer impérativement le couple qu'en cas de dissociation de celui-ci, les embryons ne seront pas conservés, sinon, je ne vois pas comment, aux progrès biologiques, nous pourrions opposer l'affranchissement du temps.
En second lieu, l'Assemblée nationale s'est affranchie du délai de deux ans pour les couples non mariés.
Je crois que ce n'est pas une bonne chose, parce que l'assistance médicale à la procréation présente un inconvénient majeur. Tous ceux que vous rencontrez généralement au cours des auditions sont des obstétriciens, des gynécologues, des spécialistes de la stérilité qui veulent régler le problème des couples souffrant en face d'eux. Mais qui s'exprime au nom de l'enfant ? Qui s'exprime au nom des conditions dans lesquelles l'enfant pourrait être conçu, naître et être élevé ?
J'estime que tout doit être fait dans cette loi pour que la démarche faite pour pallier la stérilité du couple soit gouvernée par le désir d'accueillir l'enfant dans les meilleures conditions possibles. C'est, je crois, de la responsabilité du législateur. On pourra naturellement aller plus loin si vous le désirez tout à l'heure.
Le troisième sujet que je veux aborder est celui de l'embryon.
Il est exclu, dans mon esprit, que l'on revienne sur l'article 16 du code civil, qui dit bien que tout être doit être respecté dès le commencement de sa vie. C'est un fondement essentiel, et nous en sommes d'ailleurs tous d'accord.
Cela n'exclut pas la loi sur l'interruption de grossesse, qui est vécue comme une transgression dans un cas particulier. Chaque fois que nous allons également vers le diagnostic prénatal, nous voyons bien l'exception au principe qui doit rester fondateur : le respect de la vie dès son commencement.
A mon avis, ceci doit être rappelé, et c'est la raison pour laquelle je pense qu'il faut que nous rappelions que la recherche sur l'embryon doit être interdite parce que c'est l'interdit fondateur.
En revanche, je reviendrai, malgré certaines critiques émises ici où là, sur l'idée qu'il faut maintenir la possibilité de mener des études sur l'embryon dans la mesure où cela n'atteint pas son intégrité. Certains disent : «Cela n'a pas de sens ! Vous avez choisi le mot «études» : il fallait parler de «recherches» !».
Jusqu'à nouvel ordre, j'essaie d'utiliser les mots qui me paraissent les plus appropriés. Quand je dis qu'il faut autoriser les études sur l'embryon, études qui préservent son intégrité, j'entends, par exemple, ce que nous faisons au travers du diagnostic préimplantatoire. Nous prélevons une cellule, nous faisons un diagnostic, cela ne porte pas atteinte à l'intégrité de l'embryon. Il n'en demeure pas moins que ce diagnostic doit faire l'objet d'essais, de mises au point, et ce sera probablement la même chose le jour où nous essaierons une correction génétique.
Considérer donc l'embryon comme un objet d'études, en le respectant, me paraît un élément essentiel. Il serait d'ailleurs assez invraisemblable -et je rejoins là le problème plus spécifique de la recherche sur l'embryon- qu'au motif qu'il faut le respecter en tant que personne, on l'exclut du droit des personnes d'accéder à la médecine !
L'embryon doit rentrer dans le champ de la médecine. La médecine progresse. Elle s'est intéressée à l'enfant, puis au nourrisson, puis au nouveau-né, puis au prématuré, puis au grand prématuré. On en est à la médecine foetale. Nous en serons demain à la médecine embryonnaire. Il n'y a pas de médecine qui ne progresse sans recherches.
La recherche sur l'embryon, qui profite à l'embryon lui-même ou d'ailleurs à d'autres embryons, me paraît une ouverture indispensable, sauf à rester dans une espèce de statut assez invraisemblable où l'on dirait : «On le respecte tellement qu'on ne veut pas lui venir en aide le cas échéant !».
La recherche sur l'embryon, malgré la difficulté et malgré le fait que, dans un certain nombre de situations, cet embryon ne survivra probablement pas -mais d'autres pourront bénéficier de ces recherches- me paraît donc devoir être désormais ouverte, dans des conditions très strictes, très fermement encadrées, car la médecine en est arrivée à l'embryon, qu'elle considère comme accessible à son diagnostic et à son éventuelle thérapeutique.
La recherche sur l'embryon dans des conditions précises doit donc être à mon sens désormais autorisée. On passe insensiblement de l'étude à la recherche, et je ne vois pas comment nous pourrions l'éviter.
Se pose une autre question, beaucoup plus difficile, que vous avez abordée avec un certain nombre de spécialistes que vous avez rencontrés : celle des cellules souches.
Il faut essayer de prendre les choses simplement. L'idée est tellement simple : on s'est rendu compte que l'on pouvait remplacer les cellules vieilles ou malades par des cellules jeunes ou normales et qu'il y avait là un nouveau champ, que l'on appelle la thérapie cellulaire, absolument prodigieux, qui permettrait de guérir à terme des maladies aujourd'hui inaccessibles à tout traitement.
Naturellement, je n'accepte pas l'idée de dire que ce sont des recherches thérapeutiques, car permettez-moi de rappeler qu'à mon sens, en biologie et en médecine notamment, il n'y a pas de recherches qui ne soient faites dans le but de mieux soigner les gens un jour ou l'autre. Vouloir immédiatement les qualifier de «thérapeutiques» me paraît quelquefois mensonger.
Je voudrais rappeler que, même si nous aidons toujours ce que l'on appelle de fait la thérapie génique ou le génie génétique, cela fait quand même maintenant vingt ans que nous en parlons, et qu'à l'exception des quelques malades guéris dans le service d'Alain Fischer -et encore avec la complication récente que l'on sait- il n'y a pas de malades véritablement guéris ! Parler aujourd'hui d'espoir thérapeutique immédiat est donc un mensonge.
Je le dis d'autant plus fermement que je pense qu'il faut un début à toute recherche. Je ne vais pas m'opposer à ces recherches au motif que le traitement ne serait pas immédiat. Il faut bien commencer un jour mais, dans le discours, ne trompons pas les associations de malades, ne trompons pas les patients.
C'est une longue route qui, pour le moment, repose sur un concept tout à fait juste, tout à fait valide, mais qui n'a en réalité pas commencé à produire le premier début de la moindre preuve, même sur les modèles animaux, quand on regarde dans le temps.
Cela étant dit, le concept étant bon, cohérent, scientifique, logique et valable, il faut effectivement se mettre en ordre de marche.
Se pose donc la question de savoir où on va trouver ces cellules.
Naturellement, la première cellule qui vient à l'esprit, c'est la cellule embryonnaire. Je rappelle que nous sommes issus d'une cellule qui avait toutes les capacités pour donner de la peau, du foie, des os, des cellules nerveuses, des muscles et constituer un individu différencié.
Or, les cellules les plus jeunes et les plus capables de se différencier pour donner des cellules normales sont les cellules embryonnaires. Evidemment, on butte sur l'idée de l'embryon. On voit bien le danger qu'il y aurait à instrumentaliser l'embryon, à le considérer comme matière première alimentant la recherche scientifique. On est là sur des crêtes difficiles.
Il existe d'autres voies qui sont avancées, et notamment la présence de cellules souches trouvées dans les tissus adultes, qui pourraient, dans certains cas, avoir des effets semblables de production de cellules normales, y compris de transdifférenciation, c'est-à-dire, étant prélevées dans la moelle, de donner des cellules hépatiques ou de toute autre nature.
Tout cela est vrai et a été observé de façon occasionnelle ici où là, comme les cellules du sang du cordon, qui ont fait l'objet d'études encourageantes. J'ai moi-même pensé, l'année dernière encore, que l'on pourrait faire l'économie de l'étape des cellules embryonnaires et, d'emblée, aller vers les cellules adultes.
Par honnêteté intellectuelle, je pense que, même si nous devons privilégier les recherches sur les cellules adultes, nous ne pourrons pas faire l'économie de recherches parallèles sur les cellules embryonnaires, ne serait-ce que pour éventuellement valider, le moment venu, le modèle des cellules adultes.
Nous sommes donc arrivés à un moment difficile où il nous faut savoir si c'est un refus définitif d'un progrès formidable, pour toute une série de maladies que je ne vais pas énoncer pour ne pas tomber dans une sensiblerie que je trouve dangereuse, sachant que, par ailleurs, dans bien d'autres pays, les choses avancent.
En toute honnêteté, si l'un de mes proches était atteint d'une de ces maladies et, après avoir dit non pour la France, si ces cellules étaient disponibles ailleurs, refuserais-je d'aller les chercher pour me conformer à mes propres interdits ? Je le dis très clairement : non, je me dépêcherais d'aller les chercher !
On est là devant un choix éthique qui montre le degré de tension morale sous-jacent mais, à mon sens -et c'est la solution que je vous proposerai- parce que j'ai rappelé l'interdit initial et que j'ai bien montré que l'embryon devait être respecté, j'estime que, dans certaines conditions très particulières, définies avec les précautions et l'encadrement utiles, pendant une période donnée qui pourrait être fixée à cinq ans par exemple, sur les seuls embryons conçus pour la fécondation in vitro qui n'auraient pas été transférés, dont les parents ne voudraient plus qu'ils soient transférés, et avec leur consentement, avec des protocoles clairement étudiés et validés, nous pourrions peut-être, à titre dérogatoire, faire ce que j'appelle dans mon langage une «exception législative» sur une période de temps donnée.
Croyez bien que j'ai beaucoup pesé mes propos avant de m'exprimer, car c'est un chemin qui n'était pas facile mais, comme j'ai déjà eu l'occasion de le dire, je ne crois pas que la médecine puisse progresser à des moments déterminants sans transgression, comme elle l'a fait pour l'autopsie, la transfusion sanguine ou les prélèvements d'organes.
Aujourd'hui, les conditions étant ce qu'elles sont, je ne vois pas comment proposer autre chose que d'autoriser, dans des conditions définies et pour une période déterminée, la recherche sur les cellules embryonnaires.
Evidemment, dans la même logique, je vous demanderai de revenir sur la disposition subreptice qui consiste à autoriser la création d'embryons pour la recherche.
Ceci n'est plus une transgression, mais la négation du principe que je rappelais tout à l'heure ! Autoriser la création d'embryons, fût-ce pour valider des techniques de fécondation in vitro , nous ferait franchir un pas essentiel, au sens d'« essence» : ce ne serait plus des essais sur l'homme mais des essais d'hommes ! Ce serait essayer de concevoir avec une certaine méthode un nouvel être humain et regarder comment cela marche.
Dites-vous bien que cette démarche-là commencerait par se faire in vitro, mais qu'à un moment où à un autre, il faudrait bien faire le transfert pour voir comment cela se développe in vivo !
Cette démarche-là, je ne la veux pas ! Autant je comprends les situations exceptionnelles que je viens d'exposer, autant je m'opposerai formellement à toute création d'embryons pour la recherche, pour quelque motif que ce soit !
D'ailleurs, cela nous mettrait en contradiction avec la convention d'Oviedo. Or, une de mes préoccupations est de faire en sorte que, sept ans, après, la France puisse ratifier enfin la convention d'Oviedo.
Dire que je ne veux pas de création d'embryons pour la recherche sous-tend naturellement que je ne veux pas de clonage thérapeutique, car peu importe que cette cellule soit appelée par les uns «embryon» ou par les autres «non-embryon». Ce que je sais simplement, c'est que le clonage thérapeutique nous expose à deux dangers majeurs.
Premièrement, pour réaliser un clonage thérapeutique, il vous faut disposer d'ovules en grand nombre. Cela suppose l'organisation d'un marché d'ovules.
Ceci est en contradiction avec la non-commercialisation du corps humain. Pour fabriquer un clone thérapeutique, il faut un ovule et, quand vous voulez vous lancer dans des essais multiples, il vous faut des dizaines et des centaines d'ovules !
Je viens de voir que même le professeur Frydman a annoncé qu'il renonçait au don d'ovules pour la fécondation in vitro , tout simplement parce que les femmes, en dehors d'argent, n'acceptent pas volontiers de donner des ovules, tout d'abord parce que c'est plus difficile que de donner du sperme et ensuite parce que c'est une partie d'elles-mêmes.
Il y a là une démarche conceptuelle que les femmes ont du mal à franchir et qu'elles ne franchiraient que, comme aux Etats-Unis, pour des raisons commerciales ou, comme dans les pays en voie de développement, pour des questions d'argent. On obtiendrait naturellement des ovules au terme de tractations financières, ce que je n'accepte pas.
La deuxième raison est que le clonage thérapeutique est la partie technique du clonage reproductif.
Lorsque vous avez transféré votre noyau dans un ovule, c'est potentiellement un clonage dit thérapeutique si vous le mettez en culture, mais si vous le transférez au moyen d'une pipette dans un utérus, vous avez un clonage reproductif !
Je m'oppose donc au clonage thérapeutique, car c'est la porte ouverte au clonage reproductif, dont je voudrais maintenant dire quelques mots.
Je crois, d'ailleurs, qu'il y a unanimité sur le sujet. Tout le monde est d'accord pour reconnaître que le clonage reproductif est une horreur, que c'est une atteinte à la dignité de la personne et qu'il faut donc le condamner.
En première lecture, à l'Assemblée nationale, j'ai fait valoir des arguments qui n'ont pas été retenus et que, naturellement, parce que j'ai une certaine constance, je vais vous proposer à nouveau.
Si l'on veut véritablement interdire le clonage reproductif, il faut que les sanctions qui accompagnent l'interdiction soient à la hauteur du délit.
Si c'est un simple délit de cinq ans de prison éventuels et d'une amende équivalente en euros à 200.000 francs, je crois que ce serait une interdiction tout à fait dérisoire.
Pour moi, le clonage reproductif est, au niveau de la personne, l'équivalent de ce qu'est le crime contre l'humanité au niveau collectif.
Le crime contre l'humanité est un crime contre l'espèce humaine en ce sens que, d'une façon massive et organisée, on vient porter atteinte à la dignité de la personne.
Concevoir quelqu'un en l'enfermant dans un destin génétiquement programmé, choisi et délibéré, c'est le priver de sa liberté et, le privant de sa liberté, c'est porter atteinte à sa dignité !
Je pense donc -et j'ai l'accord du garde des sceaux- vous proposer une nouvelle incrimination, basée par comparaison sur les peines les plus lourdes dans des champs voisins, en ayant d'une part, à partir de la majorité éventuelle de l'enfant cloné, une prescription trentenaire, ce qui équivaut quasiment à une imprescriptibilité, et en instituant, d'autre part, une extraterritorialité, car on peut être Français et aller se faire cloner dans des zones internationales, puis revenir en France.
Comme pour le tourisme sexuel -pardonnez-moi la comparaison, mais c'est comme cela et je peux justifier que ceci existe déjà- le clonage sera condamné en France pour des citoyens français vivants en France, quand bien même il aurait eu lieu à l'étranger !
C'est à mon avis la seule force que nous ayons pour continuer à mener notre croisade internationale et déboucher sur une interdiction formelle par les Nations-Unies.
Il me reste à aborder deux points. Je voudrais vous parler de l'Agence et de la brevetabilité des gènes.
Le projet de loi du Gouvernement précédent prévoyait l'idée d'organiser une nouvelle agence, appelée «Agence pour la procréation, l'embryologie et la génétique humaine», que j'ai immédiatement récusée, après un débat très courtois mais très ferme avec le rapporteur de l'époque.
Je trouve que la multiplication des agences finit par gêner la visibilité que l'on peut avoir dans nos politiques d'une façon générale. On en a déjà 8 ! A ce moment-là, je ne vois pas pourquoi on ne créerait pas une agence dès qu'une activité particulière apparaît !
En second lieu, cette agence me paraissait mal composée et un peu anormale quant aux compétences qu'on voulait lui attribuer. J'ai dans l'idée de vous proposer une architecture et des compétences différentes.
Pour tout dire, mon idéal -mais je ne pense pas que nous pourrons l'atteindre tout de suite- aurait été de regrouper l'AFSSAPS, l'Etablissement français des greffes et l'APEGH dans une grande agence de biomédecine et de produits de santé.
On aurait une grande cohérence avec cinq départements ayant une autonomie et une spécificité particulières : les trois départements de l'AFSSAPS -le médicament, les dispositifs et le sang- le département de transplantation des greffes et le département correspondant à l'embryon, à la reproduction et aux cellules, dont nous sommes en train de parler.
Cela aurait été, je crois, quelque chose d'assez extraordinaire, car l'on voit bien comment cette grande agence du vivant aurait pu donner une cohérence à notre système d'une façon générale, plutôt que de le morceler.
L'Etablissement français des greffes a une légitimité à s'occuper des cellules souches et du tissu hématopoïétique. Par ailleurs, l'AFSSAPS est aussi intéressée à la thérapie génique. On se trouve, je crois, dans une séparation totalement artificielle aujourd'hui !
Je pense que cette idée, pour autant que l'on veuille bien s'y pencher avec beaucoup d'objectivité, peut et doit séduire.
Néanmoins, même si mes services sont prêts -parce qu'ils sont assez séduits- à réaliser ce travail, je ne suis pas sûr d'avoir le temps de mener toute la concertation nécessaire sans déstabiliser une AFSSAPS déjà un peu fragile.
Je vais donc probablement vous proposer de faire les choses en deux temps avec, dans un premier temps, une agence qui rassemblerait l'Etablissement français des greffes et l'APEGH en gardant l'AFSSAPS en l'état, la mission de cette nouvelle agence se justifiant parce qu'il y a un continuum absolu entre organe, tissu, cellule, gène. Vouloir faire passer la barrière de façon artificielle n'est pas cohérent.
J'ajoute que, dans l'un comme dans l'autre, il y a la notion du don. J'ajoute que, dans l'un comme dans l'autre, il y a des problèmes éthiques profondément liés.
Regrouper l'Etablissement français des greffes et l'APEGH me paraît donc être d'une logique imparable, étant entendu que l'idéal à deux ans serait de préparer le rapprochement de l'AFSSAPS et de cette nouvelle agence, que j'appellerais volontiers, après fusion, si vous en étiez d'accord, l'Agence de biomédecine car, en définitive, c'est bien de biomédecine qu'il s'agit.
Quand nous faisons de la transplantation d'organes, nous transmettons des organes vivants : c'est de la biomédecine. Quand nous faisons de la thérapie cellulaire, que nous donnons la vie in vitro , c'est aussi de la biomédecine. On aurait donc là une grande agence de médecine, qui pourrait ensuite, se mariant à l'AFSSAPS, devenir agence de biomédecine et des produits de santé.
Voilà l'évolution, étant entendu que je donne à cette agence beaucoup plus de pouvoirs qu'on ne lui en avait précédemment donnés. A mon avis, il faut qu'elle ait un pouvoir d'autorisation, de contrôle, d'inspection, mais je voudrais qu'elle soit constituée pour une bonne part de gens qui ne soient pas nécessairement des scientifiques et des médecins prêchant pour leur seule paroisse. Je souhaite aussi naturellement que le ministre ait un droit de veto et d'intervention à tout moment, si une décision ne lui convenait pas.
Je pense qu'il est temps que l'on prenne cette mesure !
Quant à la brevetabilité des gènes, vous en connaissez comme moi l'histoire. La France ne veut pas que les gènes humains puissent faire l'objet de brevets.
Il n'en demeure pas moins que le Parlement européen, après avoir rejeté un premier projet de directive en 1988, puis un second en 1995, a fini par voter une directive en 1998, laquelle, défendue à l'époque par M. Allègre, pour ne pas le nommer, possède une contradiction que vous pouvez vérifier les uns et les autres, si vous ne l'avez déjà fait, dans son article 5, entre l'alinéa 1 et l'alinéa 2.
L'alinéa 1 est empreint d'une éthique à laquelle nous ne pouvons qu'applaudir. L'être vivant, tout ou partie, y compris une séquence partielle ou totale d'un gène, ne peut faire l'objet d'une invention brevetable.
L'alinéa 2, par contre, dit que tout élément isolé du corps humain, même une séquence partielle ou totale d'un gène, peut être breveté. Permettez-moi de le dire : c'est prendre les gens pour des imbéciles car, dès lors que vous voulez identifier un gène, le reconnaître, il vous faut faire un prélèvement de sang, isoler le sang du corps humain, ainsi que les cellules et l'ADN qui, par le séquenceur, peuvent du coup vous donner une séquence génétique brevetable !
Cette transposition va nous poser énormément de problèmes.
Le Gouvernement précédent, en réalité -et j'en avais longuement discuté avec le ministre Schwarzenberg- avait compris que les choses étaient trop ambiguës et ne pouvaient passer. Je rappelle qu'en 1994, dans notre loi de bioéthique, nous avions déjà pris des dispositions, car je sentais venir les choses. Pierre Mazaud ne m'avait pas facilité la tâche à l'époque, mais avait fini par saisir la difficulté.
On avait introduit, au milieu d'un texte juridique qui traitait du code civil, une disposition portant sur la propriété intellectuelle qui disait qu'on ne pouvait breveter une séquence partielle ou totale d'un gène. Je regarde Jean Chérioux, qui opine du chef !
Nous venons de répéter la même au mois de janvier, en réaffirmant notre position. Je suis effectivement d'accord avec cette optique.
La seule chose sur laquelle j'attire votre attention porte sur le fait que, la directive européenne étant la directive européenne, il faut nous mettre dans la meilleure situation possible pour obtenir la renégociation de cet article.
Je vais donc vous demander, tout en réaffirmant la non-brevetabilité des gènes humains, de réécrire la chose pour amender la directive européenne.
Je crois que je peux être au-dessus de tout soupçon dans cette affaire, étant donné la pétition que j'avais lancée sur Internet à une époque, que les groupes et les partis politiques, de tous côtés, avaient unanimement signée, tant il est vrai que c'est un combat commun.
J'avoue ne pas comprendre la position européenne de ne pas vouloir revenir sur une mauvaise écriture. Seulement quatre pays ont aujourd'hui transposé la directive, mais nous allons recevoir prochainement un avis notifié.
Le Gouvernement précédent avait prévu une transposition partielle. Mon idée est qu'il faut effectivement aller vers une transposition partielle, à condition d'avoir prévu dans notre texte une disposition que nous pourrions faire accepter à la Commission comme notre interprétation du texte.
Voilà ce que je voulais dire à propos d'un texte dont je me réjouis de débattre avec vous.
M. Nicolas ABOUT, président - Merci.
Monsieur le Rapporteur...
M. Francis GIRAUD, rapporteur - Monsieur le président, monsieur le ministre, mes chers collègues, le premier mot qui me vient à l'esprit est celui de perspicacité.
Vous nous avez démontré que ce problème, initié avec d'autres en 1994, ne peut être tranché de façon brutale, mais doit accompagner l'évolution des sciences, de la médecine et de notre société.
Vos propositions peuvent être qualifiées d'équilibrées et de sages.
En effet, dans une société démocratique, pluraliste, il est bien difficile d'amener à une prise de décision qui va être marquée dans la loi pour un certain nombre d'engagements de tous ordres des différents législateurs.
La commission proposera donc des amendements au texte qui a été voté en 2002.
Il n'est pas inutile de rappeler à nos collègues que le texte du précédent Gouvernement a été voté par une forte majorité, mais qu'il n'y a eu un nombre très faible -21- de votes contre, et un grand nombre d'abstentions.
Cela traduit bien l'évolution de la société et de la représentation nationale qui en est l'émanation.
Nous espérons que nous aboutirons à un texte qui ne pourra jamais satisfaire pleinement tout le monde, mais qui marquera un équilibre raisonnable à propos d'un problème de société très difficile.
D'autre part, pouvez-vous nous apporter quelques précisions, monsieur le ministre, sur la référence aux cellules souches adultes, le texte de loi parlant de «méthode alternative à visée médicale» ?
Par ailleurs, à propos de la multiplication des agences, je crois que ce Gouvernement a, d'une certaine façon, donné une réponse en créant un ministère de la santé qui a vocation à couvrir un certain nombre de problèmes.
Pouvez-vous d'autre part nous préciser la différence que vous faites, sur un plan technique, entre la recherche sur les cellules embryonnaires et la recherche sur l'embryon ? Dans l'esprit de beaucoup, ceci n'est pas tout à fait clair.
Enfin, en matière de bioéthique, par rapport au processus économique et industriel, comment la France peut-elle se situer dans la compétition internationale ?
En dernier lieu, je voudrais vous poser une question au nom de notre collègue Jean-Louis Lorrain qui siège ce matin même au Comité national d'éthique, où l'on discute d'ailleurs d'un problème qui est le problème de l'ICSI et de l'éthique.
Le DPI implique-t-il une ICSI ? Toute ICSI implique-t-elle dans le futur un DPI ? Le diagnostic préimplantatoire post-ICSI a-t-il une légitimité ? Faut-il modifier la loi en ce sens ? C'est assez technique, mais cela nécessite quelques éclaircissements.
M. Nicolas ABOUT, président - Monsieur le ministre, mes chers collègues, la commission est très honorée de voir que la délégation aux droits des femmes a souhaité se saisir de ce sujet et a retenu comme rapporteur notre excellente collègue Mme Desmarescaux. C'est maintenant à elle que je vais passer la parole.
Mme Sylvie DESMARESCAUX, rapporteur de la délégation aux droits des femmes et à l'égalité des chances entre les hommes et les femmes - Monsieur le ministre, monsieur le président, mes chers collègues, comme vous l'avez précisé, la délégation aux droits des femmes a été saisie à sa demande du projet de loi sur la bioéthique dont j'ai l'honneur d'être rapporteur.
Je suis consciente que c'est un sujet difficile et délicat.
Il est vrai que les femmes se trouvent au coeur de ce sujet en ce qui concerne plus particulièrement l'assistance médicale à la procréation, dont les traitements médicaux sont particulièrement difficiles et lourds.
Suite aux auditions qui se sont tenues avec la commission des affaires sociales il y a quelques jours, plusieurs questions se posent encore à moi, comme celle de la pénurie de dons d'ovocytes dans le cadre de l'AMP avec tiers donneur. Il semblerait que certains centres favorisent les couples qui se font accompagner d'une donneuse. Ce point-là reste entier pour moi. Ne faudrait-il pas préciser dans la loi qu'il est interdit de favoriser de tels couples ?
Je m'interroge également sur l'accompagnement psychologique avant, au cours du processus, voire après, quand il y a échec, pour aider sur le long chemin qui mène à l'adoption si nécessaire.
Reste bien évidemment tout le problème délicat au regard du transfert post mortem . Les questions sont multiples et m'inquiètent.
La semaine prochaine, la délégation va auditionner différentes personnalités. J'ose croire que les interventions pourront nous éclairer, mais je reste convaincue que ce sujet ne peut se traiter comme d'autres projets de loi. L'affectif, le vécu, ont une importance considérable.
M. Jean CHÉRIOUX - Monsieur le ministre, j'admire la façon dont vous avez essayé de régler ce problème, ô combien délicat, sur lequel nous avions eu bien des difficultés en 1994.
Je suis d'accord avec ce que vous avez indiqué, mais je voudrais néanmoins insister sur une ou deux modalités.
Le problème éthique sur lequel nous avions buté, à l'époque, était celui de la réification de l'embryon, mais aussi celui de sa disparition éventuelle.
Ne serait-il pas plus simple, dans le cadre du texte lui-même, d'indiquer que l'embryon ne peut être conçu que dans le cadre d'un projet parental, en liant le sort de cet embryon à l'existence de ce projet et en inversant les choses par rapport à la formulation actuelle ?
Le projet parental prendrait fin au bout d'un certain nombre de mois ou d'années, quitte à ce que les parents puissent demander à ce qu'il soit prolongé.
L'embryon surnuméraire devient à ce moment-là, sur le plan du droit, un embryon en attente d'implantation ou de transfert. Le jour où le projet parental tombe, l'embryon disparaît de sa bonne fin, comme c'est le cas dans la nature lorsqu'il ne se nidifie pas.
Cela permet de bien circonscrire le problème, ainsi que vous l'avez souhaité : pas d'embryon en dehors du projet parental et de son transfert !
Bien entendu, se pose à ce moment le problème de la science.
La transgression, telle que vous l'avez envisagée, et qui me semble excellente, peut se penser de deux façons.
Le texte de 1994 parlait d'études. Vous y avez fait référence. Il suffit de remplacer, dans ce texte, le mot «études» par le mot «recherches» pour arriver à peu près à ce que vous souhaitez.
Autre point sur lequel mon attention a été attirée : la nécessité pour la recherche de se créer des lignées d'embryons, sans toutefois en avoir un besoin permanent. Ne pourrait-on utiliser en priorité le «stock» d'embryons existant -terme affreux- qui peut suffire pour répondre aux besoins impérieux de la science et dont il faut tenir compte, quels que soient les principes éthiques des uns et des autres ?
M. Nicolas ABOUT, président - Merci.
La parole est à M. Cazeau.
M. Bernard CAZEAU - Monsieur le ministre, merci de cet excellent exposé, qui a permis de faire le point avec clarté sur les principales dispositions de ce texte.
En ce qui me concerne, j'aurais deux questions, qui ne sont pas des questions de fond. Je vous ai trouvé prudent, et même parfois un peu frileux, sur le problème de la recherche sur les cellules souches embryonnaires.
Je crois que la recherche française souhaite pouvoir utiliser ce genre de matériel.
Il ne faudrait pas, à travers l'encadrement que vous souhaitez -qui, par certains aspects, doit être fait- mettre nos chercheurs en difficulté par rapport à la recherche internationale.
Vous avez dit qu'il fallait suivre l'évolution. Je pense que celle-ci doit se faire d'abord dans le cadre européen et international. L'évolution de notre législation doit suivre, au moins dans ce domaine de la recherche.
Deuxième remarque sur l'APEGH. Votre souhait de regrouper toutes ces agences est très certainement lié à votre formation, mais ne va-t-on pas faire là de grosses machines ? Les problèmes soulevés par l'embryon et la génétique ne sont pas tout à fait les mêmes, même s'ils sont voisins, des problèmes liés au don d'organes, du moins dans la pratique, et l'on risque de se retrouver peu à peu avec des sous-agences, chacune reprenant sa liberté, pour en revenir au même résultat !
C'est en tout cas ma crainte.
M. Nicolas ABOUT, président - La parole est à présent au président Lardeux.
M. André LARDEUX - Merci de votre exposé, monsieur le ministre. On se sent un peu plus intelligent après vous avoir entendu. Vous nous avez apporté des précisions très utiles.
Je partage tout à fait un certain nombre de vos remarques, en particulier sur le fait que la loi doit être votée une fois pour toutes. On ne peut vivre éternellement dans le provisoire.
Je suis également d'accord avec vous en ce qui concerne la brevetabilité du gène.
Pour ce qui est de l'Agence, je crois que vous avez raison de vouloir unifier les choses. Bernard Cazeau parle du risque que représentent les grosses machines, mais il ne faut pas penser que ce serait forcément un organe avec une seule tête. Je pense que c'est une bonne direction.
J'ai quelques questions ou remarques à formuler. Vous avez dit -je pense ne pas trahir votre pensée- que le droit s'affranchit de la philosophie et de la morale. Cela dit, les législateurs, les citoyens, eux, ne s'affranchissent pas de la morale, de la philosophie, de la religion, ou de toute autre conviction qu'ils peuvent avoir.
Il n'est pas question d'imposer son éthique aux autres. La loi doit aboutir à une solution qui empêche que nos concitoyens, quelles que soient leurs convictions, n'aient pas le sentiment de voir leur conscience violentée. C'est en ce sens que vous allez.
A propos des cellules souches, vous avez été très clair au sujet de l'importation éventuelle de produits issus de recherches qui ne seraient pas conformes à la loi française, mais que fera-t-on si un Français décide de recourir au produit d'un clonage thérapeutique à des fins éventuellement reproductives ?
J'ai bien compris la distinction que vous faisiez à propos de la recherche sur les embryons et sur les cellules souches embryonnaires, mais qu'arrivera-t-il des surnuméraires non utilisés quoi qu'il arrive ? Il en restera forcément.
Qu'en est-il par ailleurs de la consultation et de l'information des personnes qui sont à l'origine de ces embryons ?
Certaines personnes peuvent accepter la recherche ; d'autres peuvent refuser que l'on fasse des recherches sur l'embryon non utilisé pour la reproduction.
Autre remarque sur le transfert post mortem : à titre personnel, je n'y suis pas favorable, malgré le sentiment de compassion que l'on peut avoir vis-à-vis de telles situations. Que répondra-t-on à ceux qui n'ont pas eu besoin de la PMA et qui se trouvent dans une situation qui les empêche de procréer ? Certains de ces couples peuvent, à titre de précaution, décider de recourir au don de sperme ou d'ovocyte et créer un embryon ! Je crois qu'il y a là une limite qu'il faudra fixer.
Dernière remarque sur le don d'organes des personnes vivantes. Je crois qu'il faut veiller à ce que l'intérêt propre des donneurs et de leurs ayants droit soit garanti, car une transplantation d'une partie du foie, par exemple, peut mettre la vie du donneur en péril et placer les familles -ascendants et descendants- dans de grandes difficultés. Dans ce cas, je ne vois pas où est le progrès !
M. Nicolas ABOUT, président - La parole est à M. Fischer.
M. Guy FISCHER - Je crois qu'on ne peut que remercier M. Mattei pour cet exercice de vulgarisation de haut niveau.
Vous vous prononcez, monsieur le ministre, pour l'utilisation très encadrée des embryons surnuméraires. C'est en ce sens qu'il y a de votre part, à travers l'évolution de votre réflexion, un changement. Nous sommes soumis à une pression au niveau européen et mondial et un certain nombre de lobbies poussent la France à évoluer.
D'autre part, vous avez été clair quant à votre position sur le clonage reproductif.
Je voudrais en venir au génome humain.
Dans le projet de loi, l'amendement Lefort a été adopté à l'unanimité. Il conduit -et vous en faites un de vos objectifs- à une renégociation de la directive européenne. Je crois qu'il est inutile de préciser l'importance de cet acquis qui constitue un préalable qui dépasse la loi de bioéthique.
Le professeur Munnich, que nous avons entendu, s'est prononcé pour une certaine brevetabilité. Je voudrais que vous nous expliquiez ceci.
M. Nicolas ABOUT, président - Monsieur le ministre, vous avez la parole.
M. Jean-François MATTEI, ministre de la santé, de la famille et des personnes handicapées - Merci.
Monsieur le président, monsieur le rapporteur, madame, il se trouve que je siégeais à l'Assemblée nationale en 1992, quand nous avons voté les lois de bioéthique, en première lecture, sous le Gouvernement de M. Bérégovoy. Après les élections de 1993, sous une nouvelle majorité, j'ai été chargé d'un rapport par le Premier ministre, M. Edouard Balladur. La démarche a repris au Sénat, en première lecture, sur les textes précédemment votés.
J'y vois là une répétition qui montre bien que, sur ces sujets, il n'y a ni polémique, ni esprit partisan, ni volonté de marquer une différence politique.
Nous nous sommes, je crois, rejoints sur des valeurs essentielles et nous pouvons diverger sur des points qui ne constituent pas l'ossature principale des dispositions que nous entendons prendre.
C'est la première raison pour laquelle j'ai souhaité continuer plutôt que recommencer.
La deuxième raison, c'est que l'on a déjà perdu trop de temps. Je souhaite que tout soit bouclé avant l'été 2003 et que la loi puisse être enfin promulguée !
J'ajoute qu'avant la première lecture, beaucoup de travaux de réflexion avaient été menés au Comité d'éthique, à la commission consultative des droits de l'homme, par les uns et par les autres, et ce serait faire peu de cas de ces réflexions que de recommencer à zéro !
J'en ai tenu compte et je vous rappelle -le rapporteur l'a signalé tout à l'heure- qu'il y a eu, à l'Assemblée nationale, un nombre important de votes pour et d'abstentions qui signifient qu'il n'y a pas d'opposition formelle, le vote contre ayant été très limité.
C'est donc cette petite loi que nous reprenons, qui fera néanmoins l'objet d'un certain nombre d'amendements, dont certains sont importants, notamment sur la structure de l'Agence. Après tout, c'est la première fois que le Sénat se saisit de ce texte et il est fondé à dire, sans être limité, comment il voit les choses !
Monsieur le rapporteur, vous m'avez demandé de préciser un certain nombre de choses.
Je ne crois pas qu'il soit utile, dans le texte de loi, de mentionner les cellules souches adultes ; à ce moment, il faudrait mentionner aussi les cellules du cordon ombilical. Même si c'est difficile, je souhaite en rester au principe et ne pas prendre le travers du précis de thérapeutique ou de biologie.
Après tout, qui ne dit pas que, demain, nous ne trouverons pas un nouveau type de cellules qui auront certaines particularités !
En revanche, dans votre rapport, dans nos interventions aux uns et aux autres, que nous interpellions le ministère de la recherche pour demander que des efforts particuliers soit faits pour que la France soit dans le wagon de tête des recherches sur les cellules souches d'origine adulte, bien entendu !
Lorsque j'accepte un certain nombre de positions, qui ne me sont pas faciles, sur les cellules embryonnaires, c'est parce que j'espère qu'assez vite, dans cinq, dix ans peut-être, les cellules souches adultes ou d'autres types de cellules pourront s'y substituer !
Sur le plan des agences, Monsieur le rapporteur, vous avez raison : je ne souhaite pas les multiplier ! On a l'AFSSAPS, l'Etablissement français des greffes, l'ANAES, l'IMPES, l'AFSA, etc. Il y en a huit !
Lors du débat sur la sécurité sanitaire, je voulais une grande agence dans ce domaine. Je vois bien qu'il y a, malgré tout, des conflits de compétences entre les différents domaines.
En revanche, sur le plan de la sécurité sanitaire, ce sont les mêmes problèmes qui se posent pour les cellules souches ou pour le don de gamètes. Souvenez-vous de la séropositivité éventuelle des donneurs !
C'est d'ailleurs là un des obstacles au don d'ovules. Quand on prélève, on conserve le temps de vérifier que la femme n'était pas négative, mais en période de séroconversion. On est donc dans des priorités de sécurité sanitaire, et l'Etablissement français des greffes et la nouvelle APEGH ont les mêmes préoccupations et la même démarche.
Bien sûr, chacun a sa responsabilité propre, mais on est dans le cadre de structures qui montrent bien que c'est un même ensemble permettant de préparer la suite.
Vous m'avez encore demandé de préciser la différence entre la recherche sur les cellules embryonnaires et la recherche sur l'embryon. C'est très simple : j'ajouterai simplement à ce que j'ai dit tout à l'heure que la recherche sur l'embryon est destinée à profiter à l'embryon -peut-être pas celui sur lequel on fait la recherche, mais à un embryon en tant que tel.
Comment peut-il mieux se développer ? Comment peut-on faciliter son implantation ? Comment peut-on lutter contre l'apparition de telle ou telle anomalie ? La recherche sur l'embryon est destinée à l'embryon, tandis que dans la recherche sur les cellules embryonnaires, il s'agit éventuellement de guérir les Parkinson, les Alzheimer, les diabétiques, les myopathies. C'est une recherche tournée vers la médecine.
D'un côté, c'est l'embryon qui est au centre de la préoccupation alors que, pour les cellules embryonnaires, c'est une méthode, la thérapie cellulaire. La philosophie n'est donc pas tout à fait la même.
Vous avez également raison, Monsieur le rapporteur, d'évoquer le processus économique et industriel.
Je suis scandalisé ! La France fait une proposition conjointe avec l'Allemagne pour interdire le clonage reproductif à l'ONU et les Américains ouvrent un contre-texte disant qu'il ne faut pas seulement interdire le clonage reproductif, mais aussi le clonage thérapeutique. Ce faisant, les Etats-Unis sont appuyés par la plupart des pays d'influence catholique forte, parce qu'il faut tout interdire.
Permettez-moi de vous dire que c'est une erreur -et je le leur ai fait savoir- de ne pas considérer qu'il y a des priorités et que la première est d'interdire le clonage reproductif. Clonage reproductif et thérapeutique ne sont pas de même nature ! Avec ce contre-texte, de nouveaux bébés vont naître.
Je n'accepte pas l'hypocrisie américaine. Chacun sait qu'une déclaration fédérale n'a aucun effet sur le privé ! Une dépêche datant d'hier indique que «la prestigieuse université de Standford, en Californie, a annoncé mardi qu'elle allait cloner des embryons dans le cadre de recherches sur les cellules souches».
Les Américains, au motif de vouloir à la fois interdire le clonage reproductif et thérapeutique, ont fait capoter l'interdiction du clonage reproductif. Ils savent très bien qu'ils ne prennent aucun retard en matière de recherches en énonçant de grands principes de moralité et de vertu ! Je n'accepte pas cette hypocrisie, et je souhaite que nous menions un combat basé sur nos valeurs.
Je prendrai mon bâton de pèlerin, s'il le faut, pour aller là où il faut faire comprendre que ce genre de chose est inacceptable !
Vous avez parlé, en vous faisant porteur de la question du sénateur Lorrain, du diagnostic préimplantatoire -DPI- que l'on fait sur l'embryon conçu in vitro , et de l'injection cytoplasmique du sperme -ICSI. On prend un spermatozoïde dans une micro-pipette et on le pousse de force à l'intérieur d'un ovule. Axel Kahn avait même appelé cela le «viol de l'ovule»...
Il n'y a pas de lien entre le DPI et l'ICSI. On peut avoir un DPI après une fécondation in vitro traditionnelle.
En revanche, la question de la légitimité peut être discutée, mais je ne la retiens pas. Les seuls éléments qui pourraient éventuellement amener à se poser la question, c'est qu'il semblerait y avoir une légère augmentation d'anomalies chez les enfants nés par ICSI. Il ne faut pas non plus se précipiter sur une technique et la légitimer. On en vient quelquefois à se poser la question de savoir jusqu'où pousser la logique et la cohérence. En effet, si l'on veut garantir la bonne conformité génétique, il faut faire de la fécondation in vitro . On entre là dans la démarche eugénique que -Dieu merci- nous avons tous, les uns et les autres, fermement condamnée.
Madame Desmarescaux, vous avez évoqué le don d'ovocytes. Je comprends bien la chose. Cela s'est passé au début pour les dons de sperme. Les hommes n'avaient pas dans l'idée d'aller donner leur sperme. C'est quand même une démarche particulière. Ce n'était pas très simple. On a donc privilégié les couples qui amenaient avec eux un donneur sachant, pour qu'il n'y ait pas de confusion dans les esprits, que le donneur vient alimenter une banque, le sperme utilisé pour la fécondation étant le sperme d'un autre donneur. On garde l'anonymat, sinon il n'y a pas besoin de venir le faire in vitro : il suffit de le faire dans une chambre !
Pour le don d'ovocytes, c'est pareil. Quand une femme vient avec sa soeur qui accepte de donner des ovules, ces ovules ne vont pas être utilisés pour la soeur demandeuse, mais pour alimenter une sorte de réserve, ensuite utilisée dans l'anonymat le plus strict.
Il faut voir ce que représente le don d'ovocytes, quelles que soient la volonté des professionnels et la volonté des associations de couples stériles menées par une femme dynamique, Mme Chantal Ramogida, qui a fédéré des centaines, voire des milliers, de couples stériles et qui exigent le don d'ovocytes !
Ce sont quand même des inducteurs de l'ovulation. C'est un des sujets dont on ne va pas parler ce matin, mais que l'on abordera au cours des débats. Il faut également faire une coelioscopie et l'idée qu'un peu de soi est porté dans le ventre d'une autre, n'est pas très simple.
On peut banaliser les techniques dans leur réalisation sur paillasse, mais le faire accepter dans les esprits n'est pas aussi simple. Les médecins peuvent prétendre qu'il n'y a pas de problème et dire que l'on manque d'ovocytes : nous ne sommes heureusement pas dans la règle de l'offre et de la demande livrée au marché !
Je peux comprendre, et je ne suis donc pas favorable à ce que l'on pousse les femmes à donner des ovocytes. Qu'on les informe, oui, mais je ne suis pas favorable à ce qu'on les incite à donner, car c'est parfois faire violence à certains comportements, qui pourraient se trouver interpellés.
Je suis complètement d'accord avec vous en ce qui concerne l'accompagnement psychologique, mais nous nous heurtons à un problème que je connais bien.
Avec Francis Giraud, nous avons contribué à accompagner la création de CECOS avec nos centres de génétique. Nous recevions les donneurs de sperme et nous voyions les couples. Que demandent les couples qui veulent une insémination d'ovocytes ou un don de sperme ? Ils demandent à ce que l'enfant soit conçu et, très vite, à disparaître dans l'anonymat, en oublier qu'une seringue est intervenue là où la nature ne suffisait pas.
Certains, comme Georges David, demandent la PMA-vigilance pour savoir si, dans vingt ans, ceux qui ont été conçus en éprouvette auront un peu plus de leucémies, un QI à peu près correct, etc.
Bien entendu, c'est possible, mais je ne suis pas sûr que l'on puisse le faire, car l'homme n'est pas un animal. On ne peut toujours le considérer comme un sujet d'expériences, même quand la science y trouve un intérêt.
L'accompagnement psychiatrique de ces fécondations in vitro ou de ces inséminations finit à mon avis par marginaliser les gens ou, en tout cas, en les identifiant, à les faire entrer dans une démarche selon moi plus porteuse d'anomalies que d'autres choses !
En revanche, là où vous avez raison, c'est en matière d'adoption. Oui, ces couples-là doivent être accompagnés. Vous le savez, la logique de la PMA ou de l'AMP et la logique de l'adoption sont deux logiques totalement différentes. Pour le moment, on a tendance à dire aux gens: «Si cela ne marche pas, vous adopterez», laissant sous-entendre que c'est une alternative. Ce n'est pas le cas !
Dans la démarche de l'AMP, il s'agit bien de donner la vie à un enfant, alors que dans l'adoption, c'est se donner à la vie d'un enfant, ce qui est totalement différent !
Je ne crois donc pas que l'on puisse entrer dans l'adoption parce qu'on a échoué l'AMP. Il faut faire un travail du deuil de l'enfant biologique et se sentir totalement au clair au regard de sa propre infertilité pour pouvoir s'engager dans l'adoption. C'est pourquoi je suis tout à fait favorable à une mesure de cette nature, qui pourrait proposer un accompagnement psychologique des couples après échec de l'AMP.
J'ajoute un problème que vous n'avez évoqué ni les uns ni les autres et qui, pourtant, me préoccupe beaucoup. Pourquoi ne suis-je pas forcément très allant sur le développement de toutes ces techniques d'assistance médicale à la procréation ? ... Parce que l'on commence à en voir les aspects négatifs ! Vous avez vu le rapport sur l'augmentation quasiment parallèle de la prématurité et des enfants nés prématurément, avec petit poids de naissance, voire difficultés infirmes motrices cérébrales, etc. On sait que ces techniques conduisent à transférer deux ou trois embryons conçus in vitro . Le risque de prématurés est plus grand et les registres que l'on a le vérifient.
C'est la raison de ma prudence. Je remercie M. Fischer d'avoir souligné que j'avais évolué. Oui, j'avance tout doucement. Il nous faut du temps. Le problème est que la durée de vie de l'enfant est la même que celle du médecin qui l'observe. Ce n'est pas du tout pareil que de faire des expérimentations sur des drosophiles, des champignons ou des brebis, que vous pouvez recommencer.
C'est pour cela que je suis extrêmement prudent. Nous avons un facteur limitant majeur, qui est la durée d'observation. Ce n'est pas la peine d'attendre une génération pour recommencer l'expérience du Distilbène !
Oui, ces techniques existent et on doit pouvoir les utiliser, mais on ne doit jamais ni les généraliser, ni les banaliser, ni les exposer comme étant faciles ! Je crois donc que nous devons faire preuve de la plus extrême retenue.
M. Chérioux a rappelé notre démarche commune en 1994. Cela reste un moment fort.
Je suis d'accord avec vous sur la notion de projet parental. Bien entendu, lorsque le projet parental disparaît, l'embryon disparaît dans sa bonne fin. Dès lors, si les parents sont d'accord, on peut probablement en disposer dans des conditions très précises, de manière à encadrer les choses.
Je ne crois pas que l'on puisse parler de réification de l'embryon. Je crois qu'on peut parler de réification des cellules embryonnaires. Les cellules embryonnaires ne sont pas l'embryon. C'est la raison pour laquelle, pour ma part, je fais le distinguo entre la recherche sur l'embryon et la recherche sur les cellules embryonnaires.
Je n'accepterai pas l'idée que l'on puisse fabriquer des embryons pour ensuite en émietter les cellules et les utiliser !
La question du devenir de ces embryons a déjà été posée il y a quinze ans. Je pense que la réflexion devait avoir lieu. Les choses devaient mûrir. Je suis maintenant convaincu que nous pouvons nous aventurer avec sagesse et prudence sur les voies que j'ai définies tout à l'heure, à une exception près.
Je suis, en effet, scandalisé quand j'entends certains chercheurs me dire : «Nous recherchons sur l'homme, et non sur le primate, parce que c'est beaucoup plus facile d'avoir des spermatozoïdes, des ovules et des embryons humains que de primates» ! Je pense que nous mettons là sur le même pied des choses que l'on ne peut mettre sur le même pied ! Il faut que la recherche fasse des efforts pour développer les modèles animaux.
Je souhaite que l'on aille vers la vérification et la mise au point de techniques nouvelles de reproduction et que l'on fasse d'abord tous ces clonages et ces transferts nucléaires sur l'animal, avant de se poser la question du transfert à l'homme !
Monsieur Cazeau, j'ai apprécié votre intervention. Vous m'avez posé quelques questions que j'ai notées et sur lesquelles on reviendra en séance.
Le travail sur les cellules souches embryonnaires ne signifie pas la réification de l'embryon, mais je ne crois pas non plus qu'il s'agisse d'une matière première banale, comme les tissus ou le sang humain.
On peut utiliser ces cellules embryonnaires dans des conditions très particulières, mais il ne faut pas pour autant les considérer comme une matière première banale. C'est la raison pour laquelle il nous faut absolument un cadre très strict et très précis.
Refuser de mener des recherches sur des cellules souches embryonnaires dans des conditions éthiquement définies mais accepter d'importer des cellules embryonnaires dont on ne pourrait garantir la façon dont elles ont été conçues serait une véritable hypocrisie !
Je ne sais si on pourrait garantir les principes éthiques et assurer qu'au bout de la chaîne, une femme n'a pas été payée à Singapour, en Corée ou ailleurs. Je préfère donc fixer des principes vrais, stricts, à la française, pour être à l'abri de ces dérives.
Sur le plan international, vous êtes à la fois utopique et volontaire. C'est bien. Je ne crois pas que nous puissions nous contenter de suivre. D'ailleurs, je ne suis pas certain que nous puissions nous entendre sur certains sujets.
Sur le clonage reproductif, je pense que c'est le cas. En deux ans de travaux au Comité de bioéthique européen, nous avons adopté un protocole additionnel sur les transplantations d'organes, qui est maintenant accroché à la convention d'Oviedo, mais nous avons dû constater, en dehors de principes communs de fond importants, comme la non-commercialisation du corps figurant, un désaccord absolu sur la notion de la mort.
Les pays européens n'ont pas la même définition de la mort. Nous, nous parlons de « mort cérébrale », et nous l'avons acté ; d'autres pays disent qu'à partir du moment où on qualifie la mort de «cérébrale», ce n'est pas la mort tout court !
On a donc un vrai débat là-dessus, que l'on a dû renvoyer à la décision des pays.
Deuxièmement, nous sommes sur la voie du consentement présumé en France, mais la moitié des pays européens le refusent ! Ils veulent un consentement explicite. Vous ne pouvez, par présomption, ouvrir le corps d'un mort et prélever un organe.
Nous n'avons pas pu nous mettre d'accord là-dessus, pas plus que sur l'élargissement des donneurs vivants.
Vous voyez donc que même sur des activités qui ne sont pas aussi difficiles que le début de la vie, on a, au plan international, des repères difficiles.
Je crois qu'il faut plutôt être meneurs. La France a une vocation des droits de l'homme. C'est pour cela que je voudrais, dans toute la mesure du possible, que nous adoptions ce texte à la plus large majorité possible, sinon à l'unanimité. Cela nous donnerait un poids formidable dans les discussions européennes et internationales.
Bien sûr, nos chercheurs sont toujours en compétition. Certes, si l'on va vers les cellules embryonnaires, nos chercheurs s'y mettront. Ils monteront dans le train, mais ne seront pas dans les premiers wagons.
En revanche, si on lance très vite la recherche sur les cellules souches adultes, ils pourraient être dans le wagon de tête. Un pays comme la France ne peut être compétitif dans tous les domaines. Choisissons les créneaux français qui correspondent à nos valeurs et dans lesquels nous pouvons espérer ! On passe son tour sur une technique, et on est en tête dans la technique suivante. C'est en ce sens que je pense qu'il faut vraiment encourager nos chercheurs.
Enfin, j'ai, en partie, répondu dans ma réponse au rapporteur sur l'APEGH et l'EFG : il faut l'autonomie des départements, mais ce sont les mêmes principes sous-jacents -éthique, sécurité sanitaire. Je vous demande de considérer cela avec un oeil attentif, car si c'était la première marche vers la grande agence, je crois que nous aurions fait une belle oeuvre !
Monsieur le Sénateur Lardeux, merci d'abord de vos propos très aimables à mon endroit.
Je me suis mal fait comprendre : il est clair que le droit ne peut s'affranchir de la morale, mais nous sommes aujourd'hui dans la situation d'Antigone et de Créon. On n'invente rien ! Créon défend le droit de la cité en refusant la sépulture au frère d'Antigone, parce qu'il s'est retourné contre la cité. Antigone défend le droit moral, parce que c'est son frère, et parce que c'est son frère, elle veut qu'il soit enterré !
Nous posons le problème aujourd'hui très exactement dans des termes antiques ! Nous les abordons avec d'autres arguments, mais nous ne pourrons jamais concilier l'éthique de responsabilité et l'éthique de conviction, le droit moral et le droit civil. Antigone et Créon sont éternels !
Naturellement, je vous rejoins sur la finalité de la recherche. Très souvent, on ne sait pas ce que l'on va trouver, mais on sait quelle est la thématique sur laquelle on démarre. Je crois qu'il faut clairement que le ministère de la recherche et le ministère de la santé indiquent là où l'on veut aller, d'abord et avant tout dans l'intérêt de la médecine, et dans le respect de nos principes éthiques.
S'agissant des surnuméraires, en réalité une lettre est envoyée tous les ans aux couples pour leur demander leur position.
Je dois dire, là aussi, que le temps m'a beaucoup appris. La démarche des couples qui veulent un enfant est orientée vers une grossesse, un enfant -parfois deux, mais surtout un. S'ils ont six embryons au congélateur, ils n'ont pas du tout le sentiment d'avoir six enfants potentiels. Qu'on ait conçu six embryons, à la limite, cela leur est égal. Ils ont eu leur enfant : le reste ne les intéresse plus !
Certains nous disent presque : « Pour le reste, faites ce que vous voulez ». Nous ne voulons bien évidemment pas les déresponsabiliser à ce point. Il faut retourner vers eux, leur rappeler que, malgré tout, ce n'est pas rien.
C'est tout l'intérêt qu'il y a à redéfinir les conditions de la consultation préalable. C'est dans cette consultation préalable, à mon avis, qu'on devrait clairement dire aux couples, par avance, qu'en cas de décès ou de rupture du couple, on ne garde pas les embryons, car on parle de l'embryon post mortem , mais dans les couples qui se séparent ou qui divorcent et qui ont des embryons, qui va avoir l'autorité parentale, l'autorité partagée ? Ces gens ne veulent souvent plus se parler, n'ont plus rien en commun ! Je crois que ceci doit être clairement défini si l'on ne veut pas se trouver devant des situations abominables.
Monsieur le président Fischer, je crois qu'au fil du temps, j'ai répondu à toutes vos questions, sauf à celle de l'amendement Lefort.
Pourquoi vais-je vous demander de revenir sur l'écriture de l'amendement Lefort, même si je l'ai voté et qu'il exprime, de manière frontale et directe, la volonté de ne pas voir une séquence génétique brevetée ?
Je voudrais que nous réécrivions cela pour ne pas être accusés d'être anti-progrès et anti-biotechnologies.
Pour être le plus clair possible, je veux que l'on puisse breveter la technologie et non le bio. Je veux que l'on considère que le gène, qui est la matière première vivante, n'est pas brevetable. Je m'en rends compte aujourd'hui quand je suis confronté à la mise au point du dépistage du cancer du sein familial d'origine génétique et à l'obligation de myriades, que nous allons transgresser par le biais de licences, etc.
Croyez bien que, dans le texte, sera bien spécifié ce qu'a souhaité l'Assemblée Nationale et que j'avais moi-même appelé de mes voeux en 1996, dans le rapport que j'avais fait pour l'office interparlementaire, qui avait débouché sur le vote à l'unanimité d'une proposition de résolution condamnant les brevets sur le vivant.
Si nous ne voulons pas rompre le dialogue et passer pour des gens opposés aux biotechnologies, il nous faut préciser dans un amendement que nous sommes contre le brevet de la séquence, mais pour que cette séquence soit utilisée dans une méthode qui, elle, peut faire l'objet d'un brevet. Il faut donc que nous explicitions bien ce qui, pour nous, est sanctuarisé et ce qui est, au contraire, ouvert à la commercialisation, le brevet et la libre-concurrence, pour le mieux-être des malades.
Je suis consterné de l'évolution qu'ont prises les choses -mais ce sont des responsabilités politiques partagées. Les politiques, y compris les parlementaires européens de tous bords -qu'il s'agisse du PC, du PS ou de la droite- ont voté cette directive des deux mains. Il faut dire qu'ils n'étaient pas très nombreux en fin de mandature et en fin de session, début juillet !
Le fait est que, lorsque je défends ce texte en disant qu'il est ambigu, on me répond : « Les députés l'ont voté, les commissions l'ont adopté, la commission et le conseil des ministres aussi : vous venez un peu tard ! ».
Mon souci, aujourd'hui, est que l'on puisse transposer la directive « biotechnologies » parce qu'on en a besoin, et je veux très clairement préciser notre vision de l'article 5 dans l'alinéa 2.
M. Nicolas ABOUT, président - Merci beaucoup, monsieur le ministre.
Nous sommes ravis d'avoir pu débattre avec vous de tous ces points si sensibles, et en particulier du dernier, la brevetabilité, qui est effectivement une difficulté que nous devons régler.
Merci à vous tous.
II. AUDITIONS DU MERCREDI 4 DÉCEMBRE 2002
M. Nicolas ABOUT, président - Nous abordons aujourd'hui nos travaux en séance plénière sur le projet de loi relatif à la bioéthique. Ces travaux ont été précédés par un grand nombre d'auditions organisées par notre rapporteur, le professeur Giraud. Il a eu la gentillesse d'associer tous les collègues qui le souhaitaient à ces auditions et je tiens à l'en remercier ainsi que tous les sénateurs qui y ont participé. Je les remercie de leur implication sur ce dossier si difficile et délicat de la bioéthique.
Déposé en juin 2001, le projet de loi qui nous occupe aujourd'hui a été examiné par l'Assemblée nationale du 15 au 22 janvier dernier. Nous sommes dans une situation identique à celle que nous avons connue pour les lois de juillet 1994 à savoir : un examen au Parlement à cheval sur deux législatures séparées par une alternance politique. Selon toute probabilité, le projet de loi sera discuté en séance publique au Sénat les 29 et 30 janvier prochain. La révision des lois sur la bioéthique sera alors sur les rails mais avec un retard de quatre ans sur le plan de marche fixé initialement par le législateur.
Je vous rappelle que nos auditions sont publiques et seront retransmises sur la chaîne du Sénat. Leur compte rendu intégral sera annexé au rapport de notre commission. Je souhaite, mes chers collègues, que ces auditions soient vivantes et que les échanges puissent se multiplier. Je vous demanderai de privilégier des questions courtes et je suggère à nos invités de répondre le plus complètement mais aussi le plus synthétiquement possible.
Monsieur le professeur Claude Huriet, notre rapporteur, Francis Giraud, vous a adressé, ainsi qu'à l'ensemble des intervenants, une série de questions, dont il rappellera brièvement les thèmes. Cher professeur, pourriez-vous d'abord, pendant un quart d'heure, nous faire part de vos observations sur le projet de loi et réagir aux questions de notre rapporteur ? Ensuite, je redonnerai la parole au rapporteur pour approfondir, le cas échéant, ses questions avant de la passer à l'ensemble des commissaires.
A. AUDITION DU PROFESSEUR CLAUDE HURIET, PRÉSIDENT DE L'INSTITUT CURIE
Pr. Claude HURIET - Merci, monsieur le président. Vous comprendrez, j'en suis sûr, le plaisir que j'éprouve d'être accueilli par vous, collègues et anciens collègues de la commission des Affaires sociales, et par le rapporteur, mon ami Francis Giraud. Je vous remercie de votre gentillesse qui me touche au point que je risque de bafouiller dans mes propos. J'essaierai cependant de dominer cette émotion durable et profonde.
Je commencerai mon intervention en évoquant le retard qui atteindra 4 ans pour la révision de la loi et l'incertitude quant à la date du vote final. Je m'interroge aussi à propos des délais de publication des décrets d'application en Conseil d'Etat.
Dans la perspective du débat au Sénat, est-il envisagé de débattre de la convention européenne de biomédecine, dite convention d'Oviedo, et du protocole additionnel dont la France est parmi les dernières à envisager la ratification ?
Dans le cadre du débat, la discussion des modifications éventuelles de la loi du 20 décembre 1988 et de la transposition de la directive européenne du 4 avril 2001 aura-t-elle lieu ? Si c'est le cas, je souhaiterais, sans abuser de votre gentillesse, vous faire connaître certains arguments.
Mon intervention s'appuiera non seulement sur le texte initial de la loi et sur celui adopté par l'Assemblée nationale en première lecture mais également sur les deux rapports de l'Office parlementaire d'évaluation des choix scientifiques et technologiques (OPESCT). En effet, l'un traite de l'évaluation de la loi de 1994 et avait engagé la procédure de révision, et l'autre du clonage, de la thérapie cellulaire et de l'utilisation thérapeutique des cellules embryonnaires.
Je voudrais présenter mon exposé en trois points, en commençant par « un comparatif ». En effet, je me suis livré à un exercice, pouvant rendre service au rapporteur, consistant à voir dans quelle mesure le texte du Gouvernement adopté en première lecture par l'Assemblée nationale a tenu compte de l'évaluation, a laquelle nous avions procédé, Alain Claeys et moi-même, de la loi de 1994. Le deuxième point de mon exposé comporte des remarques et des interrogations et dans la troisième partie, plus personnelle, je fais part de mes réserves et de mes oppositions.
- Etude comparative des textes
Des dispositions nouvelles vont dans le sens d'un élargissement des possibilités de prélèvement d'organes sur donneur vivant. Ces mesures sont légitimées par l'évolution des connaissances scientifiques que je ne détaillerai pas, et permettront aussi de combler, au moins en partie, l'écart entre le nombre des malades en attente et les possibilités de transplantation. L'extension se réfère à des personnes unies par un lien étroit et stable. Pour la greffe de moelle, le don entre cousins et cousines germains est justifié par de nombreux motifs que d'autres que moi pourront développer.
S'agissant du consentement, à distinguer de l'autorisation, dans la procédure mise en place par la loi, je formulerai quelques remarques sur les comités d'experts et sur l'utilité d'encadrer dans la loi la stimulation ovarienne. Ceci correspond aussi à une demande presque unanime qu'Alain Claeys et moi-même avions reçue lors de nos auditions.
Pour le transfert d'embryons post mortem , les dispositions sont conformes à notre évaluation. En effet, si les avis étaient partagés, l'opinion dominante parmi les obstétriciens et les psychopédiatres, était la quasi-impossibilité de proposer à une femme, dont le mari était décédé, l'accueil de « son » embryon par un autre couple. Je crois d'ailleurs qu'aucune application de ces dispositions de la loi n'a été effective. En revanche, le transfert post mortem est beaucoup moins simple qu'on pouvait l'imaginer. Finalement, la sagesse l'a emporté en l'autorisant, dans certaines conditions, en exigeant un délai minimum de réflexion et un délai maximum pour la décision. Pour le don de gamètes, la loi élargit le nombre d'enfants conçus par le donneur de gamètes de cinq à dix. En effet, les études génétiques ont montré que le risque de consanguinité n'existait pas pour un seuil aussi bas.
La portée de la reconnaissance de la Nation ne doit pas être minimisée. Je suis satisfait de voir que l'article L. 1211-7-1 inscrit ce principe dans la loi. Il reste à voir comment s'exprimera cette reconnaissance de la Nation pour ceux qui font don généreusement d'une partie de leur corps, de leurs tissus ou de leur sang.
- Remarques et interrogations
J'attire votre attention sur des techniques, relativement récentes, et sur lesquelles mon ami Axel Kahn pourra vous apporter des précisions. Désormais, on peut disposer de puces à ADN et de kits de diagnostics déjà largement accessibles aux Etats-Unis. Nous devons nous interroger, non pas sur le bien fondé des dispositions législatives encadrant l'utilisation et l'accès aux données génétiques, mais sur la question de savoir si la diffusion de ces procédés ne va pas changer fondamentalement l'application de la loi. En effet, rien n'empêchera des personnes ayant réalisé leur propre diagnostic génétique et disposant d'un « profil idéal », de le faire valoir auprès des assureurs, pour bénéficier d'un bonus, ou des employeurs, pour obtenir une priorité à l'embauche. Il est nécessaire, dans le cadre de l'évaluation et de la révision de la loi, de tenir compte de ces nouvelles possibilités de diagnostic.
Remarque plus ponctuelle : la loi prévoit la rémunération des membres des comités d'experts. A propos de la loi du 20 décembre 1988, les membres des comités consultatifs de protection des personnes à la recherche biomédicale, se sont vu refuser le principe d'une rémunération voire même d'une simple indemnisation. Cela devrait être revu parce que des conséquences négatives, que j'avais évoquées dans un rapport de votre commission, se répercutent sur le pluralisme des comités consultatifs de protection des personnes dans la recherche biomédicale (CCPPRB).
Un autre élément intéressant est la référence aux ULTRAS, dénuée de toute signification politique, mais terme anglais Un Related Living Transport Regulation Authority, mentionnée par le comité consultatif national d'éthique dans son avis du 27 mars 1998. Cette référence permet de relativiser le rôle de ces comités d'experts en ce qui concerne les autorisations de prélèvements sur donneur vivant après que le juge ait recueilli le consentement. Dans l'avis du Comité consultatif national d'éthique (CCNE), il est indiqué que de 1991 à 1994, l'ULTRA a été saisi de 450 demandes et a donné 28 autorisations. Ces chiffres intéressants sont toutefois nécessairement transposables en France.
J'ai beaucoup réfléchi au cas particulier des mineurs. Pour les prélèvements de moelle osseuse chez des mineurs, frères, soeurs ou, éventuellement, cousins ou cousines, le consentement, première phase de la procédure, est exprimé devant le président du tribunal de grande instance. Un confrère pédiatre m'a fait part du calvaire vécu par un petit donneur, lors de sa comparution devant le magistrat. Comment concilier la nécessité de garantir les conditions d'obtention du consentement et la sensibilité de l'enfant qui « comparaît devant un juge ». Dans les dispositions actuelles du texte, l'obligation du recueil de consentement du mineur par un magistrat n'est pas remis en cause, ce qui est bien. Mais, le petit donneur devra, en outre, comparaître aussi devant le comité d'experts, soit deux comparutions successives pour un enfant dans les conditions de fragilité psychologique que l'on peut imaginer. Je ne sais pas quelle réponse apporter mais j'attire votre attention sur des situations que le législateur ne peut ignorer.
La preuve d'une vie commune depuis au moins deux ans est une disposition contre laquelle les médecins se sont élevés vigoureusement. Ils considèrent, en effet, qu'ils n'ont ni vocation, ni moyen de s'assurer de la stabilité d'un couple, alors qu'il s'agit d'un critère permettant d'autoriser ou de refuser l'AMP. A qui confier une évaluation aussi subjective que difficile ? La période d'au moins deux ans de stabilité du couple est, en outre, contestée par les praticiens de l'AMP, surtout lorsqu'il s'agit de femmes relativement âgées. Imposer sans raison autre que « l'épreuve de la stabilité », une période de deux ans supplémentaires risque, selon eux, d'entraîner des inconvénients pour le déroulement de la grossesse.
- La médecine régénératrice
La médecine régénératrice comporte des liens étroits avec la thérapie cellulaire. Laissez moi vous en donner un exemple frappant concernant des « vessies artificielles ». On peut désormais fabriquer des vessies en partant d'un moule réalisé en substance biodégradable sur laquelle on va mettre en culture, de part et d'autre, des cellules vésicales. Il s'agit bien de culture, de thérapies cellulaires. Ces dispositifs « mixtes » sont actuellement « hors la loi » et n'apparaissent dans aucun texte national ou européen. On se posera, à l'évidence, la question de leur commercialisation, qui sera en contradiction avec le principe de la non-commercialisation du corps humain. En cette matière, le législateur a intérêt à fournir des réponses avant que les problèmes ne se posent d'une façon aiguë.
- Définition des thérapies géniques et cellulaires
Les définitions des thérapies géniques et cellulaires sont à revoir. Elles manquent de clarté. Je me demande si les articles L. 5151-1 et L. 5151-2 visent les vecteurs viraux ou autre chose. Il faut répondre.
- Thérapies géniques germinales
La réflexion doit se poursuivre. La thérapie génique germinale, selon certains généticiens, ne peut pas être catégoriquement exclue. En effet, par des manipulations génétiques, éviter la naissance d'enfants atteints de maladie génétique est une chose mais si cette technique est efficace, certains se demandent pourquoi en interdire le bénéfice aux générations sui suivront.
- Disparition de la consultation de conseils génétiques
La disparition de la consultation de conseils génétiques me paraît être une erreur : il faut revenir sur ce point.
- Réserves et oppositions
Les points suscitant réserve ou opposition sont peu nombreux, mais extrêmement importants à mes yeux. Tout permet de penser que l'essentiel du travail parlementaire va se développer sur ces éléments.
- L'APEGH (Agence française de la procréation, de l'embryologie et de la génétique humaine)
L'APEGH dispose de compétences larges, de compétences très larges, de compétences trop larges. Je m'étais exprimé avec Jacques Montagu, membre du Comité consultatif national d'éthique, dans un article retenu par le Figaro en janvier 2002. Je vous en transmets une copie, monsieur le rapporteur : cela peut vous aider à mieux comprendre mes propos nécessairement concis.
J'ai cherché dans le texte adopté par l'Assemblée nationale l'article encadrant le diagnostic préimplantatoire (DPI) que nous avions eu beaucoup de mal, Jean Chérioux s'en souvient, à introduire dans le texte de 1994. Nous y étions parvenus avec la collaboration étroite de quelques-uns de mes collègues généticiens et obstétriciens. Cette référence au DPI n'existe pas dans le texte de première lecture. Il faut chercher dans la liste des compétences de l'APEGH, la définition du DPI, c'est-à-dire la recherche sur les cellules embryonnaires. Il est inacceptable de ne pas mentionner le DPI en tant que tel dans une énumération qui comporte diverses attributions (les cellules embryonnaires et foetales, les conditions de prescription des examens des caractéristiques génétiques) qu'on transfère à l'APEGH. C'est comme si le législateur se désengageait de domaines cruciaux qui portent sur des valeurs fondamentales telles que la dignité de la personne humaine et sa place dans la société. Des champs de compétences aussi sensibles seraient ainsi transférés à l'APEGH. Certes, l'Agence devra rendre un rapport annuel, mais ses compétences doivent être revues, non pour la vider de sa substance mais pour définir précisément ce qui peut lui être délégué et ce qui doit impérativement relever de la responsabilité de la représentation nationale. C'est un point d'autant plus important que l'agence « autorise » les protocoles de recherche sur l'embryon et sur les cellules embryonnaires et ne se limite plus à « donner un avis », selon un amendement adopté par l'Assemblée nationale. La Haute Assemblée doit être particulièrement vigilante sur ce point. Les missions du Haut Conseil seront définies par décret en Conseil d'Etat. Je n'ai rien contre le Conseil d'Etat mais, dans un domaine aussi sensible, c'est une autre façon pour le Parlement de se dessaisir d'une part de ses responsabilités.
- L'assistance médicale à la procréation (AMP)
En cas de désaccord entre les deux membres d'un couple, l'article L. 2141-4 du projet de loi tranche en optant pour la destruction de l'embryon surnuméraire. Cela signifie qu'au sein d'un couple qui se déchire, l'avis le plus négatif, si j'ose dire, l'emporte.
L'article L. 2151-3 porte sur la recherche sur l'embryon et les cellules embryonnaires et les compétences de l'APEGH. Je voudrais dire pourquoi je suis très réservé quant à l'évaluation préalable de toute technique d'AMP. On affirme qu'en aucun cas on ne peut autoriser de produire des embryons humains pour la recherche, mais une disposition de la loi précise que toute nouvelle technique d'AMP doit être précédée d'une évaluation. Or, évaluer c'est comparer et je ne vois pas comment on peut comparer en l'absence de lots d'embryons humains témoins qui, ne pouvant être implantés dans un utérus et devant être détruits, auraient été conçus pour la recherche. On ne peut pas affirmer une chose et écrire le contraire. La conception in vitro d'embryons humains à des fins de recherche est interdite sans préjudice de l'évaluation.
« Les embryons sur lesquels une recherche a été conduite ne peuvent être transférés à des fins de gestation. » Je ne comprends pas cette phrase. Signifie-t-elle que les embryons peuvent être transférés à d'autres fins ? Cela soulève, en outre, insidieusement l'interrogation sur le clonage thérapeutique. Les choses ne sont pas claires.
Je relève aussi une phrase qui m'étonne et qui n'est pas dénuée d'humour : « Le consentement des deux membres du couple est révocable à tout moment et sans motif » . Que signifie cette disposition si le couple revient sur sa décision après que l'embryon surnuméraire eût été utilisé à d'autres fin.
- Le clonage
A plusieurs reprises apparaît la phrase « gamètes d'un homme et d'une femme en vue de faire naître un enfant » . Mais la mention de l'utilisation possible des cellules souches adultes n'apparaît nulle part. Ne pas les évoquer d'une façon ou d'une autre risque de tronquer un débat qui sera difficile. Il faut éviter d'alimenter l'idée fausse selon laquelle si la loi interdit l'utilisation des cellules souches embryonnaires, elle condamne au désespoir les malades atteints de maladies graves et incurables, qui espèrent en bénéficier.
Je termine, monsieur le président, en évoquant le délai de réexamen de quatre ans mentionné dans le projet de loi, alors que nous n'avons déjà pas été capables de respecter le délai de cinq ans inscrit dans la loi de 1994. Le point important, l'expérience le montre, porte non seulement sur le délai de la révision de la loi mais aussi sur le délai de parution des décrets. Bien sûr, cela ne peut pas être mentionné dans la loi. Mais, dans le rapport d'évaluation de la l'OPECST, nous avions souligné que certains textes d'application n'avaient été publiés que quatre ans après la promulgation de la loi.
M. Nicolas ABOUT, président - Merci beaucoup. Claude Huriet, chacun s'en souvient, était l'un des membres les plus illustres et les plus éminents de notre commission. Il a marqué nos travaux et nous nous apercevons encore ce matin qu'il le fait toujours. Claude Huriet, vous avez été, vous le rappeliez tout à l'heure, en 1999 avec Alain Claeys l'auteur d'un rapport de l'Office parlementaire des choix scientifiques et technologiques. Ce texte fut très important puisqu'il a constitué le prélude de la révision de cette loi sur la bioéthique. Je voulais vous remercier tout particulièrement d'avoir accepté d'ouvrir cette journée. Nous souhaitions en effet qu'elle soit ouverte par quelqu'un avec qui nous avons des liens d'amitié très anciens et profonds.
M. Francis GIRAUD, rapporteur - Merci monsieur le président. Monsieur le conseiller d'Etat, cher Claude, peu de commentaires sont nécessaires. La commission a ressenti dans votre exposé toute la réflexion, la maturation et le travail de très nombreuses années. Nous vous en remercions beaucoup. Vous avez répondu à nos questions et je ne reviendrai pas sur le détail. Je vous poserai deux questions, une générale et une plus particulière. Vous avez participé en tant que parlementaire aux travaux sur les lois de bioéthique de juillet 1994. Quel regard portez-vous sur l'évolution scientifique et des mentalités intervenue depuis lors ? Cette question, d'ordre sociologique et non pas technique est, de mon point de vue, assez importante. La deuxième question, plus précise est la suivante. Quel sort devrait être, selon vous, réservé aux embryons dits surnuméraires aujourd'hui conservés et qui n'ont pas ou plus de projet parental ? Sur un plan pratique, que devons-nous faire ?
M. Nicolas ABOUT, président - Professeur Huriet, quel est votre regard et quel est votre avis sur le sort des embryons ?
Pr. Claude HURIET - L'évolution scientifique s'est accélérée, notamment dans le domaine de la génétique. En 1994, lors des travaux préparatoires, ce domaine n'avait pas atteint sa maturité. Mais maintenant, je le disais à propos des puces à ADN, nous sommes face à des réalités. Le progrès se développe rapidement dans le domaine des biotechnologies, des sciences de la vie et de leurs applications à l'homme. Ce progrès suscite bien des espoirs : en ce qui concerne l'évolution des mentalités, nous constatons par rapport à 1994 plus qu'une simple curiosité, un souhait d'une large partie de l'opinion de s'impliquer dans la réflexion et de participer au débat. Nous sommes quelques uns à être de plus en plus sollicités pour venir parler de bioéthique devant des auditoires nombreux et divers. Les mentalités évoluent, nous sortons du cénacle des chercheurs et des scientifiques, l'opinion s'intéresse de plus en plus à ces questions difficiles, surtout quand sa propre santé est concernée. Se manifeste aussi le sentiment de toute-puissance de la médecine, avec pour corollaire le refus de la maladie et quelquefois de la fatalité de la mort. Nous sommes dans le contexte d'une société citoyenne qui s'intéresse et veut s'impliquer davantage dans ces réflexions. Je pense que le Parlement s'honorera en en tenant compte.
Au sujet des embryons surnuméraires sans projet parental, ma position est connue. Je l'évoquais dans la dernière partie de mon exposé. Le nombre d'embryons surnuméraires doit actuellement dépasser 100.000, mais nous ne savons pas trop le chiffre exact. Leur existence pose la question de savoir si la loi doit mettre en place des dispositions visant à en limiter le nombre si cela est techniquement possible. L'exemple allemand, cité volontiers il y a quelques années, est en train d'évoluer puisque le Bundestag s'interroge pour savoir si la loi protectrice de l'embryon doit être amendée. Ma position personnelle concernant la reconnaissance de la dignité de l'embryon humain dès son origine m'amène à considérer qu'il vaut mieux mettre un terme à sa conservation plutôt que de l'instrumentaliser quelles que soient les fins pouvant justifier son utilisation. C'est un des points fondamentaux du débat à venir.
M. Nicolas ABOUT, président - Je vais donner la parole au rapporteur de la loi de 1994 sur la bioéthique, Jean Chérioux.
M. Jean CHERIOUX - Je vous en remercie, monsieur le président. Le sujet est tellement vaste qu'il faut choisir. Mon choix se portera, cela n'étonnera pas le rapporteur, sur la recherche sur l'embryon. C'est d'ailleurs dans ce domaine que se posent le plus grand nombre de vos interrogations, monsieur le conseiller d'Etat. Vous avez dit, très justement, que nous avions affaire à des citoyens qui réfléchissaient beaucoup à ces problèmes. Mais, mon inquiétude est que leur réflexion se situe dans le contexte particulier de la fascination de la thérapie génique. Au nom de celle-ci, ne risquons nous pas de nous trouver devant des dérapages assez graves ? Vous avez vous-même indiqué que l'introduction dans la loi d'une référence aux cellules souches adultes est souhaitable. En effet, si elles peuvent avoir et rendre les mêmes effets que les cellules souches embryonnaires, le problème peut être réglé. Mais ma question est la suivante. Admettons qu'il soit possible de faire des recherches sur l'embryon. C'est une porte ouverte. On commencera par étudier les quatre ou huit cellules de base et après jusqu'où ira-t-on? Cela ira-t-il jusqu'à une sorte d'enfantement artificiel de l'embryon comme dans « Le meilleur des mondes » ? Sur quoi déboucheront ces recherches ? Nous pouvons envisager les recherches à partir des cellules. Mais, après, jusqu'où cela peut-il nous mener ? N'y a-t-il pas un risque considérable ? Comme vous l'avez très justement précisé, en définitive, la décision revient à un organisme chargé de tout régler à la place du législateur. C'est très commode pour le législateur mais, aujourd'hui, cela nous pose un problème déterminant.
Pr. Claude HURIET - Je ne sais pas si nous pouvons parler de fascination de la thérapie génique. Il y a deux ans, à l'occasion du rapport de l'OPECST se manifestait, c'est vrai, un certain enthousiasme en faveur de la thérapie génique. Les premiers désenchantements sont intervenus aux Etats-Unis quelques mois après. En France, les succès d'Alain Fischer ont permis d'adopter une vision d'autant plus mesurée que nous avons vu les applications possibles et les éventualités de réussite thérapeutique. On a constaté concrètement les difficultés pour maîtriser un processus de prolifération cellulaire sur la nature de laquelle on s'interroge. Des espoirs et des possibilités apparaissent au fur et à mesure que progresse la connaissance du génome. Raison de plus pour regretter l'absence de référence explicite au diagnostic préimplantatoire. Une question grave risque de se poser. Au fur et à mesure que nous allons découvrir, individualiser, les gènes responsables ou prédisposant à des maladies, allons-nous envisager de traiter ces maladies par thérapie génique ? Prenons l'exemple de certaines formes de cancer du sein à prédisposition familiale. Ne va-t-on pas être tentés d'étendre les indications du DPI plutôt que de recourir, si elle est possible, à la thérapie génique plus aléatoire et plus coûteuse ? Ne serons-nous pas confrontés à un choix entre les possibilités des thérapies géniques et une sélection par le DPI permettant de caractériser les embryons porteurs d'anomalie génétique afin de les éliminer plutôt que de chercher à les traiter ?
M. Nicolas ABOUT, président - Merci beaucoup. Je suppose que nous reviendrons sur tous ces sujets avec chacun des intervenants tout au long de la journée.
M. André LARDEUX - Merci, d'abord, de votre exposé qui était très clair et très passionnant. L'un des arguments qui va nous être opposé est celui de l'action des autres pays. Qu'en pensez-vous ? Comment pouvons-nous nous protéger ? Des sectes ou des personnes très médiatiques comme M. Antinori prétendent réaliser des choses hors normes. Comment, en France, à partir de la législation qui est proposée, pouvons-nous éviter ces dérives ?
Pr. Claude HURIET- - Les références à M. Antinori et au mouvement raëlien ne sont pas les plus préoccupantes car, dans l'opinion internationale, il existe un fort rejet du clonage reproductif. Cela ne signifie pas pour autant qu'il n'interviendra jamais. Mais votre interrogation concernant la compétition internationale en matière de recherche est extrêmement importante. Les défenseurs de la recherche sur l'embryon de l'utilisation des embryons humains surnuméraires et sans projet parental disent qu'ils ont les moyens de mener ces recherches mais que la loi leur interdit de participer à la compétition internationale pour les perspectives d'utilisations thérapeutiques. Cet argument nécessite une réflexion en profondeur. Nous n'avons pas le droit d'interdire aux personnes qui refusent cette possibilité de faire valoir leurs arguments. A vrai dire, la compétition internationale ne concerne pas seulement l'utilisation de l'embryon humain. Est-ce parce les Pays-Bas autorisent l'euthanasie que l'on doit considérer que la France est en retard et qu'elle doit adapter sa législation ? Cette question est d'autant plus compliquée qu'elle est souvent assortie de la réflexion suivante. Le jour où, et ce n'est pas pour demain, les indications thérapeutiques seront cohérentes, irait-on jusqu'à interdire l'importation des moyens thérapeutiques pour répondre aux attentes des malades français ? En cela, les perspectives d'utilisation des cellules souches adultes seront intéressantes pour autant qu'elles soient elles aussi confirmées. L'utilisation thérapeutique des cellules embryonnaires laisse encore de nombreuses incertitudes. Si une solution alternative apparaît, le dilemme sera moins tragique.
M. Guy FISCHER - D'après votre très grande expérience et votre connaissance du dossier et pour prolonger les propos de notre collègue André Lardeux, constatez-vous, en France, de plus en plus de voix se faisant entendre pour l'utilisation des embryons surnuméraires sans projet parental ? Sentez-vous une pression au niveau du monde scientifique et de la part de lobbies qui pourrait avoir des conséquences sur le débat et le contenu de ce projet ?
Pr. Claude HURIET - Je ne sais pas si les prises de position sont de plus en plus nombreuses. En tout cas, elles s'expriment de plus en plus fortement. On comprend pourquoi, dans la mesure où ce qui pouvait apparaître comme hypothèse incertaine il y a quelques années devient plus crédible. Le débat dans lequel les scientifiques ont tout à fait le droit de s'exprimer correspond à une réalité proche. Nous savons que la science par elle-même n'est ni morale ni immorale. C'est finalement au niveau de l'éthique et de la loi qu'il faut réfléchir aux conséquences. Mais, les chercheurs, surtout dans le domaine des sciences de la vie ont une responsabilité particulière. Dans le domaine des biosciences, il peut y avoir conflit quand à la primauté à donner à l'intérêt de la société sur celui de l'individu. De tels conflits justifient la réflexion en matière de bioéthique. Nous n'avions pas tellement besoin d'y réfléchir il y a vingt ans.
M. Dominique LECLERC - Je voudrais juste demander une précision à M. Huriet. Il a évoqué tout à l'heure 100.000 embryons surnuméraires. Si j'ai bien compris, dans le cadre de la loi de 1994, un délai de cinq ans est précisé pour restituer les embryons dans le cadre de projets parentaux. Ces 100.000 embryons conservés correspondent-ils à ceux qui n'ont pas eu de projet parental ?
Pr. Claude HURIET - Le chiffre de 100.000 est un ordre de grandeur qui inclut les embryons qui continuent de faire l'objet de projets parentaux. Il n'est pas possible et pour cause, de faire la part de ceux qui ne bénéficient plus d'un projet parental et les autres d'autant qu'il s'agit de flux avec des entrées et des sorties. Le couple est tenu par la loi de faire connaître, chaque année, ses intentions. Quand il ne le fait pas ou ne le fait plus, le projet parental est considéré comme abandonné.
Pour le délai de cinq ans, Jean Chérioux le confirmera, la loi de juillet 1994 avait autorisé qu'il soit mis fin à la conservation d'embryons antérieurs à la promulgation de la loi. Mais elle a, en outre, interdit la destruction des embryons conçus postérieurement jusqu'à la révision de la loi. Comme nous sommes bien au-delà des cinq ans, cela explique l'accroissement significatif du stock.
M. Jean CHERIOUX - Nous avons supprimé ceux qui existaient à cause de l'absence de contrôles sanitaires. Pour les autres, nous espérions que des solutions scientifiques seraient trouvées pendant ces cinq ans. Malheureusement, nous n'avons pas encore débouché sur des résultats tangibles. De plus, le délai s'est révélé beaucoup plus long que prévu puisque nous en arrivons à huit ou neuf ans.
Pr. Claude HURIET - L'accueil de l'embryon était une possibilité offerte par la loi. C'est une des dispositions pour laquelle les décrets d'application n'ont été publiés que près de quatre ans après la promulgation. Nous savions bien que cette disposition, défendue avec passion par Jean Chérioux, serait difficile à mettre en oeuvre et que sa portée serait sans doute limitée. De plus, le retard de parution des décrets ne permet pas d'en apprécier le résultat.
M. Nicolas ABOUT, président - Combien d'embryons étaient concernés en 1994 ?
Pr. Claude HURIET - Je n'en sais rien. Monsieur le rapporteur de 1994 devrait savoir.
M. Jean CHERIOUX - Je ne me souviens pas exactement. Je crois que c'est plus de l'ordre de 20.000 ou 30.000 que de 10.000.
M. Nicolas ABOUT, président - Il nous reste à remercier Claude Huriet de nous avoir fait à la fois le plaisir d'être à nouveau parmi nous et de nous avoir apporté ses lumières sur ce sujet si délicat.
B. AUDITION DU PROFESSEUR AXEL KAHN, DIRECTEUR DE L'INSTITUT COCHIN, DIRECTEUR DE RECHERCHE À L'INSTITUT NATIONAL DE LA SANTÉ ET DE LA RECHERCHE MÉDICALE (INSERM)
M. Nicolas ABOUT, président - Mes chers collègues, nous avons le plaisir d'accueillir le professeur Axel Kahn, pour la deuxième fois dans le cadre de ce travail puisque le professeur Giraud, notre rapporteur, l'a déjà entendu. Mais, il a jugé nécessaire que le professeur puisse revenir devant l'ensemble de la commission en audition publique nous faire part de ses observations. Monsieur le rapporteur, sur quels points souhaitez-vous particulièrement interroger à nouveau le professeur Axel Kahn ?
M. Francis GIRAUD, rapporteur - Mon cher collègue nous sommes heureux de vous entendre à nouveau. Nous vous avons communiqué, hier, le canevas des points importants que nous aimerions que vous exposiez devant la commission. Nous connaissons tous vos travaux et votre rôle important dans la recherche en France par le biais de l'INSERM. Vous êtes l'un des rares à pouvoir nous donner des réponses très précises.
Le sujet le plus important est, nous l'avons vu lors de la première audition, la recherche sur l'embryon. Quelles réflexions vous inspirent les dispositions votées par l'Assemblée nationale en janvier 2002 ? Que pensez-vous de la possibilité offerte par le projet de loi de créer des embryons dans un but d'évaluation des nouvelles techniques de PMA ?
Ensuite, nous voudrions connaître où en sont, dans les pays ayant une législation peu ou pas contraignante, les recherches menées sur les cellules souches embryonnaires et sur les cellules souche adultes. L'objet de notre débat est de connaître les résultats même s'ils ne sont pas immédiats. En effet, le système médiatique brouille un peu les pistes et comme nous entendons parler de cellules de l'espoir, nous voudrions connaître le délai dans lequel il peut se réaliser. Nos collègues sont avertis de ces problèmes mais ils ont besoin de réponses précises et je sais que vous pouvez nous les apporter. Ensuite nous évoquerons le problème d'organisation de l'APEGH, à savoir si c'est le politique ou un conseil d'administration qui doit décider. Cependant ce n'est pas aussi fondamental que le problème de l'utilisation d'un embryon. Une autre question abordera le transfert d'embryons post mortem et les dons d'organes, mais je ne mets pas sur le même plan ces réponses. Enfin, nos collègues vous interrogeront plus en détail.
Pr. Axel KAHN - Merci beaucoup, monsieur le rapporteur, monsieur le président, mesdames, messieurs les sénateurs. D'abord, concernant le texte sur la recherche sur l'embryon voté en première lecture par l'Assemblée nationale, ma première observation est que, de toute façon, une relecture de la loi de 1994 était indispensable. Cette modification se justifie non seulement du fait de l'évolution des techniques, mais également parce que la loi de 1994 n'était pas totalement satisfaisante. En effet, elle se fondait sur l'idée que toute recherche sur l'embryon était interdite mais que certaines études ne nuisant pas à son développement pouvaient être autorisées.
Bien évidemment, la différence entre une recherche et une étude est élusive. La manière simple de raisonner en lisant ce texte était que l'on pouvait mener des études sur l'embryon mais qu'il devait, ensuite, être déposé dans l'utérus d'une femme. D'une certaine manière, le résultat de cette recherche serait visible à l'état de l'enfant tel qu'il naîtrait. Cela était une horreur absolue...
Par conséquent, cette loi devait être réécrite et seules deux positions sont envisageables. La première est que toute recherche sur l'embryon est interdite et la seconde est l'autorisation de la recherche sur l'embryon dans des conditions précises. Il est normal, par conséquent, que le législateur se soit ressaisi de ce texte. Dès 1994, (personnellement ce n'est pas un élément scientifique mais une position morale que je défends depuis huit ans), il m'a semblé que l'interdiction de la recherche sur l'embryon, quel que soit le sentiment quant à la singularité de l'embryon, n'était pas bien fondée. Même en considérant que l'embryon était une personne de pleine humanité, cela n'était pas suffisant pour le disqualifier de toute recherche dès lors que nous menons de la recherche à tous les âges de la vie humaine. Mais on me rétorquait immédiatement, que la recherche sur les personnes humaines n'aboutit pas à la mort du patient, alors que la recherche sur cet embryon conduirait à sa destruction.
Dès lors, se pose le problème de ces embryons surnuméraires. Certains ont proposé, et je le dénie totalement, que dès qu'il ne fait plus l'objet d'un projet parental, il ne soit plus considéré comme un embryon. En effet, à fonder la réalité d'un objet biologique, son humanité potentielle, et à le baser sur la volonté nous pouvons aboutir à des conceptions parfaitement abominables. Nous pourrions tout aussi bien débuter une grossesse que l'on va interrompre à trois ou quatre mois dès lors que la volonté n'est pas de faire naître un enfant mais d'obtenir des organes pour des greffes. Bien évidemment, il faut arriver à une possibilité de définir un objet biologique indépendamment de sa destination. Or, un embryon peut éventuellement se développer pour donner un enfant. Au minimum cette possibilité de transformation en un objet biologique, dont le but de l'éthique est de reconnaître le droit à la dignité, exige la reconnaissance d'une singularité de l'embryon. Elle m'amène à considérer que le législateur a été sage en refusant la création, par quelque procédé, d'embryons pour les détruire. En effet, dès lors que l'embryon serait créé afin de le détruire, plus aucun obstacle réel n'existerait entre cet embryon et une chose aussi utile fut-elle. Cette singularité de l'embryon justifie qu'il ne soit créé que dans l'espoir de faire un enfant, ce qui est le cas de ces embryons surnuméraires.
Cela dit, je vous rappelle, mesdames et messieurs les sénateurs, que lorsqu'un homme et une femme essayent d'avoir un enfant par les procédés les plus traditionnels -mes chiffres peuvent être discutés sur la marge- sur dix embryons conçus, deux ou trois donneront un enfant. La condition normale est que huit sur dix des embryons conçus disparaissent. La situation ne diffère pas tellement des conditions de l'assistance médicale à la procréation où, sur dix embryons créés pour faire un enfant, sept ou huit ne seront pas utilisés dans ce but. Dès lors, leur destruction, ou plutôt leur non-évolution vers une personne humaine, n'est pas le résultat de la recherche mais du fait que, quoique ayant été procréés dans le but de faire un enfant, ils n'ont pas été utilisés pour cela. Dès lors, il y a déconnexion entre la recherche que l'on peut mener et le non-développement vers une personne humaine. Il me semble singulier de considérer que le seul âge de la vie humaine sur lequel nous ne pourrions pas mener de recherche soit l'âge embryonnaire. On ne m'a jamais démontré la lucidité et la sagesse de cette affirmation. C'est donc vraiment une position de principe que je développe depuis 1994.
Est-il utile de faire une recherche sur l'embryon ? Je ne vais pas parler des buts scientifiques même si beaucoup pourraient être poursuivis sur des embryons animaux, de primates notamment. En revanche, si la recherche sur les cellules souches doit être menée, l'utilisation d'un embryon humain et de cellules humaines dérivées de cet embryon est un passage obligatoire. En effet, il n'existe aucune possibilité de prédire les propriétés d'une cellule souche embryonnaire à partir des connaissances acquises grâce aux travaux menés sur une espèce particulière. Ainsi, nous travaillons depuis vingt ans sur les cellules souches embryonnaires de souris que nous maîtrisons parfaitement bien mais nous sommes encore incapables d'établir des cellules souches embryonnaires de rats, espèce de rongeur pourtant proche. De la même manière, la connaissance que nous pourrions acquérir sur des cellules souches embryonnaires de primates serait intéressante mais ne nous permettrait pas d'en prédire des propriétés particulières pour les cellules souche embryonnaires humaines. Donc, si l'on considère la légitimité de cette recherche, cela exigerait de travailler avec des cellules souches embryonnaires prélevées d'embryons humains provenant soit de France, soit d'ailleurs. Alors se poserait le problème de l'importation de cellules souches.
A ce stade, je voudrais livrer un élément de définition important car parfois, quoique certainement pas au sein de cette assemblée très informée, une ambiguïté existe entre la cellule souche embryonnaire et l'embryon. Un embryon est un stade du développement qui, dans des conditions favorables et par lui-même, peut donner un organisme indépendant, un petit bébé dans le cas d'un embryon humain. A ce titre, une cellule souche embryonnaire n'est en aucun cas un embryon humain puisqu'elle est totalement incapable, dans quelque condition que ce soit, de donner un petit bébé. Greffées sur une personne, elles donnent un cancer et certainement pas un petit bébé. En revanche, la cellule souche embryonnaire est prélevée sur un embryon humain. Il est bon d'établir la distinction entre ces deux objets biologiques définis par un qualificatif important et signifiant puisqu'ils sont tous les deux humains.
Maintenant, voyons quelles sont les perspectives de la médecine régénératrice qui pourrait utiliser des cellules souches adultes ou embryonnaires. D'abord, où en sommes-nous de la recherche sur les cellules souches embryonnaires humaines ? Elle est menée dans trois pays et deux sont particulièrement en avance, Israël et la Chine, quoique les publications scientifiques restent rares. En Israël, deux équipes ont réussi, dans des conditions in vitro, à commander à ces cellules souches embryonnaires de devenir du muscle, notamment cardiaque, mais également des cellules hématopoïétiques dont nous ne savons pas si elles pourraient s'établir in vivo après leur transplantation chez un malade ; et aussi, récemment, des cellules vasculaires, appelées cellules endothéliales. Je vous rappelle que ces cellules souches embryonnaires sont prélevées sur un embryon six jours environ après la procréation, à partir de la masse cellulaire interne qui se trouve au fond de la cavité de l'embryon qui, à ce stade, a la forme d'un kyste, d'où son nom de blastocyste.
Nous savons qu'en Chine, les progrès sont importants, cependant aucune publication n'est parue dans une revue scientifique. Ce sont des bruits de couloir et une enquête menée par un journaliste de la grande revue américaine Science , qui nous permettent d'en savoir un peu plus. Une activité très importante semble y être menée quant à la commande à volonté de la différenciation des cellules souches embryonnaires humaines en cellules différenciées et même quant à un, -entre guillemets- clonage thérapeutique, c'est-à-dire la fabrication d'embryons humains par transfert de noyau à partir d'une cellule somatique. Ces cellules souches embryonnaires humaines sont-elles totipotentes ? Ce terme s'applique, par exemple, à une cellule souche embryonnaire de souris qui, ajoutée à l'embryon de souris, peut contribuer à la fabrication de tous les organes de l'animal. Bien évidemment, l'expérience n'a pas été menée chez l'homme. C'est la raison pour laquelle on a pu parler, dans la grande presse, d'êtres hybrides souris-hommes. En effet, certains ont proposé, avec légèreté tant sur le plan moral que scientifique, de rajouter des cellules souches embryonnaires humaines à un embryon de souris et de regarder si elles contribuaient également à la fabrication humanisée, en l'occurrence, des organes de souris. Sans même discuter l'aspect moralement choquant de l'expérience, elle n'est pas raisonnable d'un point de vue scientifique. Effectivement, l'embryon de souris se développe en vingt et un jours et l'embryon humain en neuf mois, si bien que lors de la naissance du souriceau, je ne vois pas à quel stade de développement pourraient se trouver les cellules souches embryonnaires humaines. Cela me permet de vous montrer que nous ne savons pas si les propriétés des cellules souches embryonnaires humaines sont équivalentes à celles des souris que l'on connaît depuis bien plus longtemps.
Aujourd'hui, quelles sont les perspectives thérapeutiques ? Nous savons que ces cellules souches embryonnaires humaines sont difficiles à cultiver mais nous arrivons à maîtriser, petit à petit, ce processus. Nous réussissons de mieux en mieux à commander leur différenciation et, pour le reste, nous sommes obligés de nous fier au résultat chez l'animal. Chez lui, pour résumer, ces cellules souches possèdent un inconvénient majeur. En effet, quand on les transfère avant leur différenciation en cellules de foie, de poumon ou de cerveau, suivant la maladie à soigner, elles sont très cancérigènes. Le seul projet thérapeutique passerait par le contrôle de la transformation de ces cellules embryonnaires en cellules de l'organe à soigner puis, par le transfert de ces cellules, en s'efforçant d'éliminer toutes celles non correctement différenciées. D'autre part, la possibilité in vitro de fabriquer des cellules adultes d'organes capables de fonctionner normalement est très incertaine et varie selon les organes. Des résultats intéressants ont été obtenus, récemment, sur des greffes de cellules neuronales dérivées de cellules embryonnaires de souris sur des modèles animaux de maladie de Parkinson. En revanche, les essais menés pour guérir des diabètes ou pour rétablir le système hématopoïétique, c'est-à-dire les cellules fabriquant le sang, à partir de cellules dérivées de cellules embryonnaires, se sont soldés au mieux par des demi-succès. En effet, les cellules de pancréas sécrétant de l'insuline obtenue à partir de cellules embryonnaires ne produisaient que 2 % de l'insuline fabriquée par les cellules pancréatiques normales. En outre, cette sécrétion de l'insuline disparaissait au bout de quelques mois. De même, sur le système hématopoïétique et immunologique, dans une expérience célèbre et popularisée d'un éminent collègue allemand travaillant aux Etats-Unis, Rudolf Joenisck, le rétablissement immunitaire n'a été que de 2 %.
En résumé, une voie intéressante est à suivre ici. Il faut certainement apprendre à maîtriser la différenciation de ces cellules mais des obstacles importants demeurent, éléments jouant en faveur de la poursuite de la recherche. Bien évidemment, nous sommes très loin de prévoir le moment où les essais cliniques utilisant un tel matériel pourront être menés. Vous avez parlé, monsieur le rapporteur d'un délai de quelques années ou de quelques dizaines d'années. Je ne saurais pas vous répondre. Mais je ne le vois pas à court terme, improbablement à moyen terme et donc plutôt à long terme. L'hypothèse d'une dizaine d'années me semble plus raisonnable que celle de quelques années.
Les cellules souches dites adultes sont de deux types. D'abord existent les cellules siégeant au sein de nos organes et à la réparation desquelles elles contribuent (refabrication du foie, cicatrisation de la peau, rétablissement d'un système sanguin après une hémorragie ou une aplasie médullaire d'un malade soigné pour cancer ou leucémie). Nous les connaissons fort bien et l'utilisation de ces cellules souches caractéristiques d'organes est déjà entrée en clinique (greffe de moelle, de peau, certains essais de greffes de cellules pancréatiques, et même d'hépatocytes pour des maladies du foie). Des milliers de malades ont bénéficié de ce type de thérapie cellulaire. L'autre catégorie de cellules souches existe chez l'adulte et plus généralement dans les organismes différenciés. Nous pouvons en trouver dans le sang de cordon. Ces cellules sont singulières et ressemblent étrangement à celles progénitrices de la couche inférieure de la peau, des tendons, des os et des muscles que l'on appelle les cellules mésenchymateuses. Nous savons que ces dernières peuvent être également les progénitrices des vaisseaux sanguins. Certains ont proposé de les appeler les mésangioblastes, « mé- » comme mésenchymateuses et angioblaste comme les cellules progénitrices des vaisseaux sanguins. Ces cellules ont déjà démontré un intérêt dans deux types d'essais cliniques chez l'homme récemment.
Plusieurs dizaines de malades en Allemagne et en Angleterre ont bénéficié d'un transfert de ces cellules originaires de la moelle pour renforcer et hâter la guérison du coeur affecté par un infarctus du myocarde. Ces résultats, encore très préliminaires, ont été rapportés récemment au dernier congrès international de la pathologie cardio-vasculaire aux Etats-Unis. Des résultats expérimentaux chez l'animal ont également été annoncés récemment quant à l'intérêt de ces cellules pour améliorer les suites d'une attaque cérébrale ou bien de certaines maladies de la rétine. Les perspectives semblent, ici, tout à fait intéressantes. Personnellement les résultats me semblent convaincants mais ils méritent d'être confirmés. Il pourrait même se faire que, dans certaines conditions, ces cellules mésangioblastiques ne se limitent pas à fabriquer des cellules de vaisseaux ou de muscle mais qu'elles soient capables de produire pratiquement toutes les cellules de l'organisme. Je fais référence, ici, entre autres, aux travaux de Catherine Verfaillie.
Aujourd'hui, dans le monde, quatre équipes ont rapporté que ces cellules de type mésangioblastique, d'origines diverses suivant les chercheurs, auraient la capacité d'engendrer des cellules caractéristiques de tous les organes. Certains connaissent des difficultés à obtenir des résultats semblables mais d'autres, au contraire, les confirment. Nous sommes au coeur du domaine de la recherche. En conséquence, nous nous trouvons avec deux ou trois familles de cellules progénitrices. La thérapie cellulaire à partir des cellules progénitrices d'organes est déjà une réalité clinique. Cette dernière accélère le passage à l'essai clinique à partir de ces cellules disposant d'un avantage considérable par rapport aux cellules embryonnaires puisqu'elles ne sont pas cancérigènes. Elles ont un inconvénient s'il s'agit de soigner des maladies dégénératrices de personnes très âgées. Il est probable, voire presque sûr, que l'abondance de ces cellules souches adultes est moins importante chez le grand vieillard qui en aurait le plus besoin. C'est, d'ailleurs, un problème éthique sous-tendant l'activité commerciale des sociétés suggérant de prélever des cellules souches à la naissance de l'enfant parce que, plus tard, il pourrait en avoir besoin.
Sur l'embryon, le dernier point très important se réfère à une possible exception à cette conviction selon laquelle la reconnaissance d'une singularité de l'embryon interdisait d'en créer pour les besoins de la recherche. Mais qu'en est-il de la recherche sur l'infécondité ? Ces dernières années des situations tout à fait anormales ont pu être relevées alors même que M. Huriet et ses collègues avaient très précisément indiqué les conditions dans lesquelles de la recherche sur l'homme pouvait être menée avec la création des CCPPRB. Des faits absolument aberrants ont été rapportés. Un collègue nous a fait part qu'une biopsie testiculaire avait été réalisée chez un homme incapable de produire non seulement des spermatozoïdes mais même leurs précurseurs. Une maturation artificielle de ce bout de testicule par traitement hormonal a été obtenu et des cellules éventuellement fécondantes ont été injectées dans des ovules. Suite à cela, trois enfants seraient nés, quoique l'information soit douteuse. Bien évidemment, les risques pris pour l'enfant sont absolument considérables.
Je ne peux pas entrer dans le détail mais nous savons que le temps nécessaire à la maturation des spermatozoïdes, délai où s'établit ce que l'on appelle le sceau parental, où s'échangent les fragments d'un chromosome à l'autre, est probablement indispensable à la qualité des gamètes. Il se trouve que les conditions dans lesquelles les chercheurs peuvent se lancer dans des essais d'Homme restent peu codifiées. Bien évidemment, il est légitime d'essayer d'améliorer les moyens de lutte contre l'infertilité. Cela passe nécessairement, à un moment donné, par le test du caractère fécondant d'un gamète traité pour améliorer son potentiel de fécondation.
Ces démarches supposent effectivement la création d'embryons à des fins de recherche. Alors, de deux choses l'une, ou bien la recherche n'est pas un succès. Ces embryons n'ont aucune capacité de donner un bébé parce que l'on se rend compte très rapidement qu'ils ont, par exemple, trois jeux de chromosomes ou que, pour une autre raison, ils n'ont aucune possibilité de se développer en petit bébé. Ils ne correspondent alors pas à la définition que j'ai donnée de l'embryon et leur destruction dès lors ne pose aucun problème.
Ou alors, la recherche semble être un succès, c'est-à-dire qu'à la suite d'un traitement pour améliorer le potentiel fécondant de gamètes, un embryon est créé qui commence à se développer, en culture, dans de bonnes conditions. Lorsque cet embryon a quatre cellules, on peut prélever un blastomère et vérifier que son lot chromosomique est normal. Il serait possible que, dans de tels cas, l'embryon ne soit pas détruit et qu'il soit congelé. Et, la science progressant, il pourrait être proposé au couple donneur de gamètes de le recevoir, après l'acquisition d'autres informations sur ses chances de se développer normalement. Cela pourrait constituer une des possibilités pour concilier ce besoin absolu de recherche et la non-création d'embryons humains à des fins uniquement scientifiques.
J'aborde immédiatement le sujet de l'APEGH. Sur la « recherche d'hommes », un CCPPRB doit être mis en place rapidement.
M. Nicolas ABOUT, président - Monsieur le professeur, nous devons rappeler pour tous ceux qui nous écoutent que l'APEGH est l'Agence de la procréation, de l'embryologie et de la génétique humaine.
Pr. Axel KAHN - Cette Agence s'est vu conférer, dans le texte voté en première lecture, différents rôles. Celui d'un CCPPRB pour les recherches de lutte contre l'infécondité est incontestable. Une étude technique jugeant la recevabilité d'un protocole de recherche dont le but est d'améliorer la fécondité d'un couple stérile est nécessaire, mais n'est pas bien organisée aujourd'hui. Une agence créée dans ce but est une absolue nécessité. En revanche, nous pouvons considérer que les autres prérogatives confiées à l'APEGH sont très larges. Elle a également un rôle important dans l'évolution de la considération éthique des problèmes et sa composition ne la prépare pas bien à cette tâche. De l'extérieur, la présence importante des professionnels dans cette Agence pourrait entraîner l'accusation qu'ils sont juge et partie dans l'évaluation du caractère légitime d'une innovation. Je ne serais pas personnellement choqué par une relecture des prérogatives de cette Agence.
Je voudrais maintenant aborder rapidement la brevetabilité, problème d'une extrême difficulté. L'article 12 bis voté en première lecture, si vous me permettez d'être un peu brutal, ne convient pas. Il dit : « Un élément isolé du corps humain ou autrement produit par un procédé technique, y compris la séquence ou la séquence partielle d'un gène ne peut constituer une invention brevetable. » Cet article ne me choque pas mais il est un peu dangereux. En effet, dans l'histoire des biotechnologies, une des premières grandes innovations ayant nécessité une très grande créativité intellectuelle a été de reconnaître l'érythropoïétine, de cloner son gène, de le fabriquer par un procédé technique utilisant l'ADN recombinant et de l'employer en thérapeutique. Est-il anormal de demander, suivant la logique des brevets, que je ne veux pas ici remettre en cause, à ce titre, un brevet sur l'erythropoïétine recombinante ? Je ne le crois pas et si jamais nous devions en arriver à rendre impossible cela, ce serait un obstacle très important à l'évolution des biotechnologies. En revanche, le texte de la loi antérieure me semblait tout à fait correct. Il disait qu'en tant que telle, la connaissance totale ou partielle d'un gène ne pouvait faire l'objet d'un brevet.
J'en arrive aux contradictions entre le nouvel article 12 bis et l'article 5 de la directive 98/44 CE. Selon cette dernière, lorsqu'on a trouvé la fonction d'un gène et qu'il se trouve hors de sa situation naturelle, il peut faire l'objet d'un brevet. De plus, il est ajouté que la revendication d'un brevet sur la séquence du gène en tant que telle est légitime. La loi française, quant à elle, déclarait qu'un brevet dérivé de la séquence du gène peut être légitime, en revanche en tant que telle la connaissance du gène doit rester libre pour pouvoir réaliser tout ce qui n'a pas été prévu par le premier breveté. Cette position est scientifiquement juste. En effet, l'idée selon laquelle un gène n'a qu'une fonction est scientifiquement fausse : un gène a une très grande quantité de fonctions. Un inventeur peut isoler un gène, en trouver une fonction importante, fabriquer un médicament, par exemple une protéine recombinante et demander, à mon avis légitimement, une propriété industrielle sur cette invention. En revanche, qu'il en arrive à considérer que le gène en lui-même, ou la séquence du gène, est un objet brevetable pour toute utilisation possible, même celle dont la plausibilité n'a pas été établie par le premier breveté, n'est pas légitime et me semble contraire à l'intérêt bien compris des biotechnologies.
La situation est difficile, parce qu'en 1998, cette directive a été votée notamment avec l'appui soutenu de la France. Cela ne la met, d'ailleurs, pas dans une position facile lors de ces discussions avec la Commission de Bruxelles pour la renégociation de cette directive. Aujourd'hui, elle n'a été transposée que par six pays et donc pas par les neuf autres, ce qui montre l'extraordinaire réticence des Etats. Parmi ceux n'ayant pas procédé à la transposition, au moins deux sont sur la même longueur d'onde, à savoir l'Allemagne et la France. L'idée selon laquelle cette directive n'est pas bonne me semble aujourd'hui gagner du terrain. Tout travail législatif laissant ouverte la possibilité de préciser la signification ou de réviser la directive me semble extrêmement bénéfique.
Vous m'avez également demandé de m'exprimer sur le transfert d'embryons post mortem . Le Comité d'Ethique en a été saisi et a raisonné de la manière suivante. Une femme décide avec son conjoint d'avoir un enfant, le conjoint meurt. Cette femme, dans un premier temps, n'a pas effectué son deuil et n'a pas une idée très claire de son existence probable si elle décide d'avoir cet enfant. Il faut empêcher, ici, tout acte précipité. Toutes les dispositions doivent également être prises pour permettre à cette femme d'avoir un commerce intellectuel lui permettant de faire son deuil, de comprendre l'intérêt de l'enfant à naître, le sien et d'envisager d'avoir un nouvel enfant de l'amour avec un père vivant. Cela étant dit, malgré tout, la femme peut persévérer dans ce désir que l'embryon soit déposé dans son utérus. Nous en arrivons ici à quelque chose nous rappelant l'eugénisme. Pendant une période, la société a considéré que, dans certains cas, elle en savait assez pour décréter ce que l'on devait faire des embryons de qualité insuffisante pour naître. Nous sommes revenus de cela. Je me méfie beaucoup d'une situation où la société, pour quelque raison que ce soit, considère que son droit sur un embryon est supérieur à celui de la mère. En cas de difficulté, le Comité d'Ethique s'est demandé, qui avait plus de droits que cette femme pour déterminer ce qu'il convenait de faire. En ce sens, je suis favorable au texte tel que voté en première lecture.
M. Francis GIRAUD, rapporteur - Je crois que nous avons tous été très satisfaits de votre exposé. Avant de laisser la parole à nos collègues, je voudrais revenir sur une question précise. Aujourd'hui, combien d'équipes travaillent en France à l'étude des cellules souches adultes ? De quels moyens financiers disposent-elles ?
Pr. Axel KAHN - Je ne vais pas vous donner un chiffre exact, il s'élève certainement à plusieurs dizaines. En revanche, si vous me demandez si ces équipes disposent de moyens financiers suffisants, je vous dirais certainement non. D'ailleurs, je vous dirais également non si vous me demandez si les équipes, à l'heure actuelle, travaillant globalement dans la recherche médicale en France, disposent de moyens suffisants. En outre, la situation s'est aggravée dernièrement, permettez-moi tout de même de le dire. Cela est vrai notamment pour ce qui concerne le travail sur les cellules souches adultes. En revanche, une incitation européenne et nationale, parfaitement légitime est apparue, suggérant une priorité double, scientifique et sanitaire on l'espère, mais aussi un choix politique en faveur de la recherche sur les cellules souches adultes. Nous ne pouvons l'affirmer à ce jour mais s'il s'avère, dans quelques années, que nous pouvons réaliser sur des cellules souches adultes ce que nous pouvons imaginer ne pouvoir faire aujourd'hui que sur des cellules souches embryonnaires, cela serait parfaitement satisfaisant.
M. Jean-Louis LORRAIN - Après un aussi brillant exposé nos questions peuvent apparaître quelque peu simples. Néanmoins nous sommes aussi les vecteurs de nos concitoyens et nous essayons de traduire ce qui les préoccupe. Vous vous êtes largement prononcé sur le clonage reproductif. Y a-t-il une marge aussi large que cela entre le clonage thérapeutique et le clonage reproductif ? Pourriez-vous repréciser l'approche du clonage thérapeutique ? Dans l'opinion publique, se développe la notion de clonage notamment pour la constitution de réserves d'organes. Après avoir décrypté le génome nous voulons savoir comment tout fonctionne mais beaucoup de problèmes apparaissent. Quid des ovocytes ? Comment se les procurer ? D'où viennent-ils ? N'avez-vous pas le sentiment que dans tous les débats auxquels, bien sûr, vous participez, vos collègues adoptent de plus en plus une démarche utilitaire ? Ce discours est bien sûr sous-tendu par les demandes et les souffrances existantes. Nous débordons peut-être ici l'approche du texte, néanmoins j'essayais de vous exprimer une préoccupation forte.
Pr. Axel KAHN - Monsieur le sénateur, je vais répondre à votre question d'abord de manière purement scientifique et médicale en procédant comme nous le faisons habituellement pour juger de l'acceptabilité d'une technique médicale. Les médecins sont forcément utilitaristes puisque le but de leur activité est de minimiser la douleur et d'optimiser les chances de guérison, véritable référence morale de l'utilitarisme. Ce que je dis là ne vaut pas pour toute ma philosophie morale mais un médecin est forcément utilitariste. Cela nous amène, à un moment, à dresser le bilan des avantages et des inconvénients. L'avantage théorique des cellules souches embryonnaires prélevées d'un embryon non point obtenu par procréation mais après transfert de noyau est qu'elles seraient, en pratique, compatibles sur le plan immunologique. Après avoir été transplantées, elles ne seraient pas l'objet d'un rejet de greffe. Cela ne correspond pas, aujourd'hui, à un espoir vraiment important notamment si nous lisons les articles sur le clonage thérapeutique parus dans Science ou Nature ou les écrits des spécialistes du domaine comme Janet Rossant et Roger Pederson. Aujourd'hui, les partisans du clonage thérapeutique sont obligés de le justifier pour des raisons de recherche et non plus par l'urgence d'une utilisation à visée médicale. En effet, imaginons qu'il faille renforcer mon coeur affaibli par un infarctus du myocarde en me greffant des cardiomyocytes différenciés aux dépens de cellules embryonnaires prélevées sur mon embryon jumeau. On m'aurait alors prélevé des cellules de la peau et on se serait procuré probablement des centaines d'ovules. Je dis cela parce que si l'on se réfère au mammifère que l'on connaît le mieux, la souris, la fréquence avec laquelle des lignées de cellules souches embryonnaires sont obtenues à partir d'embryons clonés est de l'ordre de 2 à 3 %. Chez les primates, tout le monde sait que c'est beaucoup plus difficile. Faisons l'hypothèse que nous accomplissions de grands progrès chez les primates et que, dans de nombreuses années, nous acquérions la même technicité que chez la souris. Pour obtenir trois embryons, chiffre peu élevé pour entreprendre une recherche de ce type, chaque malade aurait besoin de 100, 200 ou 300 ovules. A ce stade, je ne me pose pas la question de leur origine. Ensuite, ces ovules seraient énucléés et leur noyau remplacé par un noyau de ces cellules de ma peau. Nous obtiendrions, dans un petit nombre de cas, des blastocystes, nous prélèverions des cellules embryonnaires, et leur commanderions de se transformer en cardiomyocytes, tout en rappelant que l'incertitude sur la fonctionnalité de ces cardiomyocytes reste totale. D'autre part, l'élimination des cellules non différenciées serait également impérative, d'autant plus qu'ici il n'y aurait aucun rejet de cellules, notamment de cellules tumorigènes. Nous en arrivons donc à une technique si lourde, compliquée et incertaine qu'il est impossible aujourd'hui de l'investir de perspectives médicales réalistes. Cela étant dit, si aucun inconvénient n'est relevé, nous pourrions éventuellement mener une telle expérience sur des personnes très riches.
En fait, les éléments négatifs existent et sont de trois types. Le premier, pour ceux qui, et j'ai dit que je n'étais pas loin d'en faire partie, considèrent que la reconnaissance de la singularité de l'embryon requiert de ne pas le fabriquer pour le détruire. Or, dans cet exemple, ce serait le cas. Le deuxième élément est que la nécessité, pour soigner ces malades richissimes et cacochymes de nos pays, de disposer de centaines d'ovules, risque de faciliter l'établissement d'un trafic d'ovules aux dépens de femmes impécunieuses, éventuellement de pays en voie de développement. Le troisième élément se rapproche de M. Antinori, de Mme Boiselier et des raëliens que vous avez évoqués tout à l'heure avec Claude Huriet. Aujourd'hui, ils se vantent mais, comme Claude Huriet, malheureusement, je suis persuadé que naîtront un jour des enfants clonés. Cependant, je ne crois pas qu'ils arriveront dans quelques mois, puisque jusqu'à preuve du contraire, la plupart des gens ayant essayé de fabriquer des embryons clonés humains ou de singes n'y sont pas parvenus. Des progrès techniques, si j'ose appeler cela des progrès, ont été réalisés dans ce domaine à Singapour sur des primates et probablement en Chine sur des embryons humains. Le premier scientifique qui, soi-disant pour les besoins d'un clonage thérapeutique dont l'utilité thérapeutique n'est pas claire, publiera dans une grande revue scientifique la technique « clés en main » pour fabriquer des embryons humains, donnera rapidement et très simplement à M. Antinori et aux raëliens la technique qui leur manque peut-être aujourd'hui pour passer à l'acte. Finalement, l'utilité thérapeutique paraît incertaine et celle pour la recherche possible. Les éléments négatifs me semblent donc, aujourd'hui, l'emporter de loin sur les éléments positifs.
M. Jean CHERIOUX - Monsieur le professeur, j'ai une observation et une question. L'observation est que, contrairement à ce que vous semblez penser, le législateur de 1994 était, surtout, modeste. C'est pourquoi il a pris les positions qui ont été retenues. Je vous rappelle que ce texte portait, en ce qui concerne l'embryon, essentiellement sur la procréation médicalement assistée. L'aspect de l'utilisation de l'embryon était tout à fait secondaire et a été introduit dans le texte uniquement à cause de l'ajout du DPI. C'est la raison pour laquelle, ne voulant pas fermer toute possibilité nous avions retenu la notion d'étude. A partir de cette réflexion vient ma question. Que voulez-vous dire quand vous déclarez mener des recherches sur l'embryon ? Cela signifie-t-il que des études sont menées uniquement sur les cellules de l'embryon, ou peut-on aller jusqu'à cultiver l'embryon et le pousser plus loin dans son développement ? Le législateur est modeste parce qu'il est conscient qu'il va ouvrir la boîte de Pandore et il ne perçoit pas tous les risques. Nous savons que, le jour où la porte est ouverte, c'en est terminé.
Pr. Axel KAHN - Monsieur le rapporteur, tout d'abord, j'ai bien suivi, comme vous le savez, votre discussion parlementaire en 1992-1994. Je connais très bien les conditions dans lesquelles cet article de loi a été écrit. Il n'y avait dans mes propos aucune condamnation. Je remarquais simplement que, naturellement aujourd'hui, ce texte méritait d'être repris. Pour ce qui est de la recherche sur l'embryon, j'appellerai de mes voeux, si jamais les parlementaires choisissent de l'autoriser, que les conditions dans lesquelles elle peut être menée soient clairement précisées. Toute culture d'embryon au-delà d'un stade vraiment à préciser et impératif devra être interdite. Comme je vous l'ai dit, la singularité de cet embryon ne m'échappe point et elle doit commander l'action du législateur. L'utilisation d'un embryon surnuméraire voué à n'être jamais un bébé pour prélever ces cellules dans un but de recherche me semble moralement acceptable et scientifiquement justifiable. En revanche, une expérience de culture expérimentale de l'embryon qui le rapprocherait d'un petit bébé, même de quelques semaines, serait sur le plan moral parfaitement inacceptable.
M. Louis SOUVET - Monsieur le professeur, je ne suis ni médecin, ni chercheur et vous voudrez bien me le pardonner. Je ne pourrais vous poser qu'une question d'ordre purement général. Vous avez parlé de la législation française, j'éviterai de la qualifier en précisant qu'elle est ce qu'elle est. Vous avez cité les exemples de l'Angleterre et de l'Allemagne où des chercheurs ont pu conduire des travaux sur des cellules semble-t-il mésangioblastiques, encore que mes propos peuvent être entachés d'imprécision. Je voudrais savoir si, dans votre esprit, notre pays court un risque de voir ses chercheurs les plus en pointe partir dans d'autres pays où la législation serait plus souple.
Pr. Axel KAHN - Je vous apporterai une réponse en deux temps, monsieur le sénateur. D'abord, je me méfie toujours de ce type d'arguments en permanence proposés. Ils ont tellement servi qu'ils gagneraient à n'être avancés qu'avec discernement. En outre, la raison principale pour laquelle des jeunes scientifiques français partent à l'étranger et ne reviennent pas, n'est pas parce qu'ils ne peuvent pas travailler sur l'embryon mais parce que les carrières en France s'avèrent insuffisamment attractives. L'aide à la recherche est trop faible et, dans bien des pays, les moyens de recherche offerts sont globalement supérieurs à ceux proposés en France. L'argument que vous évoquez peut toutefois être considéré en soi mais je ne crois pas qu'il soit important. Une recherche fondamentale sur le développement embryonnaire peut être menée sur le monde animal, sur les primates. D'autre part, j'appelle de mes voeux une recherche sur la cellule souche embryonnaire humaine. L'hypothèse selon laquelle des légions de chercheurs français se mettent à émigrer parce que l'on ne considère pas légitime de les autoriser à fabriquer des embryons humains clonés me semble tout à fait irréaliste.
M. Nicolas ABOUT, président - Monsieur le professeur, il me reste juste à vous remercier. Nous avons plaisir à vous écouter et ce que vous avez à dire se révèle toujours très intéressant.
C. AUDITION DU PROFESSEUR ARNOLD MUNNICH, CHEF DU SERVICE GÉNÉTIQUE MÉDICALE DE L'HÔPITAL NECKER-ENFANTS MALADES, DIRECTEUR DE RECHERCHE À L'INSTITUT NATIONAL DE LA SANTÉ ET DE LA RECHERCHE MÉDICALE (INSERM)
M. Nicolas ABOUT, président - Monsieur le rapporteur, je vous laisse le soin d'accueillir le Professeur Arnold Munnich et de préciser ce que vous souhaitez qu'il aborde dans son propos liminaire.
M. Francis GIRAUD, rapporteur - Mes chers collègues, nous accueillons ce matin le Professeur Arnold Munnich, pédiatre exerçant à l'hôpital Necker-Enfants malades où il dirige un service de génétique de pointe, le plus important de notre pays. J'ai souhaité que le Professeur Munnich vienne nous entretenir de bioéthique parce que, bien qu'il dispose d'un cursus scientifique de haut niveau, il est avant tout praticien. Il passe sa vie à recevoir des familles et des enfants ayant des infections génétiques et à réaliser du conseil génétique. Il se trouve donc au coeur de ce monde de la souffrance des familles et des enfants. Comment la loi a-t-elle organisé l'administration, si l'on peut dire, de la bioéthique dans notre pays par l'intermédiaire de l'APEGH ? Que pense-t-il de la brevetabilité du corps humain et du transfert d'embryons post mortem ? Ensuite, je l'interrogerai plus spécifiquement, puisqu'il en est l'un des spécialistes, sur les problèmes liés au DPI et au bébé de remplacement ou bébé médicament. Nous allons donc entendre, avec grand plaisir, un praticien de la bioéthique.
Pr. Arnold MUNNICH - Je vous remercie, tout d'abord, de me donner cette occasion de m'exprimer devant vous. Je vais le faire avec beaucoup de modestie, première qualité d'un médecin et d'un scientifique. Pardonnez-moi, dans un premier temps, de resituer ma légitimité, comme M. Giraud vient de le faire. Je ne suis ni un philosophe, ni un élu, mais un praticien et un homme de terrain. A l'aune de cette expérience auprès de nos concitoyens, je suis, d'une certaine manière aujourd'hui, comme vous l'êtes, leur porte-parole puisque je les écoute et les assiste dans leur douloureuse expérience.
Je voudrais énoncer quatre réflexions préliminaires à des niveaux très différents puisque M. Giraud m'en a donné la possibilité. La première est la question de savoir si la science est bonne ou mauvaise. A mon avis, elle n'est pas bonne ou mauvaise, elle est les deux à la fois. La deuxième réflexion porte sur le fait que la science se joue de nous quotidiennement et je vous en donnerai quelques exemples. Je finirai sur des questions plus pratiques me concernant au plus haut point, à savoir l'impact sur nos concitoyens des promesses non tenues, les déceptions des thérapies géniques, les promesses de thérapies cellulaires, l'évocation des cellules de la vie et de l'espoir. J'entrevois pour demain, encore, des paroles non tenues, et il n'y a pas pire souffrance pour un enfant malade que d'avoir cru à l'espoir de la guérison et de vivre, outre la maladie, la déception des promesses non tenues. Enfin, puisque M. Giraud m'y invite, je parlerai de la transgression au sens où j'ai la sensation qu'elle nous guette. Si vous me le permettez, j'exposerai en quelques minutes ces quatre points et, ensuite, j'essaierai de répondre à vos questions très importantes.
M. Henri Atlan écrit « la science n'est pas bonne ou mauvaise mais bonne et mauvaise à la fois ». A mon avis, la dimension nouvelle est son évolution foudroyante qui ne nous donne même pas le temps de réfléchir avec nos valeurs propres à l'impact de ces avancées sur nos conceptions essentielles. De plus, cette accélération fait l'objet, immédiatement, de la mainmise des lois de la concurrence et du marché.
A cela s'ajoute notre difficulté collective à définir le vivant. Jadis, l'âme d'un côté et le corps de l'autre fondaient notre foi. Aujourd'hui, les scientifiques nous disent que cette discontinuité entre le vivant et le non vivant n'existe pas, de sorte qu'il n'est plus possible d'opposer le matériel et le spirituel. Les barrières naturelles ne tiennent plus. Auparavant, une femme qui était inféconde le restait et elle envisageait d'autres procédures, l'adoption ou le renoncement à un projet d'enfant. Aujourd'hui, d'une femme stérile on peut faire une femme féconde. La science, là, me semble bonne. Mais quand nous faisons cela nous produisons des embryons surnuméraires.
Se pose alors le problème des conséquences de notre bonne action, et là, la science peut devenir mauvaise. Nous devons alors construire de nouvelles barrières non plus naturelles mais artificielles, humaines, c'est-à-dire, messieurs les sénateurs, des lois, je l'espère reflets d'une morale, d'une culture et d'une valeur fondamentale de notre société. Nous Français, nous devons les énoncer haut et fort. Je regrette, d'ailleurs, que la présence de la France dans le débat bioéthique international soit si pâle et si discrète. Nous avons, non pas le droit, mais le devoir de dire notre différence.
D'autres pays latins de forte culture judéo-chrétienne (le Portugal, l'Espagne, la Grèce, l'Italie) sont attentifs à notre discours. Nous n'avons pas de raison de nous incliner devant le diktat éthique anglo-saxon et nous avons le devoir d'énoncer notre différence. Il y a quelques jours, j'ai été envoyé par notre directeur général de l'INSERM, Christian Bréchot, en compagnie de notre président du comité d'éthique, Didier Sicard, au Bundestag. Ces députés et ministres allemands m'ont demandé de leur parler de ce qu'ils ont appelé « die französisch model », le modèle français. Je leur ai demandé pourquoi ils nous faisaient l'honneur de parler de modèle français. Ils m'ont répondu qu'ils savaient que nous disposions d'une éthique à la française. Cela les intéressait dans leur pays traumatisé par l'histoire et à la veille d'édicter des lois de bioéthique. Ils souhaitaient connaître nos pratiques, nos pensées, nos convictions, nos certitudes et nos références. Cela m'a fait très plaisir que des collègues allemands en appellent à la position de la France et je me suis dit que, plus que jamais, nous devions articuler haut et fort notre différence.
Le deuxième point concerne le point de vue du scientifique. Là encore, je ferai preuve d'une grande modestie parce que la conception d'une science triomphante me paraît particulièrement déplacée. Nous n'avons aucune raison de faire preuve de triomphalisme, à cause d'un certain nombre d'échecs, encore tout récemment dans notre espoir majeur de traitement des maladies génétiques. Des moratoires s'imposent. Il suffit de regarder en arrière pour s'apercevoir que la science brouille les cartes à chaque instant, et change à tout moment les termes du problème tel qu'il se pose à la société et au législateur.
Je vais vous donner quelques exemples pour vous dire notre difficulté et donc la vôtre. En science, nous sommes habités par des dogmes. L'histoire du prion en constitue un parmi beaucoup d'autres. Jamais nous n'avions imaginé qu'un agent pathogène pourrait n'être pas un être vivant et qu'un être vivant pourrait ne pas être doté d'une molécule d'ADN. Le prion nous est apparu comme un véritable bouleversement puisque nous sommes en présence d'une molécule infectieuse qui n'est pas de l'ADN. C'est un dogme qui s'effondre. Nous pourrions parler longtemps de tous ces dogmes ayant habité l'histoire de la pensée humaine scientifique et qui se sont écroulés les uns après les autres. Je suis personnellement associé, en tant que scientifique du diagnostic prénatal, à un autre exemple : celui des cellules foetales circulant dans le sang maternel. Dans ce cas, la science, ou plutôt la technologie, brouille les cartes. En effet, nous possédons de bonnes lois mais la technologie, en nous apprenant que circulent dans le sang de la mère des cellules foetales pouvant être prélevées par une simple prise de sang, à quelques semaines, bien avant le terme de l'IVG, tout notre édifice législatif se trouve ébranlé. Il y a également cette possibilité de faire un être vivant avec un noyau et une cellule somatique alors que personne n'aurait pu l'imaginer. Mais cet être vivant, doté d'un noyau et d'une cellule somatique, s'appelle-t-il un embryon ?
Le troisième point sur lequel je voudrais insister nous ramène sur terre. C'est la question des promesses non tenues et de l'impact des progrès de la science sur nos concitoyens. Nous ne pouvons pas promettre impunément, dans les médias, les discours scientifiques, pour demain la guérison sans en avoir un jour à en rendre compte. D'ailleurs, nous avons aujourd'hui à rendre des comptes. Nous ne disposons toujours pas de thérapie génique, médicamenteuse ou cellulaire pour la mucoviscidose ou la myopathie de Duchêne alors que nous avons identifié les gènes, il y a quinze ou vingt ans. Les promesses de thérapie cellulaire devraient être envisagées à l'aune de cette expérience. Les scientifiques doivent se souvenir des espoirs déçus suscités auprès de nos enfants malades. C'est un premier coup terrible pour des enfants ou des parents d'avoir une maladie génétique, c'en est un second d'expérimenter la déception d'une promesse non tenue.
Je voudrais finir mon exposé liminaire en vous parlant de la transgression. Je ne pense pas que l'on passe du bien au mal d'une seconde à l'autre, c'est par touches successives que nous en arrivons au drame. L'histoire récente nous rappelle que ce n'est pas au lendemain de l'élection du Führer qu'il y a eu Auschwitz. Pardonnez-moi, il n'y a rien de comparable. En fait, la transgression avance petit à petit et chaque disposition peut avoir un prix qui se révélera très cher dans quelque temps.
Quelles réflexions m'inspirent les dispositions du projet de loi relatives à l'ouverture de la recherche sur l'embryon ? Que pensez-vous de la possibilité offerte par le projet de loi de créer des embryons afin d'évaluer préalablement de nouvelles techniques d'assistance médicale à la procréation ?
Je répondrai à ces deux questions en même temps. Je voudrais me référer, à titre liminaire, au projet de loi, aux articles L. 2151-2 et L. 2151-3, « la conception in vitro d'embryons humains à des fins de recherche est interdite sans préjudice des dispositions prévues par l'article » et « Est autorisée la recherche menée sur l'embryon humain et les cellules embryonnaires qui s'inscrit dans une finalité médicale . » Je crois que ces deux dispositions doivent être discutées parce qu'elles peuvent paraître opposées. En effet, je ne vois pas comment nous pouvons mener une recherche à finalité médicale sans mener, préalablement, une recherche scientifique permettant d'évaluer nos pratiques. Par conséquent, dans la perspective d'un projet médical, je souhaite que la loi nous autorise d'avancer dans nos pratiques car il s'agit de rien moins que d'évaluer ces procédures nouvelles.
Je voudrais prendre, ici, un contre-exemple, au motif que nous n'avions pas cette possibilité réglementaire, il y a quelques années. Une des techniques de procréation médicalement assistée, l'injection intracytoplasmique de sperme est passée dans la pratique sans aucune évaluation préalable. Par conséquent, nous surveillons les enfants nés de ces pratiques avec anxiété. Pour n'avoir pas mené ces études préalables sur l'enfant fécondé in vitro , nous nous exposons à connaître demain des complications non plus chez des embryons mais chez des enfants nés ainsi. Par conséquent, toujours dans la perspective d'un projet médical, un certain élargissement des dispositions réglementaires est nécessaire, y compris la possibilité de créer des embryons dans le but d'évaluer ces nouvelles pratiques de PMA. Sinon nous risquons de nous réveiller demain avec de très mauvaises surprises.
Dans le cadre d'un projet médical, qu'il s'agisse d'ICSI ou d'autres pratiques, j'éprouve le besoin d'être autorisé à un certain élargissement de nos pratiques. Je vais prendre l'exemple, car j'en suis l'un des praticiens, des maladies dites mitochondriales, maladies portées par des mères qui les transmettent à tous leurs enfants sans distinction de sexe. Des générations entières sont décimées par ces maladies très fréquentes. La seule possibilité d'aider ces couples à avoir des enfants indemnes est d'évaluer comment s'opère la ségrégation ultra précoce, dans l'ovule fécondé in vitro d'une mère à risque, de ces mitochondries portant les gènes malades.
Sans avoir mené ces études préalables, je ne me lancerais pas dans un diagnostic génétique préimplantatoire car je n'aurais pas entre les mains les éléments nécessaires me permettant d'avancer avec précaution. Donc, l'interdiction de l'étude de l'embryon fécondé in vitro même dans un projet médical, conduit des milliers de femmes à se résoudre à la douleur de ne jamais avoir d'enfant. Par conséquent, dans un certain nombre de cas médicalement parfaitement identifiés, un certain élargissement de la loi s'impose pour que nous puissions faire avancer nos pratiques sans risque pour les mères et pour leur descendance.
Quant aux chances de thérapies cellulaires à court terme, je ne peux que partager avec M. Kahn mon scepticisme. Je ne les vois pas pour demain, par contre je connais l'existence de thérapies sur des cellules souches adultes qui me posent beaucoup moins de problèmes. De nombreuses études sont menées sur ce type de cellules (cellules médullaires, cardiomyocytes, myoblastes). Ces recherches, naturellement, ne me posent aucun problème personnel éthique car le don, en l'occurrence, ne compromet pas l'existence du donneur. Ce n'est pas le cas avec les embryons surnuméraires pour lesquels se pose le problème du sacrifice d'une vie biologique d'un donneur potentiel pour un receveur. Si nous y réfléchissons bien, il s'agit du seul cas de la médecine où un donneur fait le sacrifice de son existence biologique au bénéfice d'un receveur. A ce titre, je suis très attentif et plein d'espoir quant aux thérapies cellulaires sur des cellules souches adultes. Nous pourrions peut-être attendre l'avancée des travaux dans ce domaine avant d'aborder un autre problème.
Je suis totalement incompétent sur le point numéro deux et, si vous me permettez, je vais le sauter pour vous dire un mot sur le troisième point à propos de la non brevetabilité du corps humain.
Quelles réflexions vous inspire l'article 12 bis qui prend l'exact contre-pied de la directive européenne de 1998 ? Au risque de heurter certains, je pense qu'une certaine brevetabilité se défend. Il faut bien distinguer une découverte d'une invention et si l'on peut breveter une invention cela ne doit pas être possible pour une découverte. Je veux dire que nous pourrions envisager de breveter les applications de l'identification du gène. Cependant, il n'est pas question de breveter des gènes, le génome ou le vivant. Par contre, breveter les applications de la découverte de gènes me paraît licite.
J'aurais mauvaise grâce à vous dire le contraire, ou à signer des pétitions car mes collaborateurs et moi-même avons breveté la vingtaine de gènes responsables de maladies génétiques et de handicaps sévères dont nous avons fait la découverte. Quand l'incidence de la maladie et les perspectives thérapeutiques paraissaient légitimes à l'organisme, l'INSERM a pris des brevets sur la découverte de ces gènes. Donc, je ne peux pas, en même temps, prendre des brevets sur les gènes que je découvre et signer une pétition me déclarant contre le brevetage du vivant.
Je voudrais, si vous le voulez bien, en arriver au don d'organes et ensuite terminer en parlant de notre exercice du DPI et donc à vous dire quelques mots sur la transgression. Je pense que le don d'organes est quelque chose de merveilleux. Je vois bien les risques encourus en culpabilisant un donneur potentiel ne faisant pas le choix d'un don. Je comprends très bien et j'imagine la difficulté pour un frère ou une soeur de décliner la demande d'un don d'organe dès lors que son germain est en danger de mort. Je mesure parfaitement les difficultés résultant d'un don par un sujet en relation étroite et stable, puisque c'est le terme de la question, avec le receveur potentiel. Il n'en reste pas moins que c'est une merveille de pouvoir sauver son frère ou sa soeur et c'est une avancée fantastique que de pouvoir le faire.
Ceci me sert de transition pour vous parler de l'expérience de René Frydman et moi-même à Béclère et de mon collègue et ami Nisand à Strasbourg, en matière de diagnostic génétique préimplantatoire. Je vais vous livrer ma perception sur les demandes relatives à ce que l'on appelle, en de très mauvais termes, « l' enfant médicament », ce qui me heurte énormément. Beaucoup d'émotion a été soulevée autour du DPI et je voudrais témoigner après deux années d'activité de ces pratiques.
Après avoir vu 300 couples en consultation avec René Frydman, je n'ai pas eu la sensation, une seule fois, d'un dérapage de notre part. J'ai eu au contraire, à tout moment, la sensation d'un souci constant de bonne pratique tant de la part du corps médical que de la part des demandeurs. Les Français ne sont pas des personnes fantaisistes. Nous avons eu, dans l'immense majorité des cas, des demandes parfaitement légitimes. J'ajoute une information très importante à mon sens.
Lors de ces 300 consultations de DPI, nous avons pris le temps de délivrer aux couples des connaissances que, bien souvent, ils n'avaient jamais entendues. En effet, en amont de la consultation de DPI, il n'y avait pas eu de consultation de génétique correcte. Après avoir été informés des alternatives, des bonnes pratiques, des conditions d'exercice du diagnostic prénatal, de sexe ou de possibilités thérapeutiques, 100 des 300 couples demandeurs ont opté pour une fécondation naturelle.
C'est une information importante à relever que dès lors que nos patients sont correctement informés, ils peuvent faire un choix éclairé et, souvent, ils optent pour une grossesse naturelle sous couvert du diagnostic prénatal ou en y renonçant même parfois.
Dans un certain nombre de cas, nous avons été confrontés à des demandes concernant effectivement le DPI d'une maladie génétique, l'anémie de Fanconie, assortie d'une demande d'HLA compatibilité dans la perspective d'un don de moelle ou de cordon dans l'éventualité où le premier enfant malade développerait une rechute de sa leucémie. En face de moi, les parents ont fait preuve d'une très grande maturité, d'un très grand sens des responsabilités et ne m'ont à aucun moment donné l'impression d'être des fous furieux.
Je souhaite que les dispositions réglementaires nous autorisent à faire, non seulement le diagnostic génétique préimplantatoire de l'anémie de Fanconie, mais également à identifier parmi les embryons ceux susceptibles de devenir des enfants potentiellement donneurs de sang, de cordon ou de moelle pour aider un aîné leucémique. Cette disposition va dans le bon sens. Que l'on ne me dise pas que l'enfant va être asservi à un quelconque projet d'instrumentalisation. Pensez une seconde à ce qui attend l'enfant à naître s'il n'est pas un donneur compatible et s'il survit à son germain décédé alors qu'il aurait pu être son sauveur ! Nous sommes plus ou moins les thérapeutes de nos frères et soeurs, comme disent les psychanalystes. Au fond, je suis persuadé que l'on ne peut pas être mieux accueilli dans une famille que lorsque l'on a sauvé, en arrivant à la vie, son frère ou sa soeur. Je crois que cet enfant, loin d'être mal reçu, ne sera pas instrumentalisé. Il serait réductionniste de le considérer comme un enfant médicament, c'est plutôt un enfant sauveur, un petit « Messie ». Nous devons surtout garder les pieds sur terre puisque ces demandes sont rares. Ne nous agitons pas pour des problèmes devant s'arbitrer dans l'intimité du dialogue singulier.
Mon problème, et je finirai par là, est bien plus délicat et douloureux lorsque des couples, dont un premier enfant présente une hémopathie maligne avec une deuxième ou troisième rechute, viennent réclamer l'assistance de la PMA pour identifier l'embryon potentiellement sauveur de son frère ou de sa soeur.
Dans ce contexte particulier, nous sommes hors la loi. Or, il n'y a pas de risques pour l'embryon à naître lorsqu'il s'agit d'utiliser la PMA ou la HLA compatibilité. Pourtant, c'est un premier accrochage à l'esprit de la loi. C'est très difficile de dire non, croyez moi. Nous ne pouvons pas dire oui, c'est très douloureux de dire non. Dans le dialogue singulier, je vous le confesse, j'ai eu la faiblesse, monsieur le sénateur, collègue et praticien, de donner des adresses à l'étranger aux couples me demandant de recourir à la PMA. Nous ne pouvons pas rester indifférents à la souffrance de couples en larmes. Alors, je ne me suis pas cru autorisé à me substituer au Créateur et à leur dire non. Je n'ai dit ni oui, ni non, j'ai donné une adresse.
Le problème va être de plus en plus délicat à mesure que les techniques de PMA se répandent. En effet, vous savez que 10 % des couples sont inféconds en France, donc les demandes de PMA sont très nombreuses. Nous avons de plus en plus de situations où nous sommes à l'intersection entre une demande de PMA pour une infécondité et pour un petit problème génétique, qui, dans d'autres circonstances, n'aurait pas fait l'objet d'un DPN. Je veux parler d'infections qui ne sont pas incurables au moment du diagnostic (maladie de Charcot Marie, facioscapulomirale, etc). Des couples nous disent : « Nous sommes un couple infécond et nous allons procéder à une fécondation in vitro. Lorsque vous aurez les embryons devant vous, vous pourrez en profiter pour identifier celui atteint de l'infection puisque vous savez le faire. » C'est là, précisément, que commence la glissade.
M. Nicolas ABOUT, président - Merci beaucoup, monsieur le professeur, en particulier pour la profondeur et la sincérité de vos propos. En effet, nous concevons de telles auditions uniquement de cette manière. Vous devez nous apporter ce que nous ne percevons pas véritablement et ce que vous avez évoqué tout à la fin est, bien évidemment, un problème de frontière. Je vais donner la parole à Jean-Louis Lorrain.
M. Jean-Louis LORRAIN - Dans le cadre d'une interrogation comme la nôtre, souvent faite de simplicité et de sérénité, je dois vous dire que la vie se présente autrement, en particulier sur le plan médiatique. Hier soir au vingt heures de France 2, quelques fractions de minutes ont été consacrées au DPI, présenté comme accepté et faisant l'objet d'une pratique par le comité national d'éthique. J'ai été très surpris. On a présenté une famille en détresse demandant une sélection pour une maladie de Duchêne, qui appartient à une grande liste de maladies pouvant être dépistées. En même temps, on nous présente en amalgame, l'enfant médicament, ce qui vous fait horreur.
Bien sûr, nous ne devons pas nous arrêter à cette présentation médiatique. Quel est le devenir des demandes qui vont apparaître ? L'intérêt du DPI consiste, c'est vrai, à éviter des avortements thérapeutiques en cours de grossesse. Nous sommes tout à fait d'accord là-dessus mais les perspectives sont tout à fait inquiétantes. Que va-t-on faire des embryons sains mais non compatibles avec l'enfant nécessitant une thérapeutique ? Le DPI n'est-il pas une arme très dangereuse qui, au quotidien, nous met dans des situations d'interrogation excessivement douloureuses ?
Pr. Arnold MUNNICH - Ma réponse sera technique, monsieur. Lors d'une fécondation in vitro pour un diagnostic génétique préimplantatoire, nous rompons la coque de l'embryon et prélevons une ou deux cellules. Une fois cette coque rompue, les possibilités de conservation et de décongélation à d'autres fins sont très réduites. Donc, nous compromettons bien plus gravement l'utilisation d'embryons surnuméraires par le DPI que par la PMA. Nous sommes, pratiquement, incapables de faire repartir le développement d'un embryon sur lequel nous avons prélevé quelques cellules. Le risque, à mon avis, avec ces embryons est quasi nul et bien inférieur au danger de dérive avec les embryons surnuméraires dans les projets de PMA. Le DPI est moins compliqué au regard de l'embryon surnuméraire que la PMA traditionnelle. En effet, pour des raisons techniques, nous ne pouvons pas congeler un embryon à qui on a pris deux cellules. C'est un faux problème scientifique.
M. Jean CHERIOUX - Cette réponse m'inquiète. Tout à l'heure, vous avez fait part de votre impossibilité, sur le plan juridique, à procéder à certaines études sur des embryons que vous demandaient les parents, avant de faire un DPI. Vous avez cité un certain nombre d'exemples de parents venant vous voir pour une étude que vous ne pouvez pas réaliser.
Pr. Arnold MUNNICH - Je ne peux pas les réaliser au motif que je ne suis pas autorisé à faire des recherches de faisabilité sur l'embryon fécondé in vitro . Nous ne pouvons pas mener de recherche pour évaluer la pratique médicale.
M. Jean CHERIOUX - Dans le texte de 1994, il est précisé qu'à titre exceptionnel l'homme et la femme formant le couple peuvent accepter que soient menées des études sur leur embryon. Celles-ci ne peuvent-elles pas aboutir, justement, à l'implantation, après, de cet embryon ?
Pr. Arnold MUNNICH - Vous voulez dire que nous pourrions déjà pratiquer ces études ?
M. Jean CHERIOUX - J'étais rapporteur du texte et c'est pour cela que je vous pose la question. L'article L. 152-8 parle de l'interdiction de la recherche et de l'implantation, et précise qu'à titre exceptionnel l'homme et la femme formant le couple, peuvent accepter que soient menées des études sur leur embryon. Ces dernières, telles que prévues dans les textes actuels, répondraient-elles aux souhaits que vous avez formulés ?
Pr. Arnold MUNNICH - Tout à fait.
M. Jean CHERIOUX - Ce texte n'était donc pas totalement inutile.
Pr. Arnold MUNNICH - Vous voulez dire que c'est réglementairement possible dès à présent. Lorsque nous en avions discuté entre nous, nous avions la sensation que c'était hors du cadre de la loi.
M. Nicolas ABOUT, président - Il faut l'autorisation du couple.
M. Jean CHERIOUX - Exactement, mais cela répond à un souci important dans la démarche de M. le Professeur.
M. Nicolas ABOUT, président - Oui, mais cela ne répond peut-être pas au cas, cité par le Professeur, d'un couple ayant un enfant présentant une hémopathie maligne et qui voulait opérer un tri sur le second.
M. André LARDEUX - Merci, monsieur le professeur, de votre témoignage qui était très intéressant. Je vous poserai une question sémantique. Vous avez évoqué l'article L. 2151-3 qui a provoqué des discussions en commission à l'Assemblée nationale. Quelle différence faites-vous entre « finalité médicale » et « finalité thérapeutique » ? Les termes « finalité médicale » sont extrêmement larges, ceux de « finalité thérapeutique » sont par contre très restreints.
Pr. Arnold MUNNICH - Dans le sens où je l'entends, il s'agit de mener des recherches pour répondre à la demande d'un couple pour un projet d'enfant et non pas d'asservir l'embryon à un projet de thérapie. Est-ce le sens de votre question ? Dans le sens où je lis cet article, il s'agit d'optimiser les pratiques médicales, pour répondre à la demande d'un couple à risque pour une maladie génétique d'une particulière gravité. C'est un problème de diagnostic, et non thérapeutique.
M. André LARDEUX - Cela suppose que le législateur soit vigilant sur les termes et leurs positions dans le texte du projet de loi.
M. Nicolas ABOUT, président - Nous aurons certainement à réécrire le texte en essayant de soutenir la position du législateur de 1994 et d'adapter le texte de l'Assemblée nationale à ce qui a été dit.
M. Gilbert BARBIER - Monsieur le professeur, vos propos liminaires nous interpellent. Lorsque vous évoquez le problème de l'éthique à la française, cela signifie qu'elle serait définie par le législateur français. Votre propos veut-il dire que le législateur français doit ou peut précéder le scientifique ? C'est la question de base qu'il faut se poser. Cette loi à la française que vous développez doit-elle émaner de notre morale ? La morale française doit-elle être unique ? Si nous nous engageons dans cette discussion, nous allons très rapidement tomber dans l'ordre moral ou la pensée unique. Je trouve vos propos très en retrait par rapport au scientifique que vous êtes. La question est simple, devons-nous vous précéder ou vous suivre ? C'est peut-être de la philosophie plus que de la science.
M. Nicolas ABOUT, président - Monsieur le professeur, l'éthique se rapporte-t-elle aux limites que la société donne à sa propre liberté ou à celles que les scientifiques donnent à la leur ?
Pr. Arnold MUNNICH - Je ne voulais pas heurter. Il ne s'agit pas de faire preuve de sentiment nationaliste mais une loi est le reflet d'une culture nationale et régionale. Autour de toutes ces pratiques, une forte inspiration judéo-chrétienne et un courant de pensée latin, je ne vous apprends rien, se distinguent du monde anglo-saxon inspiré par d'autres valeurs. Donc, en parlant sous votre contrôle, une loi est l'expression de la culture d'un peuple et de la sensibilité d'un pays. Par conséquent, elle ne précède ni ne suit. Il n'est pas question de courir derrière ou de précéder mais de cheminer de concert.
Votre question me surprend puisque vous n'êtes pas sans savoir que les positionnements diffèrent sur ces pratiques selon les pays qui n'ont, pour certains, pas même de loi. La France a souhaité voter une loi, c'est une très bonne chose, c'est l'expression de la sensibilité, de la culture et des valeurs d'un peuple. Et Dieu sait que la France a apporté des valeurs fondamentales à l'Humanité toute entière depuis 1789 et peut-être même avant. Ne sommes-nous pas, là encore, à un moment névralgique, où nous devons affirmer notre différence et l'articuler courageusement, quitte à prendre des coups ?
M. Nicolas ABOUT, président - Merci beaucoup, monsieur le professeur. Toutefois notre culture judéo-chrétienne et notre histoire gréco-latine nous laissent en matière d'éthique, quelquefois plus de questions que de réponses. Prenons l'Antiquité, par exemple, pendant laquelle, les êtres étaient traités d'une drôle de façon lorsqu'ils n'étaient pas tout à fait conformes aux souhaits. Nous ne rappellerons pas Sparte.
Mme Michelle DEMESSINE - Monsieur le professeur, je voudrais d'abord vous remercier d'avoir pris le temps de nous faire un préambule philosophique. Je pense que, revenir au fond d'une pensée pour pouvoir aborder des problèmes extrêmement complexes, nous aide vraiment.
J'ai été très intéressée par votre expérience sur le DPI et sur les 300 couples. J'avais participé en 1994 au débat sur la loi de la bioéthique. Nous avions alors pris notre décision en notre âme et conscience. En l'absence d'expérience nous nous basons sur notre opinion propre et notre sensibilité, même si nous sommes des citoyens responsables parce que nous sommes des élus. Cette expérience de vécu est extrêmement importante puisqu'elle relativise aussi notre propre pensée.
Vous avez développé ce qui arrive dans la réalité à propos de l'enfant sauveur. Ce problème nous interpelle beaucoup d'abord pour l'enfant sauveur lui-même, même si c'est une question moins grave que celle de celui qu'il va sauver. Nous lui conférons une tâche culturellement nouvelle qu'il lui faudra assumer. On ne peut pas concevoir un enfant dans un but différent du but habituel. Je voudrais également avoir une indication de la réussite médicale dans ce domaine. L'enfant sauveur sauve-t-il toujours son frère ou sa soeur ? J'écoutais, tout à l'heure, l'interrogation de mon collègue Lorrain au sujet du DPI. Dans ce cas, nous ne sommes pas dans le cadre de l'eugénisme, il y a un consensus dans notre pays là-dessus. De plus, vous avez bien montré notre obligation de nous donner un degré dans la souffrance. Cependant, il est extrêmement difficile à évaluer. La souffrance est, j'imagine, immense, pour chaque famille, même celles avec un antécédent génétique que vous estimez faible. Pouvons-nous instituer, par rapport à l'utilisation du DPI, un degré pour une souffrance acceptable ?
Pr. Arnold MUNNICH - Le taux de succès du DPI est faible. Les chances de développer une grossesse après ces pratiques sont de 20 à 25 %. Nous avons eu 30 couples sur 150 qui ont donné naissance à un enfant dans les deux dernières années à Béclère. Les chances qu'un enfant, un peu identique à son germain atteint de faconie, puisse lui sauver l'existence sont énormes dès lors que l'HLA compatibilité est parfaite ;c'est le donneur parfaitement compatible, l'équivalent d'un jumeau au plan de l'immunité.
Je suis très sensible à ce que vous avez dit à propos du degré de la souffrance. Personne n'a qualité pour dire qui souffre beaucoup ou pas. D'ailleurs, le législateur s'est montré extrêmement prudent en ne dressant pas la liste des affections éligibles du DPN ou du DPI. Vous avez décidé, en conscience, et vous nous avez fait confiance. Je pense qu'aujourd'hui la représentation nationale peut légitimement en être fière. Il n'est donc pas question de lister des indications du DPN ou du DPI. Nous ne pouvons pas décider qui souffre et évaluer cette souffrance. Je connais des couples qui ont gardé des enfants avec des maladies très graves et d'autres qui n'ont pas pu supporter un risque me paraissant faible. Je me souviens d'avoir reçu, un jour, un monsieur pour une paraplégie spastique. Je lui faisais la morale de manière maladroite, en lui disant qu'il avait 45 ans, deux enfants splendides, une position professionnelle remarquable, une femme charmante. Je lui demandais alors la raison de sa demande de DPN pour un handicap qui me paraissait compatible avec une existence d'une très bonne qualité. Il m'a tout de suite interrompu en me faisant remarquer que ce n'était pas moi qui vivais le handicap, mais lui. Par conséquent, je suis très sensible à vos propos. L'appréciation de la souffrance d'un couple relève de la mission médicale et de la décision intervenant dans le dialogue singulier.
C'est pourquoi je voudrais disposer de deux minutes, à la fin, pour passer quelques messages hors de l'ordre du jour de cette réunion, notamment pour souligner l'importance du dialogue singulier. Il faut redonner à toutes ces pratiques leur dimension médicale. Nous ne sommes pas des apprentis sorciers mais dans un projet médical d'assistance à un couple ou à des enfants en souffrance.
M. Nicolas ABOUT, président - Vous avez, monsieur le professeur, les deux minutes que vous souhaitiez pour conclure.
Pr. Arnold MUNNICH - Je voulais attirer votre attention sur deux problèmes au-delà des sujets de la plus grande importance sur le plan des principes dont nous avons parlé.
Je voudrais évoquer un enjeu majeur pour un grand nombre de citoyens, qui est l'exercice de la pratique des tests génétiques selon la loi du 4 février 1995 dont, vous vous souvenez qu'elle est bonne. Des décrets encadrent effectivement les tests génétiques, mais cinq ans après leur promulgation, ils n'ont pas été accompagnés des circulaires devant mettre en application les règles de bonne pratique. Ce problème concerne, non la poignée de couples concernés par les maladies dont nous avons discuté, mais des centaines de milliers de Français. Les conditions réglementaires des tests génétiques restent d'un flou total et nous sommes à la veille d'une dérive retentissante. Nous ne savons pas qui prescrit le test, comment il est pratiqué, rendu, et si une consultation génétique intervient préalablement à la prescription. Des catastrophes arrivent dans la mesure où, en France, des résultats d'examens prescrits à la légère, parfois par téléphone, sont rendus par courrier sans être accompagnés de la moindre explication. Ils sont transmis par le médecin généraliste, qui n'y connaît rien, à des patients qui comprennent encore moins. S'agissant d'un grand nombre des Français, j'appelle votre attention sur la nécessité de publier des circulaires d'application de ces dispositions réglementaires.
Le deuxième problème relève du secret médical au regard du statut génétique des sujets. Nous avons, encore tout récemment, été confrontés à des difficultés liées à ce secret. Ces maladies ne sont pas seulement celle d'un individu, elles éclaboussent toute la famille. Au regard du droit, le respect de la vie privée des gens l'emporte sur l'assistance à personne en danger. Il n'est malheureusement pas exceptionnel, j'en ai fait la douloureuse expérience samedi dernier, qu'une mésentente intrafamiliale aboutisse à la maladie et à la mort de plusieurs enfants apparentés éloignés. Lorsque nous nous retournons vers les personnes qui auraient pu, ou dû, prévenir leurs apparentés, elles se retranchent derrière le respect de la vie privée et du secret médical. J'attire donc votre attention sur le fait -nous y avons été confrontés avec la contamination intraconjugale dans le SIDA- que ce problème réglementaire est extraordinairement douloureux. Le législateur pourrait envisager une disposition selon laquelle, lorsque la vie des apparentés est en danger, une obligation est formulée d'aller au-devant des personnes à risque.
M. Nicolas ABOUT, président - Monsieur le professeur, merci beaucoup. Vous avez certainement contribué à faire avancer la réflexion sur tous ces sujets délicats.
D. AUDITION DU PROFESSEUR ISRAËL NISAND, CHEF DE SERVICE DE GYNÉCOLOGIE-OBSTÉTRIQUE AU SIHCUS-CMCO DE STRASBOURG
M. Francis GIRAUD, rapporteur - Monsieur le président, mes chers collègues, tout le monde connaît le Professeur Israël Nisand qui a joué un rôle très important dans différents dispositifs législatifs. Il possède, lui aussi, une expérience de praticien dans le domaine de la PMA et de tous les sujets s'y attachant. Ayant assisté ce matin à nos débats, il connaît les questions qui nous intéressent. Il y répondra à la lumière de son expérience.
M. Nicolas ABOUT, président - Monsieur le professeur, je vous accueille aussi avec grand plaisir.
Pr. Israël NISAND - Monsieur le président, Monsieur le rapporteur, je vais également faire usage de modestie. En effet, j'ai dû remanier totalement mon propos au fur et à mesure de l'écoute des orateurs précédents. Je souscris en effet totalement aux discours tenus par les Professeurs Huriet, Kahn et Munnich. Je tenterai cependant d'apporter quelques réponses personnelles aux questions que vous me posez, Monsieur le rapporteur.
D'entrée de jeu, il me semble indispensable de rappeler qu'un expert n'est jamais neutre, surtout dans le domaine de la bioéthique. Je n'échappe pas à cette contamination par mes propres valeurs. Ce serait en effet prétentieux de ma part que de dire que les propos que je vais tenir émanent exclusivement d'une analyse d'expert. Personne ne peut sortir de l'ambiguïté qui provient de l'éclairage que l'on obtient à la lueur de ses propres valeurs. Mes valeurs, ma culture et mon histoire interfèrent donc avec la position que je vais exprimer devant vous.
La deuxième difficulté à laquelle toute la société française est confrontée, est le problème de la contemporanéité (ici imposée) entre l'avancement du droit et l'avancement de la science. Jamais la situation n'a été aussi critique de ce point de vue. En effet, habituellement le droit peut prendre de la distance par rapport aux événements et éviter la difficulté qu'il y a à dire le droit trop tôt. Mais ici le sujet est difficile car il touche à la définition de l'humain. Les chercheurs des biotechnologies pourraient remettre en cause la définition de l'être humain et ceci de manière assez grave. Ces recherches sensibles imposent donc un exercice de style délicat pour les juristes et les élus, celui de limiter la recherche. Ce travail est dangereux car le fait de pouvoir chercher appartient à la liberté de l'homme par nature curieux. Mais pour la première fois dans notre histoire, et pour des raisons éthiques, nous sommes tenus à tout le moins d'encadrer cette recherche.
La première solution pourrait consister à dire que, cette recherche étant dangereuse, il faut l'interdire. Cette attitude est bien sûr impossible et le serait même si nous étions isolés dans le monde. Nous avons des frontières et d'autres pays existent qui pourraient constituer à l'avenir des paradis génétiques. Nos chercheurs seraient obligés de s'expatrier pour ne pas perdre pied dans les domaines de la biologie de la reproduction ; cas de figure à éviter bien sûr.
De plus, l'homme est particulier dans la mesure où il a toujours fait le meilleur et le pire de ses découvertes. Quelles que soient les lois que la France se donnera, nous savons bien qu'ailleurs, tout ce qu'il sera possible de faire sera fait. Ceci ne dispense absolument pas de légiférer. Ce n'est pas parce qu'ailleurs le pire pourrait être commis qu'il faut l'admettre chez nous.
La révision des lois dites bioéthiques de 1994 devait intervenir en 1999. Le retard apporté à cette révision de la loi nous rassure, car la lenteur du législateur ici montre sa pondération, son angoisse et ses difficultés face à une science qui cavale tant sur le plan qualitatif que quantitatif.
Il existe un réel contraste entre les vitesses d'accomplissement de ces deux modèles, le modèle légal et le modèle scientifique. Cette différence de vitesse justifie totalement de confier à une agence une antenne de surveillance de la recherche et des pratiques, en quelque sorte un pôle avancé du législateur pour évaluer, en temps réel, les activités de recherche dans ce domaine.
Cette Agence (APEGH) pourrait avoir, monsieur le rapporteur, une composition différente de celle qui se trouve dans le projet de loi voté par l'Assemblée nationale. Je suggère qu'il y ait plus de représentants de la société civile, du monde de la pensée (des philosophes par exemple mais aussi des juristes et des élus) et moins de représentants du corps médical qui sont souvent juges et parties. Les médecins doivent être invités à donner leur avis en tant qu'experts sur l'opportunité des recherches et sur leurs limitations. Cette Agence pourrait avoir la mobilité nécessaire à l'évaluation des dossiers, ce que ne peut faire le législateur qui se doit de prendre du recul. Nous ne savons pas quelles seront les avancées scientifiques de demain. Même avec la plus grande précision dans l'élaboration d'un texte, celui-ci serait dépassé dès sa publication. Même une cadence de révision de la loi de cinq ans deviendra insuffisante pour les réactions rapides que ne nécessiteront les progrès à venir.
Une telle agence relève donc d'une précaution du législateur devant un problème inédit et ne le dessaisit pas, bien au contraire, de son pouvoir régalien. La Commission nationale de biologie de la reproduction et du diagnostic prénatal avait des pouvoirs limités puisque, par exemple, elle ne pouvait se rendre dans les hôpitaux pour évaluer sur place les actions engagées. Ses moyens financiers étaient insuffisants et sa rapidité de prise en compte des dossiers en souffrait.
Augmenter les attributions de l'Agence par rapport à cette Commission nationale de biologie de la reproduction me semble légitime et de surcroît astucieux. Si la France participe au travail de recherche sur l'embryon, il est nécessaire qu'un comité de sages puisse encadrer ce travail, le limiter après l'avoir autorisé et enfin en vérifier les résultats.
Le projet d'agence me semble donc bon, à l'exception de sa composition, qui doit subir quelques modifications dans le sens d'une plus grande ouverture à des personnes étrangères aux intérêts scientifiques proprement dits.
Avant de répondre très précisément aux questions que vous me posez, monsieur le rapporteur, je voudrais faire deux autres remarques préliminaires : l'une concerne la définition de l'eugénisme et l'autre concerne les problèmes éthiques soulevés respectivement par le diagnostic préimplantatoire (DPI) et le diagnostic prénatal (DPN).
En ce qui concerne l'eugénisme, un des sénateurs de la commission faisait remarquer que le diagnostic prénatal ne constitue pas de l'eugénisme puisqu'il est librement consenti par tout le monde. Il y a là un réel problème de définition du mot eugénisme. En effet, l'eugénisme est, pour une partie du concept, la sélection des enfants à naître. L'autre partie du concept traite des moyens divers d'améliorer l'espèce humaine. Lorsqu'une femme par exemple choisit comme compagnon un bel homme dans le but de faire avec lui de beaux enfants, son choix entre parfaitement dans la définition de l'eugénisme.
On peut donc se poser la question de savoir s'il y aurait un bon et un mauvais eugénisme ou plutôt un eugénisme acceptable et un eugénisme non acceptable et quelle serait dans cette hypothèse la ligne de démarcation ? C'est un philosophe américain, Philip Kitcher, qui, par l'analyse du concept, peut nous aider dans la compréhension de ce mot complexe. Selon lui, un programme eugénique peut être envisagé et analysé selon quatre angles différents et dans chacune de ces catégories le programme peut être plus ou moins acceptable. Ces catégories sont :
- l'aspect coercitif ou non du programme ;
- l'aspect discriminatoire ou non du programme ;
- la qualité des fondements génétiques du programme ;
- le but et l'enjeu du programme.
En effet, lorsque l'on parle d'eugénisme, le grand public effectue souvent un rapprochement avec la médecine qu'exerçaient les médecins nazis (qui ont fait l'objet du procès de Nuremberg bis, un des fondements modernes de la bioéthique). On ne peut bien sûr pas comparer cette médecine là au diagnostic prénatal en les rangeant toutes deux sous la même bannière de l'eugénisme. Si l'on compare ces deux programmes (la médecine nazie et le diagnostic prénatal) sous chacun des angles d'analyse de Philip Kitcher, on peut dire que la médecine nazie était coercitive alors que le diagnostic prénatal ne l'est pas, qu'elle était discriminatoire, ce qui n'est pas le cas pour le diagnostic prénatal, qu'elle reposait sur un fondement génétique erroné alors que le diagnostic prénatal a des fondements génétiques scientifiquement élaborés et corrects et enfin que le but de la médecine nazie était d'obtenir une amélioration de la race aryenne alors que le propos du diagnostic prénatal est d'avoir des enfants en bonne santé. Les deux programmes sont eugéniques mais l'un est inacceptable, alors que l'autre (qui répond bel et bien à la définition philosophique de l'eugénisme) est parfaitement accepté par une large majorité de la société française.
On peut donc dire à mon sens qu'il y a un eugénisme acceptable et un eugénisme non acceptable et la difficulté est précisément de définir les limites que notre société accepte et de poser les valeurs qu'elle ne souhaite pas franchir ou profaner.
Le deuxième point qui me semble important concerne les pudeurs et les difficultés éprouvées par la société française au moment de l'institution dans notre pays des centres réalisant le DPI. Le DPI au bout de trois ans de fonctionnement dans notre pays a permis la naissance à ce jour d'une trentaine d'enfants et concerne tout au plus 150 à 200 couples par an, au maximum, dans notre pays. Il consiste à rechercher une anomalie génétique transmise par les parents sur un embryon et à réimplanter les embryons qui ne sont pas porteurs de l'anomalie héréditaire de la famille. Il me semble beaucoup moins porter préjudice à la dignité humaine que le DPN où l'on recherche, et ceci de manière industrielle, sur la totalité des grossesses françaises, des anomalies embryonnaires et foetales, pour le cas échéant, interrompre les grossesses.
Il est intéressant et révélateur de se préoccuper avec tant de force du DPI dont la marginalité est extrême en oubliant totalement le DPN quasiment généralisé, aux enjeux éthiques bien plus lourds. Il y a tout lieu de penser que cette préoccupation extrême sur le DPI et l'absence de préoccupation sur le diagnostic prénatal sont symptomatiques d'un état d'esprit de notre société.
Et je voulais donc rappeler que si des problèmes éthiques importants se posent c'est bien dans le DPN et pas dans le DPI où la loi française est parfaitement bien écrite et mesurée. Le poids de la société française qui souhaite être rassurée sur la qualité des enfants à naître pousse, à l'instar d'une demande de soins, les médecins à proposer des tests de DPN de plus en plus sophistiqués.
Et si demain l'on était capable de détecter chez l'enfant à naître, par un moyen ou par un autre, l'existence d'une agressivité excessive, il y aurait fort à parier que nous serions sollicités par des demandes d'avortement comme cela s'est produit récemment dans le centre où j'exerce à propos de la détection fortuite d'un caryotype comportant un double Y.
On peut donc dire que notre société a, à l'évidence, un véritable penchant eugénique qui actuellement se renforce, compte tenu de la difficulté qu'éprouvent les parents d'enfants handicapés au quotidien. La boucle d'un eugénisme institutionnel a d'ailleurs failli être bouclée totalement lorsque l'on a tenu pour responsable au plan médico-légal des médecins n'ayant pas détecté une anomalie, permettant ainsi aux parents de ces enfants d'être «indemnisés» de l'absence de diagnostic prénatal. Nous étions de ce point de vue en train de faire fausse route collectivement puisque là où la solidarité nationale doit prendre en charge l'enfant différent, c'est au contraire que l'on assistait, avec les actions récursoires des caisses de sécurité sociale.
Vous m'avez demandé, monsieur le rapporteur, de donner mon opinion sur la recherche sur l'embryon.
Je pense que la France ne pourra pas éviter de mettre en oeuvre des programmes de recherche sur l'embryon, même si, pour l'instant les possibilités thérapeutiques qui peuvent résulter d'une telle recherche sont plus que douteuses. On pourrait même avancer l'hypothèse qu'une telle recherche n'aboutira peut-être jamais à rien. Mais a-t-on pour autant le droit de l'interdire ou de ne pas y participer ? Le chercheur qui a découvert la pénicilline ne faisait pas de la recherche sur les antibiotiques. Toutes les découvertes sont le fruit du hasard et d'une rencontre épistémologique entre deux types de discours et de langage. Si, demain, la loi de la France interdisait de mener des recherches sur l'embryon, ce serait, de manière certaine, une grosse erreur pour l'avenir que nous serions sûrement amenés à regretter.
Comment donc concilier la dignité de l'embryon humain (fut-il microscopique) et cette obligation d'autoriser la recherche sur l'embryon. Comment concilier le conflit d'intérêt entre le respect de la dignité de l'être humain et la quasi obligation de continuer à avancer dans les domaines de la connaissance pour ne pas risquer qu'un jour des recherches auxquelles nous n'aurions pas participé s'avèrent profitables et que notre pays profite des résultats de ces recherches sans avoir consenti d'y participer. En effet, si demain nous avons les moyens de soigner une pathologie grave grâce à des techniques issues de la recherche sur l'embryon, il sera impossible d'expliquer aux français que ces thérapeutiques ne seront pas disponibles sous prétexte qu'elles ont été obtenues grâce à la recherche sur l'embryon. Même si nous ne savons pas à quoi vont aboutir ces recherches (ce qui est une règle quasi constante dans le domaine de la recherche) je crois qu'il faut y participer.
Mais notre participation peut s'accompagner d'une immense prudence dont la première et sûrement la plus efficace est l'établissement d'un comité des sages qui, selon la loi, pourrait comporter des scientifiques extérieurs à la communauté nationale (le monde des chercheurs en biologie de la reproduction dans notre pays est petit et il serait nécessaire de se protéger d'un éventuel copinage entre des équipes très liées entre elles).
En s'assurant d'une analyse méticuleuse de la qualité des projets de recherche, en vérifiant la qualité des chercheurs qui les soutiennent, en analysant correctement les résultats de la recherche animale sur les mêmes sujets, on pourrait faire en sorte que le travail de recherche français sur l'embryon humain soit réduit à sa plus simple expression mais également à sa plus nécessaire légitimation.
Si une recherche est encore possible sur l'animal, elle ne devrait pas pouvoir prendre en compte des embryons humains. Une telle recherche devrait pouvoir être limitée dans le temps et dans le nombre d'embryons nécessaires et être suivie en temps réel par un contrôle spécifique.
J'irai même plus loin sur ce point de la recherche sur l'embryon. Si la France signe le texte de la convention d'Oviedo, il ne sera plus possible de créer des embryons spécifiquement pour la recherche. Or il y a au moins un exemple où il semble légitime de créer des embryons pour la recherche. C'est celui des jeunes filles traitées par chimiothérapie pour une maladie de Hodgkin ou une leucémie. Nous serons probablement capables d'ici quelques années de cultiver in vitro le tissu ovarien de ces jeunes femmes prélevé et congelé avant leur traitement et maturer in vitro leurs ovocytes. Ceci pourrait nous permettre, après guérison, d'obtenir des grossesses par procréation médicalement assistée chez des femmes qui actuellement sont condamnées à n'avoir pas d'enfant alors que nous sommes capables de les guérir de leur maladie.
Mais ne peut-on décemment réimplanter les premiers embryons obtenus par de telles techniques sans avoir vérifié préalablement la qualité de ces embryons ? Ce ne serait à l'évidence pas raisonnable ou ressemblerait à une expérimentation sur du « matériel humain » bien plus critiquable que de tester préalablement la qualité des embryons. Ma réponse est donc double. Non seulement je pense qu'il faut que notre pays se ménage une possibilité étroite et très encadrée de recherche sur l'embryon, mais il faut également avoir la possibilité de créer des embryons pour la recherche dans des situations très strictes et très encadrées. C'est de la qualité de cet encadrement que dépend la dignité que l'on accorde à ces embryons humains, c'est-à-dire la différence par rapport à un simple matériel biologique.
Je voudrais simplement rappeler qu'il y a quatre ans lorsqu'il s'est agi de créer des centres de DPI en France, seuls les centres qui avaient envoyé un chercheur à l'étranger pour se former au travail sur l'embryon humain ont pu avoir un agrément. Il y a là quelque chose d'un peu malsain d'envoyer des chercheurs se former à l'étranger sur les embryons des autres pour ensuite récupérer leurs compétences dans notre pays. Plutôt que de conserver ce type d'hypocrisie, ayons le courage de mettre en place chez nous les contrôles nécessaires pour éviter une dérive qui dans ce domaine serait inacceptable.
En ce qui concerne la brevetabilité du corps humain. Il nous faut faire face actuellement à une pression utilitariste car aucun industriel n'acceptera de consacrer d'importantes sommes d'argent à une recherche dans le domaine des biotechnologies s'il n'a pas une certaine assurance d'obtenir un retour sur son investissement. Par conséquent, il ne faut pas tarir les possibilités qu'offre la recherche en supprimant l'investissement émanant des structures privées.
Il y a bien sûr une différence entre une invention et une découverte et une solution pourrait être de limiter la durée de la propriété industrielle dans le domaine des biotechnologies. Le délai au-delà duquel les découvertes tomberaient dans le domaine public pourrait être plus court. Une position médiane en tous les cas pourrait éviter le tarissement du financement privé dans la recherche en génétique qui serait à mon sens catastrophique car l'argent serait alors investi, mais dans d'autres pays.
En ce qui concerne le transfert d'embryon post mortem . J'ai été confronté, à titre personnel et de manière très vive, par deux fois, à des demandes de femme qui disaient en substance : «dans l'état actuel de la loi, vous me dites que je peux donner mes embryons à une autre femme ou les jeter mais que je ne suis pas autorisée à les réimplanter dans mon propre utérus. Si c'est ce que dit la loi de la France, ceci n'est pas entendable».
Dans cette question du transfert d'embryon post mortem , l'analyse pourrait se faire en terme de cas particuliers. En effet, la meilleure manière inventée par l'espèce humaine pour résoudre un conflit d'intérêt, c'est la négociation, un chemin mené avec la patiente pour essayer de lui faire comprendre où est son réel intérêt et quels sont exactement les enjeux de sa demande.
Qui peut dire à une patiente confrontée à la perte d'un compagnon ce qu'elle a à faire dans ce domaine ? Qui peut savoir ce qui s'était dit à l'intérieur du couple avant la mort du compagnon ? Il est rigoureusement impossible de jeter la pierre à une femme qui accomplit une démarche d'aboutissement d'un projet débuté initialement avec un homme depuis décédé. Il ne s'agit pas là d'encourager la constitution de familles monoparentales mais tout simplement de traiter de manière humaine de situations exceptionnelles et toutes différentes les unes des autres.
Ici aussi un comité des sages pourrait intervenir au cas par cas (il doit y avoir 5 à 10 cas par an en totalité pour toute la France). Il me semble que cette option serait meilleure que de régler cette question par la loi, avec toute la rigidité que cela sous-entend, et qui, ici, ne me semble pas justifiée.
Le dernier point que je souhaite aborder concerne les maladies à révélation tardive dont l'exemple le plus connu est celui de la maladie de Huntington. Cette maladie dont le diagnostic prénatal est possible se transmet à 50 % des enfants d'un sujet malade. La maladie commence entre 40 et 50 ans et se termine dans une déchéance psychiatrique difficilement tolérable.
80 % des enfants ayant un de ses parents atteint de la maladie de Huntington ne veulent pas connaître leur propre statut génétique. Cette attitude est légitime car il n'y a aucun traitement préventif disponible. La situation se complique bien sûr lorsque ces personnes, en pleine santé, décident de concevoir un enfant. Le diagnostic prénatal, pour un couple dont le mari ou la femme ne veut pas connaître sa situation génétique personnelle, pourrait aboutir, en cas d'atteinte de l'enfant, à ce que la révélation du statut génétique se passe contre la volonté de l'individu de manière indirecte : si l'enfant est atteint, c'est qu'à coup sûr son parent transmet la maladie. Il est donc aussi un futur malade lui-même. Le diagnostic prénatal ne peut donc pas servir à protéger ces couples de la naissance d'un enfant malade lorsque l'un des membres du couple ne souhaite pas connaître son statut génétique personnel par rapport à cette maladie.
Le DPI permet de repérer chez les embryons les chromosomes issus des grands-parents porteurs de la maladie et permet d'éviter de réaliser l'analyse au niveau parental.
Cette situation se retrouve dans beaucoup de maladies à révélation tardive. La loi votée par l'Assemblée nationale, dans son article L. 2131-4, comporte dans son troisième alinéa les mots «chez l'un des parents» à la suite desquels est insérée la mention «ou l'un de ses ascendants immédiats dans le cas de la maladie de Huntington». Je vous propose de supprimer la restriction à la maladie de Huntington car d'autres maladies à révélation tardive nous placeront dans le besoin d'analyser les chromosomes des grands-parents pour savoir ceux que l'embryon a hérité. La situation de la maladie de Huntington devrait se produire pour d'autres maladies à révélation tardive et ne pas alors nécessiter une modification du texte de loi.
Je rappelle à ce propos que toutes les demandes de DPI sont analysées préalablement par les centres pluridisciplinaires de diagnostic prénatal qui doivent donner leur accord après analyse du dossier. Si la maladie de Huntington est pour l'instant la seule maladie à révélation tardive, elle ne restera pas la seule et il n'y a pas de risque à laisser simplement la mention de « l'un des ascendants immédiats » sans préciser le type de maladie que l'on recherche.
A la question posée au départ de cette intervention du «faut-il légiférer ?», ma réponse est désormais tout à fait claire et positive. Bien que le sujet soit difficile, du fait de son évolutivité exponentielle, il faut légiférer de manière très générale, en déléguant à une agence le soin d'une analyse de détail en temps réel.
Je ne vois pas d'autre dispositif qui permette d'allier la nécessité de légiférer et la rapidité des évolutions dans ce domaine.
Voici, monsieur le président, monsieur le rapporteur les quelques éléments de réflexion que m'inspire le texte de loi que nous analysons.
M. Francis GIRAUD, rapporteur - Je crois que le Professeur Nisand a parfaitement répondu à notre attente. En effet, il a complété très heureusement cette matinée en nous apportant, élément capital, le poids de son expérience et de sa réflexion sur tous ces problèmes. Sur beaucoup de points, la commission des Affaires sociales devra réfléchir et se prononcer en tenant compte de ce qu'il nous a livré ce matin. Nous le remercions beaucoup.
M. Jean Louis LORRAIN - Si vous le permettez, monsieur le professeur, je voudrais vous poser une question brève. Lors de votre approche, nous nous sommes bien rendu compte que nous vivions une période de profonde tension. Il semble que nous nous écartons de plus en plus de la morale kantienne qui nous aidait jusqu'ici et dont la finalité était l'intérêt de l'être et, nous avons l'impression que toutes ces idées sont en train de se diluer.
En ce qui concerne la pression que nous ressentons, croyez-vous vraiment que les lois éthiques et non pas celles du législateur freinent la science ? Par ailleurs, j'ai vu tout l'intérêt que vous portez à la création d'une agence particulière. Nous sommes un petit peu mesurés parce que nous avons l'expérience des conseils d'éthique qui nous semblent remplir leur tâche, en particulier sur le plan national et notamment pour les maladies de Huntington ou de Franconi. Vous savez bien que des avis très récents sont parus sur le sujet. Nous partageons avec vous l'idée d'une Agence plus spécialisée.
Ma question, à laquelle, je sais, vous ne répondrez pas, se rapporte au statut de l'embryon. Faut-il, dans le cadre du prolongement de cette loi, s'atteler à la tâche de définir le statut de l'embryon ? Loin de nous l'idée de vouloir sacraliser des cellules débutantes mais cette question est liée à la notion de développement. Devons-nous aborder le problème de la personne lorsque nous parlons de l'embryon ?
En précisant et en menant une réflexion de fond sur le statut de l'embryon, nous pourrions apporter un éclairage, des comportements voire des choix scientifiques différents, même si nous craignons ce qui peut se passer ailleurs.
Pr. Israël NISAND - Je pense tout à fait, monsieur le président, monsieur le sénateur, que les parlementaires ne pourront pas faire l'économie d'une discussion difficile et très contradictoire (car les valeurs sont très différentes) sur le statut de l'embryon et du foetus. Un événement récent où une femme a perdu son foetus à la suite d'un accident de la voie publique à la veille de son accouchement a laissé l'opinion publique sans voix lorsqu'il a été dit que le foetus n'était pas une personne.
Le débat sera en effet difficile car l'opinion publique est favorable à 90 % au maintien du droit à I'IVG. Il faut donc trouver une solution pour créer un statut de l'embryon tout en maintenant le droit des femmes à accéder, lorsqu'elles le souhaitent, à une interruption volontaire de la grossesse.
Je ne partage pas par exemple l'opinion qui consiste à dire qu'il vaut mieux jeter un embryon plutôt que de mener une recherche très encadrée sur lui avant de le jeter. Je n'arrive pas à comprendre où est la différence de dignité entre ces deux démarches. La démarche du don qui concerne les embryons aussi bien que les organes ne porte pas non plus atteinte à la dignité humaine. En effectuant une analyse génétique sur un embryon avant de la détruire, nous n'attentons pas à la dignité humaine. En revanche, je nourris une opposition personnelle au clonage reproductif. Les forces du marché sont telles que des équipes de recherche peuvent être amenées à le réussir et à le proposer. Or il porte atteinte à la liberté individuelle et ceci de manière grave et n'a aucun intérêt médical ni même aucun intérêt scientifique.
L'interdire en France ne suffit pas et il me semble qu'à cette occasion la France devrait demander, même si elle est isolée dans cette démarche, de faire du clonage reproductif un crime contre l'humanité. Celui-ci pourrait dès lors être poursuivi, sans prescription, par un tribunal pénal international.
C'est le seul moyen d'éviter une issue inéluctable et caractéristique de l'espèce humaine «l'homme a toujours fait le meilleur et le pire de ses découvertes». Être comptable devant nos enfants du monde que nous leur laisserons, c'est s'être opposé avec la plus grande véhémence au clonage reproductif, même si d'autres nations, subverties par les forces du marché, n'ont pas la même analyse que nous. Ce ne serait pas la première fois que la France fait entendre seule sa voix. C'est alors qu'elle a le plus de poids.
E. AUDITION DU PROFESSEUR LAURENT DEGOS, CHEF DU SERVICE D'HÉMATOLOGIE DE L'HÔPITAL SAINT-LOUIS, DIRECTEUR DE L'INSTITUT UNIVERSITAIRE D'HÉMATOLOGIE
M. Nicolas ABOUT, président - Monsieur le rapporteur, nous avons maintenant le plaisir d'accueillir le professeur Laurent Degos. Souhaitez-vous le présenter et rappeler vos questions ?
M. Francis GIRAUD, rapporteur - Merci, monsieur le président, chers collègues, nous avons le grand plaisir de recevoir le Professeur Laurent Degos. Je vous le présenterai en indiquant qu'il est, d'abord et avant tout, un soignant et un médecin, avec une carrière très prestigieuse dans la recherche médicale. Il est chef de service d'hématologie et porte assistance et secours à ses patients. Cette tâche ne l'empêche pas, et au contraire, l'amène à réfléchir de manière très importante, aux problèmes de la bioéthique, tout en dépassant le cadre de sa spécialité. Dans la lignée des auditions de ce matin, il nous fera part de ses réflexions sur le texte de loi voté par l'Assemblée nationale en janvier 2002, notamment sur l'organisation de l'APEGH. Nous lui demanderons également son avis sur la non-brevetabilité du corps humain, les transferts d'embryons post mortem et sur les dons d'organes qu'il connaît particulièrement. Enfin, sachant qu'il a saisi le comité national d'éthique de ce sujet, il pourra évoquer les problèmes éthiques soulevés par les essais de médicaments anticancéreux.
Pr. Laurent DEGOS - Merci beaucoup, monsieur le président, monsieur le rapporteur, mesdames et messieurs les commissaires et tous ceux qui vous entourent.
L'homme est un sujet et non un objet. Ce postulat pose deux questions : quand devient-on homme ? et quand l'homme n'est pas encore homme ou n'est plus homme qu'est-il ? Il n'est sûrement pas un objet. Si la mort, recaractérisée récemment dans nos sociétés occidentales selon le critère de mort cérébrale et non plus d'arrêt du coeur, est bien définie, ce n'est pas le cas pour le début de l'homme. De même que la mort a été redéfinie sous la pression de la pratique médicale de greffes d'organes, nous sentons, actuellement, une demande de signification du début de l'homme dans la perspective médicale du clonage thérapeutique. Nous pouvons certes définir des moments biologiques de la mise en place de l'individualité ou du cerveau, mais la question de savoir quand débute la personne se posera toujours. Même si une date est fixée pour le début de la personne, il faudra statuer sur la nature de l'organisme entre la fécondation et ce commencement de personne.
L'embryon avant d'être homme est-il une chose ? Sûrement pas. A-t-il des valeurs humaines ? Peu avant la mort, l'homme est-il une chose ? Sûrement pas. Après la mort, l'homme n'est pas non plus une chose. Alors, avant d'être homme, quelles sont les valeurs humaines qui appartiennent à l'embryon ?
La première valeur humaine est celle de la finalité. L'homme est dans la nature parce qu'il apporte ses compétences et hors nature car, lorsqu'il n'en dispose plus, on ne le jette pas comme un mouchoir utilisé. Cette valeur de finalité n'est pas remise en question au moment de la mort puisqu'un homme décédé est respecté et sa destinée, en tant qu'organisme, n'est autre qu'une sépulture que l'on ne peut profaner. Il ne devient pas matière première pour des transformations, même si ses organes peuvent être prélevés à des fins thérapeutiques. Mais qu'en est-il de l'embryon ? Cette question reste sans réponse.
Parallèlement, nous devons nous prononcer sur l'éventualité, à mon avis dangereuse, de dresser des catégories d'embryons. Existe-t-il des embryons utilitaires, et d'autres dont le destin est de créer un enfant ? Le racisme appliqué aux embryons potentiellement humains selon lequel nous disons que nous nous servirons uniquement des embryons surnuméraires est une notion dangereuse, d'autant que la société n'a pas défini le début de la vie humaine. Pareillement, nous ne pouvons pas affirmer que l'embryon surnuméraire possède plus d'humanité en servant la recherche qu'en mourant naturellement. Ici, nous ne pouvons pas faire valoir une notion de hiérarchie d'humanité, ce qui conduirait à des débordements en fin de vie.
La deuxième valeur mentionne la protection de l'homme dans son intégrité. Nous pouvons alors nous demander à qui appartient l'embryon : aux parents, à la société, aux chercheurs, à Dieu ou à lui-même ? Tant que nous ne pouvons répondre à cette question, je ne vois pas comment on peut utiliser des embryons.
La troisième valeur morale est la gratuité, l'homme et ses éléments ne peuvent pas faire l'objet de profits. L'article 6 de la directive européenne de 1998 spécifie que l'exploitation industrielle et commerciale des embryons humains est exclue et que tout brevet est interdit. Cependant, certains chercheurs, dans d'autres pays européens, affirment que les embryons non viables ou créés par parthénogénèse ou transfert de noyau ne sont pas concernés. En Espagne, le terme nucleovulo sert pour définir l'embryon par transfert de noyau. En modifiant le nom, l'intention est de changer de concept. Un embryon est un embryon, c'est-à-dire qu'il est potentiellement humain s'il est transféré dans un utérus. L'industrie privée est entrée dans le domaine des traitements cellulaires embryonnaires avec un but affiché : le profit. Jamais les éléments de l'homme (le sang, le sperme, les organes, les tissus et même les cellules souches du cordon ombilical) n'ont fait l'objet de profit en France. Ils sont donnés, distribués et utilisés sans profit, même après tri ou modification. Pourquoi, et au nom de quoi, l'embryon et, en général, le traitement cellulaire ferait-il l'objet de profit ? D'où viendrait cette dérogation ? Le prétexte donné est la rapidité de la découverte lorsque les sociétés privées prennent en charge une étude, mais cet argument n'est-il pas une injure à la recherche publique ? Nous devons nous souvenir que la découverte des groupes d'histocompatibilité, c'est-à-dire des marqueurs qui permettent de réaliser des greffes d'organes, s'est effectuée en peu de temps grâce à une collaboration internationale de laboratoires publics. Il est impératif de garder cette valeur humaine de gratuité en considérant, au moins, que l'embryon est un élément de l'homme et que ni lui, ni ses cellules transformées, triées, modulées ne peuvent faire l'objet de profit.
La quatrième valeur morale se rapporte non pas à l'embryon lui-même mais à la vision de fins thérapeutiques où il est toujours demandé d'évaluer le rapport bénéfice-risque. Or, actuellement, la thérapie cellulaire embryonnaire, clonée ou non, n'a jamais prouvé son efficacité. Aucun traitement de maladie dégénérative n'a été démontré chez l'animal. Tout au plus, il a été rapporté récemment que des cellules transférées restent fonctionnelles mais ne sont pas réparatrices. Si aucun bénéfice n'a encore été démontré par le traitement des cellules embryonnaires, celles-ci provoquent, même très fortement différenciées, après transfert, un risque important de cancer appelé tératocarcinome. La dernière étude sur la souris a montré que, sur dix-neuf transferts de cellules très différenciées et fonctionnelles, cinq animaux ont développé un cancer. Avant de faire croire au rêve, comme pour bon nombre d'autres concepts en médecine, il serait préférable d'avoir une preuve thérapeutique sans risque.
Après ce préambule, je commenterai le projet de loi.
Premièrement, l'homme en fin de vie, reste toujours un sujet et ne constitue pas un objet d'expérimentation. Je vous proposerai un amendement afin de bien le spécifier et modifier les recommandations actuelles de l'Agence française de sécurité sanitaire des produits de santé reprenant les « guide lines » de décembre 1996 de l'Agence européenne du médicament (EMEA). Lorsqu'un médicament anticancéreux est donné pour la première fois chez l'homme, essai de phase 1, ces agences demandent de rechercher la dose maximum tolérée sans avoir aucun objectif d'efficacité. Pour cette raison, il est proposé d'entreprendre ces essais uniquement chez les malades atteints de cancer en fin de vie en excluant tout malade ayant une chance raisonnable de vie prolongée. Il est recommandé d'élaborer des cohortes de trois patients par dose, et de l'échelonner jusqu'au maximum toléré. Nous savons ce que ce mal maximum induit signifie chez un malade atteint de cancer en fin de vie. En outre, non seulement l'Agence demande de tester sur trois patients cette dose maximum tolérée, mais encore prescrit-elle de la donner à six patients pour acquérir la certitude que c'est bien la dose maximum tolérée. Ceci est en total désaccord avec la directive européenne, se référant à la déclaration d'Helsinki selon laquelle un essai clinique peut être entrepris uniquement si les risques et inconvénients imprévisibles ont été pesés au regard du bénéfice attendu pour le sujet participant à l'essai. Or, dans ce cas, les risques et les inconvénients ne sont pas imprévisibles mais bien provoqués ; en outre, un bénéfice attendu n'est pas exigé. Le bénéfice collectif ne se substitue pas au bénéfice individuel si la personne est malade. Suivant cette recommandation nous pouvons tout à fait essayer un médicament contre le cancer de la prostate chez une femme ou contre un cancer du rein chez quelqu'un avec une tumeur du cerveau. Pourquoi rechercher, dans le cas du cancer, une dose maximum tolérée alors que la personne est fragile et sa mort prochaine ? Nous devrions, au contraire, avoir pour elle le plus d'attention, de précaution et de compassion. Cette directive est basée sur un faux raisonnement selon lequel plus un produit est toxique, plus il est efficace. Actuellement, ce n'est pas en recherchant la dose la plus toxique que nous obtiendrons la meilleure efficacité, bon nombre d'exemples le prouvent. C'est pourquoi je vous demanderais de spécifier par amendement que, dans tout essai thérapeutique même appliqué au cancer et même en phase 1, il soit obligatoire de mêler le double objectif d'efficacité, parfois présumée, et de description des effets adverses, et, par ailleurs, de ne pas rechercher la dose maximum tolérée si la dose efficace est déjà connue. Le comité consultatif national d'éthique a émis récemment dans ce sens l'avis n°73.
Deuxièmement, je commenterai quelques articles du projet de loi au sujet du début de la vie.
La première interrogation vise à savoir si nous pouvons mener des recherches en vue du clonage thérapeutique. Selon l'article 16-4 du code civil, toute intervention ayant pour but de faire naître un enfant ou de développer un embryon humain, non directement issu de gamètes d'un homme et d'une femme, est interdite. Mais, alors, comment définissez-vous le mot développer ? Le passage d'une à deux cellules est-il un développement ? Dans ce cas, toute recherche sur le clonage thérapeutique serait exclue. Dans l'article L. 1251-3, il est mentionné : « Est autorisée la recherche menée sur l'embryon humain et les cellules embryonnaires qui s'inscrivent dans une finalité médicale. » La seule finalité médicale du traitement par cellule embryonnaire étant bien le clonage thérapeutique, il faudra choisir entre ces deux articles ou être plus précis. Est ajouté « La condition d'une méthode alternative d'efficacité comparable, en l'état des connaissances scientifiques, supprime cette autorisation ». Or, rien n'est plus difficile que de définir une efficacité comparable d'autant plus dans la perspective d'une recherche où le produit fini ne peut pas être connu à l'avance. Ce flou risque d'aboutir à un non-respect de l'esprit de la loi.
Deuxièmement : pouvons-nous dresser des catégories d'embryons ? L'article L. 2141-1-1 pose : « Aucune nouvelle technique d'assistance médicale à la procréation ne peut être mise en oeuvre avant une évaluation préalable. ». Quelle est la signification du terme « nouvelle » technique puisque interviennent toujours un nouveau geste, un nouvel instrument, même dans les pratiques déjà connues ? C'est le principe même de l'évolution des pratiques. Selon cet article, toute pratique effectuée à partir de ce jour doit suivre ce nouveau texte. Or, il est précisé : « A l'issue du processus d'évaluation, les embryons dont la conception résulterait de cette évaluation ne peuvent être conservés, ni entrer dans le cadre d'un projet de recherche. « Il n'y aurait alors plus d'embryons surnuméraires, même pour la recherche dans le futur. Alors pourquoi permettrions-nous une recherche sur les embryons déjà existants alors que ce serait impossible sur les embryons futurs ? Si l'autorisation de conservation ou de projet de recherche sur quelques embryons issus de ces thérapeutiques est supprimée, pourquoi ceux-ci auraient-ils un destin différent des autres ? Un embryon est un embryon et il ne peut y avoir des catégories d'embryons. Il est ajouté au point 4 de ce même article « S'ils n'ont plus de projet parental, les membres du couple peuvent consentir à ce que les embryons fassent l'objet d'une recherche. » Cette disposition semble en contradiction avec la mesure précédente. L'ambiguïté perçue entre la permission, ou non, de la recherche sur des embryons surnuméraires sous-tend la difficulté de se prononcer sur leur statut particulier. A mon avis, il n'existe pas plusieurs types d'embryons potentiellement humains, certains utilitaires et d'autres avec un projet parental, certains avec plus d'humanité que d'autres.
La dernière question se rapporte à la possibilité de faire du profit avec des éléments humains. J'ai, peut-être, mal lu le projet de loi mais je n'ai pas trouvé de mention sur la commercialisation des cellules embryonnaires à des fins de recherche ou thérapeutique en dehors de l'article 12 bis ne mentionnant que le brevet. L'interdit de brevet et de commercialisation devrait englober toute cellule humaine, qu'elle soit l'embryon lui-même, prélevée sur ce dernier ou transformée en un autre type cellulaire, modulée ou ayant une fonction particulière. Nous respectons cet interdit pour des éléments du sang. Pourquoi y aurait-il une dérogation de ce principe que l'homme et ses éléments ne peuvent faire l'objet de profit, lorsqu'il s'agit de thérapie cellulaire utilisant certaines cellules et non d'autres ?
Je conclurai par trois principes fondamentaux : l'interdiction de catégoriser les hommes durant, avant et après leur vie en raison de finalités différentes, la limite de prendre de la vie pour en donner et le fait que l'homme et ses éléments ne peuvent faire l'objet de profit. Je n'ai peut-être pas répondu à toutes vos questions ne les ayant reçues que ce matin, mais je peux le faire oralement.
M. Francis GIRAUD, rapporteur - Vous avez déjà évoqué dans votre propos préliminaire le problème de la recherche sur l'embryon. Votre position est d'une clarté limpide et sous-tendue par des arguments assez forts. D'autres sénateurs voudront peut-être vous interroger à ce propos.
Quelle est votre réflexion sur l'APEGH qui est inscrite dans la loi et dont les compétences et pouvoirs sont étendus ? Cela vous paraît-il convenable et quel rôle assigneriez-vous à cette agence ?
Pr. Laurent DEGOS - D'abord, préalablement à l'installation d'une agence, nous devons tous être d'accord à propos de la recherche sur l'embryon. Ensuite, nous devons savoir quelles valeurs dites humaines garderait l'embryon par rapport à l'homme en tant qu'homme. Nous devons nous accorder pour savoir s'il peut perdre la valeur de finalité et donc être à la fois utilitaire et un homme potentiel. La deuxième valeur se réfère à qui appartient l'embryon, c'est-à-dire s'il bénéficie d'une protection ou non. Tant que nous n'aurons pas répondu à ces questions, l'Agence rencontrera des difficultés pour gérer ces embryons. Enfin, si nous ne pouvions garder qu'une valeur, je conserverai la troisième qui est la non-profitabilité. En effet, l'embryon, modifié ou non, ne peut être commercialisé à aucun stade, que ce soit au moment du prélèvement, de la transformation ou de la distribution. Une firme privée ne peut pas distribuer des cellules humaines au public. Une réflexion, ici, est à mener sur les valeurs que garderait l'embryon. Mais, si nous admettons qu'il est totalement dépourvu de valeur humaine, une telle Agence serait utile. La décision de sa création doit, à mon avis, être discutée en parallèle de votre décision sur le statut d'embryon et ses valeurs qui permettraient de pouvoir s'en servir ou non. Ma réponse n'est pas directe mais elle sous-tend une condition, celle de mieux définir ce qu'est l'embryon. Afin de réunir les compétences, ne faudrait-il pas regrouper les agences en une seule Agence de biothérapie (greffe, sang, cellule tissu, embryon...) ?
M. Francis GIRAUD, rapporteur - Nous souhaiterions connaître votre avis sur la non-brevetabilité du corps humain, notamment en rapport avec la directive européenne de 1998. En effet, l'Assemblée nationale a introduit un amendement qui pose problème.
Pr. Laurent DEGOS - A cette question, on répond souvent non-brevetabilité assortie de la référence à la distinction entre découverte et invention. Ce distinguo est un premier élément très fort qui doit être respecté. Mais la donnée supplémentaire en ce qui concerne le corps humain est que c'est l'homme lui-même qui est concerné ici. Le monde vivant suit bien la différenciation entre invention et découverte mais l'homme est homme. Nous ne pouvons ni breveter, ni acheter, ni vendre un homme. Vous êtes tous d'accord avec moi. Nous n'avons pas le droit de breveter, acheter ou vendre un organe. Nous avons encore tous le même avis sur ce sujet. Il est interdit de breveter, d'acheter ou de vendre du sang ou des cellules du sang. Nous partageons la même opinion là-dessus. Finalement, nous en arrivons, progressivement, à nous demander si une limite nous donnant une permission existe ou non. A mon avis, l'embryon dispose de plus de valeur qu'un globule rouge. Il est potentiellement humain. Maintenant, nous allons aussi nous poser la question à propos du gène. En ce qui me concerne, je suivrai jusqu'au bout la trajectoire humaine en interdisant tout brevet pour tout ce qui touche l'homme jusqu'à ses gènes. Toutefois, une commercialisation à partir du gène après modification est éventuellement envisageable. Le gène diffère peut-être d'une cellule. Pour celle-ci, même après modification, à mon avis, nous ne pouvons pas tirer de profit. J'ai vu que l'Assemblée nationale avait rajouté le gène spécifiquement, en tant que tel, non modifié. Personnellement, je suivrai ce texte.
M. Francis GIRAUD, rapporteur - Que pensez-vous du transfert d'embryons post mortem ?
Pr. Laurent DEGOS - Sur ce sujet, je n'ai pas beaucoup d'idées et je ne peux décemment vous répondre, n'en étant pas un spécialiste. La réaction consisterait plutôt à demander si nous ne perturbons pas beaucoup d'éléments familiaux en l'autorisant. La réponse ne relève pas vraiment d'un interdit biologique. L'Espagne le pratique déjà depuis longtemps, en tout cas pour la fécondation par sperme. C'est plus, comme vous l'avez bien mentionné, un problème juridique.
M. Francis GIRAUD, rapporteur - Quelles réflexions vous inspirent les dispositions de la loi sur les dons d'organes, à propos de l'élargissement du cercle des donneurs vivants à toute personne ayant avec le receveur une relation étroite et stable ?
Pr. Laurent DEGOS - Le problème ne réside pas tant dans la personne en relation étroite et stable parce que nous avons tous une vie privée qui est respectable mais plutôt dans la possibilité même de réaliser des greffes d'organes à partir de donneurs vivants. J'y suis tout à fait favorable pour le rein, mais ces pratiques doivent être très encadrées lorsque des techniques chirurgicales difficiles se révèlent nécessaires, comme pour le foie. En effet, quand un foie est prélevé sur un donneur vivant, la moitié de son organe est transféré à un receveur en très mauvais état. Prélever un demi-foie sur une personne vivante ne se révèle pas une opération simple, d'autant que toutes les précautions sont prises pour recueillir les vaisseaux et conduits en bon état et de bons calibres afin de pouvoir les « rabouter » sur le receveur. A mon avis, ces procédures devraient relever de la recherche et non pas de la pratique médicale. Nous devons, peut-être, réfléchir sur la limite entre ce qui relève de la pratique médicale, comme la greffe de rein par exemple, et ce qui concerne la recherche, comme la greffe d'un lobe de foie. Nous ne pouvons peut-être pas aller aussi loin dans la loi, mais en tant que médecin, je vois une très nette différence entre un prélèvement d'une partie de foie et d'un rein.
M. Nicolas ABOUT, président - Auriez-vous tenu le même raisonnement face au Professeur Hamburger lors des premières transplantations de rein ?
Pr. Laurent DEGOS - Je n'aurais pas eu cette réflexion parce que nous disposons de deux reins et que si nous en enlevons un, l'autre continue de fonctionner. Par contre, nous ne possédons qu'un foie, qui est, de plus, un organe très fragile. Certaines équipes peuvent réaliser ces opérations et je respecte leurs prouesses qui en sont de réelles. Mais nous ne pouvons pas dire que de telles opérations peuvent se pratiquer dans tout centre. Par contre, une greffe de rein à partir de donneur vivant peut avoir lieu dans tout CHU français.
M. Nicolas ABOUT, président - C'est peut-être, encore, une technique insuffisamment contrôlée.
Pr. Laurent DEGOS - Pour l'instant, seulement quelques centres en Europe la pratiquent. Cependant, il ne faudrait pas, que certains, à ce propos, se disent capables de l'utiliser, sans précautions et évaluations préalables.
M. Francis GIRAUD, rapporteur - J'ai une dernière question à vous poser. Vous nous avez déjà répondu sur les cellules embryonnaires et les espoirs possibles de leur utilisation thérapeutique.
Quelle est votre opinion et quelle idée avez-vous de la recherche en France sur les cellules souches adultes ? De nombreuses équipes travaillent-elles dessus ? Sont-elles encouragées et aidées ? Quels sont les espoirs et à quel terme pouvons-nous envisager que ces cellules souches apportent un résultat positif à des souffrances humaines ?
Pr. Laurent DEGOS - Cela paraît être l'alternative proposée dans la loi. La présence des cellules souches adultes provoquent encore des doutes. En effet, certains disent qu'elles n'existent pas et qu'elles sont le résultat des fusions entre deux cellules. Mais, pratiquement, pour un médecin, l'idée qu'une cellule du foie résulte d'une fusion entre une cellule médullaire et une autre hépatique ne dérange pas si elle peut servir à la fabrication du foie.
En ce qui concerne les recherches, nous disposons de beaucoup plus de résultats avec les cellules souches adultes qu'avec les cellules embryonnaires. Vous connaissez les résultats de Philippe Ménasché avec des cellules musculaires adultes. Il existe d'autres exemples pour traiter des sphincters.
Bien sûr, on va vous faire remarquer que les cellules thérapeutiques et les cellules traitées sont des cellules apparentées. Mais cette contestation est plus scientifique que pratique car, finalement, le but est bien médical. Les cellules de muscle strié peuvent aider les cellules cardiaques. Donc, si des cellules de muscle strié cultivées et donc modifiées peuvent réparer le muscle cardiaque, cela est déjà un résultat médical important. Ce n'est certes pas la prouesse consistant à transformer une cellule hépatique en cellule musculaire. Petit à petit, les chercheurs trouveront et manipuleront ces cellules. Une autre voie de recherche s'ouvrira, à mon avis, celle de la différenciation.
Toutes les cellules de notre corps sont fonctionnelles et leur spécialisation n'existe que par la fermeture de programmes. Un embryon peut tout fabriquer, par contre, une cellule de la peau ne produit plus que de la kératine et les cellules de globules rouges que de l'hémoglobine. Avec le temps, les cellules ferment progressivement des programmes et arrivent à devenir des cellules très spécialisées. Nous essayons, c'est le but de ma recherche, d'ouvrir à nouveau les programmes fermés. Cependant, nous essayons de le faire progressivement en faisant revenir la cellule à un état plus flexible, plus « embryonnaire ». Nous connaissons mieux la mécanique dans le noyau de la cellule, qui permet de rouvrir les programmes.
A mon avis, nous y arriverons dans le futur. La preuve en est que, lorsque vous mettez un noyau adulte très mûr dans un ovule, comme pour la création de Dolly, nous ouvrons tous les programmes. Toutes sortes de tissus ont pu être fabriqués et cela a donné un être entier. L'ouverture de programmes est donc possible, à nous scientifiques de la trouver. Il est préférable d'utiliser une cellule adulte et de lui faire rouvrir progressivement des programmes qu'une cellule très embryonnaire et très jeune risquant de provoquer un cancer. Il vaut peut-être mieux aller de la maturité vers l'immaturité et maîtriser ce processus plutôt que l'inverse, bien que la facilité soit de prendre des cellules embryonnaires pluripotentes. En effet, le scientifique peut cultiver, conserver et modifier autant qu'il veut des cellules souches embryonnaires. Cette voie est certes la plus facile actuellement mais avec beaucoup de risques et de rêves.
M. Jean CHERIOUX - Monsieur le professeur, merci de cet exposé qui nous a ouvert bien des perspectives et qui en a fermé certaines, d'ailleurs. Nous avons pu constater votre attachement au respect de la finalité pour l'embryon.
N'estimez-vous pas que la loi de 1994 et le projet actuel ont le grand défaut de mélanger les problèmes de la procréation médicalement assistée et de la recherche sur l'embryon ?
J'étais rapporteur du texte de 1994 et, à l'époque, nous nous intéressions plus à la procréation médicalement assistée. Puis, nous nous sommes trouvés devant les problèmes du stock d'embryons, de leur devenir et du diagnostic préimplantatoire. Dès lors, nous avons dérivé sur les problèmes de recherche. Deux règles éthiques existent ici, dont je ne dirai pas qu'elles s'opposent mais qu'elles sont en parallèle. La première relevant de la PMA proprement dite, consiste à poser la question de mettre fin ou non à un embryon non transféré. La deuxième considère l'embryon comme une chose. Elle envisage le fait de pouvoir le donner. Ne pensez-vous pas qu'il faille régler les deux problèmes, l'un sans tenir compte de l'autre, d'autant plus que, comme vous l'avez dit, la science évolue et peut très bien conduire au tarissement du seul réservoir d'embryons pour la recherche, constitué par la PMA ?
Pr. Laurent DEGOS - Cette question est difficile. L'embryon existe pour lui-même et la réalisation d'une PMA a bien pour but la vie de l'embryon. Dans ce cas, nous conservons donc cette finalité de vie pour l'embryon, nous agissons pour lui. Or, la thérapeutique à partir de l'embryon ne poursuit pas son intérêt mais celui de quelqu'un d'autre. Le point, ici, se révèle alors différent.
Avec la PMA ou le DPI, ce que nous recherchons est de tout mettre en oeuvre pour que l'embryon vive et bien. La permission de son accueil ou de son adoption poursuit le même but de vie de l'embryon. Par conséquent, pour moi, toutes ces procédures vont dans le même sens.
L'idée est différente quand il s'agit de fabriquer un embryon pour réaliser un traitement. C'est ici qu'il doit y avoir un consensus, à mon sens citoyen, pour savoir si nous admettons, ou pas, que l'embryon change de finalité. Je ne veux pas intervenir ici, chacun a ses propres idées mais il doit y avoir un consensus. En effet, on a vu au Japon que l'absence de consensus sur la mort cérébrale a été très mal ressentie. Il faut donc adopter une position en parallèle de l'opinion de la population.
Pour l'instant, la population ne conçoit pas l'embryon comme une chose qui soit possiblement malléable, etc. Parallèlement, comme j'ai déjà dit, si nous changeons sa finalité, c'est-à-dire que nous admettons qu'il est à la fois potentiellement humain et utilitaire, je vous demanderai de ne pas établir de catégorisation de l'embryon. Nous ne devons pas déduire des embryons surnuméraires qu'ils sont utilitaires et que les autres sont différents. En effet, si nous commençons à catégoriser des organismes potentiellement humains, je ne vois pas où nous nous arrêterons dans l'humain.
Quant à le laisser mourir, cela est le propre de nous tous puisque nous naissons et nous mourons. Il suffit de supprimer l'azote liquide, comme on arrête les machines en cas d'acharnement thérapeutique, pour qu'il meure.
M. Nicolas ABOUT, président - Monsieur le professeur, souhaitez-vous donner un dernier message ?
Pr. Laurent DEGOS - Je vous ai apporté certains points vous paraissant, peut-être, un peu trop rigides. Cependant, il faut rester conscient que la médecine peut faire rêver sans aboutir.
Un vrai modèle pertinent chez l'animal nous montrant la possibilité d'une guérison d'une maladie dégénérative sans risque de transmission de tératocarcinome (cancer embryonnaire) nous amènerait peut-être à avoir une réflexion différente aujourd'hui.
M. Nicolas ABOUT, président - Je vous remercie infiniment pour ce dernier message. En vous remerciant, je vais accueillir le professeur Didier Sicard, président du comité consultatif national d'éthique pour les sciences de la vie et de la santé.
F. AUDITION DU PROFESSEUR DIDIER SICARD, PRÉSIDENT DU COMITÉ CONSULTATIF NATIONAL D'ÉTHIQUE POUR LES SCIENCES DE LA VIE ET DE LA SANTÉ
M. Nicolas ABOUT, président - Monsieur le professeur et président, je vous remercie beaucoup d'avoir accepté de venir devant nous. Vous avez déjà eu des entretiens avec le rapporteur qui va résumer en quelques mots l'état de votre réflexion et les sujets qu'il souhaite vous voir aborder.
M. Francis GIRAUD, rapporteur - Monsieur le président du Comité consultatif national d'éthique, vos responsabilités vous ont amené à réfléchir depuis longtemps sur les problèmes importants concernant la loi de bioéthique. Avant de vous poser des questions plus précises sur le texte voté par l'Assemblée nationale en janvier 2002, je vous demande d'indiquer le regard que vous portez sur l'évolution scientifique et des mentalités intervenues depuis les lois de bioéthique de 1994.
Pr. Didier SICARD - Le regard porté depuis 1994 sur le progrès scientifique en matière de procréation et de réparation du corps humain me paraît privilégier, de façon quelquefois un peu excessive, une sorte d'avenir radieux de la recherche, comme si la société n'avait plus de débat de conscience et qu'elle ne se plaçait que sous la bannière du progrès scientifique. Nous sommes fascinés devant le clonage animal, la fécondation d'un ovule par un spermatozoïde, les avancées promises par les cellules souches adultes, d'ailleurs inimaginables pour moi il y a dix ans. Mais autant ces progrès sont fascinants, autant ils doivent nous encourager à une grande prudence dans notre façon d'aborder notre humanité et les principes sur lesquels nous sommes fondés. Ce n'est pas du conservatisme ou du fixisme mais l'accélération doit nous encourager à un regard de plus en plus large alors que, paradoxalement, il se rétrécit sur quelques avancées spectaculaires. Je suis aussi fasciné qu'inquiet.
M. Francis GIRAUD, rapporteur - Nous souhaiterions également, Monsieur le Président, connaître vos réflexions sur la recherche sur l'embryon, la création et l'organisation, prévue dans la loi de l'APEGH, la brevetabilité du corps humain, le transfert post mortem d'embryons et les dons d'organes. Toutefois, notre principale préoccupation, depuis ce matin, concerne les problèmes de recherche sur l'embryon. De nombreux points peuvent être soulevés et l'ont été particulièrement à propos de la recherche sur les cellules embryonnaires. Peut-elle être menée à partir des embryons surnuméraires notamment ? Quels sont les résultats déjà obtenus ? Quels espoirs, entre guillemets, pouvons-nous envisager ? Parallèlement à cette recherche sur les cellules embryonnaires et aux bénéfices que nous pourrions en tirer pour les malades, où en sommes-nous pour ce qui concerne les cellules souches adultes ? Quels bénéfices pouvons-nous en attendre et à quel terme ? Ce problème visant à améliorer la santé des malades pose des problèmes éthiques et nous souhaiterions savoir si vous pensez qu'il est licite d'utiliser ces embryons surnuméraires et les cellules pouvant en être obtenues.
Pr. Didier SICARD - Je vais essayer d'être clair vu la vaste étendue des sujets. Pouvons-nous au XXI e siècle mener une recherche sur l'embryon ? J'aurais tendance à répondre très simplement oui. En effet, nous ne jouons pas à pile ou face la vie et je crains que notre humanité ne reporte sur l'enfant ou sur le foetus, ainsi projeté dans une sorte de recherche post conceptuelle, ce qu'elle n'aurait pas voulu réaliser sur l'embryon.
Mon idée repart de la question, sans doute déjà évoquée à plusieurs reprises, celle de l'ICSI qui est désormais la technique quasiment majoritaire pour la procréation assistée avec près de 20.000 tentatives en France. Le pourcentage de naissances avec cette technique est de l'ordre de 25 à 27 %. Nous pouvons donc dire que l'ICSI est devenue actuellement la méthode numéro un de procréer in vitro .
Comme vous le savez, cette technique a été mise au point quasiment sans expérimentation animale dans les années 60. Nous pouvons, par conséquent, nous interroger sur le fait de conduire des expérimentations sur l'être humain né ou intra-utérin avant de le faire sur l'embryon d'autant plus qu'actuellement, des projets d'introduction, intra ovocytaires non plus de spermatozoïdes mais de cellules jeunes et immatures, des spermatogonies (cellules souches de spermatozoïdes) apparaissent. Cela me paraît de la folie de jouer ainsi avec la vie en affirmant que puisque nous ne pouvons pas travailler sur l'embryon, nous allons tenter de fabriquer un foetus, un être humain constitué qui va naître à l'occasion d'une expérimentation. Comme nous sommes dans une situation scientifique qui, depuis 25 ans, a fait de l'embryon congelé au nom de la procréation in vitro une sorte de non-retour possible, la notion même de recherche sur l'embryon me paraît s'intégrer dans ce que la médecine a toujours fait, c'est-à-dire travailler sur l'être humain tout en respectant un certain nombre de concepts.
Ce n'est pas mépriser ou considérer l'embryon comme une chose que de pouvoir travailler sur lui-même et améliorer ainsi le futur de la conception in vitro . Toutefois, quand nous affirmons cela, nous ne disons pas grand-chose.
En effet, les 80.000 ou 100.000 embryons surnuméraires à notre disposition en France, sorte de matière première disponible, même s'il peut être scandaleux de les qualifier de la sorte, nous posent un problème éthique majeur. En effet, ils ont été constitués dans un but de procréation pour donner un être humain ; l'objectif futur, justement, est que les embryons surnuméraires n'existent plus. Nous ne pouvons donc pas projeter sur ces embryons surnuméraires le futur de l'embryon pour la recherche. Pouvons-nous les utiliser actuellement ? Nous devons être très humbles.
A partir du moment où les parents sont informés de ce projet, un travail psychologique considérable est, ici, à mener et doit, éventuellement, être plus marqué dans la loi. Ce n'est pas parce que les embryons vont être utilisés pour la recherche qu'ils ne sont pas respectés, simplement le projet parental est abandonné. Commencer une recherche sur des embryons surnuméraires, dans des conditions extrêmement rigoureuses, me paraît possible et, actuellement, je ne vois pas d'autre possibilité. En effet, créer des embryons pour la recherche nous bloque dans une sorte d'interdit fondateur ; c'est un peu comme si notre humanité portait un regard méprisable sur ce qui la fonde. Mais l'ambiguïté apparaît si nous proposons que les spermatogonies, dans le cadre d'un projet d'enfant, pour subir une évaluation doivent passer par une tentative de fécondation avec un ovocyte, et donc par la création d'un embryon, voué à la destruction...
Que signifie, en pratique, l'évaluation de la faisabilité de cette technique sans la création, de facto , d'un embryon pour la recherche ? Nous pouvons éventuellement interdire formellement, définitivement, l'utilisation de spermatozoïdes immatures dans un cadre de projet de procréation, mais, dans la situation actuelle, en l'absence d'expérimentation animale valable et toujours difficilement adaptable à l'espèce humaine, nous devrions peut-être admettre cette transgression majeure de créer, dans ce cas, un embryon pour la recherche.
En effet, je ne vois pas comment nous pouvons nous lancer dans une expérimentation humaine sur l'enfant plutôt que sur l'embryon. Pouvoir utiliser les embryons surnuméraires comme donneurs de cellules embryonnaires et pouvoir évaluer leur capacité à produire des lignées cellulaires me paraît, dans l'histoire de la science, une possibilité. En la refermant, nous risquons, paradoxalement, la création, dans d'autres pays, d'embryons pour la recherche et cela pourrait nous contraindre à une transgression encore plus grande.
Nous devons, dans un premier temps, nous approcher progressivement de ce qui est réalisable, avec le consentement d'une société, qui a, probablement, accepté que des recherches, permettant de savoir si les lignées cellulaires sont orientables, puissent être menées sur des embryons nécessairement voués à la destruction. Cela me paraît, actuellement, un projet acceptable.
En revanche, créer spécifiquement un embryon pour la recherche en dehors de tout projet de procréation me paraît, dans l'état actuel de notre société, inacceptable. Or, le projet de loi me semble, dans ce domaine, créer une certaine ambiguïté puisqu'il interdit la création d'embryons pour la recherche et, en même temps, il impose l'évaluation des nouvelles techniques médicales de procréation. Je ne vois pas comment on peut, en même temps, interdire la création d'un embryon pour la recherche et évaluer une nouvelle technique de procréation. Nous pouvons simplement énoncer que l'insuffisance de l'expérimentation animale, qui ne donnera jamais la réponse, suppose que, pour les nouvelles techniques d'assistance médicale à la procréation, la prudence l'emporte sur l'enthousiasme comme si le futur de la médecine dépendait de la recherche sur l'embryon.
Je ne suis pas un spécialiste des cellules souches embryonnaires, vous avez entendu les remarquables spécialistes que sont Axel Kahn et Arnold Munnich. Mon sentiment, assez extérieur, est que même si la recherche à ce propos s'active dans le monde entier, en particulier en Angleterre et que les publications s'accumulent, il est incertain d'en déduire un futur thérapeutique proche. Je suis toujours gêné par cette coalescence entre les discours scientifiques et de la recherche et le futur thérapeutique.
Autant la recherche sur l'embryon, sur l'homme, sur la connaissance fondamentale, permettant de découvrir la manière dont les premiers gènes forment des protéines, orientant l'organisation du foie par exemple, est riche, que ce soit pour le cancer ou l'ensemble de la génétique. Autant affirmer que la recherche sur les cellules souches embryonnaires doit être menée d'urgence car le futur de la sclérose en plaque ou d'une autre maladie neuro-dégénérative va en dépendre me semble, non seulement bien trop précoce mais aussi bien ambigu dans la façon de vouloir récolter immédiatement des fonds pour obtenir les moyens de fonctionnement.
Cependant, je me suis déjà trompé car je n'imaginais pas, il y dix ans, que l'ICSI pourrait donner des enfants et parce que je n'ai pas anticipé le clonage de Dolly. Au fond, la science ne survient jamais dans la prévision mais toujours dans la brutalité et par crises. Notre connaissance actuelle des cellules souches embryonnaires me semble fondamentale sur le plan de la recherche, mais dans le domaine thérapeutique elle me paraît infiniment plus hasardeuse. En outre, avec les risques que nous constatons chez l'animal de oncogénicité, c'est-à-dire de cancer, lié à ces cellules souches un être humain accepterait difficilement de recevoir des cellules souche embryonnaires. Des tentatives d'introduction de cellules embryonnaires issues d'embryons provenant d'avortement ont eu lieu, mais les résultats sont moyens. Les promesses thérapeutiques sur le plan nerveux ne sont pas aussi impressionnantes que ce que l'on peut affirmer.
Quant aux cellules souches adultes, elles ne posent pas tellement de problèmes éthiques car elles sont théoriquement disponibles et leur emploi thérapeutique existe depuis vingt ans. En effet, une greffe de moelle est, par excellence, une greffe de cellules souches adultes hématopoïétiques.
J'interrogeais, il y a une heure et demie, le professeur Duboc, l'un des premiers, en France, à avoir mis dans le myocarde des cellules hématopoïétiques, de la moelle. Il avait alors eu la surprise de constater que, dans un infarctus du myocarde, ces cellules de la moelle, à visée hématologique, se transformaient en cellules cardiaques. Il m'affirmait cependant que cela reste de la recherche et qu'il ne faut pas imaginer de changements considérables pour le futur. Des cellules souches adultes ont également été mises dans les artérites. Les tentatives existent donc, mais ces promesses des cellules souches adultes s'inscrivent dans le long terme. Nous ne pouvons pas en faire la panacée et pas non plus ne pas mener de travail sur les cellules souches embryonnaires au prétexte que les cellules souches adultes vont donner des réponses satisfaisantes. Nous sommes actuellement à une période de balbutiement et même si dans vingt ans cela paraîtra peut-être enfantin, nous ne devons pas formuler de promesses trop tôt.
A propos de l'APEGH, je ne peux qu'être favorable à ce qu'une Agence bien structurée fonctionne. Cependant, elle doit disposer de moyens matériels pour que, vu ses ambitions, elle ne se retrouve pas dans les conditions, quelquefois misérables, de fonctionnement de la précédente commission de la biologie de la reproduction. Si elle est soutenue au niveau matériel, elle ne peut qu'être utile en permettant de concentrer les projets.
En revanche, j'émettrai deux réserves. Premièrement, la notion d'autorisation me gêne, c'est-à-dire faire de cette Agence une commission de censure, ou d'agrément aboutirait à court-circuiter le débat parlementaire. Si, dans ce domaine si difficile, la société, délègue au Parlement le soin de prendre ces décisions importantes, ce dernier doit garder la capacité de dire oui ou non après la réception d'un avis éclairé de cette commission, elle-même extraordinairement soutenue et sérieusement constituée.
Vous allez penser que je prêche pour le CCNE mais mon deuxième point de réserve concerne la mention, dans le projet de loi, selon laquelle cette commission n'est pas obligée mais « peut » saisir le CCNE sur les problèmes éthiques qu'elle rencontre. Sur le plan éthique, la relation entre le comité et cette commission devrait être plus confiante et plus étroite ; « doit plutôt que peut » s'applique à la relation entre CCNE et cette nouvelle commission.
Le troisième point, la non-brevetabilité du corps humain, entraîne des débats d'un volume considérable. A mon avis, nous devons revenir à des choses très simples. Nous sommes dans une situation très grave dans laquelle la science est obsédée, pour des raisons financières, par la brevetabilité du gène. Les jeunes chercheurs d'une trentaine d'année me frappent par leur obsession notamment encouragée par leurs instances scientifiques, c'était peut-être insuffisamment le cas il y a trente ans, de breveter un gène ou des cellules souches.
A mon avis, dans quelques années, l'embryon humain sera brevetable. Nous profiterons d'une lignée cellulaire obtenue à partir d'un embryon humain dans lequel nous aurons inséré un gène l'encourageant à fabriquer des cellules souches embryonnaires d'excellente qualité pour le coeur ou le foie. Quelques cellules souches embryonnaires se développeront beaucoup plus vite avec ce nouveau gène de croissance. Cet embryon humain, comme la souris de Harvard, sera alors breveté. Une sorte d'enchaînement, venu de la notion de brevetabilité du gène existe ici.
Mais à mesure que les années passent, nous nous apercevons que notre société est de plus en plus résistante à cette notion fictive de la brevetabilité d'un gène. En effet, un gène est une fiction en même temps qu'une réalité. Ce n'est qu'une structure continuellement encouragée, découragée et stimulée puisqu'un gène n'a d'efficacité que parce qu'il interagit avec un autre. Certains exemples de gènes totalement autonomes existent mais ils sont probablement très rares. Un gène éteint, par exemple, va pouvoir être « réveillé » par la stimulation d'un autre gène.
Par conséquent, breveter un gène « hors » du corps humain ou « dedans » ne diffère pas tellement. Breveter un gène en tant que tel, fut-il hors du corps humain, me paraît être un péché contre l'esprit. J'ai le sentiment, en Europe, d'une résistance croissante à cette vision très économique et commerciale de la recherche sur le gène. Paradoxalement, cela peut empêcher la recherche dans la mesure où, Axel Kahn a dû vous en donner quelques exemples, si un chercheur veut s'approcher d'un gène pour travailler dessus avec un objectif radicalement différent, il va se trouver obligé de payer des « royalties ». On m'opposera qu'elles ne sont pas considérables et que le chercheur doit bien être indemnisé. Cependant, elles constituent, de fait, un obstacle à un travail de recherche exploratoire.
Le transfert d'embryons post mortem ne me semble pas un sujet si important que cela, peut-être moins que les autres. Les débats, à propos d'affaires médiatisées, me paraissent excessifs. Transférer un embryon post mortem signifie que l'enfant sera né d'un père mort. Nous ne pouvons pas tirer argument du fait qu'un enfant issu d'une famille monoparentale a autant de chances que les autres, et les débats sont un peu vains dans ce domaine. La seule idée pouvant être avancée est qu'à partir du moment où la fécondation in vitro se fonde sur la congélation d'embryons, si le père meurt, la possibilité de transfert post mortem pourrait être alors un encouragement à cette pratique ; l'habitude d'implanter un embryon lorsque le père est décédé pourrait ainsi augmenter. Mais, à mon avis, les cas seront tellement rares et encadrés par la loi que, devant ces situations exceptionnelles, la société avec indulgence, compassion ou générosité pourrait les autoriser sous le contrôle de l'Etat et de cette éventuelle commission sans en produire ni encouragement, ni en faire une interdiction. A mon avis, ce n'est pas le problème fondamental de la procréation in vitro .
Sur le don d'organes, l'élargissement du cercle des donneurs vivants ayant avec le receveur une relation directe et stable pose-t-il un problème ? Nous voyons très bien le risque de déviance. La France, dans ce domaine, est en retard car si la greffe, avec l'Etablissement français des greffes, a réalisé des progrès énormes, nous ne sommes pas encore en tête du don d'organes. Par rapport aux Catalans, par exemple, nous accusons un certain retard. En Europe, nous sommes parmi ceux qui prélèvent le moins à partir de donneurs vivants. L'élargissement doit être mis en place puisqu'un rein prélevé sur un donneur vivant est de meilleure qualité que celui d'un donneur mort. Ici encore, une commission doit pouvoir statuer sur le risque d'une pression psychologique excessive.
En Angleterre, un enfant peut donner son rein à son père ou à sa mère, ce qui me choque profondément car, pour moi, il est éthiquement insupportable de profiter de ses enfants. Les Anglais trouvent cela bien et il serait imaginable que la loi, par l'encouragement fait ainsi aux donneurs vivants, permette ce transfert de l'enfant vers ses parents. Nous pouvons envisager tous ces types de déviances. Mais, en tout cas, l'élargissement des possibilités de don me paraît acceptable en particulier pour le rein. Pour le foie, cela demeurera rare compte tenu du risque létal. Encadrer en fonction du caractère « affectif » me paraît extrêmement difficile, mais il faut quand même rester très vigilant. Toutefois, la loi me semble, dans ce domaine, aller dans le bon sens. Je ne vois pas comment nous pourrions interdire cet élargissement.
M. Jean CHERIOUX - Tous les propos entendus depuis ce matin nous donnent un sentiment d'effroi car, finalement, nous devrons décider de ce que sera la loi, et suivant que nous ouvrons une porte ou la laissons fermée, nous pouvons aboutir à des situations absolument extraordinaires qui pourraient se révéler dangereuses. Vous nous avez expliqué la nécessité de la recherche sur les embryons surnuméraires notamment à cause des dangers de l'ICSI. Lors de l'élaboration de la loi en 1994, nous comptions, justement, sur ce type de pratiques pour essayer d'éviter les embryons surnuméraires. Vous nous affirmez qu'un danger existe à cause de l'absence de possibilités de réaliser des expérimentations. Ne pouvez-vous pas, quand même, recueillir des renseignements sur les enfants nés ainsi et évaluer les éventuels inconvénients par l'étude de certaines cellules ou tissus ? Au cas où cela s'avérait très dangereux, la meilleure solution ne serait-elle pas, pour le moment, de l'interdire et, dans le cadre de la procréation médicalement assistée, de n'admettre que certaines pratiques ?
Pr. Didier SICARD - Comme toujours, toute interdiction comporte des désavantages. Actuellement, nous travaillons sur l'ICSI de façon très importante car nous avons été saisis par la Défenseure des enfants. Nous savons que l'ICSI ou la fécondation in vitro double, approximativement, le risque d'avoir un enfant porteur d'une malformation congénitale, génétique ou d'une stérilité. L'enfant pourrait donc hériter d'une stérilité transmise. Pour le moment, ce n'est qu'un risque puisque les enfants concernés ne sont âgés que de dix ans. Les Australiens semblent cependant avoir déjà démontré, je ne sais pas comment, que quatre fils nés par ICSI d'un père stérile seraient stériles. Le contournement de la stérilité peut probablement la transmettre.
Nous sommes face à une question éthique majeure dans la mesure où nous encourageons, quasiment consciemment, la mise au monde d'enfants porteurs d'une mutation ou d'une malformation. Mais mes propos sur l'ICSI et les embryons surnuméraires se plaçaient dans deux cadres différents.
Dans le cadre d'un consentement de projet de recherche, une étude sur le développement des cellules des embryons surnuméraires, peut, éventuellement, de façon très liminaire, être menée sur ceux voués à la destruction. Ici, à mon avis, un travail considérable de peut-être dix ans est à mener mais il ne nous apportera pas énormément de résultats sur l'ICSI. L'ambiguïté est que toute nouvelle technique de procréation expérimente sur l'enfant et non pas sur l'embryon. Cela me paraît grave dans la mesure où nous allons reporter sur ces 20.000 tentatives le soin de répondre dans quinze ou trente ans. Ces personnes développeront-elles, par exemple, des cancers du rein ou des gliomes ? Notre société oublie qu'elle joue avec la procréation en privilégiant l'immédiat, le fait d'avoir un enfant. Elle oublie les conséquences pouvant en découler justement sur ces enfants.
Depuis dix ans, l'ICSI a permis à des stérilités masculines, c'est-à-dire environ 40 ou 50 % des stérilités, d'avoir des enfants se portant, apparemment, parfaitement bien et, dans 98 %, procurant un grand bonheur à eux-mêmes et à leurs parents d'être nés. Nous ne pouvons donc pas diaboliser l'ICSI, mais dire simplement que notre pays souffre d'une faiblesse structurelle d'évaluation. Nous sommes le dernier pays européen à évaluer, nous lançons toujours des initiatives mais nous ne sommes jamais capables d'apporter au monde et à l'Europe des chiffres précis. L'évaluation du suivi des enfants nés par fécondation in vitro aurait dû être une priorité et elle devrait encore l'être, il est encore temps. Mais cette évaluation fait un peu crier, certains affirmant que cette évaluation supposerait une discrimination. Les enfants nés par fécondation naturelle ne sont pas surveillés, pourquoi le feriez-vous uniquement sur les enfants nés par ICSI ? Nous pouvons tout à fait mettre en place des groupes témoins, ce n'est pas du tout un obstacle. En tout cas, le suivi me semble fondamental et devrait faire partie des fonctions de la nouvelle Agence. En effet, nous ne pouvons pas nous interroger sur le début si nous ne disposons pas de la réponse quelques dizaines d'années après.
M. Jean CHERIOUX - Monsieur le professeur, pourquoi être plus exigeant en matière de suivi et d'étude des conséquences de la naissance de l'enfant lorsqu'il est fécondé in vitro alors que nous ne préoccupons pas de ceux nés par les méthodes naturelles ? Vous voulez absolument tout savoir sur le devenir de ces enfants issus d'une fécondation in vitro alors que vous ne posez pas la question sur les millions d'enfants naissant autrement.
Pr. Didier SICARD - Non, car nous ne pouvons pas transformer les 758.000 naissances en un processus d'évaluation biologique. Nous transformerions alors la condition humaine. Pour quelle raison chaque être humain ne serait-il pas obligatoirement évalué ? Cela pourrait se révéler attentatoire à une sorte de liberté fondamentale. Ce n'est pas pour obtenir des résultats scientifiques que chaque être humain vivant doit être observé ; certains échapperont toujours, et ce seront peut-être ceux qui donneront des informations. En revanche, et la santé publique en est capable, comme dans toute étude, d'établir des groupes témoins, la fécondation in vitro devrait réellement être évaluée, parce qu'elle concerne entre 10.000 et 15.000 enfants par an. Les chiffres nous manquent en France, nous sommes l'un des pays réalisant le plus de fécondations in vitro mais nos résultats ne sont plus, comme dans les années 90, les meilleurs, pour plusieurs types de raisons. L'une des exigences absolues de santé publique, c'est un lieu commun, est de pouvoir apporter une réponse non dans les trois ou six mois mais à deux, cinq ou dix ans, en particulier au moment de l'âge scolaire. Cependant, nous devons l'effectuer avec beaucoup de subtilité pour éviter une stigmatisation de l'enfant. Ce serait tout à fait monstrueux, par exemple, de convoquer pour un entretien, le jeudi à 16 heures avec le médecin psychologue les enfants numéro deux ou quatre nés par fécondation in vitro . Effectivement, cet enfant a peut-être le droit d'ignorer les conditions de sa naissance. Les problèmes psychologiques posés ici sont plus difficiles que l'on peut l'imaginer.
M. Nicolas ABOUT, président - Monsieur le professeur, le professeur Degos a commencé son exposé par des pensées très philosophiques sur « l'homme est-il sujet ou objet ? », « quand, où apparaît ou disparaît le sujet ? » . Vous, par contre, avez débuté votre propos en posant la question de savoir si notre société ne privilégiait pas une sorte d'avenir radieux de la recherche comme si elle se plaçait sous la bannière unique de la science. Ne proposiez-vous pas, alors, d'adopter, pardonnez-moi l'expression, une éthique élastique suggérant de nous lancer puisque, de toute façon, d'autres vont le faire ? Basez-vous vos propositions sur des valeurs que vous estimez transcendantes ou premières ?
Pr. Didier SICARD - A mon avis, l'éthique opportuniste ne peut se prévaloir du mot éthique. Les pays ne peuvent pas se rallier au moins disant éthique. Nous ne devons pas être obsédés par une recherche menée aux Etats-Unis qui bafouerait nos valeurs et, sous prétexte d'un avenir radieux justement, nous obligerait à nous aligner. A mon sens, les valeurs sont supérieures aux promesses. La question est « en quoi notre regard sur l'homme, nos références, est-il de nature à maintenir une certaine dignité de lui-même ? » Mon inquiétude est toujours de voir comment le désastre peut être fondé sur une sorte d'interdiction de la recherche car celle-ci favorise le contournement. Nous devons mieux, quelquefois, être conscient que l'homme a toujours été un objet de recherche et qu'il est en même temps sujet et objet. Laurent Degos a raison, quand nous sommes malades, nous sommes objet du soin et nous restons un sujet. Cela crée, d'ailleurs, l'ambiguïté contemporaine à propos de la recherche sur l'embryon. J'ai beaucoup travaillé avec les Allemands, qui ont inscrit dans l'article un ou deux de la Constitution l'interdiction absolue de travailler sur l'embryon. Cette interdiction est formelle ; mais paradoxalement, les Allemands font des contournements, avec la plus grande bonne foi, pour essayer de pouvoir travailler sur l'embryon en maintenant cet article constitutionnel. Cela risque d'aboutir à des perversions avec l'importation de cellules embryonnaires à l'origine incertaine. Les objectifs thérapeutiques ne doivent pas être mis en avant sans interrogation fondamentale d'ordre éthique. Ethiquement, l'objectif de recherche fondamentale sur la connaissance me paraît l'emporter sur la recherche thérapeutique.
M. Nicolas ABOUT, président - Nous avons entendu tout au long de cette journée, que nous devions accorder plus de mérite aux cellules souches adultes. Cependant, mon souvenir était que les résultats ne se révélaient pas encore extrêmement probants. Par exemple, dans l'utilisation de cellules au niveau cardiaque nous arrivions à des différenciations vers une fibre musculaire mais nous ne parvenions pas à coordonner la contraction de ces cellules avec celles du myocarde. Par conséquent, nous doutions encore complètement de l'efficacité de ces cellules que nous réussissions à développer in situ . Dans votre spécialité, vous obtenez des résultats avec les cellules souches, mais des résultats véritablement probants sont-ils constatés dans d'autres secteurs ?
Pr. Didier SICARD - Je ne suis pas spécialiste de la question. Un article est sorti il y a quelques mois sur le traitement des artérites par des cellules souches alors que je ne m'attendais pas à ce que cela soit possible. Je ne voyais pas comment une artère bouchée pouvait en bénéficier. L'introduction de cellules souches hématopoïétiques a permis la création de néovaisseaux aboutissant à une amélioration. Cependant, nous en sommes vraiment à une ère balbutiante et tout peut s'écrouler. L'espace nous séparant d'une réalité thérapeutique est beaucoup plus grand que ce que l'on croit.
M. Gilbert BARBIER - Le législateur est confronté au véritable problème de définir les limites de la recherche hexagonale face à l'universalité de cette dernière. Nous risquons de retrouver, comme par le passé, nos chercheurs obligés de franchir des paliers parce qu'ils n'ont pas suivi les évolutions ailleurs dans le monde. Ne courons-nous pas le risque de nous enfermer dans un carcan trop pesant et précis et laissant notre pays en retard ?
Pr. Didier SICARD - C'est l'éternelle inquiétude. Mais, par exemple, si le Vanuatu, dans des conditions absolument sauvages, en injectant des cellules d'enfants dans des êtres humains, s'aperçoit que cela guérit une maladie, nous ne devrions pas pour autant nous aligner. J'ai pris le Vanuatu parce que c'est, pour moi, un pays presque imaginaire, mais c'est un mauvais exemple car justement c'est un pays qui a une grande tradition culturelle ! Si une équipe scientifique, sans réflexion éthique, obtient des résultats inattendus nous ne sommes pas coupables pour autant de ne pas la suivre. La recherche fondamentale doit précéder la recherche appliquée qui, au fond, dépend de l'excellente qualité de la première. C'est la recherche sur le processus cellulaire qui devrait être financée ; malheureusement, ce n'est pas le cas. Le financement d'une recherche fondamentale relève, éventuellement, du rôle de l'Etat en France plus que de l'investissement de laboratoires privés généralement plus indifférents aux questions éthiques. En même temps, il ne faut pas être trop angoissé. C'est la raison pour laquelle, d'ailleurs, j'avais suggéré, un travail commun entre Français et Allemands. En effet, les Allemands bloqués vont importer leurs cellules embryonnaires d'Israël, d'Australie ou d'Argentine. Nous aurions pu, calmement, mener une recherche fondamentale entre Français et Allemands qui sont, au fond, dans la même culture. Nous aurions pu, éventuellement, commencer à travailler, prochainement sur les embryons surnuméraires, mais l'interdiction absolue de la recherche sur l'embryon nous placerait dans une situation bloquée.
M. Nicolas ABOUT, président - Monsieur le professeur Sicard, vous pouvez nous délivrer un dernier message. Vous souhaitez certainement aborder des domaines qui ne l'ont pas été.
Pr. Didier SICARD - Mon premier point se réfère à l'extension du dépistage préimplantatoire. A partir du moment où les parents consentent une recherche sur leur embryon, nous pouvons très bien imaginer une extension à l'infini du DPI. Nous devons faire attention à un eugénisme rampant pouvant surgir à cette occasion. Nous avons été saisis, par exemple, de la possibilité ou non de la conception d'un embryon indemne d'une maladie génétique et, en même temps, compatible sur le plan immunologique avec son frère ou sa soeur déjà nés pour lui venir en aide. Finalement, avec beaucoup d'embarras, nous avons pensé que c'était possible si l'embryon était indemne d'une maladie génétique. Cependant, nous ouvrons une porte gigantesque. Ici, nous sommes dans un nouveau rapport au temps. La mère ne supporte pas que son enfant meure et se demande si la médecine ne peut pas lui venir en aide. Mais en même temps, quel est le destin de l'enfant à naître ? Nous sommes dans une aporie dans le rapport au temps avec une situation immédiate d'un côté et, de l'autre, un enfant à naître, donc toute une vie. Le rapport entre les deux est quasiment impensable. La limite à l'extension du DPI, doit, à mon avis, s'inscrire de façon plus rigoureuse dans la loi.
Le deuxième thème peut sembler dérisoire mais peut-être pas sur le plan culturel. L'article L. 1211-7-1 dans le livre II du titre VIII, je crois, se rapporte à la « reconnaissance de la Nation ». La France a toujours été un pays qui a beaucoup aimé donner un brevet à ceux qui témoignent, de leur générosité aux donneurs de sang, par exemple. Les médailles pour ces derniers ne m'ont pas toujours paru très éthiques, parce qu'elles encouragent celui qui veut obtenir une médaille de vermeil, et cela peut être ambigu. La notion de reconnaissance de la Nation à celui qui donnerait son corps ne me paraît pas forcément à encourager. En effet, il s'agit ici du domaine du privé et de l'intime et de donner un gage de reconnaissance de la Nation ne me paraît pas nécessaire. Enfin, ce point de vue est marginal. Aucun autre pays ne me semble avoir inscrit une telle disposition et cette spécificité française peut, paradoxalement, sembler ambiguë.
Mon point suivant aborde l'autopsie qui a disparu en France, comme dans un très grand nombre d'Etats, sauf dans les pays scandinaves. Les Etats-Unis sont dans la même situation que la France. Le projet de loi actuel reprenant la loi de 1994, ne change quasiment rien. Nous avions souligné que les données de santé publique, fondées sur une imagerie, ne donnent pas d'information réelle sur les causes de la mort. Nous avons moins de données épidémiologiques sur les causes de la mort en 2002 qu'en 1982. Systématiquement demander le consentement de la famille a abouti, de fait, à une impossibilité de l'autopsie. En effet, nous ne supportons pas que des gens que nous aimons soient autopsiés alors que nous-mêmes sommes probablement indifférents à cette situation. Nous nous trouvons dans une situation antagoniste entre le consentement personnel et celui de la famille. Par conséquent, le progrès sur les maladies dégénératives, cérébrales est totalement interrompu depuis une dizaine d'années à cause de cette interdiction. Sur le plan médical, c'est une relative tragédie puisque nous avons d'un côté de très grands projets sur les cellules souches embryonnaires et adultes et de l'autre une interdiction absolue de l'autopsie de fait. Au lieu de travailler sur l'embryon, nous devrions pouvoir continuer à mener des études sur l'homme mort. Une autopsie médicale ne signifie pas un non-respect de la personne décédée. Dans ce domaine, la loi n'a pas pris en compte nos propositions sur le retour à l'autopsie. Cependant, certains considéraient que la loi protégeait l'être humain de l'autopsie comme si elle était une agression, ce que je ne crois pas.
Enfin, je veux aborder le sujet de notre structure, le Comité consultatif national d'éthique. Elle est, non pas fragile, mais comme elle dépend, pour son intendance, de l'INSERM, une certaine ambiguïté est créée par ce manque d'autonomie. En effet, l'INSERM dispose de son propre comité d'éthique et même s'il n'intervient en aucune façon dans les débats, nous voudrions une indépendance plus grande. Une structure non dépendante de l'INSERM apporterait plus de clarté et de maturité. D'ailleurs, les comités nationaux d'éthique se créant dans le monde ont une autonomie supérieure à la nôtre et la loi pourrait en tenir compte.
M. Nicolas ABOUT, président - Parlez-vous d'une autonomie financière, d'une absence de tutelle, etc. ?
Pr. Didier SICARD - J'avais demandé au Président de la République son accord pour lui être rattaché comme le comité national allemand l'est à la Chancellerie. Il m'avait fait part de son embarras et précisé que beaucoup d'organismes formulaient cette demande. Je suis réintervenu à plusieurs reprises pour demander le rattachement, comme celui, par exemple de la commission contre le dopage qui est soumise au seul contrôle de la Cour des Comptes. Par exemple, je ne peux pas inviter des Américains ou des Allemands à un colloque, je suis bridé par des questions de choix de mise à disposition de ressources sur lesquelles mon autonomie est dérisoire. Nous vivons dans des conditions de grande rigueur et plus d'indépendance nous serait favorable.
M. Nicolas ABOUT, président - Je vous remercie beaucoup de la réflexion que vous nous avez apportée.
G. AUDITION DE M. SADEK BELOUCIF, PROFESSEUR D'ANESTHÉSIE-RÉANIMATION AU CHU D'AMIENS, M. MICHEL GUGENHEIM, GRAND RABBIN, DIRECTEUR DU SÉMINAIRE ISRAÉLITE DE FRANCE, M. PATRICK VERSPIEREN, THÉOLOGIEN, DIRECTEUR DU DÉPARTEMENT D'ÉTHIQUE BIOMÉDICALE DU CENTRE SÈVRES, M. GEOFFROY DE TURCKHEIM, PRÉSIDENT DE LA COMMISSION oeCUMÉNIQUE DE LA FÉDÉRATION PROTESTANTE DE FRANCE, M. STÉPHANE MEYER, MÉDECIN, CONSEILLER DE L'ORDRE DU GRAND ORIENT DE FRANCE
M. Nicolas ABOUT, président - Messieurs, en vous invitant à participer à cette table ronde sur la bioéthique, nous souhaitons donner au débat toute sa dimension philosophique et humaine, au sens le plus noble du terme. Comme le rappelait l'un des professeurs, il s'agit de l'homme sujet et non pas objet et qui, donc, doit être respecté dans son intégrité et dans son être. Nous souhaitons donc bénéficier de vos réactions, remarques et propositions sur ces sujets.
Notre table ronde est retransmise sur Public Sénat, notre débat doit donc être le plus animé possible et les interventions brèves et synthétiques. Afin d'éviter une succession de monologues, nous aborderons les différents thèmes les uns après les autres.
M. Francis GIRAUD, rapporteur - Depuis ce matin, à l'occasion de ce projet de loi relatif à la bioéthique, nous avons entendu de nombreux exposés passionnants. L'un des sujets les plus importants de notre réflexion concerne la recherche sur l'embryon, non pas uniquement dans un but cognitif, mais également à cause des espoirs suscités dans l'opinion publique, dont on nous a rappelé aujourd'hui qu'ils n'étaient pas envisageables à court terme et qu'ils demeuraient incertains, que ce soit pour les cellules embryonnaires ou adultes. Nous aimerions avoir vos réflexions sur ce qui peut être réalisé avec l'embryon. Dans le projet de loi, il est inscrit que la recherche est interdite mais une ambiguïté existe avec une mention qui autoriserait la recherche à partir d'embryons surnuméraires conçus dans le cadre d'une PMA. Vos avis sur cette question fondamentale seront écoutés très attentivement car les choix se révèlent extrêmement difficiles.
Pr. Sadek BELOUCIF - Je vous remercie de me permettre de représenter l'expression d'une sensibilité. Je n'entends pas vraiment parler de religion dans un espace laïc, républicain et citoyen au sens rappelé par le professeur Huriet, mais exprimer une valence spirituelle ou humaine. Pour l'Islam, l'homme est unique.
Le Coran indique : « Nous vous avons créés d'un mâle et d'une femelle. Nous vous avons constitués en peuples et tribus pour que vous vous connaissiez entre vous. Le plus noble d'entre vous auprès de Dieu est le plus pieux d'entre vous » (...) « Si Dieu avait voulu, Il aurait fait de vous une communauté unique : mais Il voulait vous éprouver en Ses dons. Faites assaut de bonnes actions vers Dieu. En Lui, pour vous tous, est le retour. Il vous informera ce qu'il en est de vos divergences. »
J'interprète cette unicité de l'homme comme une condamnation du clonage reproductif. L'embryon ou l'embryogenèse sont décrits avec beaucoup de détails dans le Coran. Il s'agit de rappeler son origine humble à l'homme par ces phrases : « Nous avons créé l'homme d'une quintessence d'argile puis Nous en fîmes une goutte de liquide, déposé en un réceptacle sûr, puis ce peu de liquide, Nous le créâmes adhérence, et créâmes l'adhérence mâchure, et créâmes la mâchure ossature, et revêtîmes l'ossature de chair, après quoi Nous le promûmes d'une toute autre création . »
Pour un musulman, cela renvoie au concept d'animation retardée et au débat théologique persistant entre une animation immédiate ou retardée. Personnellement, je ne sais pas si la fécondation est un mystère ou une énigme. Avec la notion d'animation retardée, je me demande si le vrai changement de paradigme n'intervient pas avec la nidation, au moment où cette goutte s'accroche dans un réceptacle sûr. Nous pourrions, dès lors, imaginer que cette espèce de grumeau de cellules et la personne humaine potentielle après l'accrochage sont différents.
M. Nicolas ABOUT, président - Cette remarque est très intéressante puisque c'est également une nidation qui va permettre l'organisation spatiale de cet amas cellulaire.
Dr. Stéphane MEYER - En tant que médecin, ce passage de la nidation, de l'accrochage de l'oeuf me semble intéressant. Cependant pour élargir le débat et ne pas rester dans la théologie de chacun au sein de notre république laïque, nous devons prendre du recul par rapport à toutes les émergences religieuses afin de rester laïc et républicain.
L'intérêt de vos questions et de votre quête porte, pour moi, sur cette recherche sur l'embryon créé un peu par hasard et dont nous pourrions nous servir parce qu'il est là. Pire encore, cette recherche pourrait concerner les embryons issus des IVG avec les difficultés humaines se présentant, pour la mère, d'accepter que l'enfant qu'elle a refusé puisse servir et non pas uniquement disparaître. A mon sens, au risque de provoquer, ce symptôme révèle notre besoin d'embryons pour le progrès de la science, bien entendu encadrée par les lois et les médecins. Cette nécessité de recherche nous met mal. Mais nous devons aller au-delà et nous, vous, les décideurs, devons réfléchir aux moyens d'aider l'évolution de la science dans un but, évidemment humaniste et médical et surtout pas mercantile. Vous savez à quel point la France se trouve seule dans le mercantilisme ambiant au niveau planétaire. Nous devons donc rester très vigilants sur ce qui sera fait.
M. Nicolas ABOUT, président - Estimez-vous, docteur, que la recherche ne doit pas être simplement menée sur des embryons surnuméraires mais que vous envisagez, éventuellement, la création d'embryons pour la science ?
Dr. Stéphane MEYER - Nous, les décideurs, devrons peut-être un jour poser cette question pour faire avancer le débat. Tout le monde n'est peut-être pas mûr aujourd'hui pour entendre cela mais nous serons peut-être obligés de nous poser cette question tous ensemble.
M. Geoffroy de TURCKHEIM - La question sur la recherche sur l'embryon est évidemment la plus difficile de celles que vous nous avez soumises. Les églises protestantes, que je représente, disposent de l'avantage et de l'inconvénient d'être diverses, nous sommes une fédération d'églises et donc une seule opinion protestante n'existe pas. Par conséquent, et cela concerne tous les citoyens français, votre décision fera à la fois des satisfaits et des mécontents. Je ne dis pas dans quelle proportion puisque cela n'a pas d'importance. Enfin, toutes les églises s'accordent pour la nécessité d'une décision rapide car nous ne pouvons pas rester dans le flou actuel avec toutes les possibilités de contournement déjà évoquées.
Même en ayant suivi attentivement les débats de ce matin, je ne suis pas compétent pour affirmer si le projet de loi comporte des ambiguïtés comme cela semble avoir été relevé, notamment sur le sujet de savoir si oui ou non la loi autorise la création d'embryons. Ici, nous devons vous faire confiance, législateurs, pour améliorer ce passage.
Parmi les différentes églises, les satisfaits et les mécontents seront aussi nombreux et nous retrouverons un peu la même ligne de partage que pour l'IVG. D'ailleurs, nous parlons moins de cette question mais j'ai aimé l'idée du professeur Nisand suivant laquelle la réflexion n'avait peut-être pas été suffisante sur la portée morale de l'IVG. La fédération protestante avait approuvé la reconduction de la loi Veil en 1979. Mes références s'expliquent car, pour certaines églises, le recours à l'embryon surnuméraire, qui peut s'assimiler à une IVG, sera une deuxième chance pour l'embryon qui aura quand même une utilité. Au contraire, pour d'autres églises ce sera comme une deuxième mort.
M. Nicolas ABOUT, président - Je tiens à vous remercier ainsi que M. Beloucif car vous avez pu assister quasiment à la totalité des auditions. Je souhaiterais que, plus tard, vous nous donniez votre sentiment pour savoir si votre approche en a été modifiée dans certains domaines.
M. Patrick VERSPIEREN - Je suis amené à représenter une sensibilité catholique. Tout grand courant de pensée a le droit et le devoir de s'exprimer parce que tout citoyen a le droit de faire part de ses convictions et d'être représenté de différentes façons. A propos de l'utilisation d'embryons humains pour la recherche, les catholiques sont appelés à voir en l'embryon humain un être, en toute première phase de développement, qui appartient déjà à l'humanité. Ce qu'il est ne peut pas dépendre, uniquement, du genre d'attentes placées en lui. Par conséquent, je ne veux pas me placer dans la perspective de ceux qui pensent qu'un regard différent peut être porté sur l'embryon selon qu'il est porteur de telle attente ou tel projet. Ce qu'est l'embryon ne dépend pas non plus purement et simplement de son seuil de développement. En tout cas, l'Eglise catholique appelle à voir en l'embryon, dès la conception, un être humain qui ne peut pas être un objet disponible ou traité comme une chose. L'Eglise catholique va donc réprouver ce qui serait de l'ordre de la chosification ou, en termes un peu plus savants, de la « réification » ou de l'instrumentalisation, c'est-à-dire la soumission à une recherche suivie de rejet. Le Parlement et le Sénat, en 1994, avaient décidé de ne pas s'opposer à toute recherche, mais à celles qui lèsent l'embryon avec une règle analogue, par certains côtés, à celle concernant la recherche sur l'être humain, adulte ou enfant.
Nous parlons, aujourd'hui, de l'utilisation d'embryons humains pour le prélèvement de cellules souches embryonnaires au sujet desquelles les scientifiques nourrissent beaucoup d'espoirs. Mais, la question est de savoir si un embryon humain peut être utilisé ou instrumentalisé ainsi pour recueillir ces cellules. Dans cette chosification, je vois une certaine négation de l'humanité de l'embryon, l'instauration d'un seuil d'humanité. Ici, je fais référence à la tendance actuelle, de vouloir réserver la notion de personne et même peut-être d'humanité à ceux qui possèdent certaines capacités. Si nous commençons à penser que l'humain ne doit pas être respecté à une phase particulière parce qu'il n'a pas encore acquis telle ou telle capacité, le grand danger est d'en venir à manquer de respect à ce que l'on peut appeler « l'homme sans qualité », celui notamment qui a perdu toutes ses capacités mentales. Le respect de l'humain est indivisible de la conception à la mort, même si les modalités du respect peuvent changer.
Nous disposons de nombreux embryons en congélation qui ne pourront pas être transférés. Cependant, avoir fécondé sans prudence des milliers d'ovocytes ne donne pas, pour autant, le droit d'utiliser ces embryons. En fait, l'un des véritables problèmes éthiques est celui de la limitation des fécondations. Le projet de loi prévoit un droit à la parole donné aux parents à propos du nombre de fécondations. C'est une question essentielle car la loi n'a pas encore abordé le sujet du nombre d'embryons créés au moment d'une PMA. Des milliers d'embryons ne pourront plus être transférés mais cela n'aurait pas de sens de continuer la conservation de ces embryons indéfiniment. Il faudra donc, sous le regard de la loi, prendre la décision d'y mettre fin. Mais cela ne justifie pas d'employer ces embryons humains pour la recherche ou pour prélever sur eux des cellules. Cela serait déjà une instrumentalisation. Un degré supplémentaire serait franchi avec la création d'embryons pour la recherche ou comme réserves de cellules. Le projet de loi a vraiment raison de distinguer, d'une part, l'utilisation et, d'autre part, la création d'embryons pour la recherche.
M. Nicolas ABOUT, président - Monsieur Michel Gugenheim, êtes-vous plus proche de la théorie selon laquelle l'embryon a un statut dès sa conception, de l'idée d'après laquelle cela commence à la nidation ou du propos suivant lequel on fait ce que l'on veut ?
M. Michel GUGENHEIM - Je vous remercie, monsieur le président de m'avoir invité pour faire entendre la sensibilité juive.
Le judaïsme dispose, en ce domaine, d'un point de vue qui lui est propre, le fameux concept des quarante jours. Le Talmud à plusieurs reprises, énonce cette formule étonnante a priori , selon laquelle jusqu'à quarante jours, c'est de l'eau et que donc, le statut de l'embryon n'existe pas vraiment. Cela ne signifie pas pour autant que l'IVG soit autorisée aux yeux du judaïsme. La grande originalité du judaïsme, à mon sens, est, qu'au-delà du statut de l'embryon, existe l'argument de la potentialité. En effet, si nous n'avons pas encore un embryon mais quelque chose faisant que, potentiellement, le futur embryon deviendra un être humain, nous ne pouvons déjà plus nous opposer à son développement. Cette idée débouche sur la différence fondamentale entre un embryon in vivo et in vitro . Pour nous, c'est totalement différent. Si, par exemple, un congélateur conservant des éprouvettes tombe en panne et provoque la destruction des embryons, nous ne considérons pas que c'est une mise à mort, un avortement comme lorsqu'il est mis fin à une grossesse en gestation in vivo . Notre argument est logique puisque la potentialité n'existe pas ou elle est beaucoup plus faible. En effet, un bébé in vivo naît au bout de neuf mois sans avoir besoin de quelque manipulation technique que ce soit. Par contre, si vous ne touchez pas à un embryon congelé, deux siècles plus tard il en sera toujours au même stade. Le projet de loi concernant la recherche sur les embryons surnuméraires, par définition embryons congelés, se révèle, donc, pour nous, tout à fait acceptable. De plus, cela contribue à l'avancée de la recherche, sur laquelle le judaïsme porte un regard très positif puisqu'elle fait partie de la mission donnée à l'homme de garder le jardin, mais aussi de le cultiver. Nous ne posons donc pas d'obstacle fondamental à la mise en place d'une recherche sur les embryons surnuméraires.
Par contre, le deuxième point m'a beaucoup étonné car, lors de ma lecture du projet de loi, je n'avais pas vu la possibilité offerte de créer des embryons. Une ouverture de ce type serait un problème complètement différent. Créer un embryon, pour nous, se révèle tout un problème pour des raisons qui vous paraîtront probablement saugrenues. En effet, pour créer un embryon, à moins de passer par un clonage, ce qui a été radicalement exclu, un prélèvement de sperme est obligatoire. Cela nous pose un problème très grave. Nous l'autorisons, bien sûr, pour venir en aide à un couple infertile car, dans ce cas ce n'est pas une extraction vaine. Il s'agit simplement d'étendre l'insémination de manière un peu plus artificielle et, au final, un projet de naissance est envisagé. Par contre, pour un projet de recherche, le prélèvement de sperme est totalement impossible.
M. Francis GIRAUD, rapporteur - Pour expliciter le deuxième alinéa, je précise que la loi avait effectivement prévu, pour l'évaluation des techniques de PMA, de créer des embryons. Un problème se pose effectivement ici et nous devrons trancher ce débat.
M. Jean CHERIOUX - Ce qu'a dit M. Beloucif à propos de la nidation a attiré mon attention puisque c'est le seul moyen pour que la transposition dans la loi suive de près la nature. L'embryon créé in vitro l'est pour être implanté et ce transfert est la nidation réalisée artificiellement. Donc, s'il n'est pas transféré à ce moment, il change en quelque sorte de nature et se trouve dans la même situation que l'embryon qui n'a pas été nidé naturellement et qui se trouve expulsé. En outre, d'après les informations délivrées tout à l'heure, 80 % sont expulsés naturellement. Le sort normal de l'embryon n'ayant pu être transféré est sa disparition. Comme l'a dit l'un des professeurs, nous ne le supprimons pas, mais nous mettons fin à sa conservation. Ensuite, il disparaît comme celui qui ne s'est pas nidé dans le corps de la femme.
M. Nicolas ABOUT, président - En effet, cet amas de cellules ne s'oriente pas, ne se structure pas, ne se différencie pas. Une potentialité existe donc, mais pas véritablement une organisation. C'est la nidation qui crée une réaction, une auto-induction permettant le développement.
Mme Gisèle PRINTZ - Toutes les auditions auxquelles nous avons assisté ont été présentées par des hommes. Nous ne parlons jamais de la femme et ces sujets sont abordés de façon un peu froide...
M. Nicolas ABOUT, président - Nous n'avons pas non plus parlé du père.
Mme Gisèle PRINTZ - Je trouve que ce discours est un peu froid et cela me gêne. Je voudrais aussi ajouter que tous les sujets abordés aujourd'hui suscitent des peurs quand nous voyons ce que nous pourrions réaliser avec des embryons.
Dr. Stéphane MEYER - Nous ne devons pas pouvoir faire ce que l'on veut, selon l'une des hypothèses du Président. La loi doit pouvoir brider tout le mercantilisme pouvant graviter autour de ce douloureux problème des maladies génétiques. En effet, c'est douloureux pour ceux qui en souffrent, qui perdent un enfant par une IVG ou autrement, pour ceux qui sont stériles. Le chercheur a un devoir de recherche et nous, au moins au sein de cette assemblée, devons lui donner les moyens de travailler légalement et à l'abri du mercantilisme. Ces deux notions sont, pour moi, fondamentales.
Voici maintenant une notion qui n'a rien à voir mais qui me semble importante. Autant la vie, la mort et l'avant-vie sont profondément sacrées, autant nous semblons admettre moins difficilement la recherche sur les cadavres. Depuis Ambroise Paré, qui ne pouvait pas effectuer tout ce qu'il voulait, nous avons réalisé beaucoup de progrès. D'ailleurs, un intervenant, tout à l'heure, demandait d'autoriser les autopsies pour faire avancer la science. Généralement, tout le monde peut comprendre cela relativement facilement. Par contre, l'avant-vie, je veux dire que je ne vivais pas du temps de Napoléon ou des rois mages, s'ils ont existé, et que je ne serai plus là demain, doit aussi être prise en compte pour la survie de l'espèce et pour que les chercheurs travaillent en toute sérénité.
Pr. Sadek BELOUCIF - Pour reprendre les propos du docteur Meyer, nous avons effectivement eu une discussion, dans le pays, sur la fin de vie au sujet des patients en réanimation et qui souffrent entourés d'un appareillage compliqué. L'avis du comité d'éthique avait fait appel à un texte du Pape, assez ancien, qui distinguait, entre guillemets, des moyens ordinaires et extraordinaires de maintien de la vie. Cela déborde sur la question de savoir si c'est de l'euthanasie passive de remettre en cause les moyens extraordinaires mis en oeuvre par le médecin, animé d'une obstination déraisonnable proche de l'acharnement thérapeutique.
Nous avons parlé de potentialité. L'intention, celle de l'homme qui vaut plus que ses actes, est aussi une notion forte. Nous pouvons imaginer que les embryons dits surnuméraires, la sémantique n'est pas anodine, qui sont dans un congélateur à - 80°, survivent par des moyens extraordinaires. Dès lors, si leur destinée est la conservation ad vitam aeternam ou la destruction, nous pouvons nous demander si nous pouvons l'utiliser à des fins de recherche.
Personnellement, j'imagine soit un distinguo subtil similaire à celui de 1994 du Parlement énonçant l'autorisation d'études mais l'interdiction de recherches soit, plutôt que la destruction, une ouverture limitée et très encadrée de la recherche. En effet, les embryons étaient créés au départ par la recherche et non pour elle, l'intention était donc là. Elle est tout à fait différente. Dès lors, nous pourrions choisir le moindre des deux maux.
M. Bernard CAZEAU - Je voudrais revenir sur la notion de nidation. Dans le cursus de l'embryogenèse, la nidation arrive après la fécondation. L'organisme, il est vrai, en rejette 80 % pour des raisons très diverses, qui peuvent être pathologiques ou dues à une mauvaise embryogenèse. Il ne faut pas non plus oublier, concernant les méthodes de contraception, que les dispositifs intra-utérins empêchent, justement, la nidation. Nous pouvons donc nous accorder ou pas sur le stade, ce qui n'a rien à voir avec le problème de la destination de l'embryon, mais nous ne pouvons pas affirmer, comme il a été dit, je crois, que c'est de l'eau jusqu'au moment de la nidation.
M. Nicolas ABOUT, président - Ceci est symbolique, notamment avec la traversée du désert.
M. Patrick VERSPIEREN - Sur la notion de fin mise à la conservation, nous pouvons très bien le faire pour des embryons humains sans prendre position sur ce qu'ils sont. Les conserver pourrait se rapprocher de la notion de « traitement extraordinaire » qui renvoie à une très longue tradition. De même que, pour des humains pleinement reconnus comme tels, arrêter des moyens de préserver la vie est sage dans certaines situations, de même, pour l'embryon, stopper la conservation n'est pas forcément une prise de position sur ce qu'il est. Je plaide pour cette distinction entre la notion de fin mise à la conservation et celle de l'utilisation pour la recherche.
M. Geoffroy de TURCKHEIM - J'ajoute juste une précision sur le fait que vous laissiez entendre, Monsieur le président, que les autres églises ou religions admettaient que l'on puisse faire ce que l'on voulait. Je ne suis pas intervenu sur la question du statut de l'embryon, expression souvent utilisée, et semble-t-il abandonnée, au moins sur le plan législatif, car les théologiens protestants ont renoncé à donner un statut à l'embryon de même que, dans les textes de lois de bioéthique, l'homme n'a pas de statut particulier, il est un sujet moral et peut être aussi objet. L'embryon est un élément de vie, à l'évidence, mais il n'a pas de statut particulier transcriptible sur le plan juridique et qui permettrait d'énoncer des autorisations ou des interdictions.
M. Nicolas ABOUT, président - Ceci est un vrai problème, même en droit français. En effet, un médecin n'ayant pas voulu volontairement mettre fin à la vie d'un foetus n'est pas poursuivi. A l'inverse, s'il laisse vivre un enfant, des arrêts célèbres le montrent, porteur d'une maladie sans l'avoir informé, il fera l'objet de poursuites. Il s'agit donc d'un vrai sujet de fond pour tout le monde.
M. Francis GIRAUD, rapporteur - Je souhaiterais que les membres de cette table ronde puissent nous livrer leur idée sur l'évolution des mentalités de la population française depuis 1994, notamment par rapport à la médiatisation assez forte sur tous ces problèmes. Quelles sont les réactions des courants de pensées que vous représentez ?
Ensuite, la deuxième question concerne l'inscription de la brevetabilité du corps humain dans cette loi et à sa mise en concordance ou non avec les directives européennes.
Nous souhaiterions donc connaître votre avis sur l'évolution des mentalités et la brevetabilité du corps humain.
M. Michel GUGENHEIM - Au sujet de la brevetabilité, on ne peut pas parler véritablement de position, officielle ou non, du judaïsme et cela relève plus de la réflexion personnelle. La difficulté, ici, réside, en fait, dans la tension entre deux intérêts, entre le risque, en brevetant, de brider l'accueil aux soins, et ne le faisant pas, de manquer de moyens commerciaux pour la recherche. Sur ce point, il n'y a pas véritablement de point de vue religieux pouvant, à mon sens, s'exprimer. Simplement, d'une certaine manière, on pourrait demander un brevet sur une découverte sur le corps humain même si ce n'est pas une invention. En effet, nous sommes quand même en face d'un savoir-faire, et nous comprenons que le découvreur ait un droit dessus, notamment de le monnayer. Cependant, si, dans ce cas, cela aboutit à une interdiction de l'accès aux soins, cela devient un peu comme un trouble de l'ordre public.
M. Nicolas ABOUT, président - M. Meyer me semble suivre votre avis ?
Dr. Stéphane MEYER - Je suis tout à fait d'accord. En fait, la grande différence classique entre découvrir et inventer existe. Les découvertes, au niveau du génome, doivent rester dans le patrimoine planétaire et, en aucun cas, une appropriation ne doit être possible. Là-dessus, la France, avec votre aide, conserve une position très ferme, contre l'avis de la majorité de l'Europe, qu'il faudra maintenir pour contrer tous les projets mercantilistes de rachat du corps humain sous toutes ses formes. A l'inverse, l'invention d'une thérapeutique provient de la recherche et a un coût. Par conséquent, ces médicaments ou thérapeutiques pourraient être brevetés voire monnayés. Toutefois, le risque est que leur accès soit réservé aux plus riches au détriment des plus pauvres. Ici encore, nous nous trouvons à la limite entre ce qui doit être fait et ce qui est intolérable. Nous sommes dans la même situation pour le sujet qui nous préoccupe puisque nous naviguons entre les innovations thérapeutiques et l'eugénisme. Vous, législateurs, devez trouver le juste milieu entre ces deux extrêmes pour les uns exceptionnels et pour les autres intolérables.
M. Patrick VERSPIEREN - Mon point de vue est assez personnel mais je l'ai exprimé devant les instances de mon église. La principale question me paraît être une question de justice sociale et internationale, plus encore que du respect du corps. Au nom de quoi un découvreur, parce qu'il dispose d'une petite avance, va accaparer les connaissances ? Nous devons réfléchir sur cette question difficile. Personnellement, il me paraît sage de bien marquer la différence entre découverte et invention. Mais, j'insisterai, moi aussi, sur la question de justice sociale.
M. Nicolas ABOUT, président - Monsieur de Turckheim, partagez-vous l'idée de la nécessité de faire une différence entre la découverte et l'invention ? Peut-on breveter un gène ou une technique permettant, par exemple, de corriger une anomalie ?
M. Geoffroy de TURCKHEIM - Cette distinction reste tout à fait pertinente. Elle était très chère à France Quéré qui nous disait souvent, en comité d'éthique, qu'une découverte n'est pas brevetable, contrairement à une invention. Je suis sensible à certains arguments, développés ce matin, selon lesquels certains procédés découlant de découvertes devraient, hélas, dans la logique du système, être brevetés. Le législateur ne pourra pas éviter, ici, une certaine ouverture mais dans le domaine des inventions et surtout des applications.
Sur la brevetabilité, le professeur Degos a attiré notre attention sur la commercialisation. Que l'homme, ou une partie de son corps, puisse devenir un objet de commerce est ce qui suscite le plus de peurs.
A propos des mentalités, point sur lequel nos églises sont assez vigilantes, le concept même de bioéthique est passé dans les moeurs et est pris très au sérieux aujourd'hui alors que, tout à fait au début, certains philosophes qui ne voulaient pas s'enfermer dans une démarche éthique particulière et qui pensaient qu'elle était une discipline générale qui n'avait pas à s'instrumentaliser dans un domaine particulier, formulaient des réticences. Evidemment, ce sont les gens les plus sensibles à ces questions, et parfois aussi les plus audacieux, entre guillemets, qui se montrent sensibles à la réflexion bioéthique pour, en quelque sorte, s'encadrer eux-mêmes. J'ai entendu parler ce matin, je ne sais pas si le terme « mentalité » était utilisé mais il était quand même sous-jacent, de mentalité latine, judéo-chrétienne ou anglo-saxonne. J'ai alors un peu tressailli car ce sont des concepts relevant aujourd'hui de l'image d'Epinal et ce sont des schémas un peu douteux. En effet, par exemple, pour le don d'organes, la Norvège, pays luthérien à 90 %, a le même genre de pratique que le Portugal, pays catholique et latin. D'autre part, la France et l'Allemagne partagent des points de vue très rapprochés, pour des raisons d'ailleurs différentes. Nous savons évidemment le grand souci de l'Allemagne concernant toutes les questions d'eugénisme. J'ai beaucoup apprécié ce que disait le Professeur Munnich, tout en contestant ses références à la latinité, sur le modèle français. Celui-ci est effectivement cité en référence dans d'autres pays. A mon avis, il pourra faire ses preuves s'il pose des interdictions, s'il reste très ferme sur certaines positions, s'il sert, d'abord à encadrer, mais aussi si, parallèlement, il demeure ouvert, audacieux et permettant quelques transgressions dans certains domaines. J'utilise, ici, l'expression du ministre Mattei qui expliquait récemment que la médecine avait souvent progressé, entre guillemets, par des transgressions. Elles doivent cependant être provisoires. La recherche sur l'embryon est, d'ailleurs, un type de transgression pour lequel les médecins nous demandent de franchir le pas. Mais, c'est dans le cadre de ce modèle français, que nous pourrons prendre des décisions sages.
Pr. Sadek BELOUCIF - Au sujet des brevets, je reste touché par la différence entre invention et découverte. Nous pourrions, par rapport au gène, opposer de façon binaire deux conceptions, l'une considérant qu'il constitue un nouveau Far West ou une nouvelle frontière, et l'autre prenant en compte une inspiration plus rousseauiste. La proposition du professeur Axel Kahn de revenir à la formulation ancienne : « en tant que telle, la connaissance totale ou partielle d'un gène ne peut faire l'objet d'un brevet » permet pleinement de différencier le travail mécanique d'un séquenceur automatique par rapport à la valeur ajoutée intellectuelle qui doit mériter salaire.
Pour les conséquences sociales ou l'évolution des mentalités, nous craignons tous les dérives de certains scientifiques, espèces de docteur Folamour ou Frankenstein, qui seraient des fabricants de raison sans foi. Bien sûr, le Prophète disait : « les savants sont les héritiers des prophètes . » Cette parole signifie que la science, quand elle est belle, est synthétique et intègre le sacré et le profane. Elle est élaborée par des scientifiques responsables de leurs connaissances, et plus nous sommes savants, plus nous devons être responsables. Cette peur peut entraîner des réactions sociales fortes. Il y a plus de dix siècles les philosophes mutazilites, les rationalistes de l'Islam, disaient aux Omeyyades qui les persécutaient : « Nul n'est tenu d'obéir à une créature, fut-elle un calife, lorsqu'il s'agit d'entrer en rébellion contre le Créateur . » Nous pourrions tous nous dire que nous avons nos propres desseins et destins et récuser ces lois, un peu comme Antigone s'opposant au roi Créon proclamait : « Je ne croyais pas tes édits, qui ne viennent que d'un mortel, assez forts pour enfreindre les lois sûres, les lois non écrites des dieux . » Cependant, l'ensemble de ce qui nous réunit est bien plus fort que ce qui nous distingue ou nous sépare. Sur ce sujet, c'est la république qui va élaborer le religio ou le religare .
M. Nicolas ABOUT, président - Oui, cependant lorsque nous essayons de définir la bioéthique, nous ne faisons que tenter d'approcher ces lois non écrites. Cette tâche se révèle bien difficile.
M. Gilbert BARBIER - Nous abordons la question fondamentale, notre charge de légiférer sur ce sujet. En écoutant vos conceptions sur les problèmes de l'embryon, nous n'avons jamais évoqué le fait qu'une trop grande restriction pourrait empêcher de sauver des vies. En effet, cette recherche a quand même pour but d'essayer de soulager certains de nos concitoyens, notamment atteints de maladies dont la guérison pourrait passer par les thérapies évoquées. Même si ce travail sur l'embryon doit être extrêmement encadré et soumis à quelques interdictions, en ne l'autorisant pas du tout, nous nous privons, tout de même, de soulager et, éventuellement, de sauver des vies. C'est cette question que nous devons garder à l'esprit.
Ma deuxième question serait de connaître votre attitude face à des chercheurs qui, tout en appliquant la loi, transgresseraient les données de votre religion. En ce qui me concerne, j'ai un souvenir très douloureux, Nicolas About s'en souvient. Je suis catholique et, étant parlementaire en 1979 au moment du renouvellement de la loi Veil, j'ai reçu des menaces d'excommunication de dignitaires de l'Eglise. Cela m'a profondément marqué parce que j'ai voté la reconduction de la loi. Bien sûr, depuis 1979, les choses ont beaucoup changé. Quelle serait votre attitude devant l'évolution de la loi ?
M. Nicolas ABOUT, président - A l'époque, nous avions une tâche effectivement difficile. M. Beloucif évoquait, à l'instant, une époque où le prophète et le savant étaient deux personnages. Nous sommes en présence de deux personnes différentes mais, dans le temps, elles n'étaient qu'une, donc, il était simple pour le prophète de penser ce que devait penser le savant, et pour le savant de savoir ce que devait penser le prophète. Aujourd'hui, nous sommes dans l'obligation d'écrire la loi et nous nous tournons vers vous pour tenter de recevoir l'avis, peut-être pas des prophètes, mais, en tout cas, de ceux qui réfléchissent encore plus que d'autres à ces sujets.
Dr. Stéphane MEYER - Vous parliez, tout à l'heure, du discours ambiant. Malheureusement, notre recherche du bien-être à tout va n'est pas compatible avec ce que nous voudrions aujourd'hui faire. L'important, aujourd'hui, est l'éradication de la maladie. Nous allons peut-être nous trouver face à des cancers, qui n'ont pas lieu d'être évoqués ici, nous ne sommes pas en séance médicale. Mais, nous devons nous demander de quels moyens nous sommes capables de nous doter au-delà du bien-être moral ou physique de chacun. En parlant de bien-être moral, j'évoque toutes les restrictions intellectuelles de chacun, pour le bien-être physique je pense à l'eugénisme que pourrait engendrer le simple fait de procéder à une échographie pour choisir le sexe de l'enfant. Le coeur du débat réside dans cette question : sommes-nous capables, aujourd'hui, de nous donner les moyens, au risque d'une excommunication, d'aller jusqu'à la volonté d'éradiquer une maladie potentielle ou non, quelles que soient les inimitiés ou le mal-être pouvant être engendrés ?
M. Patrick VERSPIEREN - Pratiquement tout le monde, dans la société française, s'accorde pour donner une grande importance à la valeur santé. Notre pays doit se mobiliser contre la maladie. C'est un grand acquis de notre histoire et nous n'avons pas à revenir dessus. Les églises ont, d'ailleurs, beaucoup travaillé en ce sens et l'histoire montre que ce sont elles qui se sont investies au départ. En fait, la question est celle des limites.
Mon point de vue, depuis un certain temps, reposant d'ailleurs sur des expériences personnelles et douloureuses, mais rejoignant l'intuition de fond du christianisme, est que nous risquons de perdre le respect et le souci des personnes très âgées affaiblies par des polypathologies et ne relevant plus d'une médecine très technique. Cette question me hante. N'oublions-nous pas alors nos préoccupations de santé ? Que faisons-nous, notamment dans les services de gérontologie, pour les personnes très âgées ? Personnellement, j'ai connu une personne très âgée qui n'intéressait plus personne. Elle était, par exemple, acceptée dans un service de pneumologie, pour des prélèvements dans le poumon, en chirurgie pour tel acte chirurgical, mais ensuite il n'y avait pas de service de médecine générale apte à l'accepter. J'insiste beaucoup sur ce problème et je pense que tout cela rejoint le respect de l'embryon. D'accord, nous devons oeuvrer contre la maladie, mais cela ne signifie pas aller toujours plus loin dans la recherche. Il faut, certes, la développer, mais nous devons, aussi, avoir d'autres préoccupations, notamment celle de l'accueil des personnes qui ont besoin surtout de « soins ».
M. Geoffroy de TURCKHEIM - J'ai, peut-être, manqué de clarté, mais des églises comme l'église luthérienne d'Alsace et de Moselle approuvent le principe de la recherche sur les embryons et, en particulier, sur les surnuméraires. Ils développent sensiblement les mêmes arguments que ceux invoqués lors de l'approbation de la reconduction de la loi Veil, à savoir que ce recours à l'avortement était légitime en cas de situation de détresse y compris, comme en 1984, en cas de détresse sociale de la mère. Donc, un peu de la même manière, dans le cas de situation de détresse thérapeutique, nous savons que nous pouvons y mettre fin. J'ajoute, sans aucun esprit de provocation ni même sans que ce soit une demande, que certaines églises évangéliques plutôt conservatrices sur le plan des moeurs, notamment à propos de l'IVG, auraient préféré que les recherches soient menées sur les embryons issus du clonage thérapeutique que sur les surnuméraires. Elles ont une intuition éthique à propos de ces derniers les conduisant à penser que ce n'est pas bien de les utiliser. Cela rejoint la question de M. Degos : un embryon est-il un embryon ? Je n'insiste pas mais vous voyez qu'il y a là quelque chose.
M. Francis GIRAUD, rapporteur - Nous allons aborder le problème des dons d'organes. Effectivement, ce n'est pas une nouveauté mais la loi promulguée en janvier 2002 a, en particulier, élargi le cercle des donneurs vivants à toute personne ayant avec le receveur une relation étroite et stable. Que vous inspire cette modification de la loi française ?
Pr. Sadek BELOUCIF - Je n'ai pas de commentaire particulier. On peut donner parce qu'on est doué, on a reçu le don d'être compatible à cet être cher. Je me placerai peut-être plus sur un plan médical en reprenant la distinction du professeur Degos entre les organes uniques et doubles. Le don de rein ne me pose pas de problème à condition qu'une information pertinente et claire soit transmise. Les dons de foie, par contre, occasionnent des soucis d'anesthésie et de réanimation tout à fait particuliers.
M. Nicolas ABOUT, président - Quelle est votre position sur la greffe du foie ?
Pr. Sadek BELOUCIF - Les chirurgiens hépatiques peuvent réussir à dédoubler un foie. Cette question n'est pas philosophique mais médicale. Vous savez que deux donneurs de foie sont morts et cela pose des soucis d'information. Il faut bien se rendre compte que ce qui se passe est parfois soucieux.
M. Gilbert BARBIER - Pouvez-vous élargir votre réflexion au prélèvement d'organes post mortem ?
Pr. Sadek BELOUCIF - Pouvoir donner est non seulement un acte de gentillesse mais également un acte de grâce. L'Islam n'est absolument pas réfractaire au don d'organes. Au contraire, une première réunion en Jordanie en 1986 ou 1987 énonçait que c'était faire preuve d'adoration que de pouvoir donner. Une deuxième conférence multirégionale se réunit au Caire en décembre et la France va être représentée par son ambassade et le professeur Houssin, accompagné de membres du comité d'éthique pour pouvoir plaider dans ce sens.
M. Michel GUGENHEIM - Les autorités rabbiniques ne voient aucun problème en ce qui concerne le prélèvement d'organes sur des personnes vivantes. La question du lien plus ou moins éloigné entre le donneur et le receveur ne pose strictement aucun problème. Par contre, la problématique renvoie au risque pour le donneur. La question n'est pas tellement « avons-nous le droit » mais plutôt « est-ce recommandé ou même obligatoire ». La réponse consiste à dire que le prélèvement est d'autant plus recommandé qu'il n'y a aucun risque pour le donneur et d'autant moins quand un danger existe. Sur ce plan, je me suis aperçu que le débat entre les autorités rabbiniques ne provient pas, finalement, du principe rabbinique, mais des différents médecins, avec des avis différents sur le prélèvement de rein, par exemple, consultés par les rabbins. En tout cas, nous n'avons aucune opposition si nous nous en tenons au projet de loi qui autorise mais, bien sûr, en demandant l'accord express du donneur.
Paradoxalement le sujet deviendra plus délicat pour un prélèvement post mortem , ceci pour une raison simple, c'est que, pour le prélèvement sur vivant, la personne est là pour donner son accord. A notre avis, le bât blesse un peu quand on présume d'un consentement nullement exprimé. Effectivement, si la personne n'a pas donné l'autorisation de son vivant, il est difficile de présumer qu'il l'a donnée. En outre, dans le judaïsme, le respect dû au corps est une valeur extrêmement importante, plus que dans le monde ambiant où, bien sûr, une dépouille ne va pas être maltraitée inutilement. Cependant, d'un autre côté, comme la personne est morte, on considère que son corps peut être utilisé. Nous ne partageons pas cette idée : pour nous, le corps qui a vécu et été l'écrin d'une âme, conserve un statut sacré. Pour sauver une vie, toutefois, mais seulement hic et nunc , il est possible de porter atteinte à ce corps, mais uniquement dans ce cas. Par contre, un prélèvement dans le cadre de la recherche est strictement interdit car la démarche s'inscrit dans le long terme.
M. Nicolas ABOUT, président - Vous ne formulez pas d'opposition si l'accord a été donné par le défunt avant sa mort.
M. Michel GUGENHEIM - S'il y a son accord, nous n'avons aucun problème.
M. Gilbert BARBIER - Le droit appartient-il à la famille ?
M. Michel GUGENHEIM - C'est un problème de droit complexe qui n'a pas été réellement tranché. A priori nous pourrions avancer que la famille n'est pas titulaire des droits du défunt. Le judaïsme est aussi attaché à l'affirmation que le défunt reste titulaire de ce qui lui appartient après la mort. De quel droit même un frère, ou un fils, pourrait-il s'approprier ce qui ne lui appartient pas ?
M. Patrick VERSPIEREN - Dans le don d'organes, le catholicisme voit un véritable geste de générosité et de solidarité humaines. Il approuve donc véritablement le don d'organes. Cependant, cette approbation porte sur le don, ce qui suppose une véritable liberté et la gratuité. Si ce n'est pas gratuit, s'il n'y a pas une véritable liberté et si la décision est prise sous certaines pressions trop fortes, il n'y a pas vraiment don. C'est le problème principal du don d'organes par un donneur vivant.
Paradoxalement, une certaine distance vis-à-vis de la famille permet, éventuellement, une plus grande liberté. Ayant organisé un colloque sur le don d'organes du vivant, j'ai perçu qu'il existait des pressions familiales. Votre responsabilité comme législateur est de prendre des mesures pour préserver, dans la mesure du possible, un don suffisamment libre. Vous prenez certaines précautions avec, notamment, le comité d'experts dont je ne sais pas s'il est bien nommé. Un problème est celui d'un éventuel commerce lorsque le donneur est extérieur à la famille. Vous devez prendre des précautions pour éviter cela, mais la liberté concerne la famille. Vous devez vous assurer qu'une certaine distance est respectée, que tout sera arrêté si trop de pression est perçue. Le comité d'experts pourrait-il recevoir toute personne proposant un don ? Je pose cette question à titre personnel. La loi doit également protéger la personne contre un excès de générosité. Je pense ici à des prélèvements présentant des risques, comme celui d'une partie de foie, spécialement sur des personnes présentant des fragilités de santé. Renvoyez-vous toute la responsabilité sur le médecin préleveur ? Exigerez-vous, en plus de la loi, des bonnes pratiques cliniques, pour résoudre ce problème de la protection contre des risques trop importants ? Cela me paraît une question importante.
Sur le prélèvement post mortem , le corps après la mort n'appartient à personne, et évidemment pas à la famille. Cependant, là n'est pas la question. Au nom de mon église, je suis très réservé quant à tout ce qui traiterait le corps après la mort comme un objet, une pure chose ou une forme de nationalisation des corps. Cela suppose que des paroles soient échangées. Un consentement du défunt avant sa mort doit être recherché mais en l'absence de cela, je cite ici les évêques français, « il ne serait pas humain de prélever en cas d'opposition de la famille ». Il ne s'agit pas de propriété mais de sensibilité et de tradition. La famille a un rôle et j'ai même entendu des médecins, travaillant dans les prélèvements d'organes, parler de leur épreuve quand il s'est agi d'un de leurs enfants. Ce genre d'événement est très traumatisant et, donc, il faut s'organiser pour permettre la parole. Il ne faut pas résoudre la question en optant systématiquement pour le prélèvement, ce n'est pas humain. Un grand effort a été justement réalisé dans les hôpitaux avec la mise en place de coordinatrices qui permettent l'échange de paroles. Je terminerai en affirmant qu'il ne serait pas humain de prélever en cas d'opposition de la famille car elle peut n'être pas persuadée de la mort dans la mesure où la personne, lors du prélèvement, présente des apparences de vie.
M. Geoffroy de TURCKHEIM - Je ferai une réponse analogue sur ces sujets dans le sens où ce sont des actes graves et risqués méritant d'être accompagnés sur le plan psychologique. En même temps, sur le plan moral ou éthique, de telles dispositions ne paraissent pas condamnables. Ce sont des gestes graves mais pas condamnables moralement. Je reprendrai, ce n'est peut-être pas la question, les propos récents du ministre selon lesquels les conditions de prélèvement d'organes sur les personnes décédées doivent être améliorées. Je constate auprès de l'opinion publique, des aumôniers d'hôpitaux et des familles que la loi est soit mal connue, soit interprétée de travers. Les médecins semblent très réticents à l'appliquer à la lettre. Pour les raisons venant d'être évoquées, ce sujet est très difficile mais une possibilité doit être trouvée pour sortir, non pas de ce flou juridique car la loi est claire et même trop pour être appliquée telle quelle, mais de cette situation.
Pr. Sadek BELOUCIF - Je veux juste évoquer un point très court pour aller dans le sens de la protection que plaidait M. Verspieren face aux donneurs vivants. Dans le projet de texte apparaît une ambiguïté suite à une modification de la rédaction. En effet, au départ la commission devait donner un avis non motivé, mais un amendement a modifié cette disposition en indiquant que, désormais, il doit l'être. A mon avis, ne pas motiver l'avis permet de garder le secret professionnel et une meilleure relation entre le médecin et la famille. Comme médecin, je pourrais révéler qu'un prélèvement n'est plus possible à cause d'une sérologie positive alors que je préférerais ne pas en informer la famille. Je plaiderai, donc, pour une non-motivation de l'avis.
Dr. Stéphane MEYER - Evidemment, je suis pour le don d'organes avec une information à tous les niveaux pour le donneur vivant, aussi proche soit-il, sur les risques encourus. Cette disposition paraît absolument nécessaire. Nous ne pouvons pas tuer un donneur au bénéfice d'un receveur. L'information doit également être diffusée pour tenter d'obtenir le maximum de donneurs pré mortem ou post mortem . Beaucoup de campagnes sont menées dans ce sens et c'est très important. En effet, nous manquons cruellement d'organes, de nombreux receveurs attendent et nous devons essayer de pallier cette carence, bien entendu sans trafic, en restant anonyme et complètement gratuitement. Un énorme travail d'information est à réaliser sur tout le monde, chacun jugeant avec sa sensibilité, mais actuellement cette tâche n'est pas encore assez menée en profondeur.
M. Nicolas ABOUT, président - Nous arrivons au terme de notre table ronde. Chacun de nos invités peut, pendant cinq minutes, aborder un sujet qui ne l'a pas été et au sujet duquel il souhaite nous laisser un message fort. Ainsi, les commissaires seront parfaitement informés de leurs pensées.
Pr. Sadek BELOUCIF - Je voudrais vous remercier car j'ai beaucoup appris. On me confiait, tout à l'heure, que le bruit ne faisait pas de bien et que le bien ne faisait pas de bruit. Cependant, vous devez pouvoir lancer le débat dans la population générale de manière éventuellement plus forte car ces sujets sont fédérateurs et indépendants des querelles politiques et autres. Nous pouvons louer nos amis allemands qui, cet été, ont publié dans le Frankfurter Allgemeine Zeitung , une sorte de feuilleton éthique où, quotidiennement, des arguments étaient présentés pour ou contre la recherche sur l'embryon. La Haute assemblée dispose peut-être de la vocation de lancer ce débat dans une atmosphère sereine et apaisée.
A la question du sénateur Barbier demandant si nous appliquerions une loi transgressant nos convictions, je répondrai brièvement : Dura lex sed lex . L'intérêt général prime l'intérêt particulier, nous pouvons d'ailleurs nous référer à l'avortement. Quelles que soient mes convictions personnelles à ce propos, comme responsable hospitalier, je me dois d'assurer une continuité du service public. Bien entendu, ce n'est pas parce que c'est légal que c'est moral, cette distinction pourrait être source d'enrichissement du débat entre nous. Le comité d'éthique a pu naître du rapport au droit mais nous pouvons nous demander si notre attitude générale, la morale ou l'éthique ne procèdent pas d'un acte de foi, si ce n'est en Dieu au moins en l'homme.
M. Michel GUGENHEIM - D'abord, à propos du transfert d'embryons post mortem , les autorités du rabbinat sont elles-mêmes encore partagées. Personnellement, ce qui me choque dans ce problème, est la création, a priori , d'un orphelin et j'ai pitié de ce pauvre enfant qui n'aura pas de père. Ce qui m'a choqué dans le projet de loi est que la faculté est présentée lorsque s'engage le processus. Autant je peux comprendre, et c'est dans ce cas que les rabbins sont partagés, une demande formulée de façon expresse par une épouse éplorée voulant, en quelque sorte, une trace de son ex-mari, par contre, aller au devant des gens et leur proposer cette possibilité alors qu'ils n'y ont probablement jamais pensé me paraît aller un peu loin en besogne.
Plus généralement, je voulais dire que, lorsque je siège dans les assemblées comme ici, mon propos, en exprimant la parole du judaïsme, n'est bien sûr pas de penser que notre point de vue va être suivi puisqu'il est strictement minoritaire. Toutefois, l'idée peut servir à éclairer. Cependant, le point important, pour moi, comme représentant d'une minorité n'est pas que l'examen de la loi fasse droit à notre point de vue mais qu'il permette, au moins, à cette minorité de vivre tranquillement dans son pays. A ce propos, la clause de conscience dans le projet de loi est satisfaisante puisqu'elle permet, par exemple, à un praticien de ne pas pratiquer l'IVG si c'est contraire à ses convictions. En outre, plus généralement, un consentement express, éclairé et libre est toujours demandé. A partir du moment où ces deux principes sont respectés, nous sommes finalement bien protégés. Je voudrais conclure, sur ce point, en relevant les quelques exceptions à la loi qui ne paraissent pas logiques. Par exemple, lorsqu'un consentement est présumé, il est passé outre le principe de consentement express. Cela me paraît difficile dans la mesure où nous allons ici au-delà de la liberté individuelle. J'ai également été frappé que les parties pénales du projet de loi n'entrent en vigueur que lorsque, par exemple, le protocole n'a pas été suivi, mais pas dans le cas où le médecin ne s'est pas intéressé à rechercher comme il le fallait le point de vue du défunt. Cela montre bien la relative minoration de ce point par le législateur. Je souhaitais mettre l'accent là-dessus pour conclure.
M. Patrick VERSPIEREN - Sur la question du transfert d'embryons post mortem , je serai très bref en vous avouant ma grande perplexité, je ne vous en dirai donc pas plus.
A propos de l'Agence prévue dans le projet de loi, il est sans doute sage qu'une instance soit chargée de veiller au respect de règles fixées par le droit. Cependant, c'est à ce dernier qu'il revient de les édicter et le législateur ne doit pas se défausser de ses responsabilités sur un établissement, fut-il public, ou sur un fonctionnaire agissant au nom de l'Etat comme précisé à l'article 14-17. Cependant, cette réflexion n'est pas une prise de position contre l'Agence mais consiste à signaler que nous devons faire attention : ce n'est pas la création d'une telle structure qui résout des problèmes éthiques et juridiques difficiles.
D'une manière générale, tous ces débats me confirment, dans cette vision, que la santé est une valeur très importante dans une société. La recherche médicale doit, évidemment, être favorisée mais la grande question est celle des limites à poser, ce qui relève notamment du rôle de la loi et du législateur. A mon sens, ces limites doivent être axées sur le respect de l'homme.
Nous sommes attirés par le scientifique et le technique, mais nous risquons d'oublier le soin tout court. Il importe de redécouvrir la dignité de l'homme et de tout homme, même, et peut-être surtout, s'il ne bénéficie plus des ressources de ces technosciences biomédicales.
Comme dernière remarque, je noterai que nous devons faire oeuvre de sagesse et résister à la fascination des modes, qui existent même dans le domaine scientifique. Je citerai ici tous les espoirs mis dans la thérapie génique. L'une des questions que je posais, il y a douze ans, dans un colloque, était de demander si c'était vraiment la voie à privilégier. Ne devrions-nous pas plutôt comprendre les maladies génétiques ? On m'a répondu : oui, mais cette démarche est très difficile et, donc, nous nous sommes lancés dans la thérapie génique. Bien sûr, nous pouvons en attendre des résultats ; mais, pour le moment, ils s'avèrent limités. Nous pouvons nous souvenir des discours tenus, en 1988, sur le séquençage du génome, qui était censé nous faire découvrir les secrets de la vie. Finalement, le génome a été séquencé et nous avons obtenu une carte, comme nous pouvions nous y attendre. Actuellement, le sujet porte sur les cellules souches embryonnaires : une espèce de fascination apparaît à propos de la recherche sur l'embryon. Ne serait-il pas rationnel d'observer une certaine distance face à cette fascination ? La sagesse consiste parfois à résister à certaines modes.
M. Geoffroy de TURCKHEIM - Je me demande si le texte de loi aborde suffisamment la question des cellules souches adultes dont nous avons beaucoup parlé. Je ne suis pas juriste et je ne sais pas si autoriser des pratiques un peu évidentes et ne posant pas de problème moral, pourrait servir. Cependant, une précaution serait peut-être à aborder à ce sujet.
L'expression, à l'article 21-51 alinéa 3, selon laquelle une expérience ne peut être menée qu'à condition qu'elle ne puisse être poursuivie par une méthode alternative d'efficacité comparable, m'a un peu choqué. En effet, nous avons envie de dire que votre oui soit oui, et que votre non soit non. Sur le plan moral, cela doit être permis ou pas, mais pas les deux.
La question de l'élargissement du champ d'action du DPI suscite une interrogation toute personnelle, je n'en ai pas discuté sur le plan fédératif. En effet, lorsque j'ai appris l'avis du comité consultatif d'éthique, j'ai été très étonné, connaissant la sagesse de cet organisme.
Sinon, nous partageons avec beaucoup une inquiétude à propos de l'Agence. Cet organisme donne l'impression de disposer d'un champ d'action et, donc, d'un pouvoir considérable. Dans cette structure se retrouveraient des politiques et des scientifiques, ce qui est très bien, mais nous nous sommes demandés ce matin si, dans le cadre d'une instance à l'apparence très professionnelle et technicienne, des risques de dérive entre des partenaires complices ne peuvent pas apparaître. Un comité des sages a été évoqué, ce serait peut-être la solution mais nous restons perplexes.
Je termine en répondant à votre question sur mon idée à propos des débats de ce matin. J'ai été très agréablement surpris, je dis cela sans flagornerie, car je ne pensais pas qu'une loi était discutée aussi sérieusement par les parlementaires. Les consultations ont été très écoutées, les sénateurs attentifs et ne faisant pas usage de la langue de bois. Le débat est vraiment important et cela fait plaisir.
M. Nicolas ABOUT, président - Croyez bien que nous savons l'importance des sujets que nous traitons et qu'ils amènent des discussions vraiment en profondeur, comme cela a été le cas avec le handicap, auquel nous avons consacré beaucoup de temps en auditions. Nous en aurons encore d'autres lorsque nous atteindrons le stade d'une proposition. En effet, nous réfléchissons en amont et, ensuite, nous faisons valider nos propositions en aval, avant même de voter.
Les sujets sont trop importants et je suis d'accord avec votre idée sur « que votre oui soit oui et que votre non soit non ». Cependant, en matière de bioéthique, nous devrons, sans arrêt, remettre l'ouvrage sur le métier et nous vous réinviterons dans quelques années pour connaître l'évolution de vos pensées. Nous avons besoin de vous et, comme vous l'avez très bien précisé, une erreur manifeste dans la composition de l'Agence existe. Certes, des scientifiques ou des politiques sont nécessaires mais il faudrait intégrer ceux qui ont pour mission, non pas de jouer les prophètes, mais de guider et d'approfondir la réflexion. Cela est très utile et nous avons beaucoup à faire dans ce domaine.
Dr. Stéphane MEYER - Je voulais aborder le point important des subventions pour la recherche d'Etat. Ce serait très grave de laisser l'industrie monopoliser la recherche parce qu'elle s'approprierait très vite toutes les découvertes que nous pourrions faire, avec malheureusement toutes les dérives possibles. Messieurs, vous avez un rôle important à jouer pour permettre aux chercheurs de rester en France et d'y travailler en toute tranquillité. C'est un point important à aborder.
Pour terminer, comme l'énonçait l'un des intervenants, associer deux mots, comme bio- de biologie, et éthique, ne peut pas être facile puisque c'est le mélange de l'eau et du feu. En effet, si la biologie peut être binaire, scientifique pure et mathématique, l'éthique restera toujours dans le domaine du ternaire, de l'intuitif et de la personnalité de chacun. C'est, peut-être, la raison pour laquelle certaines personnes plus férues d'éthique ont une place auprès de vous.
M. Francis GIRAUD, rapporteur - Nous arrivons ce soir à un terme fondamental de ces auditions menées depuis six mois, et auxquelles vous avez été nombreux à participer. La journée d'aujourd'hui est significative avec l'accueil, ce matin, de chercheurs et de médecins et, cet après-midi, cette table ronde avec la représentation des courants de pensée, religions et philosophies. Comme l'a précisé un collègue, la tâche du législateur n'est pas facile parce que nous ne sommes ni un comité scientifique, ni des représentants d'églises ou de philosophies. Nous devons écouter tout le monde comme, je crois, nous l'avons fait. Ensuite, nous allons essayer, le mot semble-t-il a été prononcé et le Sénat s'honore, d'adopter une telle attitude devant des textes difficiles, de décider en sagesse. Cependant, comme cela a été précisé, il sera impossible de satisfaire tout le monde. Cependant, la loi peut, en apportant des repères et des limites et en tentant, autant que possible, de ne pas figer des situations, rester attentive à une évolution éventuelle. Notre collègue M. Chérioux, grâce à sa large participation aux lois de 1994, sait bien que le fait d'avoir fixé un délai de cinq ans, a permis neuf ans plus tard d'entamer la révision. Il ne faut peut-être pas inscrire un terme fixe dans la loi mais permettre au Parlement, et vous ne nous en voudrez pas puisque nous représentons la population française, d'avoir le dernier mot pour fixer les grandes orientations.
Nous vous remercions tous. Le président Nicolas About a beaucoup mis en oeuvre pour que ces auditions, tout au long de l'année, soient très instructives, ce qui a été le cas.
M. Nicolas ABOUT, président - Je voudrais remercier le public qui a assisté à ces auditions, tous les téléspectateurs qui vont les suivre sur la chaîne Public Sénat, tous nos invités, les commissaires présents, notre rapporteur et les collaborateurs de la commission qui ont permis de faire avancer ce difficile sujet.
TABLEAU COMPARATIF
___
* 1 Alain Claeys, Claude Huriet, rapport de l'OPECST, n° 1407 (AN) n° 232 (Sénat), session 1999-2000, p. 11.
* 2 Rapport précité, p. 21.
* 3 « L'abondance des textes d'application à élaborer (32 au total) contraste avec les moyens limités en personnel de la DGS (2 fonctionnaires du cadre A, effectif récemment porté à 3)», rapport précité, p. 21.
* 4 Rapport précité, p. 15.
* 5 Rapport précité, p. 44.
* 6 Rapport précité, p. 44.
* 7 Rapport précité, p. 49.
* 8 Rapport précité, p. 51.
* 9 Rapport précité, p. 64.
* 10 Rapport précité, p. 93.
* 11 Intra cytoplasmic sperm injection.
* 12 Rapport précité, p. 98.
* 13 Rapport précité, p. 108.
* 14 Rapport précité, p. 108.
* 15 Rapport précité, p. 108.
* 16 Rapport précité, p. 138.
* 17 Rapport précité, p. 139.
* 18 Etude précitée p.11, qui cite le rapport public de 1998.
* 19 Idem
* 20 Etude précitée, p. 13.
* 21 Rapport précité, p. 16.
* 22 Rapport précité, p. 23.
* 23 Rapport précité, p. 20.
* 24 Rapport précité, p. 21.
* 25 Rapport précité, p. 23.
* 26 Rapport précité, p. 23.
* 27 Rapport précité, p. 44.
* 28 Cf. Examen des articles, article 5.
* 29 Conseil d'Etat, étude précitée, p 67-68.
* 30 HLA : Histocompatibilité humaine.
* 31 Assemblée nationale, mission d'information commune préparatoire au projet de loi de révision des «lois bioéthiques» de juillet 1994 (n° 3208, 27 juin 2001), rapport précité p. 74.
* 32 Rapport de M. Alain Claeys, Assemblée nationale, n° 3528, p. 189.
* 33 M. Bernard Kouchner, débat Assemblée nationale compte rendu intégral, 3 e séance du 17 janvier 2002, JO p. 691.
* 34 Cf. examen des articles, article 18.
* 35 Cf. examen de l'article 18 précité.
* 36 Rapport d'information précité p. 73.
* 37 Rapport Sénat n° 174 (2001-2002) projet de loi relatif aux droits des malades et à la qualité du système de santé - 1 e lecture.
* 38 Cf. compte rendu intégral des auditions en annexe du présent rapport.
* 39 M. Bernard Kouchner, débats Assemblée nationale, 16 janvier 2002, JO, p. 581.
* 40 Convention d'Oviedo, référence précitée.
* 41 Conseil d'Etat, Etude précitée, p. 96.
* 42 Cf. compte rendu des auditions en annexe du présent rapport (c'est votre rapporteur qui souligne).
* 43 Etude précitée, p. 98.
* 44 Etude précitée, p 105-106.
* 45 Car confronté au refus de se livrer à un tel test, le juge pourra présumer la filiation.
* 46 Jules Supervielle, Shéhérazade.
* 47 M. Alain Clayes, débats Assemblée nationale, JO p. 585.
* 48 M. Bernard Kouchner, 16 janvier 2002, p. 585.
* 49 Cf. compte rendu des auditions annexé au présent rapport (c'est votre rapporteur qui souligne).
* 50 Etude précitée, p. 104. (c'est votre rapporteur qui souligne).
* 51 Conseil d'Etat, étude précitée, p. 60.
* 52 Rapport d'information précité, p. 198.
* 53 Accident vasculaire 50%, trauma 40 %, (source EFG 2001).
* 54 Rapport précité p.34.
* 55 Rapport d'information précité, p.209.
* 56 Cf compte rendu des auditions en annexe du présent rapport.
* 57 Cf compte rendu des auditions en annexe du présent rapport.
* 58 Rapport d'évaluation précité p. 45.
* 59 Rapport législatif précité, p. 102.
* 60 Alain Claeys, La brevetabilité du vivant, rapport de l'Office parlementaire d'évaluation des choix scientifiques et technologiques, n° 3502 (Assemblée nationale), n°160 (Sénat), p. 42.
* 61 Député social démocrate au Bundestag allemand.
* 62 Cf. compte rendu des auditions en annexe du présent rapport.
* 63 Cf. compte rendu des auditions en annexe du présent rapport.
* 64 Etude précitée, p. 121-122.
* 65 Il s'agit dans leur majorité de vecteurs viraux ou de vecteurs dits « inertes ».
* 66 Rapport précité p. 13.
* 67 Rapport précité, p 153
* 68 Cf. exposé général.
* 69 25 février - 1 er mars, rapport, considérant 21 et 22.
* 70 Rapport précité, p. 149.
* 71 Etude précitée, p. 50.
* 72 Cf. compte rendu des auditions annexées au présent rapport.
* 73 Ces dernières doivent, depuis 1988, réaliser un minimum de 300 accouchements par an.
* 74 Rapport précité, p. 181.
* 75 Etude précitée, p. 42.
* 76 Etude précitée, p. 42.
* 77 Cf. compte rendu des auditions en annexe du présent rapport (c'est votre rapporteur qui souligne).
* 78 Cf. compte rendu des auditions annexé au présent rapport (c'est votre rapporteur qui souligne).
* 79 Cf. présent rapport, exposé général.
* 80 Etude précitée, p.45.
* 81 Etude précitée, p. 47.
* 82 Etude précitée, p. 47.
* 83 Selon l'expression de M. Jean-François Mattei, lors de son audition devant votre commission (cf. compte rendu annexé au présent rapport).
* 84 Cf. ci-dessus commentaire de l'article 6.
* 85 Etude précitée, p. 17.
* 86 Rapport précité p. 69.
* 87 Cf. compte rendu des auditions annexé au présent rapport.
* 88 Cf. compte rendu des auditions annexé au présent rapport. Cette audition s'est déroulée le 4 décembre 2002, soit avant les « annonces » qui ont défrayé la chronique de la fin de l'année.
* 89 rapport précité p. 58
* 90 Rapport précité p. 59.
* 91 Rapport précité, p. 57.
* 92 Alain Claeys, rapport de l'Assemblée nationale précité, p. 232.







