B. DONNER À LA RECHERCHE LES MOYENS DE VALORISER SES RÉSULTATS
1. Parfaire la professionnalisation du transfert de la propriété intellectuelle
Si la France a désormais rattrapé son retard dans la création de start-ups en santé, celles-ci nécessitent néanmoins que leur soit garantie la possibilité de détenir, à terme, la propriété intellectuelle de la découverte qu'elles comptent exploiter, que cette découverte soit issue de la recherche publique ou privée. C'est à cette condition que les start-ups seront en capacité d'attirer les investisseurs disposant de la surface financière suffisante pour accompagner leur maturation dans le cadre de développements cliniques de phases 2b et 3 .
a) Faire évoluer, dans certains cas, le mandataire unique en « propriétaire unique »
Déployée à compter de 2014 8 ( * ) , la désignation d'un mandataire unique 9 ( * ) par des personnes publiques pour les brevets détenus en copropriété a été systématisée par la loi « Pacte » de 2019 10 ( * ) et son décret d'application de 2020 11 ( * ) . Plusieurs organismes auditionnés ont toutefois regretté qu'une partie des transferts de propriété intellectuelle, comme la cession des actifs de propriété intellectuelle ou l'engagement contractuel d'une cession ultérieure, échappe encore au périmètre du mandat défini par les copropriétaires 12 ( * ) .
Or ces modalités de transfert sont essentielles pour permettre à des projets à fort potentiel d'attirer des investissements et d'être soutenus financièrement tout au long du développement clinique de l'invention. Pour l'heure, lorsque le mode de valorisation n'entre pas dans le périmètre du mandataire, un comité d'arbitrage est réuni pour acter une décision de principe entre les copropriétaires qui doivent ensuite, chacun, se prononcer sur le contenu de l'accord de cession et formellement le valider. Cette procédure d'arbitrage, longue, ne fait que complexifier et ralentir la conclusion de partenariats entre la recherche publique et des investisseurs privés .
La commission appelle, par conséquent, à parachever la logique de simplification engagée par la mise en place du mandataire unique en renforçant son autonomie dans la conduite des opérations de cession de propriété intellectuelle . Les divergences entre les objectifs de valorisation des copropriétaires ne doivent plus en effet constituer un frein à la conclusion de partenariats avec des acteurs extérieurs. La commission recommande ainsi la transformation progressive du mandataire unique en un véritable « propriétaire unique » dans les cas où cela s'avérerait le plus pertinent, pour plus de lisibilité pour les industriels et les investisseurs privés , en particulier étrangers.
Ce propriétaire unique disposerait d'un mandat élargi et d'une autonomie renforcée pour la négociation et la signature de tous les contrats de transfert, y compris ceux impliquant la cession d'un résultat 13 ( * ) , sous réserve du respect d'une charte de principes partagés et d'un accord sur la répartition des revenus nets , validés par les copropriétaires dès la désignation du mandataire unique afin de ne plus réenclencher de procédure d'arbitrage à chaque opération de cession . Il redistribuerait ensuite entre les copropriétaires les bénéfices tirés de cette valorisation.
Le recours au propriétaire unique est déjà pratiqué dans un certain nombre de pays anglo-saxons afin de permettre aux industriels d'identifier un seul interlocuteur dans leurs négociations de transfert, souhait partagé par un grand nombre de groupes pharmaceutiques internationaux. Il est également pertinent dans des cas où les enjeux de valorisation impliquent, comme le souligne l'institut Pasteur, « de régler des situations précontentieuses, voire d'initier des litiges et négocier des transactions. Ces situations requièrent des réponses agiles et sans délai, incompatibles avec les règles de copropriété. Le principe du mandataire ne permet pas cette agilité, au contraire le mandat exclut les litiges et transactions. » 14 ( * ) L'évolution du dispositif du mandataire unique pourrait ainsi utilement s'inspirer du modèle britannique de valorisation et de transfert articulé autour de l'organisation LifeArc 15 ( * ) .
Proposition n° 7 : ouvrir la possibilité pour le mandataire unique de se transformer en un « propriétaire unique » disposant d'un mandat élargi et d'une autonomie renforcée pour la cession d'actifs et la conclusion de partenariats, sous réserve du respect d'une charte de principes partagés et d'un accord sur la répartition des revenus nets, validés par les copropriétaires dès la désignation du mandataire.
b) Professionnaliser et homogénéiser les pratiques de valorisation des acteurs du transfert
Les critères de transfert de la propriété intellectuelle peuvent sensiblement varier d'une société d'accélération du transfert de technologies (SATT) à une autre. En tenant insuffisamment compte des spécificités des mécanismes de certaines innovations et des besoins des acteurs de l'écosystème territorial, certaines SATT peuvent en effet prévoir des conditions de partage des résultats de la valorisation peu attractives pour les investisseurs 16 ( * ) .
En résulte une demande légitime des acteurs de
la recherche et du développement industriel, notamment au sein des
pôles de compétitivité en santé, de l'engagement
d'une véritable
démarche de
benchmark
des
pratiques de transfert de la propriété intellectuelle en
santé à l'étranger et en France
afin de garantir
une plus grande cohérence des contrats de licence et de gestion de la
propriété intellectuelle. Ce
benchmark
, qui serait
réalisé par une future agence de l'innovation en
santé
- dont les contours sont précisés au
point I. B. 2. du présent rapport -
déboucherait sur un
guide des bonnes
pratiques
de transfert
dans un objectif de professionnalisation des SATT.
Proposition n° 8 : professionnaliser l'activité de valorisation conduite par les SATT dans le domaine de la santé en s'appuyant sur un benchmark des pratiques de transfert qui déboucherait sur un guide des bonnes pratiques pour l'élaboration des contrats de licence.
2. Se donner les moyens d'une recherche ambitieuse en santé
a) Rattraper le retard dans le financement de la recherche publique
La capacité de notre pays à développer des innovations de rupture dans le domaine de la santé est subordonnée au dynamisme de sa recherche fondamentale . Le développement accéléré des vaccins à ARN messager contre la covid-19 masque près de trente ans de recherche fondamentale à laquelle l'Institut Pasteur a pris une part importante.
Or l'évolution des financements publics de la recherche et développement (R&D) en santé en France, qui ont diminué (hors CIR) de 28 % entre 2011 et 2018 17 ( * ) , contraste avec l'augmentation des moyens de la recherche en Allemagne 18 ( * ) et au Royaume-Uni où les crédits publics en R&D en santé ont progressé, respectivement de 11 % et de 16 %. Dans un rapport 19 ( * ) conjoint de mars 2021, les Académies nationales de médecine et de pharmacie font le constat d'un « recul spectaculaire du soutien à la recherche en biologie-santé » en France, avec une diminution évaluée à 25 % entre 2008 et 2020.
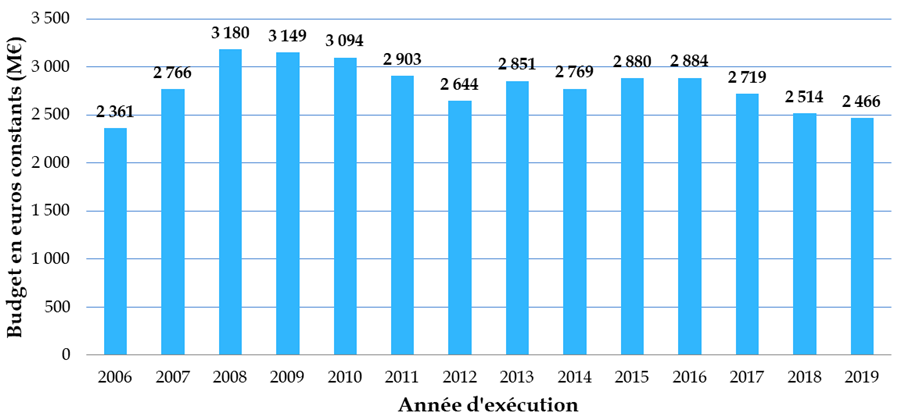
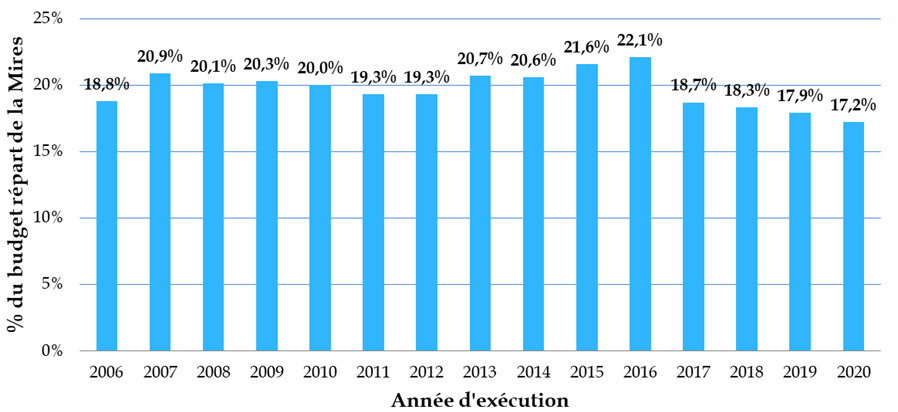
Les crédits publics consentis à la biologie-santé ne représentent finalement qu'un peu plus de 17 % du total des moyens de la mission interministérielle de la recherche et de l'enseignement supérieur (Mires) du budget de l'État, soit un niveau sensiblement inférieur à celui observé dans d'autres pays européens - « qui consacrent 35 % à 40 % de leur budget à cette recherche, et jusqu'à 50 % au Royaume-Uni » - et ce, dans un contexte marqué par une multiplication par plus de dix en quinze ans du coût des travaux dans ce domaine.
Budget consacré à la biologie-santé depuis 2006
Données Mires, en millions d'euros constants 2019
Part des crédits consacrés à la
biologie-santé
dans les moyens de la Mires depuis 2006
Source : Académie nationale de médecine et académie nationale de pharmacie, Réformer la recherche en sciences biologiques et en santé - Partie I, le financement , rapport bi-académique 30 mars 2021
La loi de programmation de la recherche pour la période 2021-2030 20 ( * ) ne comporte aucun engagement chiffré et pluriannuel concernant l'effort qui sera spécifiquement déployé en faveur de la recherche biomédicale . Encore une fois, la recherche en santé n'est pas clairement identifiée comme une priorité de l'investissement public en recherche, alors que, comme l'indique l'Inserm, la part de la France dans le total des publications scientifiques mondiales s'est érodée de plus d'un tiers de 2005 à 2017 .
Au-delà du sous-financement structurel de la recherche publique , les organismes auditionnés font le constat préoccupant d'un émiettement des sources de financement qui pénalise l'accompagnement de projets à fort potentiel qui nécessiteraient des investissements conséquents pour poursuivre leurs développements. La BPI finance une multitude de projets dans le domaine de la santé mais, en l'absence de vision stratégique, ses soutiens sont insuffisamment hiérarchisés. Quant au PIA 4 21 ( * ) , parmi ses quinze stratégies d'accélération 22 ( * ) , seulement trois concernent à ce stade directement la santé 23 ( * ) .
Dans ces conditions, la commission préconise :
- le doublement de la part des crédits de la mission interministérielle « Recherche et enseignement supérieur » dédiés à la recherche en biologie-santé, afin d'atteindre une proportion de plus de 30 % des financements publics en faveur de la recherche (hors CIR) consentis à la recherche biomédicale ;
- l'identification de quelques secteurs à haut potentiel et stratégiques dans le domaine de la santé et la priorisation pour ces secteurs de l'accès aux financements publics apportés par la BPI et l'Agence nationale de la recherche (ANR). À cet égard, l'action « Programmes et équipements prioritaires de recherche » 24 ( * ) (PEPR) du PIA 4 constituerait un levier pertinent d'accompagnement de ces secteurs prioritaires et d'accélération de leurs développements. Cette priorisation suppose que notre pays assume clairement le choix de se spécialiser dans certains segments de la recherche biomédicale (oncologie, immunologie, cardiologie, maladies infectieuses, biothérapies ou santé mentale...). Ces secteurs prioritaires seraient définis par la future agence de l'innovation en santé, après concertation des acteurs de la recherche académique (organismes nationaux de recherche, alliances scientifiques, universités...), hospitalière et industrielle et des acteurs du système de santé.
Proposition n° 9 :
remédier au sous-financement structurel de la recherche
biomédicale par :
- le doublement de la
part des crédits de la mission interministérielle
« Recherche et enseignement supérieur »
dédiés à la recherche en biologie-santé ;
- l'identification de quelques secteurs à haut potentiel et
stratégiques dans le domaine de la santé en faveur desquels
serait priorisé l'accès aux financements publics.
b) Rénover la gouvernance nationale et européenne de l'innovation en santé
Pendant la crise sanitaire, le rôle des agences américaines, telles que la « Biomedical Advanced Research and Development Authority » (Barda) et la « Defense Advanced Research Projects Agency » (Darpa), a été analysé comme décisif dans la course à l'innovation pour développer des vaccins et des traitements contre la covid-19. Comme l'a rappelé M. Franck Grimaud, président-directeur général de Valneva et président du pôle de compétitivité Atlanpole Biotherapies, la Barda 25 ( * ) est en capacité d'injecter en permanence dix à vingt milliards de dollars dans des projets prioritaires. Dès février 2020, elle a choisi d'investir dans une dizaine de projets de vaccin en soutenant chacun d'eux à hauteur de plusieurs centaines de millions de dollars. Face à une menace d'ampleur, la Barda et la Darpa se sont ainsi clairement positionnées comme des partenaires des développements, en se montrant prêtes à assumer le risque de l'innovation . Par contraste, l'Europe s'est positionnée comme acheteuse auprès des industriels du développement de vaccins, et non comme facteur d'innovation .
L'audition 26 ( * ) par la commission de Mme Kate Bingham, ancienne responsable de la cellule « vaccins » britannique 27 ( * ) , a également mis en lumière la différence d'approche entre l'Europe et le Royaume-Uni dans l'acquisition de vaccins : les négociations conduites par les autorités européennes ont été perçues comme particulièrement complexes et bureaucratiques par nombre d'industriels, quand le pragmatisme du gouvernement britannique, déterminé à accompagner par des financements massifs le développement des candidats les plus prometteurs, a été, lui, unanimement salué.
Tirant les enseignements de la crise sanitaire, la Commission européenne a lancé début 2021 une initiative pour la création d'une autorité européenne de préparation et de réaction en cas d'urgence sanitaire (« European Health Emergency Response Authority » - HERA), chargée d'investir de façon réactive dans le développement et le déploiement de contremesures et l'augmentation des capacités de production 28 ( * ) .
Cette agence, dont la création est annoncée pour 2021, devrait être appelée à coordonner les investissements stratégiques pour la recherche, le développement clinique, la production, le déploiement et la distribution de contremesures . L'enjeu est qu'elle puisse disposer d'une « force de frappe » comparable à celle de la Barda ou de la Darpa, qui se chiffre en plusieurs dizaines de milliards d'euros, afin de financer des projets innovants pour réagir à une menace sanitaire et de partager le risque au niveau européen.
Cette réflexion sur les agences publiques de soutien à l'innovation a relancé le projet de création d'une agence française de l'innovation en santé porté par un certain nombre d'acteurs du secteur, dont France Biotech, tête de réseau des biotechs en France, et le Leem. À l'appui de sa proposition, France Biotech met en avant l'expérience de l' agence de l'innovation de défense 29 ( * ) . Créée en septembre 2018, cette agence constitue un guichet unique pour le dépôt de projets innovants sur une série de thématiques prioritaires.
Lors de son audition par la commission des affaires sociales, M. Franck Mouthon, président de France Biotech, a indiqué voir dans cette agence le chef d'orchestre d'une stratégie de l'innovation en santé , en capacité de « coordonner cette politique d'amont, qui est très bien abordée par la BPI, et cette politique d'aval où on ne parle pas ou très peu et pour laquelle les acteurs ont besoin d'avis engageants, de bénéficier d'éclairages sur la pertinence de leurs développements - question à laquelle le système de santé peut répondre, que ce soit la direction de la sécurité sociale, l'ANSM, la HAS, le Comité économique des produits de santé (CEPS)... » Cette agence pourrait ainsi se voir confier, sur la base de priorités stratégiques clairement définies, le soin de « régler des problèmes sur un engagement de trois mois, sur un transfert de technologie, sur la fixation du prix au niveau du CEPS, sur l'évaluation au niveau de la HAS... »
Convaincue de la nécessité de définir une feuille de route de l'innovation en santé articulée autour de priorités répondant aux besoins de notre système de santé, la commission est favorable à la création d'une agence de l'innovation en santé à la condition que celle-ci ne constitue pas une strate administrative supplémentaire dans un paysage institutionnel de la recherche déjà peu lisible mais qu'elle soit bien un facteur de simplification et d'accélération .
Afin de ne pas créer un nouvel établissement public, l'agence de l'innovation pourrait être constituée, à l'instar de l'agence de l'innovation de défense, sous la forme d'un service à compétence nationale (SCN) placé directement sous l'autorité du ministre de la santé et doté de pouvoirs décisionnels délégués lui ménageant une autonomie d'action sous le contrôle du ministre 30 ( * ) .
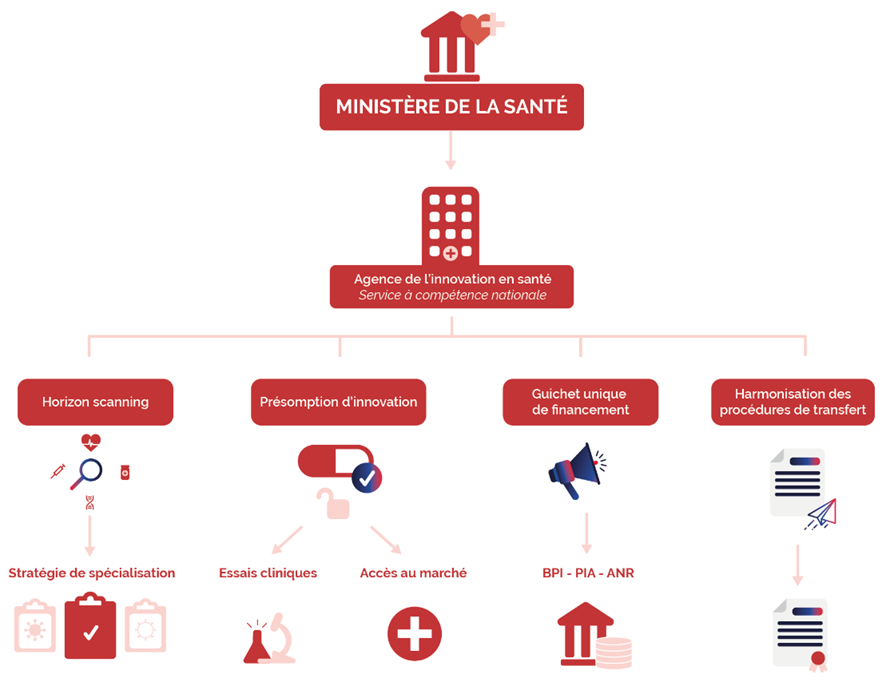
Préfiguration de l'agence de l'innovation en santé
Source : Commission des affaires sociales du Sénat
L'agence de l'innovation en santé serait alors chargée de missions très opérationnelles :
- réaliser une stratégie de veille ( horizon scanning ) des développements de thérapies innovantes les plus prometteurs afin d'élaborer une stratégie de spécialisation sur les segments de recherche porteurs de l'innovation en santé qui devront être soutenus prioritairement. La définition de ces secteurs prioritaires devra s'appuyer sur une consultation large des acteurs de la recherche académique et industrielle et des acteurs du système de santé afin de faire correspondre les développements soutenus à la satisfaction des besoins de notre système de santé ;
- attribuer une présomption d'innovation à certains développements et thérapies s'inscrivant dans les secteurs prioritaires qu'elle aura définis, qui permettra de venir en soutien, le cas échéant, d'une demande d'examen en procédure accélérée (« fast-track ») d'une demande d'autorisation d'essai clinique auprès de l'Agence nationale de sécurité du médicament et des produits de santé (ANSM) et/ou d'un comité de protection des personnes (CPP), d'une demande d'évaluation ou d'accès précoce auprès de la Haute Autorité de santé (HAS) ou d'une négociation de prix auprès du CEPS. L'agence pourra être sollicitée par un promoteur ou un industriel pour obtenir cette présomption d'innovation afin de « débloquer » l'instruction de ce type de demande. La publication des décisions de présomption d'innovation permettra également d'encourager le soutien de ces développements par des investissements privés, notamment par des fonds de capital-risque, qui verront dans la présomption d'innovation accordée par l'agence la garantie d'une mise en oeuvre facilitée des essais cliniques ou d'un accès accéléré au marché ;
- constituer un guichet unique pour le dépôt de dossiers de candidature à l'ensemble des appels d'offres pour l'obtention de financements publics de la recherche en santé, afin de flécher des investissements publics massifs sur des développements en phases précliniques ou cliniques . À ce titre, l'agence centralisera pour le compte de la BPI, du SGPI 31 ( * ) , de l'ANR et du MESRI 32 ( * ) les candidatures aux appels d'offres organisés par ces structures et permettra le dépôt d'un seul et même dossier pour plusieurs appels d'offres en lien avec l'innovation en santé, afin d'alléger la charge administrative des équipes de recherche ;
- simplifier et harmoniser les procédures de transfert de propriété intellectuelle par l'élaboration de guides de bonnes pratiques.
Proposition n° 10
: créer une agence de l'innovation en santé sous la forme d'un
service à compétence nationale placé sous
l'autorité du ministre de la santé, chargée des missions
suivantes :
- définir, à partir d'un
horizon
scanning
, une stratégie de spécialisation sur les segments
de recherche porteurs de l'innovation en santé qui devront être
soutenus prioritairement pour répondre aux besoins du système de
santé ;
- attribuer une
présomption d'innovation à des développements et
thérapies s'inscrivant dans ces segments prioritaires afin de faciliter
le lancement d'un essai clinique ou un accès rapide au
marché ;
- constituer un guichet
unique pour le dépôt centralisé d'un seul et même
dossier de candidature aux appels d'offres en faveur de l'innovation en
santé ;
- simplifier et
harmoniser les procédures de transfert de propriété
intellectuelle par l'élaboration d'un guide de bonnes
pratiques.
* 8 Décret n° 2014-1518 du 16 décembre 2014 relatif au mode de désignation et aux missions du mandataire prévu à l'article L. 533-1 du code de la recherche.
* 9 Ce mandataire est en théorie chargé de l'ensemble des activités de gestion et de valorisation des résultats d'une découverte issue de personnes publiques investies d'une mission de recherche.
* 10 Loi n° 2019-486 du 22 mai 2019 relative à la croissance et la transformation des entreprises.
* 11 Décret n° 2020-24 du 13 janvier 2020 relatif à la gestion de la copropriété des résultats de recherche, au mode de désignation et aux missions du mandataire unique prévu à l'article L. 533-1 du code de la recherche.
* 12 Le décret du 13 janvier 2020 a bien habilité le mandataire unique à procéder, à titre exclusif, à la négociation et la signature de tous les contrats de transfert y compris ceux impliquant la cession d'un résultat dans des conditions définies préalablement par les copropriétaires. Cette concertation préalable permet d'encadrer le pouvoir de cession du mandataire unique.
* 13 Voire la gestion de contrats industriels préfigurant la gestion de la propriété intellectuelle.
* 14 Réponses de l'institut Pasteur au questionnaire de la mission d'information.
* 15 Organisme non lucratif (« medical research charity »).
* 16 Des demandes de reversement à une SATT de près de 50 % du chiffre d'affaires issu de l'exploitation d'une technologie transférée peuvent logiquement déconcerter les acteurs du tissu économique local lorsqu'est en jeu une application relativement modeste au démarrage.
* 17 Données transmises par la direction générale de la recherche et de l'innovation (DGRI) du ministère de l'enseignement supérieur, de la recherche et de l'innovation (MESRI).
* 18 Les crédits publics en R&D (hors CIR) pour la santé en France sont plus de deux fois inférieurs à ceux de l'Allemagne.
* 19 Académie nationale de médecine et académie nationale de pharmacie, Réformer la recherche en sciences biologiques et en santé - Partie I, le financement , rapport bi-académique, 30 mars 2021.
* 20 Loi n° 2020-1674 du 24 décembre 2020 de programmation de la recherche pour les années 2021 à 2030 et portant diverses dispositions relatives à la recherche et à l'enseignement supérieur.
* 21 Les dotations des programmes investissements d'avenir dans le domaine de la santé s'élèvent à 2,6 milliards d'euros depuis 2011.
* 22 Dont quatre déjà identifiées par le Gouvernement et onze en cours d'élaboration et de consultation.
* 23 La santé digitale ; les biothérapies et la bioproduction de thérapies innovantes ; les maladies infectieuses émergentes - menaces nucléaires, radiologiques, biologiques et chimiques.
* 24 Selon le site de l'agence nationale de la recherche, « les PEPR exploratoires visent des secteurs en émergence avec des travaux de recherche dont les domaines d'application peuvent, pour certains, relever encore d'hypothèses de travail. Il s'agit d'explorer des champs scientifiques dont les retombées espérées peuvent être multiples. »
* 25 Qui constitue un bureau du département américain fédéral de la santé.
* 26 Audition du 16 juin 2021.
* 27 « UK Vaccin Taskforce ».
* 28 Cette initiative, qui doit se traduire prochainement par la publication par la Commission européenne d'une proposition de règlement, fait suite au souhait exprimé par sa présidente lors de son discours sur l'état de l'Union européenne de 2020 de constituer une « Barda européenne », qui a débouché sur une communication de la Commission en novembre 2020 pour la construction d'une Union européenne de la santé (communication de la Commission au Parlement européen, au Conseil, au Comité économique et social européen et au Comité des régions, « Construire une Union européenne de la santé : renforcer la résilience de l'UE face aux menaces transfrontières pour la santé », COM(2020) 724 final, 11 novembre 2020).
* 29 Dotée d'un budget d'1,2 milliard d'euros en 2019 qui devrait être porté à plus d'1,5 milliard d'euros en 2022.
* 30 Le responsable de ce service disposerait ainsi d'une délégation de pouvoir et d'une autonomie plus importante que dans l'hypothèse où le SCN aurait été rattaché à un directeur d'administration centrale du ministère de la santé.
* 31 Le secrétariat général pour l'investissement (SGPI).
* 32 Le ministère de l'enseignement supérieur, de la recherche et de l'innovation (MESRI).